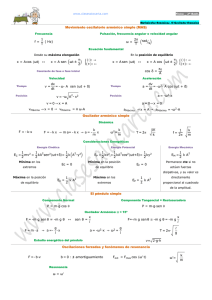
Solución de la ecuación de Schrödinger Oscilador armónico
Anuncio

SOLUCIÓN DE LA ECUACIÓN DE SCHRÖDINGER OSCILADOR ARMÓNICO Equipo 2 OSCILADOR ARMÓNICO CLÁSICO Sistema que contenga un componente sobre el que actúa una fuerza restauradora proporcional a su desplazamiento desde el equilibrio. OSCILADOR ARMÓNICO Mecánica clásica Mecánica Cuántica La energía puede tener cualquier nivel continuo La energía solo puede tener valores discretos Cambios en los niveles de energía pueden tomar cualquier valor Cambios en los niveles de energía solo ocurren en cuantos El cuerpo puede estar en reposo en x=0 El nivel de energía mínimo es No existe reposo absoluto en x=0 OSCILADOR ARMÓNICO CUÁNTICO Se puede obtener la ecuación de Schrodinger de un oscilador armónico utilizando el potencial clásico. La ecuación de Schrodinger con esta forma de potencial es: APROXIMACIÓN DE LA SOLUCIÓN Se sugiere la siguiente forma: Téngase en cuenta que esta forma (una función gaussiana), satisface el requisito de ir a cero en el infinito, por lo que es posible normalizar la función de onda. RESOLVIENDO LA ECUACIÓN DE SCHRODINGER Sustituyendo esta función en la ecuación de Schrodinger, mediante la evaluación de la segunda derivada de la función de onda. SOLUCIÓN POLINOMIO DE HERMITE Cuando la ecuación de Schrodinger para el oscilador armónico se resuelve mediante el método de series, las soluciones contienen este conjunto de polinomios, llamado polinomios de Hermite. POLINOMIO DE HERMITE ψ FUNCIONES DE ONDA ESQUEMA TRIDIMENSIONAL DE NIVELES DE ENERGÍA Y PROBABILIDAD ESQUEMA TRIDIMENSIONAL DE NIVELES DE ENERGÍA Y PROBABILIDAD PROBLEMA Curva que corresponde a la probabilidad |Ψ1² = ψ*ψ para el estado n = 10 del oscilador armónico simple. ¿Cómo ilustra este diagrama el principio de correspondencia de Bohr? CONCLUSIONES La probabilidad de encontrar cualquier valor dado de x es ψ2 el oscilador en Conforme aumenta n la función de onda presenta mas crestas en el pozo de potencial, lo cual corresponde a una longitud de onda mas corta y por lo tanto tiene mayor energía. A medida que aumenta el número cuántico, la distribución de probabilidad se parece más a la del oscilador clásico (principio de correspondencia), y para niveles bajos (moléculas), el modelo cuántico describe mejor esta distribución de probabilidad. BIBLIOGRAFIA LEVINE, Ira N. Quantum chemistry, Boston, Allyn and bacon, 1974. Pp 48-67.