historia natural y fisiopatología de la diabetes mellitus tipo ii
Anuncio
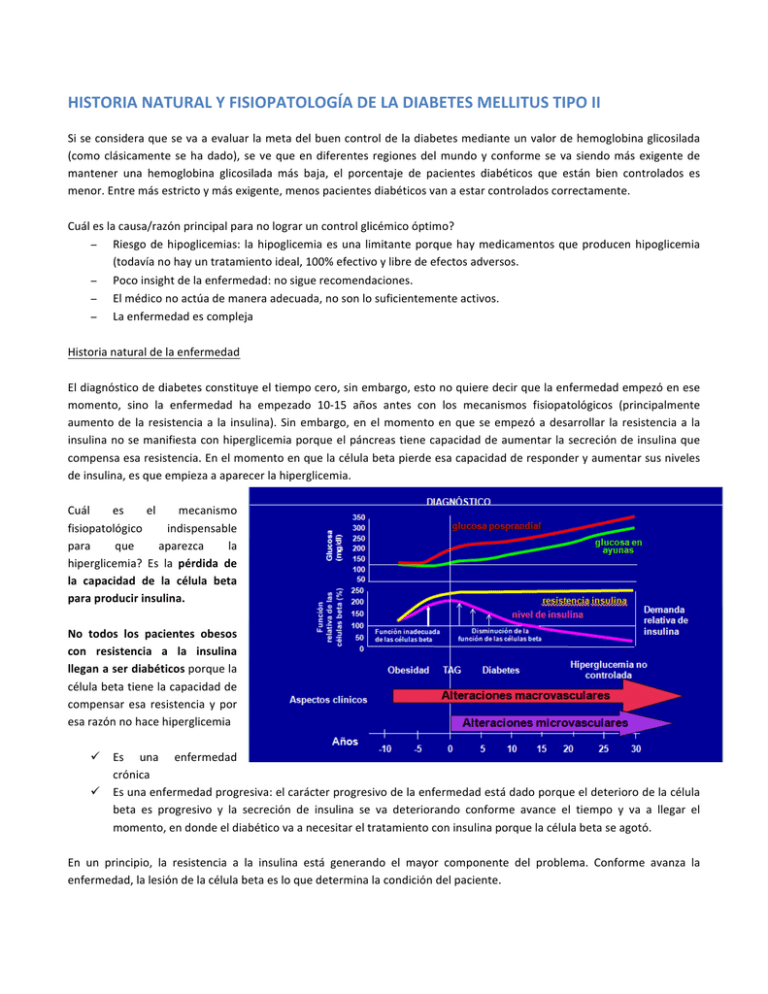
HISTORIA NATURAL Y FISIOPATOLOGÍA DE LA DIABETES MELLITUS TIPO II Si se considera que se va a evaluar la meta del buen control de la diabetes mediante un valor de hemoglobina glicosilada (como clásicamente se ha dado), se ve que en diferentes regiones del mundo y conforme se va siendo más exigente de mantener una hemoglobina glicosilada más baja, el porcentaje de pacientes diabéticos que están bien controlados es menor. Entre más estricto y más exigente, menos pacientes diabéticos van a estar controlados correctamente. Cuál es la causa/razón principal para no lograr un control glicémico óptimo? − Riesgo de hipoglicemias: la hipoglicemia es una limitante porque hay medicamentos que producen hipoglicemia (todavía no hay un tratamiento ideal, 100% efectivo y libre de efectos adversos. − Poco insight de la enfermedad: no sigue recomendaciones. − El médico no actúa de manera adecuada, no son lo suficientemente activos. − La enfermedad es compleja Historia natural de la enfermedad El diagnóstico de diabetes constituye el tiempo cero, sin embargo, esto no quiere decir que la enfermedad empezó en ese momento, sino la enfermedad ha empezado 10-­‐15 años antes con los mecanismos fisiopatológicos (principalmente aumento de la resistencia a la insulina). Sin embargo, en el momento en que se empezó a desarrollar la resistencia a la insulina no se manifiesta con hiperglicemia porque el páncreas tiene capacidad de aumentar la secreción de insulina que compensa esa resistencia. En el momento en que la célula beta pierde esa capacidad de responder y aumentar sus niveles de insulina, es que empieza a aparecer la hiperglicemia. Cuál es el mecanismo fisiopatológico indispensable para que aparezca la hiperglicemia? Es la pérdida de la capacidad de la célula beta para producir insulina. No todos los pacientes obesos con resistencia a la insulina llegan a ser diabéticos porque la célula beta tiene la capacidad de compensar esa resistencia y por esa razón no hace hiperglicemia ü Es una enfermedad crónica ü Es una enfermedad progresiva: el carácter progresivo de la enfermedad está dado porque el deterioro de la célula beta es progresivo y la secreción de insulina se va deteriorando conforme avance el tiempo y va a llegar el momento, en donde el diabético va a necesitar el tratamiento con insulina porque la célula beta se agotó. En un principio, la resistencia a la insulina está generando el mayor componente del problema. Conforme avanza la enfermedad, la lesión de la célula beta es lo que determina la condición del paciente. Extrapolación del estudio UKPDS − Se dice que al momento del diagnóstico de diabetes, se ha perdido más o menos el 50% de la masa de células beta y de la capacidad de secreción de insulina. Etapas-de-la-DM2-en-relación-al-funcionamiento− Conforme va avanzando esa masa dde-las-células-Beta e células va disminuyendo. Pèrdida del 100 50% en 5 años 75 Masa insular: 53% Función IGT célula&beta 50 Hiper& (%) glucemia Masa insular: 24% Post& Diabetes-tipoprandial 2 Diabetes-tipo25 Diabetes-tipofase-I 2 2 fase-II-y-III fase-IV 0 &12 &10 &6 &2 0 2 6 10 14 Años-de-diagnóstico Fuente:-UKPDS Estudio en autopsias − Se midió el volumen de células beta y comparado entre pacientes no diabéticos, pacientes con alteración de la glicemia en ayunas y pacientes ya diabéticos, se ve como el volumen de células beta va disminuyendo. − Esto es igual en pacientes obesos y delgados. Al principio se puede decir que hay un aumento del volumen en los pacientes obesos porque hay una proliferación/efecto compensatorio y conforme va avanzando la enfermedad, la masa de células beta va disminuyendo. Realmente se podrá detener la historia natural de la enfermedad? Se puede hacer algo? UKPDS: pacientes diabéticos tipo II recientemente diagnosticados a los cuales se les sometió a diferentes terapias: terapia convencional (dieta), medicamentos (metformina, sulfonilureas e insulina). Cuando se les daba un tratamiento farmacológico, el paciente mejoraba su control glicémico (se obtuvo ese dato por medio de la hemoglobina glicosilada). Sin embargo, independientemente del tratamiento que recibieran (se les daba una dosis y no se les modificaba a lo largo de todo el proceso), a pesar de que había una mejoría inicial, el aumento de la hemoglobina glicosilada fue progresiva con el tiempo. Por lo menos, el uso de estas terapias no garantiza que la célula beta se va a mantener viable. Eso se ha visto con otro tipo de terapias que aparecieron más adelante, como la rosiglitazona, donde igual hay una pérdida de la capacidad del control de la enfermedad con el tiempo, aunque comparativamente con otros medicamentos, se vio que la velocidad con la que se perdía ese buen control era menor. Cuando sale un nuevo medicamento, se busca que éste, además de un control adecuado de la glicemia, pueda ofrecer algún efecto adicional y la preservación de la célula beta es un elemento valioso. Estudio de prevención de diabetes del DTT − Se tomaron pacientes que tenían intolerancia a carbohidratos y se les sometió a tres ramas diferentes: • Placebo (recomendaciones) • Cambios en los estilos de vida y se les daba un entrenador y se les daba recomendaciones nutricionales con visitas periódicas con gente que le ayudaba • Metformina. − Se les siguió en el tiempo y comparativamente, los pacientes a los que se no se les dio ninguna intervención farmacológica tuvieron menor incidencia de diabetes en comparación 58% menos de progresión y un 31% menos de progresión a diabetes con la metformina. Si se interviene de alguna forma, se ve que hay una disminución en la velocidad de la progresión., por lo tanto, sí hay una posibilidad de afectar la historia natural de la enfermedad. La intervención farmacológica tiene algunos matices: estos pacientes van a tener niveles más bajos de glicemia porque hay un efecto farmacológico y por eso no están evolucionando a la diabetes. Pero esto no se consideraría una prevención, más bien se está enmascarando la progresión de la diabetes por el efecto farmacológico. Estos estudios eran mientras el paciente tomaba el medicamento. Interviniendo al paciente antes del diagnóstico de diabetes, se puede hacer que la enfermedad se retrase en su aparición. En un estudio se usó la troglitazona (medicamento que estuvo en el mercado hasta el año 2000 porque tenía efectos tóxicos a nivel hepático). Cuando se hicieron estudios de prevención, con el uso de este medicamento, la progresión a desarrollar diabetes era menor. Otro estudio con la rosiglitazona: se vio demostrado, pero hay cuestionamientos con el uso de este medicamento por el riesgo del aumento de eventos cardiovasculares por lo cual ha entrado en desuso. La prevención de una enfermedad no es con algo que es igual a con lo que se trata la enfermedad. El concepto de prevención sería utilizar algo mucho mejor y que no sea lo mismo con lo que lo trató. Estudio de Da Qing − Es de la prevención de complicaciones de la diabetes. en estos pacientes se les sometió a cambios intensivos en el estilo de vida por 6 años y luego sólo se terminó el estudio. − A aquellos pacientes que estuvieron en la rama de mayores cambios en el estilo de vida, comparados a aquellos que no hicieron el mismo cambio, a través del tiempo, hubo menos incidencia de retinopatía severa. − El hacer cambios en el peso y hábitos nutricionales, puede dar un beneficio posterior en cuanto a la aparición de retinopatía diabética. ü Entre más temprano se actue, se puede evitar complicaciones a futuro. ü Memoria metabólica: todo lo que uno haga puede quedar "grabado" y que puede dar beneficio o daño a futuro. DCCT: − Pacientes con control de 9.1% de hemoglobina glicosilada vs pacientes con 7.2% de hemoglobina glicosilada. − Al momento que termina el estudio, los pacientes tienden a equipararse. Se ha visto que conforme mejora el control glicémico, las complicaciones crónicas se reducen. Pero si el control glicémico se equipara entre los dos grupos, uno esperaría que la reducción de las complicaciones crónica también se equiparen, pero no fue así. − En los estudios de seguimiento, aquellos pacientes que estuvieron en el grupo de mejor control inicial mantuvieron una menor tasa de complicaciones a futuro a pesar de que su control glicémico se equiparó con el otro grupo. − Mantuvo esa mejoría a pesar de que el control glicémico ya era igual. Entre más temprano uno intervenga en el control glicémico mejor beneficio va a tener a futuro. La recomendación es que cuando uno inicia, debe buscar hacer un control desde un principio, mantenerlo bien controlado y por el mayor tiempo posible. Sin embargo, muchas veces eso no se hace y se actua de forma reactiva. Ej. Se hace alguna intervención, el paciente mejora -­‐-­‐> el paciente vuelve a deteriorarse -­‐-­‐> se hace otra intervención. Lo que se pretende es mas bien un efecto proactivo. En una encuesta en Estados Tratamiento*previo HbA1c*(%)! Unidos de cual era la actitud de un médico en una consulta habitual, se vio que el promedio para que el médico le • Cambios(en(estilo(de(vida 8.6 insistiera en hacer cambios en el estilo de vida era cuando el • Metformina 8.8 paciente tenía una hemoglobina glicosilada en promedio de • Sulfonilurea 9.1 8.6% y para que el médico le iniciara metformina era de 8.8% y • SU(+(metformina 9.6 para que le agregara una sulfonilurea era de 9.1% y una terapia combinada 9.6%. El médico deja que el paciente ande 5,798(pacientes((((((((1994(– 2002 Según NHANES crónicamente mal controlado para iniciar una terapia que mejore el control de la glicemia. Manejo proactivo. Se puede iniciar con cambios en el estilo de vida, pero si yo veo que eso no me está llevando a la meta, se tiene que agregar una nueva terapia con el fin de llevarlo a un control adecuado y mantenerlo ahí la mayor cantidad de tiempo posible. Dato: en Estados Unidos el 39% de los pacientes diabéticos tipo 1 están en control en atención primaria y el 82% de tipo II están en atención primaria. En Costa Rica, los tipo I la gran mayoría se concentran en los servicios de endocrinología porque no son tantos. La mayoría de tipo II van a estar en atención primaria porque son demasiados. Criterios para tamizar por diabetes a adultos sintomáticos (ADA): 2 1. Todo adulto de >20 años con IMC≥25 kg/m con 1 o más factores de riesgo adicionales: -­‐ Sedentarismo -­‐ Familiares de primer grado con DM -­‐ Razas/Etnias con alto riesgo (ej: afroamericanos, latinos) -­‐ Antecedente de parto de bebé macrosómico (> 4 kg o 9 lb) o diagnóstico de diabetes gestacional. -­‐ Hipertensión (≥140/90 mmHg o en tratamiento para la hipertensión) -­‐ Colesterol HDL < 35 mg/dl y/o niveles de triglicéridos > 250 mg/dl -­‐ Mujeres con Síndrome de Ovario Poliquístico -­‐ HbA1C≥5,7%, IGT o IFG en exámenes previos (Exámenes previos en categoría de riesgo). -­‐ Otras condiciones clínicas asociadas con la resistencia a la insulina (por ejemplo: obesidad severa, acantosis nigricans) -­‐ Historia de Enfermedad Cerebro Vascular 2. 3. En ausencia de estos factores de riesgo, iniciar el tamizaje a los 45 años. Si el resultado es normal, repetir cada 3 años o menos según el riesgo del paciente (pacientes con prediabetes examinar cada año). Esto es responsabilidad del médico. Encuesta nacional de factores de riesgo que se hizo en el 2011 por el departamento de epidemiología de la CCSS: se ve que un 16.5% de la población >20 años ya está en la categoría de alteración de la glicemia en ayunas (100-­‐125 mg/dL). Y si se le agrega el 10% de la población que ya es diabética, se está hablando de un 26.5% de la población nacional adulta que tiene algún grado de alteración de hidratos de carbono. Factores que influyen para que tenga DM: − Modificables: o Obesidad o Poca actividad física o Sedentarismo o Bajo estado socioecónomico (condiciones nutricionales, estilos de vida) − No modificables: o Etnia o Historia familiar o Pubertad (condición de riesgo, los pacientes adolescentes que desarrollan DMII) o Bajo peso al nacer (el RCIU hace que el paciente tienda a tener mayor riesgo de DM) o Exposición a diabetes en el útero o Sexo femenino o Diabetes gestacional previa. Fisiopatología Recordar que hasta hace un tiempo, la fisiopatología se resumía en dos mecanismos: − Resistencia de la insulina: resistencia a nivel del tejido adiposo y tejido muscular donde hay una menor captación de glucosa por parte de esos tejidos. En el hígado la resistencia se manifiesta por un aumento de la producción hepática de glucosa. − Pérdida de la secreción de insulina por parte de la célula beta. Actualmente, no es sólo esto, se habla de un octeto ominoso: − Páncreas: pérdida de secreción de insulina por la célula beta. − Secreción de glucagon está alterada: ya no es sólo la célula beta, sino también la célula alfa. Normalmente el glucagon debe suprimirse cuando hay un aumento de la glicemia (post prandial) o cuando hay un aumento de insulina, pero en el paciente diabético no suprime, sino mantiene niveles altos, lo cual es un factor que favorece la hiperglicemia, más que todo la post prandial. − − − − − − Aumento de la producción hepática de glucosa Disminución de la absorción de la glucosa a nivel muscular y el tejido graso Incremento de la lipólisis Efecto a nivel de las incretinas: la pérdida de la función y de los niveles de las incretinas (GLP-­‐1) Aumento de la reabsorción renal de glucosa: ya se tiene un blanco terapéutico. Disfunción de los neurotransmisores a nivel cerebral: menor capacidad de saciedad (lo hace a comer más). La resistencia a la insulina tiene factores géneticos, se nace con una predisposición a tener resistencia a la insulina. Hay muchos genes involucrados en esto. Y luego están los factores ambientales: o Embarazo o Sedentarismo o Calidad y cantidad de alimento (no son los alimentos ricos en carbohidratos, sino en grasas saturadas) o Extremos de la vida (pubertad, adulto mayor) o Tabaquismo o Obesidad (factor más importante): los siguientes son factores asociados a la obesidad: • Inflamatorios: aumento de citoquinas • Producción de hormonas en el tejido adiposo (liponectina) • Aumento de glucagon tiene que ver con mayor resistencia a la insulina. Progresión de deterioro de la célula beta: − Efecto de glucotoxicidad: esto es importante que en los ambientes con mayor concentración de glucosa van a tener un efecto directo e indirecto sobre el agotamiento de la célula beta. Se genera estrés metabólico. El paciente tiene una menor producción de insulina conforme sus niveles de glicemia son mayores. Si se corrige el valor de glicemia, la respuesta se recupera, independientemente de lo que se usa para mejorar la glicemia (dieta, insulina, sulfonilureas) − Mecanismos menos conocidos: infiltración de amiloide en los islotes pancréaticos, infiltrado inflamatorio celular, disregulación por medio de las incretinas. − La secreción de la célula beta es anormal y tempranamente se ve afectada en el paciente diabético. Uno de los mecanismo fisiopatológicos más temprano es la pérdida del primer pico de la secreción de insulina que se da ante un estímulo. Ej: es común ver pacientes que debutan con su diabetes con un estado hiperosmolar, con hiperglicemias muy severas, con hemoglobina glicosilada muy elevadas -­‐-­‐> ese paciente probablemente ya no tiene secreción de insulina, pero a ese paciente se le inicia insulina, va mejorando, va bajando sus glicemias y conforme va mejorando, hay que disminuirle la dosis de insulina. Después de seis meses, el paciente está controlado sólo con dieta. El paciente aún tiene secreción de insulina, sólo que al principio estaba muy tóxico y por eso andaba con glicemias muy elevadas. Estudio que demuestra el efecto de toxicidad: − Fueron más de 380 pacientes recién diagnosticados como diabéticos y se dividieron en varios grupos, a unos se les puso con una bomba de insulina, a otros se les puso con inyecciones múltiples de insulina y otros con hipoglicemiantes orales. − El objetivo era que en dos semanas independientemente del tratamiento, que estuvieran euglicémicos. Diagnosticados -­‐-­‐> debutan -­‐-­‐-­‐> tratamiento -­‐-­‐> en dos semanas están euglicémicos. − Luego de esas dos semanas, a los pacientes se les quitaba totalmente el tratamiento y simplemente se seguían en el tiempo. − Se ve que al año, un 26% de los pacientes que habían sido llevado a normoglicemia con hipoglicemiantes orales, se mantenían con un buen control de la diabetes. − Un 45% de los que estaban con inyecciones múltiples de insulina, se mantenían euglicémicos. − Un 51% de los que se les había dado una bomab de insulina, se mantenían bien controlados. − Estos pacientes conservaron la funcionalidad de su célula beta entre más agresivo fuera el control de la enfermedad desde el principio. El controlar la enfermedad desde un inicio, da mayor probabilidad de que la enfermedad progrese menos rápido. Características de la secreción de glucagon en personas normales: − La glicemia después de una ingesta va a tener una elevación, posteriormente se va a normalizar. La insulina se va a secretar muy cercanamente al aumento de la glicemia y se ve que el glucagon debe suprimirse conforme aumenta la insulina y la glicemia. − En el paciente diabético tipo II, hay un aumento de la glicemia mayor, disminución en la secreción de insulina y el glucagon en vez de suprimirse, más bien tiene un aumento pardójico. Esto influye negativamente en la hiperglicemia post prandial. Cuando se logra suprimir los niveles de glucagon, también se va a lograr disminuir los niveles de glicemia. La intervención terapéutica con las incretinas tiene un efecto adicional de no sólo aumentar la secreción de insulina por parte de la célula beta, sino ayudar a disminuir la secreción de glucagon por parte de la célula alfa. Recordar el efecto incretina: − Ante un estímulo, elevación de la glicemia dado por un estímulo oral vs un estímulo intravenoso de glucosa, la secreción de insulina va a ser mayor cuando el estímulo es vía oral, esto es dado por el efecto de las incretinas. − En el paciente diabético, ese efecto incretina está disminuido. − En la diabetes, los niveles de GLP1 van a estar disminuidos y si se actúa sobre este, se va a tener una mayor respuesta. Hay otras manifestaciones fisiopatológicas con esa pérdida de capacidad de la célula beta como es: − Depósito de amiloide (Alzheimer de la célula beta) en la célula beta que deteriora su funcionalidad con el tiempo. − Hay infiltrado inflamatorio de tipo celular que se ha visto que puede ser el responsable de la pérdida de secreción de insulina. No está bien establecido que es lo que lleva a este componente inflamatorio. Es un infiltrado de macrófagos, por tinciones especiales se ven en los islotes pancreáticos. Conclusión: Es una enfermedad progresiva que si la abordamos y la tratamos tempranamente, el riesgo de que la enfermedad progrese es menor y por lo tanto es menor el riesgo de complicaciones. Se tienen que pensar en todos los mecanismos fisiopatológicos que los pacientes puede que no se controlen con una sola cosa, sino puede ser necesario el utilizar varios fármacos a la vez.