Tema 2.-Los glúcidos
Anuncio

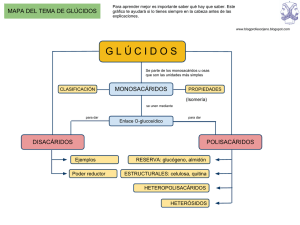
Tema 2.-Los glúcidos Los glúcidos son biomoléculas orgánicas. Están formados por Carbono, Hidrógeno y Oxígeno, aunque además, en algunos compuestos también podemos encontrar Nitrógeno y Fósforo. Reciben también el nombre de azúcares, carbohidratos o hidratos de carbono. Los glúcidos pueden definirse como polihidroxicetonas o polihidroxialdehídos. La importancia biológica principal de este tipo de moléculas es que actúan como reserva de energía o pueden conferir estructura, tanto a nivel molecular (forman nucleótidos), como a nivel celular (pared vegetal) o tisular (tejidos vegetales de sostén, con celulosa). Dependiendo de la molécula que se trate, los Glúcidos pueden servir como: Combustible: los monosacáridos se pueden oxidar totalmente, obteniendo unas 4 KCal/g. Reserva energética: el almidón y el glucógeno son polisacáridos que acumulan gran cantidad de energía en su estructura, por lo que sirven para guardar energía excedente y utilizarla en momentos de necesidad. Formadores de estructuras: la celulosa o la quitina son ejemplos de polisacáridos que otorgan estructura resistente al organismo que las posee. CLASIFICACIÓN DE LOS GLÚCIDOS Monosacáridos u osas Triosas Tetrosas Pentosas Hexosas Heptosas Aldosas Cetosas Oligosacáridos Ósidos Holósidos Polisacáridos Disacáridos, trisacáridos... Homopolisacáridos Heteropolisacáridos Heterósidos Los glúcidos se clasifican según el número de átomos de carbono que contengan. Se distinguen los siguientes tipos: Osas o monosacáddos. Son glúcidos de tres a ocho átomos de carbono. Ósidos. Son los glúcidos formados por la asociación de monosacáridos. Holósidos. Son ósidos formados exclusivamente por monosacáridos. Heterósidos. Son ósidos formados por monosacáridos y otras sustancias no glucídicas. Oligosacáridos. Son holósidos formadús por la unión de dos a diez monosacáridos. Los únicos que tienen interés son los disacáridos y los trisac~ridos. Polisacáridos. Son los glúcidos formados por la unión de más de diez monosacáridos. Se distinguen los homopolisacáridos, si 'sólo se repite un tipo de monosacáridos, y los heteropolisacáridos, si se repiten dos o más tipos de monosacáridos. LOS MONOSACÁRIDOS Los monosacáridos son sustancias blancas, con sabor dulce, cristalizables y solubles en agua. Se oxidan fácilmente, transformándose en ácidos, por lo que se dice que poseen poder reductor (cuando ellos se oxidan, reducen a otra molécula). Los monosacáridos son moléculas sencillas que responden a la fórmula general (CH2O)n. Están formados por 3, 4, 5, 6 ó 7 átomos de carbono. Químicamente son polialcoholes, es decir, cadenas de carbono con un grupo -OH cada carbono, en los que un carbono forma un grupo aldehído o un grupo cetona. Se clasifican atendiendo al grupo funcional (aldehído o cetona) en aldosas, con grupo aldehído, y cetosas, con grupo cetónico. Cuando aparecen carbonos asimétricos, presentan distintos tipos de isomería. . La isomería es una característica que aparece en aquellas moléculas que tienen la misma fórmula empírica, pero presentan características físicas o químicas que las hacen diferentes. A estas moléculas se las denomina isómeros. En los monosacáridos podemos encontrar isomería de función, isomería espacial e isomería óptica. Isomería de función Los isómeros se distinguen por tener distintos grupos funcionales. Las aldosas son isómeros de las cetosas. Isomería espacial Los isómeros espaciales, o estereoisómeros, se producen cuando la molécula presenta uno o más carbonos asimétricos. Los radicales unidos a estos carbonos pueden disponerse en el espacio en distintas posiciones. Cuantos más carbonos asimétricos tenga la molécula, más tipos de isomería se presentan. El carbono asimétrico más alejado del grupo funcional sirve como referencia para nombrar la isomería de una molécula. Cuando el grupo alcohol de este carbono se encuentra representado a su derecha en la proyección lineal se dice que esa molécula es D. Cuando el grupo alcohol de este carbono se encuentra representado a su izquierda en la proyección lineal se dice que esa molécula es L. Los isómeros especulares, llamados también enantiómeros, o enantiomorfos, o isómeros quirales, son moléculas que tienen los grupos -OH de todos los carbonos asimétricos, en posición opuesta, reflejo de la otra molécula isómera. Se consideran epímeros a las moléculas isómeras que se diferencian en la posición de un único -OH en un carbono asimétrico. Isomería óptica Cuando se hace incidir un plano de luz polarizada sobre una disolución de monosacáridos que poseen carbonos asimétricos el plano de luz se desvía. Si la desviación se produce hacia la derecha se dice que el isómero es dextrógiro y se representa con el signo (+). Si la desviación es hacia la izquierda se dice que el isómero es levógiro y se representa con el signo ( - ). Los monosacáridos se nombran atendiendo al número de carbonos que presenta la molécula: Triosas: tres carbonos Tetrosas: cuatro carbonos Pentosas: cinco carbonos Hexosas: seis carbonos Heptosas: siete carbonos Ejemplos de monosacáridos relevantes en el metabolismo son la glucosa, la fructosa, la ribosa o la desoxirribosa, entre otros muchos. Propiedades físicas. Son sólidos cristalinos, blancos, hidrosolubles y de sabor dulce. Su solubilidad en agua se debe a que tanto los radicales hidroxilo (- OH) como los radicales de hidrógeno (- H) presentan una elevada polaridad eléctrica y establecen por ello fuerzas de unión electrostática 'con las moléculas de agua, que también son polares, dispensándose así las moléculas del glúcido. Propiedades químicas. En primer lugar, recordar que una sustancia se reduce cuando gana electrones y se oxida cuando los pierde. Ciclación En disolución, los monosacáridos pequeños se encuentran en forma lineal, mientras que las moléculas más grandes ciclan su estructura. La estructura lineal recibe el nombre de Proyección de Fischer; la estructura ciclada de Proyección de Haworth. En la representación de Haworth la cadena carbonada se cicla situada sobre un plano. Los radicales de la cadena se encuentran por encima o por debajo de ese plano. La estructura ciclada se consigue en aldopentosas y hexosas. El enlace de ciclación se genera entre el carbono que posee el grupo funcional y el carbono asimétrico más alejado del grupo funcional. Cuando el carbono tiene un grupo aldehído, como grupo funcional, el enlace recibe el nombre de hemiacetálico. Cuando el carbono tiene un grupo cetona, como grupo funcional, el enlace recibe el nombre de hemicetálico. La molécula ciclada puede adquirir el aspecto de un pentágono o de un hexágono. Los monosacáridos ciclados con aspecto de pentágono reciben el nombre de Furanosas. Los monosacáridos ciclados con aspecto de hexágono reciben el nombre de Piranosas. Ciclación: 1.- Todos los carbonos se situan en un mismo plano horizontal. 2.- La estructura abierta se repliega sobre sí misma, aproximándose los carbonos extremos, y se produce un giro de los radicales del carbono 5. 3.- De esta forma quedan enfrentados el grupo alcohólico del carbono 5 con los radicales del carbono 1. 4.- El carbono 1 se hidrata y a continuación se combina el grupo alcohólico del carbono 1 con el carbono 5, desprendiéndose una molécula de agua. Se forma así un ciclo hexagonal mediante un átomo de oxígeno entre el carbono 1 y el 5. La D+ glucopiranosa tiene un valor de rotación del plano de polarización de +122,2º y la D glucopiranosa de +18,7º. Cuando se disuelve uno u otro de estos isómeros o una mezcla al azar de ambos, parte de uno se transforma en el otro isómero y se llega a un estado de equilibrio, quedando una molécula del anómero por cada dos del anómero . A este cambio gradual del poder de rotación, al disolverse las moléculas, se denomina mutarrotación. En la disolución siempre hay equilibrio éntrela forma cíclica y la forma abierta, en la glucosa la estructura lineal nunca llega al 5 por 100 del total. La ciclación puede adoptar también la estructura pentagonal del furano, como por ejemplo en la ribosa, fructosa.. Las estructuras cíclicas de la glucosa no son planas, sino que pueden adoptar dos conformaciones en el espacio , la conformación de nave y la conformación de silla , ello se debe a que los enlaces se orientan en el espacio y no en un plano. http://upload.wikimedia.org/wikipedia/commons/a/af/Glucose_Fisher_to_Haworth.gif?uselang=es Los enlaces N-glucosídico y O-glucosídico Hay dos tipos de enlace entre los monosacáridos y otras moléculas: el enlace N-glucosídico (fig. 8), entre un -OH y un compuesto aminado, y el enlace O-glucosídico (fig. 9), entre dos -OH de dos monosacáridos. Mediante el enlace N -glucosídico se forman aminoazúcares. El enlace O-glucosídico es a-glucosídico si el primer monosacárido es a, y P-glucosídico si el primer monosacárido es p. ÓSIDOS Los Ósidos son Glúcidos formados por varios monosacáridos. La unión de monosacáridos se realiza a través de un enlace especial que libera una molécula de agua y que se llama enlace O-glucosídico, ya que un monosacárido se une al siguiente a través de un Oxígeno. Se llaman Holósidos a los ósidos formados por varios monosacáridos. Se denominan Heterósidos a los ósidos formados por monosacáridos y otras moléculas distintas a los Glúcidos, como pueden ser lípidos, que forman glucolípidos, o prótidos, que pueden formar glucoproteínas, entre otros. Los Holósidos se clasifican en Oligosacáridos y en Polisacáridos. Oligosacáridos Los oligosacáridos son Glúcidos formados por un número pequeño de monosacáridos, entre 2 y 10. Se denominan Disacáridos, si están compuestos por dos monosacáridos, Trisacáridos, si están compuestos por tres monosacáridos, Tetrasacáridos, si están compuestos por cuatro monosacáridos y así sucesivamente. Los disacáridos se forman por la unión de dos monosacáridos, mediante un enlace O-glucosídico. El enlace se forma entre el carbono que forma el enlace hemiacetálico del primer monosacárido y un carbono del segundo monosacárido. Para nombrar el disacárido formado se debe indicar las moléculas que lo constituyen y el número de los carbonos implicados en el enlace. Como el nombre químico suele ser muy largo, se utiliza más el nombre más común. Maltosa - D-Glucopiranosil -(1→4) - -D-Glucopiranosa Enlace formado por dos glucosas cicladas, con el carbono anomérico en posición . Intervienen en el enlace el carbono 1 de la primera glucosa y el carbono 4 de la segunda. Es un disacárido que no se encuentra libre en la Naturaleza. Se obtiene por digestión de almidón o glucógeno. Posee poder reductor. Es un enlace que contiene mucha energía. Celobiosa -D -Glucopiranosil - (1→4) - -D-Glucopiranosa Enlace formado por dos glucosas cicladas, con el carbono anomérico en posición . Intervienen en el enlace el carbono 1 de la primera glucosa y el carbono 4 de la segunda. Es un disacárido que no se encuentra libre en la Naturaleza. Se obtiene por digestión de celulosa. Posee poder reductor. Isomaltosa -D- Glucopiranosil -(1→´6) --D-Glucopiranosa Enlace formado por dos glucosas cicladas, con el carbono anomérico en posición . Intervienen en el enlace el carbono 1 de la primera glucosa y el carbono 6 de la segunda. Es un disacárido que no se encuentra libre en la Naturaleza. Se obtiene por digestión de almidón o glucógeno. Forma los puntos de ramificación de estas moléculas. Posee poder reductor. Lactosa -D -Galactopiranosil -(1→4)- -D-Glucopiranosa Enlace formado por una galactosa y una glucosa, ambas cicladas, con el carbono anomérico en posición . Intervienen en el enlace el carbono 1 de la galactosa y el carbono 4 de la glucosa. Es un disacárido que se encuentra libre en la Naturaleza. Es el azúcar que posee la leche. Posee poder reductor. Sacarosa -D- Glucopiranosil - (1→2) --D –Fructofuranósido Enlace formado por una glucosa ciclada, con el carbono anomérico en posición , y una fructosa ciclada, con el carbono anomérico en posición . Intervienen en el enlace el carbono 1 de la primera glucosa y el carbono 2 de la fructosa. Es un disacárido que se encuentra libre en la Naturaleza. Se obtiene de la caña de azúcar y de la remolacha. Es el azúcar común. No posee poder reductor. Es debido a que no tiene ningún carbono anomérico libre. El carbono anomérico de la glucosa es el carbono 1 y el carbono anomérico de la fructosa es el carbono 2. Ambos están formando el enlace glucosídico, por lo que no pueden intervenir en la reacción Fehling. La terminación -ósido hace referencia a que no tiene ese carácter reductor. Polisacáridos Los polisacáridos son polímeros de monosacáridos, unidos mediante enlace O-glucosídico. Cuando los monosacáridos que forman la molécula son todos iguales, el polisacárido formado se llama Homopolisacárido. Cuando los monosacáridos que forman la molécula son distintos entre sí, es decir, de más de un tipo, el polisacárido formado se llama heteropolisacárido. Los polisacáridos no tienen sabor dulce, no cristalizan y no tienen poder reductor. Su importancia biológica reside en que pueden servir como reservas energéticas o pueden conferir estructura al ser vivo que los tiene. La función que cumplan vendrá determinada por el tipo de enlace que se establezca entre los monosacáridos formadores. Los polisacáridos más abundantes en la Naturaleza son el almidón, el glucógeno, la celulosa y la quitina. Almidón Aparece en células vegetales. Es un homopolísacárido con función de reserva energética, formado por dos moléculas, que son polímeros de glucosa, la amilosa y la amilopectina. La amilosa está formada por glucosas unidas por enlace (1→4). La amilopectina está formada por glucosas unidas por enlaces (1→4) y (1→6). Estos enlaces (1→6) originan ramificaciones, que se repiten en intervalos de secuencias desiguales de monosacáridos. La amilosa adquiere una estructura helicoidal y la amilopectina recubre a la amilosa. En su digestión intervienen dos enzimas: -amilasa (rompe enlaces 1-4) y la (1,6) glucosidasa para romper las ramificaciones. Al final del proceso se libera glucosa. Glucógeno Es un homopolisacárido con función de reserva energética que aparece en animales y hongos. Se acumula en el tejido muscular esquelético y en el hígado. Está formado por glucosas unidas por enlace (1→4) y presenta ramificaciones formadas por enlaces (1→6). Es un polisacárido de reserva en animales, que se encuentra en el hígado (10%) y músculos (2%). Presenta ramificaciones cada 8-12 glucosas con una cadena muy larga (hasta 300.000 glucosas). Se requieren dos enzimas para su hidrólisis (glucógeno-fosforilasa) y (1-6) glucosidasa, dando lugar a unidades de glucosa. Dado que los seres vivos requieren un aporte constante de energía, una parte importante del metabolismo de los azúcares está relacionado con los procesos de formación de almidón y glucógeno y su posterior degradación. Celulosa Es un homopolisacárido formado por glucosas unidas por enlace (1→4). Es típico de paredes celulares vegetales, aunque también la pueden tener otros seres, incluso animales. Su importancia biológica reside en que otorga resistencia y dureza. Confiere estructura al tejido que la contiene. Las cadenas de celulosa se unen entre sí, mediante puentes de Hidrógeno, formando fibras más complejas y más resistentes. Quitina Es un homopolisacárido con función estructural, formado por la unión de N-acetil--D-glucosaminas. Se encuentra en exoesqueletos de artrópodos y otros seres, ya que ofrece gran resistencia y dureza. Heteropolisacárido. Por hidrólisis dan lugar a varios tipos distintos de monosacáridos o de derivados de estos. La mayoría se encuentran formando parte de la pared bacteriana, celulósica de los vegetales o de la matriz extracelular de la animales. Pectina. Es un heteropolisacárido con enlace . Junto con la celulosa forma parte de la pared vegetal. Se utiliza como gelificante en industria alimentaría (mermeladas). Agar-Agar. Es un heteropolisacárido con enlace . Se extrae de algas rojas o rodofíceas. Se utiliza en microbiología para cultivos y en la industria alimentaria como espesante. En las etiquetas de productos alimenticios lo puedes encontrar con el código E-406. Glúcidos asociados a otras moléculas Proteoglucanos. Gran fracción de polisacáridos y una pequeña(20%) de proteínas Ej: acido hialurónico forman la matriz del conjuntivo, cartilaginoso y óseo.Heparina. Peptidoglucanos: Pared bacteriana. Nacetil glucosamina y Nacetil murámico Nacetil murámico Nacetil glucosamina Glucoproteínas. Pocos glúcidos y muchas proteínas. Mucinas de secreción, protrombina, inmunoglobulinas y glucoproteínas. Glucolípidos Cerebrósidos y gangliósidos.Lípidos FUNCIONES DE LOS GLÚCIDOS. Energética. Glucosa, almidón, glucógeno. Estructuralenlace como celulosa, quitina, ribosa y desoxirribosa en ácidos nucleicos… Especificidad de la membrana8glucoproteínas regulan el paso de sustancias por la membrana) Antibiótico como la estreptomicina, vitamina C, anticoagulante como heparina, hormonal, inmunológica Principios activos de plantas medicinales(cardiotónicos como la digitalina….)