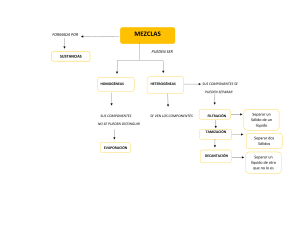
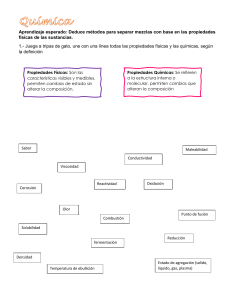
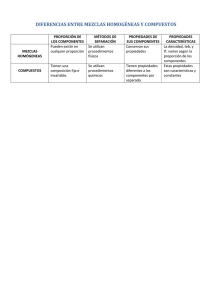
1 UNIVERSIDAD NACIONAL AGRARIA DE LA SELVA FACULTA EN INGENIERIA DE INDUSTRIAS ALIMENTARIAS IMFORME DE LABORATORIO SEPARCION DE LOS COMPONENTES DE UNA MEZCLA DOCENTE: Blass Matienzo Jose Antonio CURSO: Química General CICLO ACADEMICO: I ciclo ESTUDIANTE: Nayeli Lozano Arostegui CODIGO DE ESTUDIANTE: 0020220669 TINGO MARIA 2022 2 I. INDICE INTRODUCCION ...................................................................................................... 3 1. OBJETIVOS GENERALES ................................................................................... 3 2. OBEJTIVOS RELATIVOS ..................................................................................... 3 II. MARCO TEORICO ................................................................................................... 4 1. Sustancias: ............................................................................................................ 4 1.1 elemento: ........................................................................................................ 4 1.2 compuesto: ..................................................................................................... 4 2. Mezclas: ................................................................................................................ 4 2.1 mezcla homogénea:........................................................................................ 4 2.2 mezcla heterogénea: ...................................................................................... 4 1. Método Físicos ...................................................................................................... 5 III. PROCEDIMIENTO EXPERIMENTAL ...................................................................... 5 1. Practica n°2: separación de los componentes de una mezcla .............................. 5 v. RESULTADOS............................................................................................................ 8 IV. CONCLUSIONES ..................................................................................................... 8 V. BIBLIOGRAFIA ........................................................................................................ 8 3 I. INTRODUCCION En la naturaleza las sustancias puras se encuentran mezcladas en pequeñas impurezas que en ciertas ocasiones se necesita eliminar mediante técnicas de separación y purificación. En este informe nos enfocaremos en la separación de mezclas mediante técnicas como: filtración, dilución y extracción. Todo esto será usado en la separación de una mezcla, una mezcla se separa mediante métodos físicos aprovechando las características de los componentes para mantener la composición de la mezcla. 1. OBJETIVOS GENERALES Conocer los tipos de separación de mezclas. Identificar los métodos de la separación apropiados para una mezcla. Experimentar los métodos de separación más comunes. Separar una mezcla en estado sólido. 2. OBEJTIVOS RELATIVOS Elaborar un diagrama de flujo del proceso experimental realizado en el laboratorio de la separación de la mezcla. 4 II. MARCO TEORICO 1. Sustancias: Es aquella sustancia química que posee una composición fija y esta químicamente definida. 1.1 elemento: Llega a ser las sustancias puras que no pueden descomponerse en sustancias más simples mediante cambios químicos. 1.2 compuesto: Son las sustancias puras que pueden descomponerse mediante cambios químicos. 2. Mezclas: Una mezcla se compone de dos o más tipos de materia que pueden estar presentes en cantidades variables y pueden separarse mediante cambios físicos. 2.1 mezcla homogénea: Es una composición uniforme que aparece visualmente igual en todas partes. 2.2 mezcla heterogénea: Es aquella mezcla cuya composición varía de un punto a otro. 5 1. Método Físicos Son aquellos métodos de separación donde no existe un cambio de en la composición de la sustancia en los métodos físico tenemos: Filtración: Disolución: Extracción: Evaporación: III. PROCEDIMIENTO EXPERIMENTAL 25/ 08/ 2022 1. Practica n°2: separación de los componentes de una mezcla Problema: Materiales y reactivos embudo de vidrio vaso precipitado tetracloruro NaCl I2 6 Separar cuantitativamente cloruro de sodio, yodo y dióxido de carbono de silicio de una mescla sólida. NaCl: solido cristalino incoloro, soluble al agua y con punto de fusión de 801 c°. I2 : solido cristalino Morado oscuro, poco soluble en agua. Sublima entre 50c° y 100 c.° 𝑆𝑆𝑆𝑆𝑆𝑆2 : solido cristalino incoloro, muy poco soluble en agua y con punto de fusión en 1713C.° Diagrama de flujo NaCl, I2 , 𝑆𝑆𝑆𝑆𝑆𝑆2 H2O acuosa Disolución f. solida 𝑆𝑆𝑆𝑆𝑆𝑆2 Filtración Añadimos tetracloruro f. NaCl, I2 , Extracción 7 Procedimiento: A la mezcla solida que se encuentra en la caja de Petri la disolvimos con agua • Luego en un embudo de vidrio con papel de filtro filtramos la mezcla que • disolvimos para separar NaCl, I2 de 𝑆𝑆𝑆𝑆𝑆𝑆2 Una vez separado aplicamos la extracción en el NaCl y añadimos tetracloruro • I2 para ello En el embudo de decantación agitamos por 2 minutos la mezcla para que expulse sus gases. • Después de ello volvemos a agitar por 4 minutos en este proceso la mezcla que disolvimos se torna rosada esto debido al tetracloruro de carbono con el yodo, lo dejamos abierto por 15 minutos luego con el embudo de decantación separamos el yodo de cloruro de carbono. 8 v. RESULTADOS Los resultados obtenidos en la practica nos muestra como es posible separar mezclas mediante métodos físicos, en la práctica se observa claramente el proceso de separación de una sal, un oxido y un no metal mediante los métodos de separación usados. IV. CONCLUSIONES En conclusión, los sólidos al igual que toda mezcla pueden ser separados mediante métodos físicos y para realizar una correcta dilución siempre necesitaremos de agua ya que esta actúa como solvente universal. Además, La filtración permite que se pueda separar la sustancia en una fase acuosa y una fase solida esto debido a un proceso anterior que conocemos como dilución. Por ello los métodos físicos son importantes para la separación de mezclas sólidas. V. BIBLIOGRAFIA [En línea]. - https://www.google.com/search?. [En línea]. - https://ikastaroak.birt.eus/.