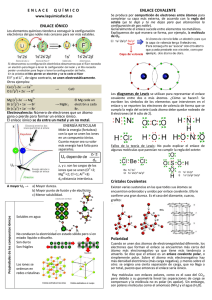
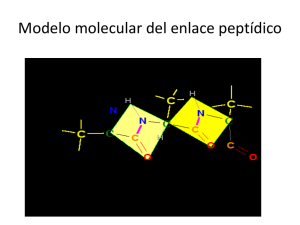
¿Que son las fuerzas intermoleculares? Las fuerzas intermoleculares se definen como el conjunto de fuerzas atractivas y repulsivas que se producen entre las moléculas como consecuencia de la presencia o ausencia de electrones. Cuando dos o más átomos se unen mediante un enlace químico forman una molécula, los electrones que conforman la nueva molécula recorren y se concentran en la zona del átomo con mayor electronegatividad, definimos la electronegatividad como la propiedad que tienen los átomos en atraer electrones. La concentración de electrones en una zona específica de la molécula crea una carga negativa, mientras que la ausencia de los electrones crea una carga positiva. Denominamos dipolos a las moléculas que disponen de zonas cargadas negativamente y positivamente debido a la electronegatividad y concentración de los electrones en las moléculas. Podemos asimilar el funcionamiento de un dipolo a un imán con su polo positivo y su polo negativo, de tal forma que si acercamos otro imán el polo positivo atraerá al polo negativo y viceversa, dando como resultado una unión. Las fuerzas intermoleculares que actúan entre las moléculas se clasifican en : Dipolos permanentes Dipolos inducidos Dipolos dispersos. Puentes de hidrógeno Dentro de los 4 grupos descritos anteriormente, las fuerzas más relevantes son las 3 primeras también conocidas como fuerzas de Van der Waals. Dipolos permanentes Este tipo de unión se produce cuando ambas moléculas disponen de cargas positivas y negativas, es decir son moléculas polares o que tienen polaridad, atrayéndose electrostaticamente y formando la unión. Dipolos inducidos Este tipo de unión se produce cuando una molécula no polar redistribuye la concentración de los electrones (tiene la posibilidad de polarizarse) al acercarse una molécula polar, de tal forma que se crea una unión entre ambas moléculas. En este caso la molécula polar induce la creación de la molécula apolar en una molécula polar. Dipolos dispersos Este último caso la unión se produce entre moléculas no polares pero que pueden polarizarse, y cuando esto último ocurren se atraen mutuamente creando la unión molecular. La unión que se crea en este tipo de dipolos tiene una intensidad muy débil y una vida muy corta Las energías de unión generadas por las fuerzas intermoleculares son muy inferiores a las energías generadas en los enlaces químicos, pero a nivel global son superiores en número a estas últimas desempeñando un paple vital tanto en las propiedades de adhesión como de cohesión del adhesivo. Van der Waals ------ 0,1 a 10 Kj/mol Enlace Covalente ------ 250 – 400 Kj/mol. En la siguiente tabla se encuentra una comparativa entre las propiedades de las fuerzas intermoleculares y los enlaces químicos: Fuerzas intermoleculares: Son muy dependientes de la Enlaces Quimicos: temperatura, un aumento de temperatura produce un decremento de las fuerzas intermoleculares. Son mas débiles que los enlaces químicos, del orden de 100 veces menor No son tan dependientes de la temperatura Son más fuertes que las fuerzas intermoleculares La distancia de unión es muy pequeña, a nivel de Amstrongs La distancia de unión es a nivel de micras Las uniones no están direccionadas. Las uniones están direccionados. Con todo esto, dentro de un material adhesivo como es un polímero, nos encontramos con uniones químicas entre átomos que forman moléculas y fuerzas intermoleculares entre las propias moléculas de los polímeros. El conjunto de estos enlaces, uniones y fuerzas son las responsables de las propiedades adhesivas y cohesivas de los pegamentos, adhesivos y sellantes.