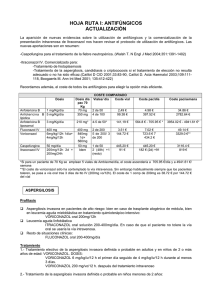
GRUPO TERAPÉUTICO
Anuncio

VORICONAZOL V FEND (Pfizer) GRUPO TERAPÉUTICO - Grupo anatómico: (J) TERAPIA ANTIINFECCIOSA, USO SISTÉMICO. - Grupo específico: J02AC. ANTIMICÓTICOS, USO SISTÉMICO. Triazoles. INDICACIÓN AUTORIZADA Aspergilosis invasiva, infecciones invasivas graves por Candida (incluyendo C krusei) resistentes a fluconazol, infecciones fúngicas graves por Scedosporium spp y Fusarium spp. ANTECEDENTES Las infecciones provocadas por hongos presentan importantes diferencias con las de origen bacteriano. Quizás una de las más importantes, por las consecuencias terapéuticas que tiene, es el hecho de que los hongos son células eucariotas, mientras que las bacterias son procariotas. Esto significa que las células fúngicas son más evolucionadas, más complejas y, en definitiva, mucho más parecidas a las células humanas. Esto implica, en última instancia, que los medicamentos activos sobre los hongos con capacidad patógena para el ser humano deben actuar mediante mecanismos bioquímicos basados en las pocas diferencias existentes entre las células fúngicas y las humanas. Precisamente, una de las más importantes peculiaridades de los hongos es su pleomorfismo; es decir, la diversidad morfológica para una misma especie. Este particularidad es observada, de hecho, en alguna de las especies más patógenas para el ser humano. En este sentido, entre las manifestaciones pleomórficas más comunes de los hongos podemos encontrar a las levaduras, consistentes en células aisladas aplanadas y redondeadas, y las hifas, constituidas por estructuras pluricelulares filamentosas que forman agregados con apariencia de tejido deshilachado, que suele ser la forma más patogénica. También pueden encontrarse pseudohifas, formadas por células aisladas con aspecto de hifas, esférulas consistentes en células aisladas con forma esférica, que frecuentemente son una forma de resistencia ante entornos biológicos poco favorables. Por último, también existen formas mixtas de levadura e hifa. Afortunadamente, la mayor parte de las infecciones provocadas por hongos en el ser humano tienen un carácter superficial (epidérmico), siendo las más comunes las producidas por dermatofitos (tiñas) y levaduras (candiadiasis superficiales y pitiriasis, entre otras). En las micosis profundas, la mayoría de las especies patógenas de hongos capaces de producir infecciones sistémicas actúan como patógenos oportunistas. Habitualmente son inhalados con el aire y son eliminados, en condiciones fisiológicas normales, por el sistema inmunológico, a través de mecanismos celulares (fagocitos). La diseminación de la infección puede producirse casi exclusivamente en pacientes inmunodeprimidos (tratamientos inmunosupresores, sida, etc). La mayoría de las micosis profundas tienen localizaciones pulmonares, ya que la vía inhalatoria es una de las más comunes. Sin embargo, muchas de ellas también tienen otras localizaciones sistémicas (esófago, riñón, corazón, sistema nervioso central, hígado, bazo, etc), así como formas diseminadas (septicemia). Dentro de su relativa rareza, las micosis profundas más relevantes son las aspergilosis, producida generalmente por Aspergillus fumigatus y, con menor frecuencia, por otras especies de Aspergillus; las candidiasis sistémicas, provocadas casi exclusivamente por Candida albicans, y la criptococosis, inducida por Cryptococcus neoformans. Esta última puede ser asintomática en algunas personas, aunque su forma más grave es la meningitis, uno de los problemas más complejos de solucionar en pacientes con sida. En otras zonas del mundo, especialmente en zonas tropicales, están presentes otros tipos de micosis profundas, como la blastomicosis (Blastomyces dermatitidis), la histoplasmosis (Histoplasma capsulatum), la ficomicosis (Basidiobolus spp. o Mucor spp.), la coccidiodomicosis (Coccidioides immitis), la paracoccidiomicosis (Paracoccidioides brasiliensis), o la esporotricosis (Sporothrix schenckii). Este tipo de infecciones son excepcionalmente infrecuentes en España. Los hongos del género Aspergillus están entre los más comunes del medio ambiente, apareciendo con frecuencia en vegetales en descomposición, materiales utilizados como aislantes en paredes o techos alrededor de vigas, en conducciones de aire acondicionado o de calefacción, así como en quirófanos y habitaciones de hospitales, utensilios hospitalarios y polvo transportado por el aire. La mayoría de las aspergilosis producidas en seres humanos son originadas por Aspergillus fumigatus y, con bastante menos frecuencia, por A. flavus, A. niger, A. nidulans y A. terreus. Es común el desarrollo de epidemias de origen hospitalario en unidades de pacientes inmunodeprimidos, con frecuencia coincidiendo con la realización de obras de construcción en el hospital o zonas adyacentes a éste. El motivo es el aumento de la concentración de esporas de Aspergillus en el aire. El hecho de que Aspergillus fumigatus sea son termófilo facilita su reproducción en los filtros de aire acondicionado, desde donde se distribuyen activamente. Las aspergilosis invasivas se suelen producir en pacientes susceptibles por inhalación de conidias o, en ocasiones, por invasión directa de la piel dañada. La inhalación de las formas de transporte aéreo, conidias, es seguida de la proliferación de hifas, que acaban invadiendo los vasos sanguíneos, provocando necrosis hemorrágica, infarto y hace posible la diseminación a otros órganos en pacientes en los que su sistema inmunológico no responde adecuadamente. Sin embargo, las aspergilosis presenten un amplio espectro de patogenias, que incluye mecanismos de tipo no infecciosos, como la aspergilosis broncopulmonar alérgica, una entidad rara que observada en individuos atópicos. Entre los principales factores de riesgo asociados a la aspergilosis pueden citarse la neutropenia, el empleo crónico o prolongado de dosis altas de corticosteroides, el trasplante de órganos (muy especialmente el de médula ósea), las patologías inmunosupresoras congénitas o adquiridas, como el SIDA. La aspergilosis invasiva superficial primaria es infrecuente, pero puede aparecer en quemaduras, bajo apósitos oclusivos, con posterioridad a una queratitis o un traumatismo corneal, así como en los senos paranasales, la propia nariz o el conducto auditivo. Puede producirse una colonización no invasiva o mínimamente invasiva del aparato respiratorio, en lesiones cavitarias pulmonares previas, con formación de una bola de hongos o aspergiloma. Este supone un crecimiento de tipo saprofítico y no invasivo de masas de hifas conjuntamente con exudado y algunas células inflamatorias, generalmente encapsulado por tejido fibroso. Por su parte, la aspergilosis pulmonar invasiva suele progresar con rapidez, hasta provocar insuficiencia respiratoria progresiva, en último término fatal, a menos que se administre tratamiento pronto e intensivo. A. fumigatus es el agente causal más común. La aspergilosis diseminada puede afectar al hígado, los riñones, el encéfalo u otros tejidos y suele ser mortal. Debido al notable incremento del número de procedimientos quirúrgicos de trasplante de órganos y de médula ósea, de terapias anticancerosas, así como de cuadros patológicos inmodepresores, muy especialmente el SIDA, la incidencia de micosis sistémicas ha aumento espectacularmente en las dos últimas décadas. En este sentido, Aspergillus constituye el patógeno de tipo fúngico más frecuente, tras Candida, siendo responsable de más del 25% de las infecciones fúngicas. Es importante tener en cuenta que la aspergilosis invasiva es uno de los cuadros infecciosos más difíciles de tratar, con una mortalidad próxima al 90% en los pacientes con mayor índices de inmunodepresión. Hasta ahora, los medicamentos disponibles para el tratamiento de las micosis diseminadas eran los siguientes: - Anfotericina B. Actúa alterando la membrana celular del hongo, por unión al ergosterol, lo que se traduce en un aumento de la permeabilidad, que debilita sus defensas. - Imidazoles (fluconazol, itraconazol, ketoconazol). Interfieren en la síntesis de lípidos de la membrana celular, especialmente del ergosterol. 1 - Flucitosina . Actúa como un análogo de bases pirimidínicas, interfiriendo la síntesis de material genético del hongo. - Caspofungina (recientemente comercializada en España). Es primer miembro del grupo de las equicandinas, actúa inhibiendo selectiva e irriversiblemente el enzima 1,3-ß-Dglucano sintasa, indispensable para la síntesis del 1,3-ß-D-glucano. Este homopolisacárido es un componente esencial para la integridad de la pared celular de la mayoría de los hongos patógenos, pero está ausente de la membrana de las células animales (incluyendo las humanas). El 1,3-ß-D-glucano provee de estabilidad osmótica a la pared celular y su presencia es determinante para el crecimiento y la división celular. El itraconazol es eficaz, pero los resultados son variables y es susceptible de provocar importantes interacciones farmacológicas con otros medicamentos. Por ello, la base del tratamiento sigue siendo la anfotericina, aunque en casos muy graves (p.e. endocarditis) se suele asociar a flucitosina o rifampicina. La caspofungina resulta eficaz clínicamente en pacientes con aspergilosis invasiva refractarios o intolerantes a la anfotericina. Ha demostrado un relativa superioridad frente a la anfotericina en cuadros de candidiasis esofágica. ACCIÓN Y MECANISMO Los antifúngicos azólicos, que forman un amplio grupo de medicamentos, actúan a través de la inhibición de la síntesis de ergosterol, un esterol análogo del colesterol, a partir del lanosterol, y que forma parte esencial de las membranas de los hongos microscópicos. En realidad el propio lanosterol permite formar la membrana fúngica, lo que ocurre es que ésta resulta un tanto anómala, siendo excesivamente permeable al flujo iónico, en especial al de hidrogeniones (H3O+). Esto proporciona a la membrana una gran fragilidad y determina su rápida degradación, lo que ocasiona irremediablemente la lisis de la célula fúngica. La fragilidad que proporciona el lanosterol a la membrana, cuando ésta se forma en ausencia o déficit de ergosterol, se debe fundamentalmente a que el grupo metilo (CH3) en la posición C14a del lanosterol es axial, es decir, sobresale del plano del núcleo esteroide y, por ello, perturba la formación de enlaces mediante fuerzas de Van der Waals entre el propio lanosterol y los ácidos grasos de la bicapa fosfolipídica de la membrana, todo lo cual inestabiliza la estructura global de la membrana. El enzima que cataliza la pérdida de este grupo metilo en el lanosterol se encuentra en los microsomas celulares y es dependiente del citocromo P-450. Este enzima es conocido como lanosterol desmetilasa o 14α-desmetilasa. El proceso de pérdida del metilo (desmetilación) es de tipo oxidativo y conduce a la formación de una insaturación (doble enlace) en la posición D14 (entre C14 y C15). El voriconazol presenta un amplio espectro antifúngico, con actividad marcada frente a varias especies de: - Candida spp (C albicans, C glabrata, C krusei, C dublinensis, C inconspicua, C tropicalis, C guillermondii), incluyendo cepas resistentes a fluconazol. - Aspergillus spp (A flavus, A fumigatus, A terreus, A niger, A nidulans, A) - Scedosporium spp (S apiospermum, S prolificans). - Fusarium spp (F oxysporum) 1 La flucitosina no está comercializada en España. Asimismo, se han han obtenido respuestas clínicas parciales o completas en infecciones fúngicas sistémicas producidas por Alternaria spp, Blastomyces dermatitidis, Cladosporium spp, Coccidiodes immitis, Cryptococcus neoformans y algunos otras especies. ASPECTOS MOLECULARES DEL NUEVO FÁRMACO Los inhibidores de la lanosterol desmetilasa suelen actuar de un forma indirecta al actuar sobre el citocromo P-450, concretamente uniéndose al grupo hemo presente en este cofactor enzimático. Gran parte de estos inhibidores son heterociclos, en mayoría derivados imidazólicos y triazólicos. Parece ser que la presencia de un par de electrones sin compartir, que pueda ser donado desde uno de los átomos de nitrógeno del heterociclo al átomo de hierro del grupo hemo del citocromo P-450, es absolutamente determinante para la eficacia del producto. El anillo heterocíclico está unido a través de un puente dimetilénico a un esqueleto de fenilmetoxi sustituido en 2 y 4 con dos átomos de halógeno (cloro o flúor) y a otras estructuras en las que son muy frecuentes los restos oxialquílicos y los anillos aromáticos (heterocíclicos o no), frecuentemente halogenados. Esta sustitución es determinante para sus propiedades físico-químicas, en especial su capacidad de atravesar barreras biológicas. Todas estas variaciones moleculares no sólo determinan las características farmacocinéticas, sino el espectro antifúngico de los fármacos. EFICACIA CLÍNICA La eficacia y seguridad clínicas del voriconazol han sido contrastadas en varios ensayos clínicos realizados sobre pacientes con micosis de carácter invasivo, generalmente afectados por inmunosupresión. En un amplio estudio (Walsh & Papas et al) de tipo aleatorizado y multicéntrico, se comparó la administración de voriconazol con la de una preparación de anfotericina B en liposomas como terapia antifúngica empírica en 837 pacientes con neutropenia y fiebre persistente. Los índices globales de éxito terapéutico fueron del 26% con voriconazol y del 30,6% con anfotericina B liposómica. La incidencia de hepatotoxicidad fue similar en ambos grupos, mientras que un 22% de los tratados con voriconazol experimentaron alteraciones visuales, frente a sólo un 1% con anfotericina B; asimismo, la incidencia de alucinaciones fue del 4,5% con voriconazol y del 0,5% con anfotericina B. En otro estudio aleatorizado (Herbrecht et al), se comparó la administración de voriconazol con la de anfotericina B como tratamiento primario de aspergilosis invasiva en 277 pacientes. A las 12 semanas, las tasas de éxito terapéutico fueron del 52,8% con voriconazol (respuestas completas en 20,8% y parciales en 31,9%), frente al 31,6% con anfotericina B (completas en el 16,5% y parciales en el 15%). La tasa de supervivencia de los pacientes a las 12 semanas fue del 70,8% en el grupo de voriconazol y del 57,9% en el de anfotericina B. El 44,8% de los tratados con voriconazol presentaron alteraciones visuales transitorias. La utilización de voriconazol en niños (9 meses a 15 años de edad) afectados por infecciones fúngicas invasivas refractarias o intolerantes a la terapia antifúngica convencional fue estudiada (Walsh & Lutsar) en un grupo de 58 pacientes con aspergilosis (42), scedosporiosis (8) o candidiasis (4) invasivas. La duración media del tratamiento fue de 93 días, encontrándose al final del tratamiento unas tasas de respuesta completa o parcial del 45%. También se evaluó (Denning et al) la eficacia y la seguridad del voriconazol en el tratamiento de aspergilosis invasiva en 60 pacientes inmunocomprometidos, obteniéndose buenas respuestas en el 48% de los pacientes (14% completas y 34% parciales). También se ha comparado el voriconazol con el fluconazol en pacientes con candidiasis esofágica en pacientes inmunocomprometidos (Ally et al), mediante un estudio multicéntrico, aleatorizado, doblemente ciego y doblemente enmascarado, sobre un conjunto de 256 pacientes. La tasa de eficacia fue del 98,3% con voriconazol y del 95,1% con fluconazol. Los efectos adversos más comúnmente observados en los ensayos clínicos realizados con voriconazol son trastornos visuales (percepción visual alterada, visión borrosa, cambios en la percepción de los colores, fotofobia, etc), así como fiebre, cefalea, náuseas, vómitos, diarrea, edema periférico, erupciones cutáneas y dolor abdominal, todos ellos muy frecuentes. Asimismo, el voriconazol es ampliamente metabolizado por diversas isoenzimas del citocromo P450, lo que conduce a interacciones potencialmente significativas con un buen número de fármacos inhibidores o inductores de estos sistemas metabólicos. ASPECTOS INNOVADORES La reciente incorporación de la caspofungina al mercado farmacéutico y la actual del voriconazol indican bien a las claras que la prevalencia de las infecciones fúngicas diseminadas está aumentando de forma manifiesta, fundamentalmente como consecuencia a la evolución y progreso de la farmacología inmunomosupresora asociada al también notable incremento del trasplante de órganos, por un lado, y a la negativa incidencia del SIDA, por otro. La anfotericina sigue siendo el antifúngico de referencia en el tratamiento de las micosis invasivas, pero la creciente frecuencia de cepas resistentes, así como la complicada farmacocinética de este fármaco y, especialmente la toxicidad asociada al mismo, han constituido motivos sólidos para justificar el desarrollo de nuevos antifúngicos sistémicos. El voriconazol forma parte de un grupo bien conocido de antifúngicos, los azólicos, iniciado por miconazol y ketoconazol. Este último, auténtico responsable de la generalización de los tratamientos antifúngicos sistémicos, fue el primer agente oral del grupo útil para cuadros sistémicos, si bien su eficacia ha sido ampliamente superada por sus “descendientes”: itraconazol, fluconazol y, ahora, voriconazol. La eficacia del voriconazol en cuadros fúngicos invasivos diversos, junto con su farmacocinética que permite la administración oral, tras las primeras dosis de choque, por vía iv, es sin duda una buena noticia terapéutica. Su utilidad en infecciones provocadas por algunas especies de hongos patógenos “exóticos”, tales como Scedosporium o Fusarium, también es un valor nada despreciable. Sin embargo, queda por determinar claramente el papel terapéutico del nuevo agente en comparación con los antifúngicos más modernos, como la caspofungina. Por otro lado, los datos clínicos no parecen mostrar una superioridad neta sobre la anfotericina B. Y además, la elevada incidencia de algunos efectos adversos, que obliga a suspender el tratamiento en el 10-15% de los pacientes. A tenor de lo indicado anteriormente, la introducción del voriconazol en el mercado farmacéutico español constituye una novedad sólo de relativo interés. El día 19 de marzo de 2002 la Comisión Europea emitió una autorización de comercialización válida para toda la Comunidad Europea para V Fend®, basada en el dictamen favorable y en el informe de evaluación realizado por el Comité de Especialidades Farmacéuticas (CPMP) emitidos el día 13 de diciembre de 2001. OTROS FÁRMACOS SIMILARES REGISTRADOS ANTERIORMENTE EN ESPAÑA Fármaco Fluconazol Itraconazol Caspofungina Especialidad Diflucan Sporanox Caspofungin MSD Laboratorio Pfizer Janssen Cilag Merck Sharp & Dohme Año 1990 1992 2002 VALORACIÓN VORICONAZOL V FEND (Pfizer) Grupo Terapéutico (ATC): J02AC. ANTIMICÓTICOS, USO SISTÉMICO. Triazoles. Indicaciones autorizadas: Aspergilosis invasiva, infecciones invasivas graves por Candida (incluyendo C krusei) resistentes a fluconazol, infecciones fúngicas graves por Scedosporium spp y Fusarium spp. VALORACIÓN GLOBAL: INNOVACIÓN MODERADA. Aporta algunas mejoras, pero no ♣♣ implica cambios sustanciales en la terapéutica estándar. Reduce la incidencia de resistencias microbianas. ⇑ BIBLIOGRAFÍA - Ally R, Schurmann D, Kreisel W, et al; Esophageal Candidiasis Study Group. A randomized, double-blind, - - double-dummy, multicenter trial of voriconazole and fluconazole in the treatment of esophageal candidiasis in immunocompromised patients. Clin Infect Dis 2001; 33(9): 1447-54. Committee for Proprietary Medicinal Products. European Public Assessment Report (EPAR). V Fend. CPMP/4049/01. European Agency for the Evaluation of Medicinal Products. http://www.eudra.org/emea.html Denning DW, Ribaud P, Milpied N, et al. Efficacy and safety of voriconazole in the treatment of acute invasive aspergillosis. Clin Infect Dis 2002; 34(5): 563-71. Herbrecht R, Denning DW, Patterson TF, et al; Invasive Fungal Infections Group of the European Organisation for Research and Treatment of Cancer and the Global Aspergillus Study Group. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N Engl J Med 2002 ; 347(6): 408-15. Rubin AI, Bagheri B, Scher RK. Six novel antimycotics. Am J Clin Dermatol 2002; 3(2): 71-81. Walsh TJ, Lutsar I, Driscoll T, et al. Voriconazole in the treatment of aspergillosis, scedosporiosis and other invasive fungal infections in children. Pediatr Infect Dis J 2002; 21(3): 240-8. Walsh TJ, Pappas P, Winston DJ, et al; The National Institute of Allergy and Infectious Diseases Mycoses Study Group. Voriconazole compared with liposomal amphotericin B for empirical antifungal therapy in patients with neutropenia and persistent fever. N Engl J Med 2002; 346(4): 225-34.