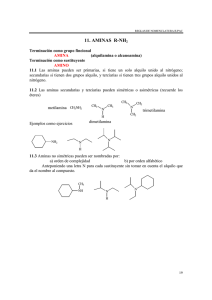
1° etapa (l )
Anuncio

TRABAJO PRÁCTICO DE LABORATORIO N° 10 Reducción de alcanfor a isoborneol con borohidruro de sodio. Adaptado por Diego Cifuente INTRODUCCIÓN Los hidruros metálicos son usados como agentes reductores. El borohidruro de sodio (NaBH4) y el hidruro de aluminio y litio (LiAlH4) son los hidruros metálicos más utilizados en el laboratorio de Química Orgánica. El NaBH4 es un sólido blanco soluble en agua, metanol, etanol e insoluble en éter. Esta sal, que contiene al ion borohidruro (BH4-) de estructura tetraédrica, se prepara por reacción entre hidruro de sodio y borato de metilo a altas temperaturas. NaBH4+ 3 NaOCH3 4 NaH + B(OCH3)3 Por otro lado, el LiAlH4 es un sólido blanco de aspecto cristalino que se prepara por reacción entre hidruro de litio y cloruro de aluminio. Es fácilmente soluble en éteres como el éter etílico, THF, glima y diglima. 4 LiH + AlCl3 LiAlH4 + 3 LiCl Reacciona ávidamente con trazas de humedad para liberar hidrógeno. Debe usarse con precaución ya que produce partículas de polvo que irritan las membranas mucosas. Además puede inflamarse y explota cuando se calienta a 120 °C aproximadamente. LiAlH4 + 4 H2O LiOH + Al(OH)3 + 4 H2 Los aniones BH4 y AlH4 son reactivos nucleófilos y por lo tanto atacan a dobles enlaces polarizados como compuestos carbonílicos, ácidos carboxílicos, derivados de ácidos carboxílicos e iminas mediante la transferencia de un ion hidruro al átomo más positivizado. El NaBH4 es mucho menos reactivo que el LiAlH4. Reduce rápidamente aldehidos y cetonas a 25 °C, pero es esencialmente inerte frente a otros grupos funcionales tales como: epóxidos, ésteres, lactonas y ácidos carboxílicos. El mecanismo propuesto es el siguiente: R - BH4 + CH3 1° etapa (l) C O CH3 H C O - BH3 H C O BH2 R CH3 2° etapa (r) CH3 H2O H C CH3 OH B(OH)3 CH3 CH3 2 CH3 H C CH3 O B H 4 C CH3 O BH 3 El alcanfor es una cetona natural que se obtiene de hervir la madera de unos árboles asiáticos (Cinnamomun canphora (L.) J. Presl) que alcanzan los 30 Química Orgánica II. Lic. y Prof. en Química metros de altura, no se puede extraer hasta que el árbol tiene los 50 años. Actualmente gran parte de la producción natural de alcanfor ha sido reemplazada por la síntesis química, basándose en compuestos contenidos en la trementina. El alcanfor es un compuesto volátil, blanco y cristalino, de fórmula C10H16O, que tiene un olor característico. Es un fuerte cardioestimulante, puede administrarse en caso de insuficiencia cardiaca, por shock o cardiopatía o como consecuencia de tifus o neumonía. En el aparato digestivo tiene efectos laxantes y antiespasmódicos. Estimula el corazón y la respiración, sube la tensión, es indicado en la depresión postoperatoria o en convalecencias graves después del cólera o tuberculosis. El presente trabajo práctico de laboratorio involucra el uso de un agente reductor (borohidruro de sodio) para transformar una cetona (alcanfor) en un alcohol secundario (isoborneol) a través de una reacción redox con transferencia de ion hidruro como se ilustra en el segundo paso de la secuencia oxidación reducción. H3C H3C CH3 H3C CH3 Oxidación CH3 Reducción OH H H3C OH Borneol H3C O Alcanfor H3C H Isoborneol El análisis de los espectros de 1H RMN de borneol, alcanfor e isoborneol permite monitorear el progreso de la reacción como así también establecer las diferencias estructurales y la relación entre los alcoholes isoméricos (El hidrógeno del carbono carbinólico resuena a 4.0 ppm para borneol y a 3.6 ppm para isoborneol). EXPERIMENTAL 1. Reducción e identificación: En un balón de 50 ml agregar 100 mg de alcanfor. Adicionar 25 ml de metanol y agitar hasta disolución total de material de partida. Añadir, cuidadosamente y en pequeñas porciones, sobre baño de hielo 60 mg de borohidruro de sodio. Una vez agregado todo el borohidruro agitar a temperatura ambiente por espacio de dos horas. Posteriormente adicionar unas gotas de agua para apagar el exceso de reactivo y eliminar el metanol en rotavapor. Extraer con éter etílico, lavar con agua y secar la fase etérea con sulfato de sodio (anh.). Evaporar el solvente en rotavapor y registrar espectros de 1H RMN y rotación específica D . Química Orgánica II. Lic. y Prof. en Química Química Orgánica II. Lic. y Prof. en Química