Clase2 - Química Orgánica
Anuncio

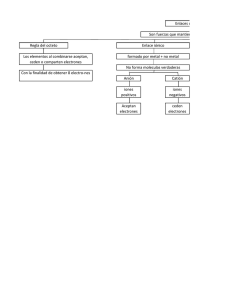
La Química Orgánica es la parte de la química que estudia los C Compuestos p de Carbono C El estudio de los compuestos de carbono comprende varias facetas, de las que las más importantes son: ESTRUCTURA Técnicas de elucidación estructural REACTIVIDAD Mecanismos de reacción SÍNTESIS Diseño de métodos eficientes APLICACIONES Desarrollo industrial, bilógico, médico... ESTRUCTURA Y ENLACE EN LAS MOLÉCULAS ORGÁNICAS ¿Cuando y porqué se forma un enlace entre átomos? Algunos Principios físicos fundamentales: 1. Las cargas opuestas se atraen: F k x q x q´ / d2 (Ley F=k (L de d Coulomb) C l b) 2. Los electrones están distribuidos en el espacio en torno al núcleo o a la molécula resultante del enlace entre dos átomo. átomo 3. Los sistemas físicos tienden a alcanzar un estado mínimo de energía 4. Los sistemas físicos tienden a alcanzar un estado máximo de entropía Dos átomos forman un enlace sólo si su interacción es favorable termodinamicamente Octete por transferencia de electrones: enlaces iónicos Representación de los electrones de valencia mediante puntos Octete por compartimiento de electrones: enlace covalente Procesos energeticamente desfavorables Enlaces covalentes sencillos Un àtomo puede donar dos electrones para formar el enlace covalente Enlaces covalente dativos ó coordinados Enlaces múltiples (dobles y triples) para alcanzar el octete Medida cuantitativa de la capacidad de donar o aceptar electrones: Potenciales de Ionización (PI) y Afinidad electrónica (AE) Escala de electronegatividad de Pauling Enlaces covalentes polares Dipolos y Momentos dipolares HF , μ = 1.82 Debye y Efecto inductivo H3C F HCl,, μ = 1.08 Debye y Repulsión electrónica y forma de las moléculas Asignación de cargas formales Formula de la Carga Formal Carga Formal = nº de electrones de valencia en ell átomo át neutro t - nº de electrones de valencia no compartidos de electrones +1/2 nºcompartidos Enlaces múltiples Estructuras de Lewis con separación de cargas Estructuras Resonantes Estructuras de resonancia no equivalentes Reglas para establecer contribución de estructuras resonantes 1. Las estructuras con un número máximo de octetes tienen preferencia 2. Las cargas se colocan preferentemente sobre los átomos mas electronegativos 3. Las Estructuras con Separación de Cargas Mínima Tienen Preferencia 4. La regla del octete puede imponer la separación de carga