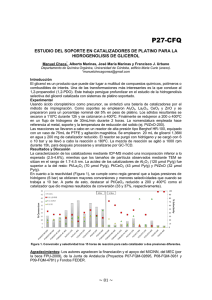
Estudio de nuevos catalizadores para la reacción de
Anuncio

Estudio de nuevos catalizadores para la reacción de oxidación preferencial de CO en presencia de H2 Erika de Oliveira Jardim Erika de Oliveira Jardim Estudio de nuevos catalizadores para la reacción de oxidación preferencial de CO en presencia de H 2 Tesis Doctoral Universidad de Alicante Departamento de Química Inorgánica Laboratorio de Materiales Avanzados Junio, 2012 UNIVERSIDAD DE ALICANTE Departamento de Química Inorgánica Laboratorio de Materiales Avanzados (LMA) Estudio de nuevos catalizadores para la reacción de oxidación preferencial de CO en presencia de H2. Memoria presentada para aspirar al grado de Doctor Erika de Oliveira Jardim Directores del trabajo: Antonio Sepúlveda Escribano Profesor Catedrático de Química Inorgánica Joaquín Silvestre Albero Profesor Titular de Química Inorgánica Junio 2012 Antonio Sepúlveda Escribano y Joaquín Silvestre Albero, profesores catedrático y titular de Química Inorgánica de la Universidad de Alicante, CERTIFICAN QUE: Dña. Erika de Oliveira Jardim, Licenciada en Química, ha realizado en el Departamento de Química Inorgánica de la Facultad de Ciencias de la Universidad de Alicante, bajo nuestra dirección, el trabajo titulado “Estudio de nuevos catalizadores para la reacción de oxidación preferencial de CO en presencia de H2” que constituye su Memoria para aspirar al grado de Doctor por la Universidad de Alicante reuniendo, a nuestro juicio, las condiciones necesarias para ser presentada y defendida ante el tribunal correspondiente. Y para que conste a los efectos oportunos, en cumplimiento de la legislación vigente, firmamos el presente certificado en Alicante, a 15 de Mayo de 2012. Fdo. Antonio Sepúlveda Escribano. Fdo. Joaquín Silvestre Albero Agradecimientos Cuando decidí hacer el doctorado fuera de Brasil, mi familia y mis amigos, a pesar de saber cómo sería de complicada la distancia, siempre me apoyaron y estuvieron conmigo. Durante esta nueva etapa aprendí muchas cosas importantes que me hicieron crecer tanto profesionalmente como personalmente. En este momento, me resulta complicado decir, en pocas palabras, el agradecimiento a toda la gente que ha hecho posible finalizar este periodo de mi vida. Hace cuatro años y medio que empecé esta nueva etapa y deseo dar mis más profundos agradecimientos a las personas que depositaron su confianza en mí para realizar esta Tesis de Doctorado. Primeramente me gustaría agradecer a aquellos que hicieron posible esta Tesis, a mis directores, Joaquín Silvestre Albero y Antonio Sepúlveda Escribano. Gracias por compartir conmigo este tiempo, por transmitir vuestro conocimiento, por la paciencia por mi portuñol, por las horas dedicadas de trabajo, por la presencia en todos los momentos, independientemente del día, por estar apoyándome y ayudándome haciéndome sentir como si estuviera en Casita, y principalmente por vuestra amistad. Gracias de todo corazón por la confianza depositada. No puedo olvidar a mis queridos profesores, Prof. Francisco Rodríguez Reinoso y Prof. Rochel Montero Lago. Sin la confianza que ustedes han depositado en mí, no estaría aquí. Reinoso, muchas gracias por ofrecerme la beca y por la confianza. Gracias por apoyarme en los momentos difíciles y por preocuparse siempre por mí, por saber cómo me siento, si estoy a gusto, si estoy bien, por cuidarme, le aprecio mucho. Brigadão Rochel por estar sempre comigo em todos os momentos de mi vida. Sei que posso sempre contar com você não somente como professor mais também como amigo (faz parte do meu treinamento). Hay un dicho popular que dice “Deus dá asas para quem não sabe voar.” Yo diría que mis padres me dieron las alas y gracias a mis profesores, fui capaz de aprender a volar. Durante esta jornada estuve fuera de España donde aprendí mucho. Thanks Professor James A. Anderson, of the Surface Chemistry and Catalysis Group, Department of Chemistry, University of Aberdeen. Thanks for receive me in your lab. In special thanks for Fiona and Steven for all the help in my stay. Además de Escocia, estuve en Portugal, mi lengua materna, donde conocí al Profesor Manuel Fernando R. Pereira y Olivia Salomé. Obrigada por todo o apoio e por estarem sempre comigo durante este tempo que estive em Portugal, por fazerem mais fácil mi estadia. Em especial, obrigada a Salomé e sua família. Me gustaría agradecer a todas las personas que conocí en este periodo. A mis amigos de trabajo del LMA. Algunos ya no presentes en el grupo pero siempre estuvieron ahí y han sido de grande apoyo en esta etapa. Muchas Gracias Rachel, Ana Valera, Enrique, Noelia, Javitín, Richard, Yoshi, Ana Silvestre, Anass, Zinab, Laura, Robison, David Carpena (Davitín), Mirian, Vasanth, Yesid, Sole, Mateus, Ivonne, Pelayo, Gonzalo y Serra. Personas como Sonia (por la amistad y por presencia), Jarito (Thanks for your frienship), Andrea (Che), Cris Botas, Franz, Mayer, JuanPa, David Salinas, Miriam, Aroldo, Noelia, Mónica, Iza, Madeleine, Lived, Juanma, Segundo, Sarah, Antonio, Ernesto, Giovanni y Ana Galindo. Gracias por los momentos de alegría y por las risas, momentos que nos hacen olvidar que estamos lejos de casa. Existen personas que han sido de grande importancia para esta Tesis. Muchas gracias a toda la gente de los servicios técnicos de investigación de la Universidad de Alicante, en especial a Chema (por el simple hecho de estar siempre presente en los momentos difíciles), a los vidrieros Javier y Juan, a Cristina, a Verónica y Andrés, a Clemente, a Fernando Coloma, a Ion y Jero y a Juan Manuel. Gracias por los análisis, por la profesionalidad y por la paciencia en momentos de prisa. No puedo olvidarme a todos los de la secretaria del Departamento; gracias Ester, Juan Cuadrado, Ana Lillo, Concha y Elisa. Por la gran labor que realizan y por arreglar todos los problemas y dudas durante esta jornada. Gracias Toya por todas las respuestas y apoyo. Por último, muchas gracias a los técnicos del Departamento, Quique, Jaime, Paco, Olga, Isidro y Eduardo, muchas gracias por todo. Y cómo no, agradecer a mi Querida Pepa, su ayuda, sus largas conversaciones durante este tiempo…muchas gracias por cuidarme. Algunas veces el apoyo de una persona te hace sentir que puedes confiar en ti. Muchas gracias a Edna y Quique, por la amistad, por transmitirme conocimientos, por la paciencia y por los pães de queijo. Cuando se está lejos de casa, pequeños gestos se hacen muy grandes. Gracias Davitín, por el simple hecho de estar ahí. Sé que siempre puedo contar contigo. En especial me gustaría agradecer a Robi, por ser un buen amigo, por estar ahí siempre en los momentos difíciles. Durante esta estancia hice muchos amigos que nunca olvidaré. Entre ellos me gustaría agradecer a las grandes amigas que siempre estarán conmigo, que llevaré en mi corazón. Brigadão Rachelita, minha amiga, por todo. Você foi muito importante nesta etapa da minha vida. Sua ajuda, seu carinho, seu amor, por sempre estar de mi lado em todos os momentos de mi vida. A distancia nunca foi um problema para manter a nossa amizade. Brigadão Mara (Amiga Maricota) de todo meu coração. Por suportar-me nos momentos mais complicados de minha vida. Sua presença e carinho sempre me ajudaram a seguir adiante, a ter força para superar esta etapa. Solecito, muchas gracias. Por siempre estar a mi lado, por saber cuando estoy triste, feliz o cuando tengo un problema y ayudarme. Algunas veces no es necesario palabras; el hecho de saber que tengo una amiga a mi lado con quien puedo contar, me tranquiliza y me conforta. Tu ayuda ha sido de mucha importancia en esta etapa, no digo sólo como labor, sino también como una buena amiga. De verdad que eres muy especial, te llevaré en mi corazón y espero verte muy pronto, sea donde sea (nuestro acuerdo todavía sigue en pie). Y finalmente, a Verito, mi Peke, que siempre estuvo ahí, en todo los momentos, de alegría o tristeza, con quien siempre conté y contaré. Además de las amistades adquiridas durante mi estancia, no puedo olvidarme de los amigos que siempre me acompañaron y estuvieron a mi lado. Juliana Tristão y Marcelo Rosmaninho, vocês fizeram parte de miha historia, sempre presente em todos os momentos, mesmo longe nossa amizade se mantém e se torna cada vez mais forte. Estar lejos de casa de la familia es muy duro, sin embargo, la distancia ha sido superada con el apoyo de “mis familias adoptivas”. Gracias a las familias de Vero, Sole y Sonia por el cariño y por hacer más fácil mi estancia en España. Existen personas que aparecen en nuestra vida, aunque sea por un corto intervalo, pero son capaces de transformarla. Me gustaría, en este momento, agradecer a Mateus y Virginia Castro por el amor, cariño y apoyo en la iniciativa de la Tesis. Zina, obrigada pelas mensagens, elas me ajudaram a seguir adiante nos momentos mais difíceis. Incluyendo a estas personas, me gustaría agradecer a Franz López, de todo corazón, por todo el amor y por estar siempre conmigo, por sacarme de la cama en los momentos de pereza, por incentivarme y por ayudarme a seguir adelante, por su presencia, por estar siempre apoyándome y por siempre dejar mi Jardim con flores. Muchas gracias Andrés, su gran amistad me ha ayudado a superar algunos momentos de conflicto en mi vida. Gracias por vuestro amor, por todo el cariño y la fuerza que me transmites día a día En especial, de forma más profunda y de todo corazón, me gustaría dar GRACIAS a mi familia: a mis primos, principalmente a mi madre (Mary), mi hermanita (Hellen), mis sobriños (Matheus y Gabriel) y mis abuelitos queridos (Vovó Santa y Vovô Doutivo). Sin vuestro amor, cariño, dedicación y todo vuestro apoyo no estaría aquí realizando esta Tesis de Doctorado. Vosotros son las personas más importantes de mi vida. Sei que passamos por momentos difíceis e que nem sempre estava presente, mais com nossa união e amor foi possível superar todos estes momentos. A todos los nombrados y no nombrados, muchas gracias!!!!!!!!!! Contenido Estructura de la tesis .............................................................................................. i CAPÍTULO 1.............................................................................................................. 1 Introducción................................................................................................................. 1 1. La problemática energética actual. .......................................................... 2 2. El hidrógeno como un vector energético................................................ 3 3. Pilas de combustible.................................................................................. 5 4. Objetivos. .................................................................................................. 11 5. Referencias................................................................................................ 11 CAPÍTULO 2............................................................................................................ 15 Técnicas de caracterización y de determinación de la actividad catalítica. . 15 1. Técnicas de caracterización. ................................................................... 16 1.1. Adsorción de N2 a 77 K. ................................................................. 16 1.2. Espectroscopía atómica de emisión por plasma de acoplamiento inductivo (ICP – OES). ............................................................. 18 1.3. Fluorescencia de rayos X (FRX). ................................................... 18 1.4. Difracción de rayos X (DRX). ........................................................ 19 1.5. Espectroscopía Raman. .................................................................. 20 1.6. Microscopía electrónica de barrido (SEM). ................................. 21 1.7. Microscopía electrónica de transmisión (TEM). ......................... 21 1.8. Espectroscopía fotoelectrónica de rayos X (XPS). ...................... 22 1.9. Reducción a temperatura programada con H2 (RTP-H2). ......... 23 1.10. Desorción a temperatura programada de CO/CO2 (DTPCO/CO2). .... 23 1.11. Desorción a temperatura programada de H2 (DTP-H2)............. 24 1.12. Espectroscopía infrarroja de reflectancia difusa con transformada de Fourier y cámara de reacción in situ (DRIFTS in situ). .. 24 2. 3. Ensayos catalíticos. .................................................................................. 25 2.1. Reacción a temperatura programada. .......................................... 28 2.2. Reacción a temperatura constante. ............................................... 28 Referencias. .............................................................................................. 28 CHAPTER 3 ............................................................................................................. 31 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H 2 (PROX). .................... 31 1. Introduction. ............................................................................................ 32 2. Experimental. ........................................................................................... 33 3. 2.1. Catalysts preparation and characterization. ............................... 33 2.2. Catalytic behaviour. ....................................................................... 34 Results and discussion. ........................................................................... 35 3.1. Textural and metal loading characterization. ............................. 35 3.2. X-ray diffraction (XRD). ................................................................. 35 3.3. (TEM) Catalysts characterization by transmission electron microscopy ........................................................................................................... 37 3.4. Temperature-programmed reduction with H2 (H2-TPR). ......... 37 3.5. X-ray photoelectron spectroscopy analysis (XPS). ..................... 42 3.6. Temperature-programmed desorption experiments of CO/CO2 (CO/CO2-TPD). .................................................................................................. 48 3.7. Catalytic behaviour in the PROX reaction. ................................. 52 4. Conclusions. ............................................................................................. 64 5. References. ................................................................................................ 64 CHAPTER 4 ............................................................................................................. 71 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. ..................... 71 1. Introduction. ............................................................................................ 72 2. Experimental. ........................................................................................... 73 3. 2.1. Catalysts preparation and characterization. ............................... 73 2.2. Catalytic behaviour. ....................................................................... 74 Results and discussion. ........................................................................... 74 3.1. Textural and metal loading characterization. ............................. 74 3.2. X-ray diffraction characterization. ................................................ 75 3.3. Raman characterization of catalysts. ............................................ 77 3.4. SEM/EDS – Chemical mapping catalysts characterization. ...... 79 3.5. (TEM). Catalyst characterization by transmission electron microscopy ........................................................................................................... 81 3.6. Catalysts characterization by temperature-programmed reduction with H2 (H2-TPR). ............................................................................ 82 3.7. (XPS). Catalyst characterization by X-ray photoelectron spectroscopy ........................................................................................................... 85 3.8. Catalysts characterization by temperature-programmed desorption of CO2 and CO (CO2/CO-TPD). ................................................... 87 3.9. Catalytic behaviour. ....................................................................... 90 4. Conclusions. ............................................................................................. 97 5. References. ................................................................................................ 97 CHAPTER 5 ........................................................................................................... 101 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalysts. ................ 101 1. Introduction. ............................................................................................... 102 2. Experimental. ............................................................................................. 103 2.1. Catalysts preparation and characterization. .................................. 103 2.2. Catalytic behaviour. .......................................................................... 104 3. Results and discussion. ............................................................................. 104 3.1. Textural and metal loading characterization. ............................... 104 3.2. X-ray diffraction analysis. ................................................................ 105 3.3. Raman spectroscopy characterization. ........................................... 108 3.4. SEM/EDS – chemical mapping catalysts characterization. .......... 111 3.5. Transmission electron microscopy. ................................................ 112 3.6. Temperature-programmed reduction with hydrogen. ................ 113 3.7. X-ray photoelectron spectroscopy. ................................................. 114 3.8. Catalyst characterization by temperature-programmed desorption of CO2 and CO (CO2/CO-TPD). ..................................................................... 118 3.9. H2-temperature-programmed desorption experiments............... 120 3.10. Catalytic behaviour. ..................................................................... 121 4. Conclusions. ............................................................................................... 127 5. References. .................................................................................................. 127 CAPÍTULO 6.......................................................................................................... 131 Catalizadores de oro soportado en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. ............................................. 131 1. Introducción. .......................................................................................... 132 2. Experimental. ......................................................................................... 133 3. 2.1. Preparación y caracterización de los catalizadores. ................. 133 2.2. Ensayos catalíticos. ....................................................................... 134 Resultados y discusión. ........................................................................ 135 3.1. Caracterización textural y porcentaje metálica. ........................ 135 3.2. Caracterización de los catalizadores mediante DRX. .............. 135 3.3. Caracterización de los catalizadores mediante TEM. .............. 136 3.4. Caracterización de los catalizadores mediante RTP-H2. ......... 137 3.5. Caracterización de Au/0,7CeO2-0,3Nb2O5 mediante XPS........ 139 3.6. Comportamiento catalítico. ......................................................... 141 4. Conclusión.............................................................................................. 155 5. Referencias. ............................................................................................ 156 CAPÍTULO 7.......................................................................................................... 159 Catalizadores de cobre soportados sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. ............................................. 159 1. Introducción. .............................................................................................. 160 2. Experimental. ............................................................................................. 162 2.1. Preparación y caracterización de los catalizadores. ..................... 162 2.2. Ensayos catalíticos. ........................................................................... 163 3. Resultados y discusión. ............................................................................. 163 3.1. Caracterización textural y porcentaje metálico. ............................ 163 3.2. Caracterización de los catalizadores mediante DRX. ................... 164 3.3. Caracterización de los catalizadores mediante espectroscopía Raman. ............................................................................................................. 165 3.4. Caracterización de los catalizadores mediante TEM. ................... 167 3.5. Caracterización de los catalizadores mediante RTP-H2. .............. 168 3.6. Comportamiento catalítico. ............................................................. 170 4. Conclusiones............................................................................................... 173 5. Referencias. ................................................................................................. 174 CAPÍTULO 8.......................................................................................................... 177 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). ...................................... 177 1. Introducción. .............................................................................................. 178 2. Experimental. ............................................................................................. 178 2.1. Preparación y caracterización de los catalizadores. ..................... 178 2.2. Ensayos catalíticos. ........................................................................... 178 3. Resultados y discusión. ............................................................................. 179 3.1. Comportamiento catalítico. ............................................................. 179 4. Conclusión. ................................................................................................. 186 5. Referencias. ................................................................................................. 186 CAPÍTULO 9.......................................................................................................... 189 Conclusiones generales. ................................................................................... 189 CURRICULUM VITAE ............................................................................................ 193 Lista de figuras Figura 1.1. Origen del hidrógeno producido en la actualidad (adaptado de las referencias [7][13])................................................................................................. 4 Figura 1.2. Funcionamiento de una PEMFC [13]. ............................................. 6 Figura 2.1. Esquema del sistema de reacción acoplado a un cromatógrafo de gases. ..................................................................................................................... 27 Figure 3.1. X-ray diffraction profiles of CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2. ..................................................................................................................................... 36 Figure 3.2. The crystal structure of the CeO2: unit cell as a ccp array of cerium atoms. The ccp layers are parallel to the (111) planes of the f.c.c. unit cell (a), the same structure redrawn as a primitive cubic array of oxygens (b) and (c). ........................................................................................................................ 36 Figure 3.3. TEM images of CeO2 support (a), Pt(N)/CeO2 (b), Pt(Cl)/CeO2 (c). ..................................................................................................................................... 37 Figure 3.4. H2-TPR profiles (H2 consumption) for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2. ............................................................................................................... 39 Figure 3.5. Mechanism proposed for the incorporation of chloride ions into the ceria lattice and the formation of CeOCl phase by Fajardie et al. [26]. ....... 40 Figure 3.6. Structure relationship between CeO2 (110) and CeOCl (010) surfaces [13]. .............................................................................................................. 41 Figure 3.7. Scheme for the mechanism proposed for the incorporation of chlorine ions into the lattice ceria suggested by Force [27]. ................................ 41 Figure 3.8. XPS spectra of Ce 3d region for the Pt(N)/CeO2 (a) and Pt(Cl)/CeO2 (b) catalysts both fresh and with the reduced temperature (RT) at 523 and 773 K............................................................................................................. 43 Figure 3.9. % Ce (III) as a function of the reduction temperature ( ) Pt(N)/CeO2 and ( ) Pt(Cl)/CeO2 catalyst. .............................................................. 45 Figure 3.10. XPS results of Pt 4f of the Pt(N)/CeO2 (a) and Pt(Cl)/CeO2 (b) catalysts, fresh and reduced in situ at 523 K and 773 K. ...................................... 47 Figure 3.11. CO2 (a) and CO (b) desorption profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K. ........................................................ 51 Figure 3.12. CO oxidation profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K (a) and at 773 K (b). ................................................... 54 Figure 3.13. CO2 selectivity profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K (a) and at 773 K (b). ................................................... 55 Figure 3.14. CO conversion for Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K and reaction temperature at 333 K and 353 K. ........................ 57 Figure 3.15. Preferential CO oxidation on the Pt(N)/CeO2 catalyst, reduced at 523 K; reaction temperature at 353 K; feed composition: 2% CO, 0.6-2% O2, 20% H2 and He as a balance..................................................................................... 58 Figure 3.16. DRIFT spectra obtained during CO oxidation under 2% CO, 10% air, 20% H2 and balance N2 feed with catalysts reduced at 523 K: CeO2 (a), Pt(N)/CeO2 (b) and Pt(Cl)/CeO2 (c). The initial temperature was 313 K and it was increased by 20 K. ............................................................................................. 62 Figure 3.17. DRIFTS spectra of CO adsorbed species on the Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts during PROX reaction at 313 K. ........................................ 63 Figure 4.1. X-rays difractograms of Pt/xCeO2-(1-x)Y2O3 catalysts (x = 1, 0.9, 0.7, 0.4 and 0). ............................................................................................................ 76 Figure 4.2. Raman spectra of xCeO2-(1-x)Y2O3 (a) and Pt/xCeO2-(1-x)Y2O3 (b) solids. .................................................................................................................... 79 Figure 4.3. SEM images for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO20.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). .................................................................. 80 Figure 4.4. SEM-chemical mapping Ce analysis (red), for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO2-0.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). .... 80 Figure 4.5. SEM-chemical mapping Y analysis (green), for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO2-0.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). .... 81 Figure 4.6. TEM images of Pt/xCeO2-(1-x)Y2O3 catalysts, x = 1 (a), x = 0.9 (b), x = 0.7 (c), x = 0.4 (d) y x = 0 (e). ............................................................................... 82 Figure 4.7. TPR profiles for xCeO2-(1-x)Y2O3 (a) and Pt/xCeO2-(1-x)Y2O3 (b), with x = 1, 0.9, 0.7, 0.4 and 0. ................................................................................... 84 Figure 4.8. XPS results of O 1s of fresh catalysts, calcined at 773 K. ............ 86 Figure 4.9. Relative amount of surface Ce (III) (%) in Pt/xCeO2-(1-x)Y2O3 catalysts, as function of the yttrium content, after reduction treatments. ......... 87 Figure 4.10. CO2 and CO desorption profiles for Pt/xCeO2-(1-x)Y2O3 catalysts (x = 1, 0.9, 0.7, 0.4, 0) reduced at 523 K (a) and (b) respectively. ... 89 Figure 4.11. CO oxidation light-off curves for Pt/xCeO2-(1-x)Y2O3 catalysts, reduced at 523 K (a) and at 773 K (b). .................................................................... 92 Figure 4.12. CO2 selectivity profiles for Pt/xCeO2-(1-x)Y2O3 catalysts, reduced at 523 K (a) and at 773 K (b). .................................................................... 93 Figure 4.13. CO preferential oxidation on Pt/0.7CeO2-0.3Y2O3 catalyst, reduced at 523 K, with the reaction temperature at 353 K; gas feed composition: 2% CO, 0.6-2% O2, 20% H2 and balanced He......................................................... 94 Figure 4.14. DRIFT spectra obtained in the CO oxidation under 2% CO, 10% air, 20% H2 and N2 as balance gas feed for Pt/CeO2 (a) and Pt/0.7CeO2-0.3Y2O3 (b) reduced at 523 K. The starting reaction temperature was 313 K, and it was increased by 20 K steps from bottom to top. ......................................................... 96 Figure 5.1. X-rays difractograms for Pt/xCeO2-(1-x)Nb2O5 catalysts, x = 1, 0.9, 0.7, 0.4 and 0. ........................................................................................................... 107 Figure 5.2. Raman spectra of xCeO2-(1-x)Nb2O5 supports (a) and Pt/xCeO2(1-x)Nb2O5 catalysts (b). ......................................................................................... 110 Figure 5.3. SEM images for the samples Pt/0.9CeO2-0.1Nb2O5 (a), Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO2-0.6Nb2O5 (c). ...................................... 111 Figure 5.4. SEM-chemical mapping Ce analysis (red), for the samples Pt/0.9CeO2-0.1Nb2O5 (a), Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO2-0.6Nb2O5 (c). ................................................................................................................................... 111 Figure 5.5. SEM-chemical mapping Nb analysis (blue and green) for the samples Pt/0.9CeO2-0.1Nb2O5 (a), Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO20.6Nb2O5 (c). ............................................................................................................. 112 Figure 5.6. TEM images of Pt/xCeO2-(1-x)Nb2O5 catalysts, x = 1 (a), x = 0.9 (b), x = 0.7 (c), x = 0.4 (d) y x = 0 (e). .............................................................. 112 Figure 5.7. TPR curves for (a) xCeO2-(1-x)Nb2O5 and (b) Pt/xCeO2-(1x)Nb2O5, where x = 1, 0.9, 0.7, 0.4 and 0. .............................................................. 114 Figure 5.8. XPS results of O 1s of different catalysts calcined at 773 K. ..... 116 Figure 5.9. Relative amount of surface Ce (III) (%) in Pt/xCeO2-(1-x)Nb2O5 catalysts, as function of the niobium content, after reduction treatments. ..... 117 Figure 5.10. XPS results of Pt 4f of the Pt/0.7CeO2-0.3Nb2O5 catalysts, reduced at 523 K.................................................................................................. 118 Figure 5.11. CO2 and CO desorption profiles for Pt/xCeO2-(1-x)Nb2O5 catalysts reduced at 523 K, (a) and (b) respectively. .......................................... 119 Figure 5.12. H2 desorption profiles for Pt/xCeO2-(1-x)Nb2O5 catalysts reduced at 523 K. ..................................................................................................... 121 Figure 5.13. CO oxidation light-off curves for Pt/xCeO2-(1-x)Nb2O5 serie catalysts, reduced at 523 K (a) and at 773 K (b). ................................................. 123 Figure 5.14. CO2 selectivity profiles for Pt/xCeO2-(1-x)Nb2O5 serie catalysts, reduced at 523 K (a) and at 773 K (b). .................................................................. 124 Figure 5.15. CO preferential oxidation on Pt/0.7CeO2-0.3Nb2O5 catalyst, reduced at 523 K and with the reaction temperature at 353 K, in the feed of 2% CO, 0.6-2% O2, 20% H2 and He as balance. .......................................................... 125 Figure 5.16. DRIFT spectra obtained to CO oxidation under 2% CO, 10% air, 20% H2 and N2 as balance feed, reduced at 523 K, for Pt/CeO2 (a) and Pt/0.7CeO2-0.3Nb2O5 (b) the initial temperature was of 313 K and increase to each 20 K of bottom to top. .................................................................................... 127 Figura 6.1. Difractogramas de rayos X de los catalizadores de Au/CeO 2 y Au/0,7CeO2-0,3MO (M = Nb o Y). ......................................................................... 136 Figura 6.2. Imágenes de TEM de los catalizadores de Au/CeO2 (a), Au/0,7CeO2-0,3Nb2O5 (b) y Au/0,7CeO2-0,3Y2O3 (c)........................................... 137 Figura 6.3. Perfiles de reducción a temperatura programada (consumo de hidrógeno) de los catalizadores de oro. ............................................................... 139 Figura 6.4. Espectros XPS para el nivel Au 4f en el catalizador Au/0,7CeO2-0,3Nb2O5 reducido a 473 K............................................................... 141 Figura 6.5. Conversión de CO (a) y selectividad hacia a CO 2 (b) para los catalizadores de oro reducidos a 473 K preparados por distintos métodos de preparación. ............................................................................................................. 143 Figura 6.6. Conversión de CO (a) y selectividad (b) para los catalizadores de oro reducidos a 473 K utilizando un flujo de 20 % de H 2, 2% de CO y O2 y He como balance. .................................................................................................... 146 Figura 6.7. Conversión de CO (a) y selectividad (b) para los catalizadores de oro reducidos y en isotermos a 343 K. ............................................................ 148 Figura 6.8. Conversión de CO para los catalizadores de Au/CeO 2 (a), Au/0,7CeO2-0,3Nb2O5 (b) y Au/0,7CeO2-0,3Y2O3 (c) reducidos a 473 K y calcinados a distintas temperaturas (TC). ........................................................... 151 Figura 6.9. Conversión de CO (a) y selectividad (b) para los catalizadores de Au/CeO2 con distintas concentraciones de O2. .............................................. 153 Figura 6.10. Conversión de CO (a) y selectividad (b) para los catalizadores de Au/0,7CeO2-0,3Nb2O5 con distintas concentraciones de O2. ........................ 154 Figura 6.11. Conversión de CO (a) y selectividad (b) para los catalizadores de Au/0,7CeO2-0,3Y2O3 con distintas concentraciones de O2. ........................... 155 Figura 7.1. Difractogramas de rayos-X de los catalizadores de 8Cu/CeO2 y 4Cu/xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4)......................................................... 165 Figura 7.2. Espectros Raman de los catalizadores de Cu/xCeO 2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4). ................................................................................................ 167 Figura 7.3. Imágenes de TEM de los catalizadores de 8Cu/CeO 2 (a,b), 4Cu/CeO2 (c), 4Cu/0,9CeO2-0,1Nb2O5 (d), 4Cu/0,7CeO2-0,3Nb2O5 (e) y 4Cu/0,4CeO2-0,6Nb2O5 (f). ..................................................................................... 168 Figura 7.4. Perfiles de reducción a temperatura programada de los catalizadores de cobre. ........................................................................................... 170 Figura 7.5. Conversión de CO (a) y selectividad a CO 2 (b) para los catalizadores con 8 % y 4 % en peso de cobre. .................................................... 171 Figura 7.6. Conversión de CO (a) y selectividad a CO 2 (b) para la serie 4Cu/CexNb1-xO (x = 1; 0,9; 0,7 y 0,4). ..................................................................... 173 Figura 8.1. Variación de la conversión de CO (a) y selectividad a CO 2 (b) en función de la temperatura para el catalizador Pt/0,7CeO 2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). ..................................................................................................................... 180 Figura 8.2. Variación de la conversión de CO (a) y selectividad (b) en función de la temperatura para el catalizador Au/0,7CeO2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO 2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). ..................................................................................................................... 181 Figura 8.3. Variación de la conversión de CO (a) y selectividad (b) en función de la temperatura para el catalizador Cu/0,7CeO 2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO 2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). ..................................................................................................................... 182 Lista de tablas Tabla 1.1. Densidades energéticas de diversos combustibles [7]. ................... 3 Tabla 1.2. Tipos más comunes de pilas de combustible y sus usos. Adaptada de las referencias [2][7][19]...................................................................... 5 Tabla 2.1. Composiciones de los gases de entrada. ........................................ 27 Table 3.1. Physical properties of the synthesized catalysts. .......................... 35 Table 3.2. Catalyst characterization by XPS. .................................................... 45 Table 3.3. CO/CO2-TPD characterization of Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts. ..................................................................................................................... 52 Table 4.1. Characterization of Pt/xCeO2-(1-x)Y2O3 catalysts. ......................... 75 Table 4.2. Crystallite size and lattice constant of the xCeO2-(1-x)Y2O3 supports...................................................................................................................... 77 Table 4.3. XPS characterization of Pt/xCeO2-(1-x)Y2O3 catalysts calcined at 673 K. .......................................................................................................................... 85 Table 5.1. Characterization of Pt/xCeO2-(1-x)Nb2O5 catalysts. .................... 105 Table 5.2. Crystallite size and lattice constant of the xCeO2-(1-x)Nb2O5 support. .................................................................................................................... 108 Table 5.3. XPS characterization of Pt/xCeO2-(1-x)Nb2O5 catalysts. ............. 115 Tabla 6.1. Contenido de Au de los catalizadores y composiciones molares y área superficial B.E.T. de los soportes. ................................................................. 135 Tabla 6.2. Caracterización por XPS del catalizador Au/0,7CeO2-0,3Nb2O5 reducido a 473 K...................................................................................................... 140 Tabla 7.1. Área superficial BET del soporte y contenido de cobre (% en peso) de los catalizadores. ..................................................................................... 163 Lista de abreviaciones AFC – Alkaline fuel cell. AIE – Agencia Internacional de la Energía. bbc – Body-centred cubic. BE – Binding energy. CO2/CO-TPD - Temperature-programmed desorption of CO2 and CO. DTP-CO/CO2 - Desorción a temperatura programada de CO/CO2. DTP-H2 - Desorción a temperatura programada de H2. DRIFTS - Diffuse reflectance infrared Fourier transformed spectroscopy. DRX – Difracción de rayos X. EL – Energía de ligadura. ffc – Face-centred cubic. FID - Flame ionization detector. FRX - Fluorescencia de rayos X. GHSV - Gas hourly space velocity. H2-TPD – Temperature-programmed desorption of H2. H2-TPR - Temperature-programmed reduction with H2. hcp – Hexagonal close-packed. HRTEM - High-resolution transmission electron microscopy. HTWGS – High temperature water gas shift. ICP-OES - Inductively coupled plasma optical emission spectrometry. LTWGS – Low temperature water gas shift. MCFC – Molten carbonate fuel cell. n.m. – Non measured. NM – Noble metal. OSC – Oxygen storage capacity. PAFC – Phosphoric acid fuel cell. PCE – Producción combinada de calor y electricidad. PEMFC – Proton exchange membrane fuel cell. PROX – Preferential oxidation. RT – Reduction temperature. RTP-H2 - Reducción a temperatura programada en hidrógeno. RWGS – Reverse water gas shift. SOFC – Solid oxide fuel cell. TCD - Thermal-conductivity detector. TEM – Transmission electron microscopy. TWG – Three way catalysts. WGS – Water gas shift. XPS - X-ray photoelectron spectroscopy. XRD - X-ray diffraction. XRF - X-ray fluorescence. Estructura de la tesis Esta memoria está estructurada en nueve capítulos. En el Capítulo 1 se describen la problemática energética actual y la utilización de la pilas de combustible para la producción de hidrógeno, como una alternativa de fuente de energía. Donde se explica, resumidamente, cada etapa de una pila de combustible, se centrando en el proceso PROX y los problemas presentados por el mismo. Además, se evidencia cómo la catálisis es una tecnología clave para el control de la eliminación de contaminantes. En el Capítulo 2 se presentan las técnicas de caracterización empleadas para obtener información sobre las propiedades fisicoquímicas de los catalizadores utilizados. Estas técnicas son FRX, ICP – OES, adsorción de N2 a 77 K, DRX, XPS, espectroscopía Raman, TEM, DRIFTS in situ, RTP-H2, desorción de CO/CO2 y H2 a temperatura programada. Asimismo se describe el sistema experimental usado para la realización de los ensayos catalíticos. Los Capítulos 3 a 8 están dedicados a la presentación y discusión de resultados experimentales. En el estudio presentado en el Capítulo 3 se presentan y discuten los resultados obtenidos para los catalizadores de platino soportados sobre el óxido de cerio. El objetivo es estudiar la influencia del precursor metálico, en este caso del platino, con la presencia o no de cloro, en la reacción PROX. En los Capítulos 4 y 5 se estudia el efecto de la adicción de itrio o niobio en el óxido de cerio, en los catalizadores de platino, en la actividad catalítica. Se han preparado dos series distintas con estos dopantes, xCeO 2-(1-x)Y2O3 y xCeO2-(1-x)Nb2O5. El objetivo es analizar la influencia de la naturaleza del soporte en las propiedades del óxido de cerio y del platino, y relacionar con su actividad catalítica. En el Capítulo 6 se estudia la actividad catalítica, de una proporción especifica de los soportes preparados en los Capítulos 4 y 5, en su caso para x = 0,7, en catalizadores de oro con el objetivo de analizar el efecto en la actividad de los catalizadores para la oxidación de CO. Se ha estudiado el efecto del método de impregnación del metal, y el porcentaje de los gases de entrada en la actividad catalítica. En el Capítulo 7 se presentan los resultados del uso de catalizadores de cobre soportados sobre la serie de óxido de cerio-óxido de niobio. Se ha Estructura de la tesis. estudiado el efecto del porcentaje de cobre y de óxido de niobio en la actividad catalítica. El objetivo de esta etapa es producir catalizadores más eficientes y viables económicamente. En el Capítulo 8 se estudia el comportamiento de los catalizadores de platino, oro y cobre soportados sobre óxido de cerio-óxido de niobio para el proceso de oxidación de CO con la presencia de CO2 y/o H2O. Cabe resaltar que la presencia de éstos gases simulan condiciones más reales a de los gases de salida de un reformado, durante la producción de hidrógeno. Por último, en el Capítulo 9 se resumen las conclusiones más relevantes obtenidas en el presente estudio. ii CAPÍTULO 1 Introducción. Abstract. This chapter will introduce the actual energetic technologies associated with the use of fossil fuels, as well as with the use of hydrogen-based fuel cells as an alternative energy source. At this point, the problems arising with the presence of a relatively low amount of CO in the feed stream will be discussed. This CO is generated during hydrogen production through hydrocarbon reforming processes. In this sense, one of the most efficient technologies to remove this residual CO, that is, the preferential oxidation of CO to CO2 in the presence of excess hydrogen (PROX) will be presented and discussed. Introducción. 1. La problemática energética actual. Los recursos energéticos constituyen un factor fundamental para el desarrollo de la Humanidad [1]. Así, el petróleo, que comenzó a extraerse a finales del siglo XIX y a utilizarse de forma generalizada a partir de la Segunda Guerra Mundial, constituye una fuente de combustibles líquidos y de productos químicos de bajo coste, que ha ayudado por un lado a la industrialización del mundo y, por otro, a aumentar la calidad de vida. Actualmente, el perfil mundial en cuanto al abastecimiento energético es crítico. Algunas fuentes sugieren que las reservas mundiales de petróleo, carbón y gas natural serán suficientes para el abastecimiento de la humanidad durante unas pocas décadas más [2][3]; es decir, que la producción convencional de petróleo a nivel mundial empezará a disminuir, mientras la demanda mundial no dejará de aumentar. Según la Agencia Internacional de la Energía (AIE), el consumo actual de petróleo es de 86,60 millones de barriles diarios, constituyendo el 40 % del consumo energético, y siendo los Estados Unidos de América el mayor consumidor de energía a nivel mundial [4]. Además, la elevada demanda de combustibles fósiles genera problemas para la sociedad, como por ejemplo: (i) problemas económicos, asociados a los altos precios de los combustibles, y (ii) problemas ambientales, debido a las emisiones incontroladas a la atmósfera de gases contaminantes (responsables del cambio climático) [3]. En este sentido, cabe destacar la generación y emisión de grandes cantidades de CO2 que pueden afectar al medio ambiente y provocar un calentamiento global del planeta [5][6]. Aunque no se sabe exactamente el tiempo de vida de los recursos energéticos no renovables, el consumo es tan elevado que el mantenimiento del mismo se torna insostenible para las próximas generaciones. Además, no se puede excluir el hecho de que las energías renovables, tales como biomasa, energía hidroeléctrica, eólica, solar y geotérmica, contribuirán positivamente para el suministro energético mundial [2][3]. La aparición de nuevas alternativas para la generación de energía eléctrica proporciona una oportunidad única para el cambio de los sistemas tradicionales, con una mejora de la eficiencia energética. Está bien establecido que la mayor parte de energía utilizada, principalmente en el sector del transporte, proviene de los combustibles fósiles. Desafortunadamente, la escasez de los recursos de petróleo y la creciente demanda de los mismos está obligando a desarrollar procesos alternativos que sean económicos y eficientes, desde un punto de vista energético, para la producción sostenible de combustibles y productos químicos. 2 Capítulo 1 En este sentido, una de las opciones energéticas más prometedoras para el futuro está basada en el hidrógeno. 2. El hidrógeno como un vector energético. El hidrógeno es considerado una importante alternativa para solucionar los problemas energéticos y medioambientales actuales, principalmente porque es (i) un combustible no contaminante, puesto que su combustión produce principalmente agua como producto final; (ii) puede ser obtenida a partir de una fuente renovable; (iii) presenta una elevada eficiencia energética, dado que su energía química puede ser convertida directamente en electricidad de forma eficiente, sin las limitaciones termodinámicas impuestas por el ciclo de Carnot y, (iv) produce energía a bajo coste [3][5][7][8][9][10]. El hidrógeno es considerado un vector energético, es decir, un portador de energía [7], que debe ser producido a partir de otros compuestos mediante el uso de otras fuentes de energía. En la Tabla 1.1 se resumen, a modo de comparación, las cantidades de energía almacenadas en diferentes combustibles. Se puede apreciar que el hidrógeno es capaz de almacenar más energía que los demás combustibles presentados. Sin embargo, presenta algunas desventajas en cuanto a su utilización: la distribución, el almacenamiento y el transporte del hidrógeno son más complicados que en el caso de los combustibles fósiles. Tabla 1.1. Densidades energéticas de diversos combustibles [7]. Energía almacenada Densidad, Kg·m-3 Volumen, kWh·m-3 Volumen, kWh·N-1m-3 Masa, kWh·Kg-1 H2 líquido (1 bar, 20 K) 70,71 2375 H2 gas (300 bar, 298 K) 20,55 690 3 33,59 H2 gas (700 bar, 298 K) 47,96 1611 Gas natural (1 bar, 298 K) 0,65 9,1 10 13,93 Butano (298 K) 550 7000 33 12,73 Gasolina 750 9270 --- 12,36 El hecho de que el hidrógeno no se encuentre de manera aislada en la naturaleza obliga a obtenerlo por distintos procedimientos. Puede ser producido a partir de fuentes no renovables, como el carbón, el petróleo y el 3 Introducción. gas natural, así como fuentes renovables, como la biomasa [6][8][11] y el agua. El hidrógeno puede ser obtenido mediante procesos térmicos como el reformado de gas natural [6][11][12], el reformado auto térmico de derivados de petróleo y gas natural [6], la gasificación de carbón [6][8][11], la disociación térmica [6], a partir de la biomasa [6][8][11] y de la energía nuclear [11], así como procesos electrónicos como la electrólisis del agua [6][8][11][12], y por procesos biológicos [6][11][12]. En la Figura 1.1 se resumen algunos de los procesos de obtención de hidrógeno. Figura 1.1. Origen del hidrógeno producido en la actualidad (adaptado de las referencias [7][13]). En las próximas décadas es de esperar que la demanda de hidrógeno, bien sea para las aplicaciones tradicionales como la fabricación de amoníaco, o bien para su uso como combustible, presente un crecimiento importante. De hecho, en la actualidad, muchos fabricantes de coches ya tienen fabricados prototipos de vehículos que funcionan con pilas de combustible que consumen hidrógeno [14]. En el caso concreto de la industria automovilística, los estudios dirigidos hacia el desarrollo de procesos alternativos para la producción de energía son cada vez más abundantes. Esto se debe por un lado a que, aunque el control catalítico de las emisiones de los coches está bastante controlado, las legislaciones medioambientales son cada vez más exigentes y, por otro, a la creciente escasez de combustibles fósiles [15]. Desde el punto de vista de las aplicaciones, la más común es la conversión directa de la energía química del hidrógeno en energía eléctrica a través de la pila de combustible, que presenta un elevado rendimiento al tratarse de un proceso electroquímico [14][16][17]. 4 Capítulo 1 3. Pilas de combustible. Una pila de combustible es un dispositivo electroquímico que convierte la energía química de una reacción directamente en energía eléctrica, mientras se suministra combustible (los reactivos) a sus electrodos [2]. Se puede utilizar en un amplio rango de aplicaciones tales como la alimentación de teléfonos móviles y ordenadores personales, coches, autobuses y otros vehículos, así como generadores eléctricos para uso doméstico o industrial [18]. Las pilas de combustible son aproximadamente dos veces más eficientes que el motor de combustión interna, y no producen agentes contaminantes primarios [2][3][7][12]. Además, pueden ser utilizadas en aplicaciones tanto estacionarias como móviles [3][12]. Existen diferentes tipos de pilas de combustibles, que se clasifican habitualmente de acuerdo con el electrolito utilizado. En la Tabla 1.2 se resumen las principales características de algunas pilas de combustible y sus aplicaciones. Tabla 1.2. Tipos más comunes de pilas de combustible y sus usos. Adaptada de las referencias [2][7][19]. Tipo de pila de combustible Temperatura de trabajo, K Electrolito Aplicaciones Membrana de intercambio protónico (PEMFC) 313-353 Polímero Transporte, viaje espacial, pequeña PCE y equipo móvil Alcalinas (AFC) 323-473 KOH Transporte y misiones espaciales Metanol directo 353-473 Polímero Transporte y equipo móvil Ácido fosfórico (PAFC) 463-483 Ácido fosfórico PCE y plantas de energía Carbonatos fundidos (MCFC) 873-923 Carbonatos fundidos PCE y plantas de energía Óxidos sólidos (SOFC). 873-1273 Óxidos sólidos PCE y plantas de energía PCE = producción combinada de calor y electricidad. De entre los diferentes tipos de pilas existentes, las más prometedoras para su aplicación en sistemas móviles son las pilas de combustible de membrana 5 Introducción. intercambiadora de protones (PEMFC) [16][17]. En la Figura 1.2 se representa un esquema de una PEMFC. Estas pilas se caracterizan por tener como electrodo una matriz polimérica conductora de protones. La estructura formada entre los electrodos y electrolito es muy fina, y suelen estar conectados mediante placas bipolares formando pilas compactas [7]. Esta pila resulta ser la más adecuada para su aplicación como fuente de energía en la industria automovilística debido a su baja temperatura de trabajo, lo que facilita el período de arranque. Sin embargo, para este tipo de pila es necesaria la utilización de hidrógeno de elevada pureza, ya que la baja temperatura de operación impide un reformado interno. Por otro lado, la cinética de la reacción electroquímica está limitada a esas bajas temperaturas, lo que hace necesario utilizar electrocatalizadores compuestos por metales nobles (platino) [7], susceptibles al envenenamiento por CO. Figura 1.2. Funcionamiento de una PEMFC [13]. Las pilas de combustible PEMFC operan a bajas temperaturas, 313-353 K, y producen energía eléctrica a partir de la oxidación electroquímica de hidrógeno en el ánodo (Ecuación 1.1) y la reducción electroquímica de oxígeno en el cátodo (Ecuación 1.2), produciendo agua como residuo final (Ecuación 1.3). El cátodo y ánodo utilizados están basados en catalizadores de Pt soportados [17]. (Ecuación 1.1) (Ecuación 1.2) (Ecuación 1.3) 6 Capítulo 1 A pesar de las ventajas que presentan estas pilas, uno de los aspectos críticos es el abastecimiento de hidrógeno como combustible. Como ya ha sido mencionado anteriormente, el hidrógeno puede obtenerse mediante diferentes procesos y utilizando una gran variedad de sustancias como fuentes primarias, tales como hidrocarburos, biomasa, carbón, etc. En la actualidad la mayor parte del hidrógeno que se produce industrialmente se obtiene a partir del reformado de hidrocarburos y alcoholes. El reformado puede realizarse de tres formas diferentes: reformado con vapor de agua, reformado con oxidación parcial (utilizando aire humidificado) y reformado auto térmico (con una mezcla de aire y vapor) [7][16][20]. De estas variedades, la más comúnmente utilizada es el reformado con vapor de agua [5]. El reformado de metano con vapor de agua [14][17][20] (Ecuación 1.4) se produce a elevadas temperaturas (>1073 K) y, normalmente, a presiones superiores a 20 atm a fin de evitar una etapa posterior de compresión de los productos obtenidos [20], siendo los catalizadores a base de níquel los más utilizados [14][17]. El metano se utiliza ampliamente como precursor de hidrógeno debido a su disponibilidad y relativamente bajo coste. (Ecuación 1.4) También existen estudios sobre la producción de hidrógeno utilizando el reformado con vapor de agua de alcoholes como etanol y metanol (Ecuación 1.5 y Ecuación 1.6), a temperaturas entre 473-873 K, con catalizadores basados en platino, rutenio, cobre, cinc, níquel, cobalto o paladio [14][17][21][22]. (Ecuación 1.5) (Ecuación 1.6) La producción de hidrógeno está termodinámicamente favorecida a altas temperaturas; sin embargo, la presencia de reacciones paralelas hace que se produzca una gran cantidad de CO indeseado, además de H2 y CO2, oscilando su porcentaje entre un 0,5 % y un 12 % [14][16][17][23][24] dependiendo del proceso utilizado. El CO debe ser eliminado de forma selectiva, dado su efecto de veneno sobre el catalizador de Pt utilizado como electrodo en el ánodo. En este sentido, un tratamiento a posteriori de la corriente anterior con vapor de agua (reacción de desplazamiento del gas de agua, WGS: water-gas shift) permite reducir el contenido de CO hasta aproximadamente 1000 ppm [17], siendo esta concentración aún elevada para la cantidad máxima tolerada por el ánodo en la pila de combustible (10-50 ppm) [14][15][16][23]. La reacción WGS consiste en la conversión de CO y H2O a CO2 y H2 (Ecuación 1.7), a través de 7 Introducción. una reacción reversible a bajas temperaturas (433-723 K). La reacción se suele realizar en dos etapas: el desplazamiento del gas de agua a altas temperaturas (HTWGS) y el desplazamiento a bajas temperaturas (LTWGS). (Ecuación 1.7) Un catalizador viable para el proceso WGS debe demostrar actividad suficiente para poder trabajar en una ventana razonable de temperaturas, tener estabilidad suficiente para trabajar entre 2000-5000 horas, y no requerir un procedimiento muy largo de activación [16]. Los catalizadores más utilizados para la reacción a baja temperatura están basados en cobre/cinc [15][20][21], mientras que para la reacción a alta temperatura se utilizan convencionalmente catalizadores basados en hierro/cromo [14][17]. En resumen, un reformado auto térmico, seguido por la reacción de desplazamiento de gas de agua, puede generar una corriente final con una composición 10% CO2, 25% H2O, ~1%CO, 30% de H2 y N2. Como se ha comentado, el proceso de WGS resulta insuficiente por sí mismo para alcanzar las concentraciones de CO tolerables por las células de combustible. En este sentido, una de las mejores alternativas que existe actualmente para reducir los contenidos de CO hasta valores admisibles consiste en la oxidación preferencial de CO a CO2 (PROX) (Ecuación 1.8 y Ecuación 1.9) con O2 y en presencia de un exceso de H2 y CO2, ambos componentes procedentes del proceso de reformado. (Ecuación 1.8) (Ecuación 1.9) Además de las dos reacciones citadas anteriormente, Ecuación 1.8 y Ecuación 1.9, hay otras reacciones que pueden afectar al rendimiento y la eficiencia del proceso, como la de reacción inversa al desplazamiento de gas de agua (RWGS) y la reacción de metanación [8][16][15][17][25]. En general, son varios los factores que pueden afectar a la eficiencia del proceso de oxidación de CO: la relación estequiométrica λ (λ = 2[O2]/[CO]) [26][27][28][29][30], la concentración de CO [28][31], la velocidad espacial [32][33] y la temperatura de reacción [34][35], entre otros. Los reactores utilizados para la reacción PROX suelen ser ¼ del tamaño de los reactores de WGS. Además, el oxígeno necesario para la oxidación se alimenta a través de un corriente de aire que se localiza próxima al reactor. Por lo tanto, el reactor puede operar a presiones atmosféricas y el compresor, que 8 Capítulo 1 introduce el aire, consume poca energía [8], siendo esto una ventaja para el proceso. El sistema PROX puede estar constituido por dos o más etapas, dependiendo de la concentración de CO y del calor disipado [17]. Lo ideal para el proceso sería una temperatura de entrada al reactor menor o igual que la temperatura de salida del reactor de WGS, dado que éste se encuentra justo arriba del reactor PROX. Este modelo facilitaría el paso de la corriente gaseosa sin la inclusión de intercambiadores de calor [8]. Como ambas reacciones de oxidación son altamente exotérmicas, es importante eliminar el calor del reactor. Aun así, la estabilidad térmica del catalizador es un factor crítico a la hora de su selección. Además los catalizadores para el proceso PROX deben presentar elevada actividad hacia la oxidación de CO a baja temperatura, alta selectividad para la oxidación del CO frente a la oxidación indeseada de H2, proceso que disminuiría la eficacia total del proceso, y buena resistencia a la desactivación causada por la presencia de H2O y CO2 [8][16][23]. La vida útil de los catalizadores para PROX es un factor crítico. Contaminantes presentes en la corriente de reformado, como por ejemplo compuestos de azufre, pueden desactivar el catalizador. También, reactores que trabajan a temperaturas elevadas o aumentos de temperatura puntuales y no previstos pueden afectar a la durabilidad del catalizador. Además, la presencia de agua suele afectar también a la estabilidad del soporte. [8]. De manera general, catalizadores con metales preciosos son selectivos para la reacción PROX [8]. En la literatura se han publicado estudios sobre diferentes metales, tales como rodio, rutenio, platino y oro, soportados sobre distintos soportes [36][37][38][39][40][41][42][43]. El proceso de oxidación de CO se puede resumir de forma sencilla de la siguiente manera: inicialmente, el CO se adsorbe cubriendo la superficie del metal; con el aumento de la temperatura de reacción, la fracción del CO adsorbido disminuye y posibilita la adsorción de O2 y, consecuentemente, la reacción de oxidación. Desafortunadamente, a temperaturas elevadas se favorecen reacciones paralelas como la oxidación de H2, las reacciones de metanación de CO y CO2, así como la reacción inversa del desplazamiento del gas de agua, con el consiguiente consumo de hidrógeno en los tres casos y, consecuentemente, la disminución de la selectividad. Adicionalmente, esas elevadas temperaturas obligan a un posterior enfriamiento de la corriente de gas antes de su utilización en las pilas de combustible. 9 Introducción. Como se ha señalado anteriormente, la oxidación preferencial de CO en presencia de hidrógeno sobre diferentes catalizadores ha sido ampliamente estudiada en la literatura. Inicialmente se investigó la reacción PROX utilizando catalizadores de metales preciosos soportados sobre zeolitas, carbones y óxidos inertes, como por ejemplo la alúmina. En este caso, la reacción de oxidación se ajustaba a un mecanismo de Langmuir-Hinshelwood, donde el CO y el O2 competían por los mismos sitios activos [8][14]. Uno de los aspectos más críticos en el diseño de catalizadores para la oxidación preferencial de CO es la interfase metal-soporte o metal-promotor. En este sentido, el uso de catalizadores basados en soportes capaces de suministrar oxígeno en la interfase metal-soporte parecen ser una alternativa para estos procesos, y aquí destaca el uso de óxidos parcialmente reducibles como soporte, por ejemplo, CeO2 y Fe2O3, entre otros. En el caso de los catalizadores que contienen soportes activos, o sea, óxidos metálicos reducibles, el oxígeno del soporte participa de la reacción según un mecanismo de Mars-Krevelen [27][36][44]. En este sentido, el CeO2 es una buena alternativa para ser utilizado como soporte para la reacción PROX debido a su capacidad para almacenar y suministrar oxígeno de forma efectiva [26][45][46][47]. De igual forma, resultan también interesantes los óxidos mixtos que contienen óxido de cerio, debido a la posibilidad de incrementar la capacidad de almacenar y movilizar el oxígeno interfacial [48][49][50]. Una de las funciones más importantes del óxido de cerio es proporcionar oxígeno a los sitios activos superficiales, actuando como un transportador de oxígeno, cuya movilidad se ve favorecida por la facilidad de alternar entre dos estados de oxidación, Ce (III) y Ce (IV) [48][51][52][53]. Estas propiedades redox se pueden mejorar cuando el óxido de cerio es dopado por otros cationes con diferentes tamaños de radio atómico y/o carga, lo que puede favorecer la movilidad del oxígeno mediante la formación de defectos en la estructura tipo fluorita del óxido de cerio. Catalizadores a base de metales nobles elevan mucho el coste de las pilas de combustible. En este sentido, en este trabajo se ha planteado, de forma adicional, el estudio de otras opciones de catalizadores más asequibles. Así, se han estudiado inicialmente catalizadores de platino soportado sobre óxido de cerio, tanto puro como modificado mediante la adición de otras especies metálicas (itrio y niobio). Estos dos dopantes harán disminuir el coste del soporte en comparación con el óxido de cerio másico. A continuación, se han estudiado catalizadores a base de otros metales de menor coste, oro y cobre, soportados en los óxidos mixtos anteriormente citados. Además, se ha 10 Capítulo 1 estudiado también la influencia de las condiciones de reacción y la presencia de gases que simulan condiciones más cercanas a una pila de combustible, tales como CO2 y H2O. 4. Objetivos. El objetivo general de este trabajo de investigación es estudiar la oxidación preferencial de CO en presencia de hidrógeno con diferentes catalizadores metálicos soportados sobre óxido de cerio puro y óxidos mixtos, empleando diferentes condiciones de reacción. Para alcanzar el objetivo general, se plantean los siguientes objetivos específicos: Preparar, caracterizar y evaluar en la reacción de oxidación preferencial de CO (PROX), catalizadores de platino soportado sobre óxido de cerio, utilizando dos precursores de platino, con y sin cloro. Preparar, caracterizar y evaluar en la reacción PROX, catalizadores de platino soportado sobre una serie de óxido de cerio dopado con itrio, con diferentes proporciones cerio/itrio. Preparar, caracterizar y evaluar en la reacción PROX, catalizadores de platino soportado sobre una serie de óxido de cerio dopado con niobio, con diferentes proporciones cerio/niobio. Preparar, caracterizar y evaluar en la reacción PROX, catalizadores de oro soportado en los soportes citados anteriormente. Preparar, caracterizar y evaluar en la reacción PROX, catalizadores de óxido de cobre soportado sobre la serie de óxido de cerio dopado con niobio. Estudiar la influencia de diferentes proporciones de gases y, adicionalmente, la influencia de la adición de CO 2 y H2O, con el objetivo de simular condiciones más reales de reacción, en la actividad catalítica. 5. Referencias. [1] E. Lorenzo, Sobre el Papel de la Energía en la Historia, Propensa, Sevilla (2006). [2] P.L.G. Ybarra, Tecnologías Energéticas y el Impacto Ambiental, McGraw-Hill, España (2001). [3] A. Demirbas, Biohydrogen – For Future Engine Fuel Demands, Springer-Verlag London Limited, London (2009). [4] Annual Energy Outlook, DOE/EIA-0383 (2011). [5] J.A Turner, Science 285 (1999) 687-689. [6] B. Kruse, S. Grinna, C. Buch, Hydrogen – Status of Muligheter, Bellona, U.S. (2002). 11 Introducción. [7] J.I.L. Hurtado, B.Y.M. Soria, El hidrógeno y la energía, Asociación Nacional de Ingenieros del ICAI, Madrid (2007). [8] K. Liu, C. Song, V. Subramani, Hydrogen and Syngas Production and Purification Technologies, Wiley, Canada (2010). [9] G.W. Huber, S. Iborra, A. Corma, Chem. Rev. 106 (2006) 4044-4098. [10] A. Corma, S. Iborra, A. Velty, Chem. Rev. 107 (2007) 2411-2502. [11] A. Züttel, A. Borgschulte, L. Schlapbach, Hydrogen as a Future Energy Carrier, Wiley, Germany (2008). [12] Basic Research Needs for the Hydrogen Economy, Report on the Basic Energy Sciences Workshop on Hydrogen Production, Storage and Use, Argonne National Laboratory, Chicago (2004). [13] R. Buitrago-Sierra, Producción de hidrógeno mediante reformado de etanol, Diploma de Estudios Avanzados, Universidad de Alicante, España (2010). [14] R.M. Navarro, M. A. Peña, J. L. G. Fierro, Chem. Rev. 107 (2007) 3952-3991. [15] D.L. Trimm, Appl. Cat. A: Gen. 296 (2005) 1-11. [16] J.M. Zlac, D.G. Löffler, J. Power Sources 111 (2002) 58-64. [17] R. Farrauto, S. Hwang, L. Shore, W. Ruettinger, J. Lampert, T. Giroux, Y. Liu, O. Ilinich, Annu. Rev. Mater. Res. 33 (2003) 1-27. [18] P. D. Vaidya, A. E. Rodrigues, Chem. Eng. J. 117 (2006) 39-49. [19] EG and G services, Fuell Cell Handbook, Morgantown, Virginia, Ed. 5 (2000). [20] J.N. Armor, Appl. Cat. A: Gen. 176 (1999) 159-176. [21] V.V. Galvita, G.L. Semin, V.D. Belyaev, V.A. Semikolenov, P. Tsiakarasand, V.B. Sobyanin, Appl. Cat. A: Gen. 220 (2001) 123-127. [22] D.K. Liguras, D.I. Kondarides, X.E. Verykios, Appl. Catal. B: Env. 43 (2003) 345-354. [23] E. Simsek, S. Ozkara, A.E. Aksoylu, Z.I. Önsan, Appl. Cat. A: Gen. 316 (2007) 169174. [24] P. Tsiakaras, A. Demin, J. Power Sources 102 (2001) 210-217. [25] N. Bion, F.Epron, M. Moreno, F. Mariño, D. Duprez, Top. Catal. 51 (2008) 76-88. [26] J.L. Ayastuy, A. Gil-Rodriguez, M.P. González-Marcos, M.A. Gutiérrez-Ortiz, Int. J. Hydrogen Ener. 31 (2006) 2231-2242. [27] F. Mariño, C.Descorme, D. Duprez, Appl. Catal B: Env. 54 (2004) 59-66. [28] O. Pozdnyakova, D. Teschner, A. Wootsch, J. Kröhnert, B. Steinhauer, H. Sauer, L. Toth, F.C. Jentoft, A. Knop-Gericke, Z. Paál, R. Schlögl, J. Catal. 237 (2006) 1-16. [29] D. Teschner, A. Wootsch, O. Pozdnyakova-Tellinger, J. Kröhnert, E.M. Vass, M. Hävecker, S. Zafeiratos, P. Schnörch, P.C.Jentoft, A.Knop-Gericke, R. Schlögl, J. Catal. 249 (2007) 318-327. [30] A. Wootsch, C. Descorme, D. Duprez, J. Catal. 225 (2004) 259-266. [31] H. Tanaka, M. Kuriyama, Y. Ishida, S-I. Ito, T. Kubota, T. Miyao, S. Naito, K. Tomishige, K. Kunimori, Appl. Catal. A: Gen. 343 (2008) 125-133. [32] M.J. Kahlich, H.A. Gasteiger, R.J. Behm, J. Catal. 182 (1999) 430-440. [33] E.C. Njagi, H.C. Genuino, C.H. King’ondu, C-H. Chen, D. Horvath, S.L. Suit, International J. Hydrogen Ener. 36 (2011) 6768-6779. [34] M. Tada, R. Atralis, J. Batista, S. Hocevar, Catal. Lett. 73 (2001) 33-40. [35] S. Xu, D. Sun, H. Liu, X. Wang, X. Yan, Catal. Commun. 12 (2011) 514-518. 12 Capítulo 1 [36] [37] [38] [39] [40] [41] [42] [43] [44] [45] [46] [47] [48] [49] [50] [51] [52] [53] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env. 58 (2005) 175-183. M. Abid, R. Touroude, Catal. Lett. 69 (2000) 139-144. L. Kepinski, J. Okal, J. Catal. 192 (2000) 48-53. Y.-F. Han, M.J. Kahlich, M. Kinne, R.J. Behm, Phys. Chem. Chem. Phys. 4 (2002) 389–397. Y.-F. Han, M.J. Kahlich, M. Kinne, R.J. Behm, Appl. Catal. B: Env. 50 (2004) 209– 218. C. Force, J.P. Belzunegui, J. Sanz, A. Martínez-Arias, J. Soria, J. Catal. 197 (2001) 192–199 G. Yi, H. Yang, B. Li, H. Lin, K-I Tanaka, Y. Yuan, Catal. Today 157 (2010) 83-88. W. Deng, J. de Jesus, H. Saltsburg, M. Flytzani-Stephanopoulos, Appl. Catal. A, Gen. 291 (2005) 126-135. W. Li, F.J. Gracia, E.E. Wolf, Catal. Today 81 (2003) 437-447. H. Vidal, J. Kaspar, M. Pijolat, G. Colon, S. Bernal, A. Cordón, V. Perrichon, F. Fally, Appl. Catal. B: Env. 27 (2000) 49-63. E. Mamontov, T. Egami, R. Brezny, M. Koranne, S. Tyagi, J. Phys. Chem. B 104 (2000) 11110-11116. C. Larese, M. López-Granados, R. Mariscal, J.L.G. Fierro, P.S. Lambrou, A.M. Efstathiou, Appl. Catal. B: Env. 59 (2005) 13-25. A. Trovarelli, C. de Leitenburg, M. Boaro, G. Dolcetti, Catal. Today 50 (2000) 353367. A. Trovarelli, Catal. Rev. Sci. Eng. 38 (1996) 439-520. A. Trovarelli, Catalysis by ceria and related materials, Imperial College Press, London (2002). M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today 68 (2001) 53-61. A. Trovarelli, F. Zamar, J. Lorca, C. Leitenburg, G. Dolcetti, J.T. Kiss, J. Catal. 169 (1997) 490-502. H. Roh, H.S. Potdar, K. Jun, S.Y. Han, J. Kim, Catal. Lett. 93 (2004) 203-207. 13 14 CAPÍTULO 2 Técnicas de caracterización y de determinación de la actividad catalítica. Abstract. In this chapter, the different characterization techniques used in this work to obtain information about the physico-chemical properties of the supports and catalysts used will be presented. These techniques were N2 adsorption at 77 K, X-ray fluorescence, inductively coupled plasma optical emission spectrometry, X-ray diffraction, Raman spectroscopy, transmission electron microscopy, X-ray photoelectron spectroscopy, hydrogen temperatureprogram reduction, temperature-programmed desorption of CO/CO2, temperature-programmed desorption of H2 and in situ diffuse reflectance infra-red Fourier transformed. The experimental system used for carrying out the catalytic tests will be also described. The preparation of the different samples (supports and catalysts) will be described in the experimental section of the corresponding chapter. Técnicas de caracterización y de determinación de la actividad catalítica. En este capítulo se describen las diferentes técnicas de caracterización empleadas para obtener información sobre las propiedades físico-químicas de los soportes y los catalizadores, además del sistema experimental utilizado para la realización de los ensayos catalíticos. La preparación de las diferentes muestras (catalizadores y soportes) se describe en la sección experimental de cada capítulo, con el fin de facilitar la lectura. 1. Técnicas de caracterización. En este estudio se han utilizado distintas técnicas para obtener información sobre las características físico-químicas de los soportes y los catalizadores. El contenido en metales (platino, oro, cobre, cerio, itrio y niobio) de los catalizadores fue determinado mediante espectroscopía de emisión por plasma de acoplamiento inductivo (ICP – OES) y fluorescencia de rayos X (FRX). Las características estructurales y químicas fueron determinadas usando adsorción de N2 a 77 K, difracción de rayos X (DRX), espectroscopía fotoelectrónica de rayos X (XPS), espectroscopía Raman, microscopía electrónica de transmisión (TEM), microscopía electrónica de barrido (SEM) reducción a temperatura programada en hidrógeno (RTP-H2), desorción a temperatura programada de CO/CO2 e H2 (DTP-CO/CO2 y DTP-H2) y espectroscopía infrarroja de reflectancia difusa con transformada de Fourier y cámara de reacción in situ (DRIFTS in situ). A continuación se describe brevemente el principio físico-químico en el que se basan las diferentes técnicas empleadas, así como los dispositivos experimentales y las condiciones de operación. 1.1. Adsorción de N2 a 77 K. Las isotermas de adsorción física de gases son ampliamente utilizadas para determinar la superficie específica y la distribución de tamaños de poros en sólidos porosos. Existen diferentes tipos de dispositivos para la determinación de las isotermas de adsorción: volumétricos, manométricos y gravimétricos, pudiendo operar en estático o dinámico. La superficie específica se determina teniendo en cuenta la cantidad de moléculas adsorbidas formando una monocapa sobre la superficie, y el área ocupada por cada una de esas moléculas. El método más utilizado para calcular la superficie específica de sólidos a partir de una isoterma de adsorción es el método BET, cuyo nombre procede de las iniciales de los investigadores que lo desarrollaron: Brunauer, Emmet y Teller [1]. 16 Capítulo 2 La ecuación BET, en su forma más conveniente para ser aplicada a los datos experimentales de las isotermas de adsorción, viene dada por: (Ecuación 2.1) donde P es la presión final de equilibrio, P0 es la presión de saturación del adsorbato a la temperatura de trabajo, n es la cantidad de gas adsorbido a una presión relativa P/P0, nm es la cantidad de gas requerida para la formación de una monocapa, y C es una constante adimensional relacionada con la energía de adsorción. El parámetro C puede ser representado por la Ecuación 2.2. (Ecuación 2.2) donde E representa el calor de adsorción en la primera capa de adsorbato y EL el calor de condensación del líquido. Cuando ambos calores difieren bastante y C tiene un valor numérico relativamente grande, las fuerzas de adsorción son elevadas, y se produce una adsorción preferente de la primera capa. De este modo, la representación gráfica del cociente P/n(P0-P) frente a P/P0 resulta una línea recta, de cuya pendiente y ordenada en el origen se deducen los valores de las constantes nm y C [2]. La aplicación del modelo BET a las isotermas de adsorción de N2 a 77 K proporciona la cantidad adsorbida en la monocapa y, conociendo el área ocupada por una molécula de N2 adsorbida, que es de 0,162 nm2 [3], se puede calcular el área superficial aparente por medio de la Ecuación 2.3, (Ecuación 2.3) donde, S es la superficie aparente del sólido adsorbente, expresada en m 2·g-1, Na es el número de Avogadro y am es el área media ocupada por la molécula de adsorbato (nm2). El intervalo de presiones relativas en el que la ecuación BET es aplicable se sitúa entre 0,05 y 0,35, aunque este intervalo depende de las características del material adsorbente. A presiones relativas inferiores a 0,05 la no aplicabilidad del método se atribuye a un incremento del potencial de adsorción debido a la presencia de microporos, mientras que por encima de 0,35 se debe a la posibilidad de condensación capilar en mesoporos. La superficie específica de los soportes utilizados en este estudio se determinó aplicando la ecuación BET a los datos de las isotermas de adsorción de N2 a 77 K. Estas isotermas se obtuvieron utilizando un aparato manométrico de adsorción en estático, diseñado y construido en el Laboratorio de Materiales Avanzados (LMA) del Departamento de Química Inorgánica de 17 Técnicas de caracterización y de determinación de la actividad catalítica. la Universidad de Alicante, modelo LMAsorb, equipado con una bomba de vacío turbomolecular. Se utilizaron aproximadamente 100 mg de muestra previamente desgasificada a 523 K entre 10-5 y 10-6 Torr, por un periodo de 4 horas. 1.2. Espectroscopía atómica de emisión por plasma de acoplamiento inductivo (ICP – OES). La técnica ICP-OES permite determinar cuantitativamente un gran número de elementos que se encuentran en concentraciones muy bajas (trazas) en una disolución acuosa. La técnica se basa en el análisis de la radiación ultravioleta/visible emitida por un elemento al ser excitado en un plasma, es decir, un gas ionizado altamente energético. En este trabajo se ha utilizado esta técnica para determinar el contenido real de platino, oro y cobre de los catalizadores. El equipo empleado fue un espectrómetro de emisión por plasma de acoplamiento inductivo Perkin Elmer, modelo Óptima 3000. Los metales se extrajeron del catalizador utilizando una disolución ácida de HCl (8 M), durante 8 horas, en un dispositivo Soxhlet. Después del proceso de extracción, la disolución obtenida se diluyó para obtener una disolución de concentración adecuada para su análisis. Los resultados obtenidos por ICP que se muestran en esta Memoria de Tesis Doctoral han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.3. Fluorescencia de rayos X (FRX). La fluorescencia de rayos X es una técnica espectroscópica que permite determinar la composición química de una muestra, analizando la emisión de rayos X de los diferentes elementos presentes en la misma al ser excitada con una radiación electromagnética adecuada. Esta técnica utiliza la emisión secundaria o fluorescente de rayos X generada al excitar la muestra con una fuente de rayos X de alta energía o con rayos gamma. Con esta técnica es posible determinar los elementos comprendidos entre el oxígeno y el uranio, tanto en muestras sólidas como en líquidos. Asimismo, mediante la utilización de los patrones adecuados, es posible realizar análisis cuantitativos. En este trabajo de investigación se ha utilizado el espectrómetro secuencial de rayos X PHILIPS MAGIX PRO (modelo PW1480) que incorpora el software analítico, SuperQ. El sistema está equipado con un tubo de rodio y una ventana de berilio. Los resultados obtenidos por FRX que se muestran en 18 Capítulo 2 la Memoria de esta Tesis Doctoral han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.4. Difracción de rayos X (DRX). La DRX es una de las técnicas más antiguas y más usadas dentro de la caracterización de catalizadores. Esta técnica se utiliza para identificar y caracterizar las fases cristalinas. Los rayos X son una forma de radiación electromagnética de elevada energía y corta longitud de onda, del orden de los espacios interatómicos en los sólidos. Cuando un haz de rayos X incide sobre un sólido, parte del haz se dispersa en todas direcciones por efecto de la interacción con los electrones asociados a los átomos o iones que encuentra en el trayecto, pero el resto del haz puede dar lugar al fenómeno de difracción de rayos X si existe una disposición ordenada de átomos o iones. En el caso de sólidos cristalinos, el solapamiento de los diferentes frentes de onda difractados por las sucesivas capas de átomos o iones puede dar lugar a interacciones constructivas o destructivas. En 1912, W.L. Bragg [4] estableció que una interacción es constructiva si se cumplen las condiciones representadas por la denominada ley de Bragg (Ecuación 2.4), que relaciona la longitud de onda de los rayos X y la distancia interatómica con el ángulo de incidencia del haz difractado. (Ecuación 2.4) donde λ es la longitud de onda de la radiación empleada, dhkl es el espaciado cristalino, n es el orden de difracción y θ es el ángulo de incidencia del haz de rayos X difractado. La representación de la intensidad de la radiación tras interaccionar con la muestra frente al ángulo de incidencia (habitualmente 2θ) se denomina difractograma, y es característico de cada fase cristalina. Esta técnica es de gran utilidad para dilucidar estructuras cristalinas, ya que aporta información sobre su estructura y la posición de los átomos en la red [4]. Sin embargo, esta técnica presenta una limitación importante para su uso en catálisis, ya que no permite analizar fases cristalinas con tamaños inferiores a 4 nm [5]. La cristalinidad de la muestra se puede deducir de la anchura del pico, que disminuye al aumentar la cristalinidad, es decir, al aumentar el tamaño de cristal. La ecuación de Scherrer (Ecuación 2.5) permite determinar el tamaño medio de los cristales (D) de un sólido cristalino [6]. (Ecuación 2.5) 19 Técnicas de caracterización y de determinación de la actividad catalítica. donde λ es la longitud de onda de la radiación empleada para obtener el difractograma, θ es el ángulo de difracción, K es la constante de Scherrer o factor de forma y β es la anchura del pico a media altura, expresada en radianes. El parámetro K puede variar entre 0,89 y 1,39 [7]; para los óxidos de cerio sintetizados en esta memoria se ha utilizado el valor de 0,94. A partir de los picos que se recogen en el difractograma de rayos X de y la ley de Bragg, se puede calcular el valor del espaciado cristalino (dhkl). El parámetro dhkl depende del sistema cristalino, y está relacionado a su vez con los parámetros de red a través de diversas fórmulas. Para un sistema con estructura cúbica podemos obtener el parámetro de red, a partir de dhkl, mediante la Ecuación 2.6 [8]. (Ecuación 2.6) donde a es el tamaño de arista de la celdilla cúbica, y h, k, y l son los índices de Miller de un plano cristalino determinado. Concretamente, en el caso del óxido de cerio se utilizó el plano (111). Las muestras han sido analizadas en un difractómetro marca Bruker, modelo D8-Advance, provisto de un generador de rayos X KRISTALLOFLEX K 760-80F que suministra, en condiciones estándar de medida, una tensión de 40 kV y una corriente de 40 mA (1,6 kW de potencia) a un tubo de rayos X de ánodo de cobre con espejo Göbel para análisis de muestras no planas. Se ha empleado una velocidad de barrido de 1º·min-1, con un incremento de paso de 0,05º, un tiempo de parada por paso de 3 segundos y un barrido angular de 2 θ = 20 a 80º. Los resultados obtenidos por DRX que se muestran en la Memoria de esta Tesis Doctoral han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.5. Espectroscopía Raman. La espectroscopía Raman es una técnica fotónica que proporciona información química y estructural de materiales orgánicos e inorgánicos, permitiendo su identificación. Esta técnica es útil en el estudio de la estructura dinámica de los diferentes estados de la materia, en particular, del estado cristalino. El estudio mediante espectroscopía Raman se basa en analizar la radiación dispersada por un material al incidir sobre él un haz monocromático. Una fracción de la radiación se dispersa inelásticamente, produciendo ligeros cambios de frecuencia que son característicos del material evaluado, independiente de la frecuencia de la luz incidente. 20 Capítulo 2 La mayoría de los estudios realizados con espectroscopía Raman están dedicados a los óxidos, para los que se obtiene información sobre su estructura y cristalinidad. El dispositivo empleado en este trabajo es un espectrómetro FT-Raman de la marca Bruker RFS/100. Este equipo posee una fuente de excitación láser en el infrarrojo cercano (1064 nm, Nd-YAG) que lo hace especialmente adecuado para el análisis de muestras que presenten problemas de fluorescencia en el visible y de un detector de Ge refrigerado por nitrógeno líquido. Además, la unidad dispone de una cámara de ambiente controlado Linkam FTIR600 en la cual se puede fijar la temperatura desde 77 K hasta 823 K, así como controlar la atmósfera en la cual se adquiere el espectro. Los espectros Raman fueron obtenidos utilizando condiciones distintas según el tipo de muestra utilizada. En el caso de las muestras con un efecto Raman muy intenso, se utilizó una potencia del láser de 100mW y 32 barridos, mientras que para otras muestras (menos intensas, por ejemplo, las que tienen más niobio) se utilizaron 200mW y entre 128 y 256 barridos. Los experimentos de espectroscopía Raman presentados en la presente memoria de Tesis Doctoral han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.6. Microscopía electrónica de barrido (SEM). La microscopía electrónica de barrido es una técnica que aporta información morfológica y topográfica de la superficie de un sólido. En este trabajo, el análisis de los catalizadores soportados se realizó con un microscopio HITACHI S-3000N. El equipo consta de un detector de electrones secundarios tipo centelleador-fotomultiplicador con resolución de 3,5 nm, un detector de electrones retrodispersados tipo semiconductor con resolución de 5 nm y un detector de rayos X tipo XFlash 3001 de Bruker para microanálisis (EDS) y mapeo químico, capaz de detectar elementos de número atómico comprendido entre los del C y el U. Las imágenes de microscopía electrónica de barrido presentadas en la presente Memoria de Tesis Doctoral han sido realizadas en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.7. Microscopía electrónica de transmisión (TEM). La microscopía electrónica de transmisión (TEM) es una técnica de observación de alta resolución que utiliza un haz de electrones para visualizar las muestras, las cuales deben estar en forma de películas muy finas para 21 Técnicas de caracterización y de determinación de la actividad catalítica. poder ser observadas. En este trabajo, el análisis se realizó con un microscopio electrónico de transmisión marca JEOL, modelo JEM-2010, que trabaja en el modo de tensión de aceleración a 200 Kv. El microscopio lleva acoplado un sistema de microanálisis (EDS) de la marca OXFORD instruments, modelo INCA Energy TEM100. EL detector es de Si (Li), con un área de detección de 30 mm2 y una resolución de 142 eV. El microscopio está equipado con una cámara de adquisición de imágenes ORIUS SC600 de la marca GATAN, que está integrada dentro del programa de adquisición y tratamiento de imágenes. Las muestras fueron suspendidas en etanol y se colocaron en rejillas de cobre de 300 mesh recubiertas con una película de carbono agujereado (lacey carbon) para ser analizadas en el TEM. Las imágenes de microscopía electrónica de transmisión presentadas en la presente Memoria de Tesis Doctoral han sido realizadas en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.8. Espectroscopía fotoelectrónica de rayos X (XPS). Uno de los aspectos más relevantes en la caracterización de catalizadores es el estudio de su composición química superficial. La espectroscopía fotoelectrónica de rayos X se basa en el análisis de los electrones emitidos desde las capas más internas de un átomo al ser irradiado con un haz de longitud de onda lo suficientemente pequeña. El análisis de la energía cinética de los electrones emitidos, que está relacionada con la energía de ligadura de dicho electrón al átomo del que procede, ofrece información sobre las especies superficiales del material analizado. Con esta técnica se pueden analizar muestras sólidas tanto cualitativa como cuantitativamente; además, permite generalmente la identificación de los diferentes estados químicos de un elemento, e incluso apreciar diferencias energéticas según el entorno en el que se encuentre el átomo [6]. Los análisis de espectroscopía fotoelectrónica de rayos X han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. El equipo usado fue un VG-Microtech Mutilab 3000 equipado con un analizador de electrones semiesférico con 9 channeltrons (con energía de paso de 2-200 eV) y una fuente de radiación de rayos X con ánodos de Mg y Al. Se ha empleado una radiación de MgKα (hν = 1253,6 eV, 1 eV = 1,6302·10-19) de 300 W, trabajando con el detector en modo de energía constante con una energía de paso de 50 eV. Previamente a la realización del análisis, la muestra en forma de polvo se prensó mediante un sistema de prensado cilíndrico de acero inoxidable para conseguir discos de muestra de 16 mm. El equipo utilizado dispone de una cámara de pre-tratamiento que puede regular la 22 Capítulo 2 temperatura, permitiendo obtener datos de XPS antes y después de llevar a cabo un tratamiento térmico in situ. La intensidad de las diferentes contribuciones se estima mediante el cálculo de la integral de cada pico, previa substracción de la línea base (S). El ajuste de la curva experimental se realiza con una contribución de curvas con forma Lorentziana (30%) y Gausiana (70%). Las energías de ligadura descritas para cada especie están referidas a la línea del C1s que aparece a 284,6 eV. Los valores de energía de ligadura obtenidos tienen una precisión de ± 0,2 eV. Los valores de la energía de ligadura y la energía cinética fueron ajustados con el software Peak-fit. Los resultados obtenidos por XPS que se muestran en la Memoria de esta Tesis Doctoral han sido realizados en los Servicios Técnicos de Investigación de la Universidad de Alicante. 1.9. Reducción a temperatura programada con H2 (RTP-H2). La reducción a temperatura programada con H2 es una técnica que permite obtener información sobre el proceso de reducción de los diferentes componentes de un sólido. Mediante esta técnica se puede obtener información acerca del grado de interacción entre la fase activa y el soporte, y determinar la extensión de la interacción de las especies metálicas, así como estudiar la posibilidad de formación de aleaciones y/o compuestos intermetálicos. Para la obtención de los perfiles de reducción se utilizó un montaje diseñado en el Laboratorio de Materiales Avanzados. El sistema está compuesto por un reactor de cuarzo en forma de U donde se deposita una cantidad de muestra de aproximadamente 100 mg. Inicialmente, las muestras se limpian a 423 K durante 1 h con un flujo de He de 50 ml·min-1; posteriormente se dejan enfriar hasta temperatura ambiente y se cambia el flujo de helio por el de un gas con una composición 95 % He/5 % H2 con un caudal de 50 ml·min-1. El sistema se calienta con una velocidad de 10 K·min-1 hasta 1273 K. Los gases a la salida del reactor se conducen a través de tuberías de acero calefactadas hasta un espectrómetro de masas de la marca Pfeiffer. La cuantificación de la cantidad de hidrógeno consumida se calculó a partir de un calibrado del sistema con una muestra de CuO. 1.10. Desorción a temperatura programada de CO/CO2 (DTP-CO/CO2). La desorción a temperatura programada es una técnica que se utiliza generalmente para estudiar la evolución térmica de diferentes moléculas quimisorbidas en la superficie de catalizadores y/o soportes. A partir de este estudio se puede obtener información sobre la interacción química de estas moléculas con el metal dispersado y con el soporte. 23 Técnicas de caracterización y de determinación de la actividad catalítica. Para la obtención de los perfiles de desorción de CO y CO2 se utilizó el mismo montaje en el que se realizaron los experimentos de RTP en hidrógeno. Para cada ensayo se utilizaron aproximadamente 100 mg de muestra, previamente reducida a 523 K durante 1 h en un flujo de H2 de 50 ml·min-1; y con una rampa de calentamiento de 5 K·min-1. Posteriormente se cambia el flujo de hidrógeno por otro de helio y la muestra se deja enfriar. Una vez alcanzada la temperatura ambiente, se realiza la adsorción de CO utilizando una mezcla con una composición de 10 % CO/He, con un flujo de 50 ml·min-1, durante 1 h. A continuación, se cambia el flujo de gas CO/He por helio, manteniendo un caudal de 50 ml·min-1 con el fin de eliminar el CO que se queda en exceso en el reactor y el que esta fisisorbido en la muestra. Finalmente, la desorción del CO que quedó quimisorbido en la muestra se realiza por calentamiento a una velocidad de 10 K·min-1 hasta 773 K. Los gases a la salida del reactor se conducen a un espectrómetro de masas para su análisis. La cantidad de CO y de CO2 se calculó a partir de un calibrado del sistema utilizando como patrón de referencia oxalato de calcio monohidratado (CaC2O4·H2O). 1.11. Desorción a temperatura programada de H2 (DTP-H2). Con los experimentos de desorción de H2 a la temperatura programada se puede obtener información acerca de dos importantes aspectos considerados en la quimisorción de hidrogeno H2, la capacidad de quimisorción del metal y las características del fenómeno de spillover que ocurre en estos catalizadores [9]. Para la obtención de los perfiles de desorción de H2 se utilizó el mismo montaje y las mismas condiciones del experimento de DTP-CO/CO2, en este caso cambiando el CO por H2 en la corriente de helio y la desorción del H2 que quedó quimisorbido en la muestra se realiza por calentamiento a una velocidad de 10 K·min-1 hasta 1273 K. 1.12. Espectroscopía infrarroja de reflectancia difusa con transformada de Fourier y cámara de reacción in situ (DRIFTS in situ). El principio de funcionamiento de la espectroscopía infrarroja se basa en el hecho de que los movimientos de rotación y vibración moleculares tienen niveles de energía discretos. Las frecuencias vibracionales vienen determinadas por la energía potencial de la molécula, la masa del átomo y, eventualmente, por el acoplamiento vibracional asociado. Como consecuencia, la frecuencia de vibración puede ser asociada con un tipo particular de enlace. 24 Capítulo 2 Por lo tanto, la excitación de los modos de vibración y rotación de los enlaces entre átomos, al ser irradiados con un haz de luz infrarroja producen, según las características de sus enlaces, absorción de radiación de una o varias longitudes de onda específicas, por lo que la especie puede ser identificada. La espectroscopía de reflectancia difusa es una técnica que se utiliza para analizar sólidos. Al irradiar un sólido pulverulento, la radiación penetra a través de la superficie, excita los modos de vibración de las distintas especies presentes y dispersa la radiación en todas las direcciones, produciéndose un espectro de reflectancia que dependerá de la composición de la muestra. El análisis por medio de espectroscopía infrarroja de reflectancia difusa con transformada de Fourier se ha utilizado para evaluar las especies adsorbidas en el catalizador en condiciones de reacción. Para los ensayos de reacción seguidos con DRIFTS in situ se utilizó un espectrómetro modelo Perkin-Elmer 100 FTIR con detector MCT, acoplado a un espectrómetro de masas de modelo Baltzers Prisma Quadrupole. La celda de DRIFTS (Harrick DRP-series) fue ajustada con una ventana de ZnSe. El procedimiento experimental consistió inicialmente en un tratamiento de reducción de la muestra a 523 K con un flujo de 40 ml·min-1 de una mezcla 33 % H2/N2, durante 1 h, con una velocidad de calentamiento de 5 K·min-1. Posteriormente, se bajó la temperatura en la cámara hasta 313 K. Una vez estabilizada esta temperatura se reemplazó el gas por una mezcla de reacción compuesta por 20% de H2, 2% CO, 10% aire y balance con N2. El flujo de reacción utilizado fue de 40 ml·min-1, con una (gas hourly space velocity) GHSV = 17000 h-1. El experimento se realizó manteniendo las mismas condiciones de velocidad espacial utilizadas en los ensayos catalíticos. La temperatura de la reacción utilizada fue de 313–473 K, con una rampa de calentamiento de 2 K·min-1, registrando espectros sucesivos tras diferentes tiempos de exposición de la muestra a la mezcla de gases reactiva a cada aumento de 20 K. Los espectros fueron registrados a una resolución de 4 cm-1 y con 10 repeticiones, entre 900 cm-1 y 4000 cm-1. Los experimentos de DRIFTS presentados en la presente memoria de Tesis de Doctorado han sido realizados en el grupo Surface Chemistry and Catalysis en el Departament of Chemistry de la University of Aberdeen, en Escocia. 25 Técnicas de caracterización y de determinación de la actividad catalítica. 2. Ensayos catalíticos. Para realizar los ensayos catalíticos se utilizó el sistema experimental que se muestra en la Figura 2.1, compuesto por una unidad de reacción y una unidad de análisis de gases (cromatógrafo de gases) acoplada on-line. La unidad de reacción está constituida por una serie de controladores de flujo másico, de la marca Brooks, que regulan de forma autónoma el caudal de las cinco balas de gases que contienen He, H2, CO, O2 y CO2, respectivamente, como gases de alimentación. El sistema contiene un saturador donde se adiciona agua ultra pura, el cual está recubierto por un baño que mantiene la temperatura constante. Los gases de entrada pasan por el saturador y arrastran el agua para ser utilizada en la reacción. La unidad de reacción consiste en un reactor de cuarzo en forma de U, donde se deposita la muestra. El reactor se sitúa en el interior de un horno. El sistema de reacción dispone de dos termopares, uno que registra la temperatura de la muestra y otro que controla la temperatura del horno. La salida del reactor está conectada a un cromatógrafo de gases de la marca Agilent Technologies, modelo 7890A, dispuesto con dos válvulas de 6 vías y dos columnas de separación Molesieve y Plot-Q, un detector de conductividad térmica (TCD) y un detector de ionización de llama (FID), para analizar los productos de reacción. Debido a la posibilidad de formación de agua proveniente de la oxidación del H2 se hace necesario el uso de dos columnas de separación, una para separar los dos principales productos formados, CO2 y H2O (Plot-Q), ya que ésta es específica para soportar condiciones de humedad, y la otra para los demás reactivos y productos, H2, O2, CH4 y CO (Molesieve). El funcionamiento del cromatógrafo con las dos columnas es el siguiente: los productos de reacción que salen del reactor se introducen de manera continua en el loop de la válvula de inyección. En la primera etapa del programa todos los productos de reacción son inyectados en la columna PlotQ (columna 1). Esta inyección va acompañada de un incremento en la temperatura del horno desde 323 K hasta 373 K, con el objetivo de garantizar que toda el H2O inyectada sea eliminada de esta columna al finalizar el análisis. En el tiempo de retención de 2,45 min. CO, H2 y O2 pasan a la siguiente columna, Molesieve (columna 2), mientras que el H2O y el CO2, productos más rezagados, permanecen retenidos en la primera columna. En ese momento, en el tiempo de retención 8 min., se acciona la válvula que une ambas columnas, de tal manera que la columna 2 queda aislada y los productos remanentes en la columna 1 (H2O y CO2) son enviados directamente al detector. Una vez estas especies han alcanzado el detector, la válvula 26 Capítulo 2 intermedia se acciona de nuevo para que los productos de la columna 2 alcancen el detector. Los tiempos de retención obtenidos para los diferentes gases son los siguientes: CO2 – 2,8 min.; H2O – 6,2 min; H2 – 9,4 min; O2 – 9,6 min. y CO – 10,9 min. Esta configuración de válvulas y columnas permite la separación de los diferentes componentes de los productos de reacción, e incluso la doble detección de productos ligeros sensibles al FID, como el metano. Mediante el calibrado de cada uno de los gases, las señales obtenidas del análisis cromatográfico y el flujo de salida, se calcula la concentración de cada gas. Figura 2.1. Esquema del sistema de reacción acoplado a un cromatógrafo de gases. Para los ensayos catalíticos se utilizaron mezclas de reacción compuestas por diferentes gases, con concentraciones que se muestran en la Tabla 2.1; el balance se completa con He. Para todas las proporciones de gases se utilizó un flujo total de 50 ml·min-1 y velocidades espaciales de 17000 h-1. Para realizar los ensayos catalíticos se utilizaron aproximadamente 100 mg de muestra. Previamente a los experimentos de reacción, las muestras fueron reducidas insitu a diferentes temperaturas, según cada catalizador. Los detalles sobre la temperatura de reducción se presentarán en el capítulo correspondiente. 27 Técnicas de caracterización y de determinación de la actividad catalítica. Tabla 2.1. Composiciones de los gases de entrada. Gas Porcentaje, % H2 20 CO 1-2 O2 0,6-4 CO2 0-5 H2O 0-5 Para determinar la actividad catalítica de las muestras se realizaron dos tipos de experimentos, que se describen a continuación. 2.1. Reacción a temperatura programada. Los experimentos se realizaron desde una temperatura inicial de 313 K, la cual se mantiene constante durante un tiempo determinado (45 minutos, aproximadamente). A continuación se incrementa la temperatura a una velocidad de 2 K·min-1 hasta 333 K, manteniendo esa temperatura constante durante 45 min, y se repite el mismo procedimiento hasta alcanzar 473 K, siempre a incrementos de 20 K. Este tipo de experimentos proporcionan información sobre la actividad de los catalizadores en un amplio rango de temperaturas, y permite determinar la temperatura a la que se obtiene la velocidad de reacción más elevada. 2.2. Reacción a temperatura constante. Este experimento permite evaluar el comportamiento del catalizador en unas condiciones más cercanas a las de la operación real. En los experimentos a temperatura constante se mantuvo la reacción durante algunas horas. Es importante resaltar que para los catalizadores estudiados en este trabajo no se observó la formación de metano, y los resultados obtenidos fueron perfectamente reproducibles. Los valores de conversión de CO y O2, así como de selectividad hacia la formación de CO2, fueron calculados utilizando las siguientes ecuaciones: 28 Capítulo 2 (Ecuación 2.7) (Ecuación 2.8) (Ecuación 2.9) 3. Referencias. [1] S. Brunauer, P.H. Emmett, E. Teller, J. Am. Chem. Soc. 60 (1938) 309-319. [2] J. Sutherland, Porous Carbon Solids, Academic Press, Londres (1967). [3] S. J. Gregg, K. S. W. Sing, Adsorption, Surface Area and Porosity, Academic Press, Londres (1982). [4] P.W. Atkins, Physical Chemistry, Oxford University Press, Oxford (1995). [5] J.W. Niemantsverdriet, Spectroscopy in Catalysis, Ed. 3, Wiley, Germany (2007). [6] D.A. Skoog, J.J. Leary, Análisis Instrumental, McGraw-Hill, España (1993). [7] L.N. Ikryannikova, A.A. Aksenov, G.L. Markaryan, G.P. Muraveva, B.G. Kostyuk, A.N. Kharlanov, E.V. Lunita, Appl. Catal. A: Gen. 210 (2001) 225–235. [8] M.R. Gallego, La Difracción de los Rayos X, Alambra, España (1982). [9] A. Trovarelli, Catalysis by ceria and related materials, Ed. 2, Imperial College Press, London (2002). 29 30 Chapter 3 CHAPTER 3 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). Abstract. In this chapter, a study on the effect of the metallic precursor (presence or absence of chlorine) in the preferential oxidation of CO in the presence of H2 on Pt/CeO2 catalysts is reported. The catalysts have been prepared using two different Pt precursors, [Pt(NH3)4](NO3)2 and H2PtCl6, in order to ascertain the actual effect of the chlorine species in the chemical properties of the support and the catalytic behaviour of these systems in the preferential oxidation of CO in hydrogen excess. The results show that chlorine species exert an important effect on the redox properties of the oxide support, due to the formation of CeOCl species. Furthermore, the chlorinated catalyst exhibits a poor catalytic activity at low temperatures as compared to the chlorine-free catalyst, which is accompanied by a higher selectivity to CO2, even at high reaction temperatures. It is proposed that the CO oxidation mechanism follows different pathways depending on the catalyst used. 31 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). 1. Introduction. In the last few years there has been a growing interest on ceria based catalysts such as CeO2-supported metals or CeO2-containing mixed oxides with fluorite-type structure. High attention has been devoted to the characteristics of the active phase and promoters present on these systems. A large number of systems involving ceria supported noble metals (NM), mainly platinum, palladium, gold and ruthenium, have been investigated [1]. This specific interest on NM/CeO2 catalysts is due to the relationship existing between these model systems and the three way catalysts (TWC) used in the control of the exhaust emissions from spark-ignited motor vehicles. The catalytic performance of these catalysts has been studied in the PROX reaction. In this sense, partially reducible oxide supports, such as ceria, are good candidates to be used in CO oxidation reactions due to their high oxygen storage capacity (OSC) [2][3][4][5]. Several mechanisms have been proposed in the literature for the PROX reaction, which may depend on the catalyst support used. For example, Mariño et al. [6][7] have shown that the CO oxidation mechanism with non-active supports occurs via a competitive Langmuir-Hinshelwood mechanism, where CO and O2 compete for the same adsorption site. However, when a reducible metal oxide is used as a support, the oxygen functionalities of the support participate in the reaction, via a Mars-Krevelen mechanism [6][7][8]. Pozdnyakova et al. [9] suggested that the reaction mechanism in Pt/CeO2 catalysts takes place via surface -OH groups. Its presence seems to suppress hydrogen oxidation while CO oxidation still takes place, as the metallic particles are covered by CO. This behaviour minimizes the possibility of a direct reaction mechanism between adsorbed CO and O2. Quinet et al. [10] suggested that the reaction mechanism over Au/Al2O3 catalysts involves -H, -OH and -OOH intermediates adsorbed on gold particles, and bicarbonates, carboxylates and hydroxycarbonyls adsorbed either on the metal nanoparticles or at the metal-support interface. Daté et al. [11] showed the effect of the presence of humidity in the reaction mixture on CO oxidation at low temperature on Au/TiO2, Au/Al2O3 and Au/SiO2 catalysts. In this case, the presence of H2O or –OH groups contributes to increase the reaction rate. In this chapter we will study the catalytic behaviour of Pt/CeO2 catalysts in the CO oxidation reaction in the presence of H2. More specifically, we will study the effect of the nature of the metal precursor by comparing catalysts prepared with a Cl-containing and a Cl–free precursor. Besides the support 32 Chapter 3 characteristics, it is well known that the nature of the metal precursor used is important because it can induce chemical and structural changes. Furthermore, catalysts prepared from chlorine-containing precursors are able to incorporate a large amount of chloride ions into the support [12][13]. Kepinski et al. [13] studied the mechanism of CeOCl formation in Pd/CeO2 catalysts prepared using a chlorinated precursor, PdCl2. These authors suggested that at low reduction temperatures Cl - ions remain strongly chemisorbed on ceria. However, an increase in the reduction temperature produces a progressive incorporation of the chloride ions into the oxygen vacancies of the support. According to high-resolution transmission electron microscopy (HRTEM) studies, it was possible to identify CeOCl species after reduction at temperatures between 423 and 573 K. An increase in the reduction temperature up to 673 K produced the growing of these CeOCl crystallites, as confirmed by X-ray diffraction (XRD). Moreover, jointly with the growing of the CeOCl crystals, an important loss of the catalyst surface area was observed. This fact indicates that the incorporation of the chlorine ions induces changes in the textural, structural and chemical properties of the support. From the described results, it is possible to anticipate that the support characteristics and the metal precursor used will have a large influence on the CO oxidation reaction mechanism. With this in mind, in this study we will evaluate the effect of the metal precursor in the CO oxidation reaction on Pt/CeO2 catalysts. Catalytic activity will be monitored by gas chromatography and diffuse reflectance infrared Fourier transform spectroscopy (DRIFTS) analysis with online mass spectrometry. 2. Experimental. 2.1. Catalysts preparation and characterization. The cerium oxide support was prepared by the homogeneous precipitation method. 13 g of Ce(NO3)3·9H2O (Aldrich, 99%) and 8 g of urea (Fluka, 98 %) were dissolved in 400 ml of ultrapure water. The mixture was heated at 363 K with constant stirring during 11 h. Finally, some ammonium hydroxide solution was added dropwise to complete precipitation. The solid was separated by filtration, washed with ultrapure water, and finally dried at 383 K overnight. The powder sample was calcined in air at 773 K for 4 h, with a heating rate of 3 K·min−1. Two different Pt/CeO2 catalysts were prepared by the wetness impregnation method. The support was impregnated with 33 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). aqueous solutions of [Pt(NH3)4](NO3)2 (Aldrich, 99.9%) or H2PtCl6 (Alfa Aesar, 99.9%), with the appropriate concentrations to achieve a 1 wt.% Pt loading. Finally, the catalysts were dried overnight at 383 K and calcined in air at 773 K for 2 h, with a heating rate of 3 K·min−1). The support and the catalysts were characterized by different techniques. N2 adsorption at 77 K was used to determine the specific surface areas, after application of the BET method. The metal content was determined by X-ray fluorescence (XRF) and inductively coupled plasma optical emission spectroscopy (ICP-OES). X-ray powder diffraction (XRD) was used to identify the crystalline phases present in the solid. Transmission electron microscopy (TEM) observations were performed to study the size of the ceria crystals and of the Pt nanoparticles. Temperature-programmed reduction experiments with H2 (H2-TPR) were carried out in order to study the reducibility of both the support and the Pt nanoparticles, which is an indirect measurement of the metal-support interactions. X-ray photoelectron spectroscopy (XPS) was used to identify the atomic species and their abundance on the catalyst surface. XPS also allows identifying the different chemical states (oxidation states) of the different surface species. Temperature-programmed desorption experiments of CO/CO2 (CO/CO2-TPD) were used to determine the thermal evolution of CO molecules chemisorbed on Pt/CeO2 catalysts together with the ability of the catalyst to oxidize the adsorbed CO to CO2 with oxygen from the support (in an inert atmosphere). Experimental details and equipments used were described in Chapter 2 of this Thesis. 2.2. Catalytic behaviour. In a first step, the catalytic activity of the different samples in the PROX reaction was evaluated at different reaction temperatures (303-473 K), at atmospheric pressure and under a gas flow (50 cm3·min−1) containing 20% H2, 2% CO, 0.6-2% O2 and He as a balance (GHSV = 17000 h-1). Reaction products were analyzed by on-line gas chromatography. For a more detailed analysis of the reaction process taking place, the catalytic measurements were also performed in a reaction chamber equipped with diffuse reflectance infrared Fourier transform spectroscopy (DRIFTS). In the same way as before, the catalytic measurements were performed at different temperatures (313-473 K), at atmospheric pressure and under a gas flow (40 cm3·min−1) containing 20% H2, 2% CO, 10% O2 air and N2 as a balance (GHSV = 17000 h-1). 34 Chapter 3 Experimental details concerning the calculation of CO and O2 conversion, as well as the selectivity and the equipments used, were described in Chapter 2 of this Thesis. 3. Results and discussion. 3.1. Textural and metal loading characterization. Table 3.1 reports the BET surface area of the ceria support, as well as the platinum and chlorine content for the chlorine-free and the chlorinecontaining catalysts. The CeO2 support prepared by homogeneous precipitation with urea exhibits a very high surface area, around 110 m2·g-1, as compared with the same material prepared by other conventional methods (e.g. ammonia precipitation (SBET 70 m2·g-1)) [14]. As expected, chlorine remains in the Pt(Cl)/CeO2 catalyst, even after the calcination treatment at 773 K. Table 3.1. Physical properties of the synthesized catalysts. Catalysts SBET, m2·g-1 Pt, wt.% Cl, wt.% CeO2 110 --- --- Pt(N)/CeO2 n.m.* 1.0 --- Pt(Cl)/CeO2 n.m.* 1.0 0.7 (*n.m. – non measured) 3.2. X-ray diffraction (XRD). The crystallinity of the oxide support and the supported nanoparticles were analysed by X-ray diffraction. The XRD patterns of Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts are presented in Figure 3.1. For all samples it is possible to observe the six main characteristic peaks of the fluorite structure of CeO 2, which are assigned to the (111), (200), (220), (311), (222) and (400) diffraction planes [15][16][17][18]. The face-centred cubic unit cell presents a space group Fm3m [1]. In this structure, each cerium cation is coordinated to eight equivalent neighbour oxygen anions at the corner of a cube, each anion being tetrahedrally coordinated by four cations. The structure is illustrated in Figure 3.2 (a). Extending this structure by drawing cubes of oxygen ions at each corner reveals the eightfold cubic coordination of each cerium cation, which alternately occupies the elementary cell as a primitive cubic array of oxygen ions in which the eight coordination sites are alternately empty and occupied by a cation, Figure 3.2 (b) and (c). This fact shows that there are a large number 35 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). of vacant octahedral holes in the structure. This feature will be significant when considering the movement of ions through the defect structural sites. CeO2 Pt(Cl)/CeO2 Intensity, a.u. Pt(N)/CeO2 CeO2 20 30 40 50 2 60 70 80 Figure 3.1. X-ray diffraction profiles of CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2. Figure 3.2. The crystal structure of the CeO2: unit cell as a ccp array of cerium atoms. The ccp layers are parallel to the (111) planes of the f.c.c. unit cell (a), the same structure redrawn as a primitive cubic array of oxygens (b) and (c). No diffraction peaks for platinum could be identified for both catalysts (see Figure 3.1), this suggest a low platinum content or, more probably, a large Pt 36 Chapter 3 dispersion [2][15][19]. The crystal size for the ceria support, estimated by the Scherrer’s equation (Equation 2.5), was 17 nm. 3.3. Catalysts characterization by transmission electron microscopy (TEM) TEM images for Pt(N)/CeO2 and Pt(Cl)/CeO2 samples are shown in Figure 3.3. In accordance with XRD measurements, CeO2 exhibits a high crystallinity with a distance between planes of about 0.28 nm. The ceria particle size could not be calculated from the TEM images, due to the high crystal agglomeration which makes difficult the determination of the particle size distribution. Furthermore, the platinum particle size could not be quantified due to the high Pt dispersion (some small nanoparticles are identified by a circle in Fig. 3.3), in close agreement with XRD results. However, the presence of platinum nanoparticles was confirmed by EDS analysis. A similar observation was described in the literature for gold catalysts [20][21]. Small gold particles supported on ceria could not be detected by TEM due to the low contrast between the metal particle and the support. (a) (b) (c) 5 nm Figure 3.3. TEM images of CeO2 support (a), Pt(N)/CeO2 (b), Pt(Cl)/CeO2 (c). 3.4. Temperature-programmed reduction with H2 (H2-TPR). The reducibility of the different catalysts was studied by temperatureprogrammed reduction under hydrogen. H2-TPR profiles (hydrogen consumption) of CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts are shown in Figure 3.4. The CeO2 support exhibits two reduction peaks: one at 760 K and another one at 1050 K. These peaks are attributed to surface and bulk reduction processes, respectively [19][22][23]. Pt addition to the CeO2 support produces important changes in the TPR curves. It is well known that cerium oxide reduction involves several processes: i) the removal of surface carbonates [23], ii) a change in the cerium oxidation state (Ce (IV) to Ce (III)) and iii) formation of -OH groups by spillover of atomic hydrogen from Pt 37 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). [23][24]. Furthermore, in the presence of Pt the surface reduction of ceria is shifted to lower temperatures [19]. This phenomenon can be explained by the ability of the noble metal to dissociate hydrogen, thus promoting the ceria reduction through hydrogen spillover from the metal to the support [25]. Interestingly, both catalysts exhibit a reduction peak at low temperature. However, the shape of this contribution is slightly different in the presence and absence of chloride. For the chlorine-free catalyst, the hydrogen consumption peak shows a main contribution at 610 K, together with a shoulder at lower temperatures (575 K). These two contributions include the surface reduction of ceria in close contact with the noble metal and the reduction of Pt species [17]. On the contrary, the chlorinated catalyst exhibits a single reduction peak centred at 590 K, which can be assigned to the surface reduction of ceria in close contact with platinum, together with the breakdown of Pt-Ce-Cl entities formed after the calcination treatment [17]. As shown in Table 3.1, the catalyst prepared with the chlorinated platinum precursor still contains, after the calcination treatment, a large amount of chlorine which could affect the reducibility of the support and, similarly, the oxygen mobility. Similar TPR profiles were previously reported by our research group for PtZn/CeO2 catalysts prepared using two different Pt precursors (with and without chlorine) [17]. For the chlorine-free catalyst a broad hydrogen consumption peak was observed at low temperatures, which could be deconvoluted into two contributions. These two contributions were explained by the presence of a high surface heterogeneity. Furthermore, in the case of the chlorinated catalyst, a delay in the metal reduction was observed due to the formation of CeOCl entities, which inhibit the metal-support interactions [17]. DRIFTS studies (shown below in this chapter) demonstrate that the chlorine-free catalyst exhibits a larger ability for carbonate formation compared to the chlorinated catalyst. Consequently, the presence of an additional peak in the chlorine-free catalyst can also be associated to the involvement of these surface carbonate species in the reduction process at low temperature. Most probably, the reduction of carbonate to formate takes place at lower temperatures in the presence of Pt, through hydrogen spill-over phenomena. In this sense, it would be expected that this phenomena is inhibited in the presence of chlorine, due to formation of CeOCl species. Two reduction temperatures were selected from the TPR analyses for the pre-treatment of these catalysts before the reaction analysis, 523 K and 773 K. These temperatures were selected in order to analyse the effect of the reduction treatment at low temperature, where only surface reduction 38 Chapter 3 processes are expected, compared to the high temperature reduction treatment, where additional reduction processes, i.e. oxygen vacancies formation, are expected. It is well known that, in the case of the chlorinated catalyst, an increase in the reduction temperature favors the formation of CeOCl entities, thus increasing the amount of Ce (III) [13][26] and, consequently, the decrease of the OSC [17]. -1 0.001 mmol H2.s .g 590 K Pt(Cl)/CeO2 H2 consumption, a.u. 300 -1 610 K 575 K Pt(N)/CeO2 1050 K 760 K 400 500 600 700 800 900 1000 1100 CeO2 1200 Temperature, K Figure 3.4. H2-TPR profiles (H2 consumption) for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2. At this point it would be interesting to highlight the important effect of the chloride ions on the properties of the ceria support and the mechanism of formation of CeOCl entities. Previous studies reported in the literature have shown that the incorporation of chloride ions into the ceria lattice could inhibit the hydrogen spillover phenomena, and also influence to some extent the metal-support interactions [26]. In fact, the formation of CeOCl entities upon reduction in hydrogen has been proposed in different catalysts prepared with chlorinated precursors, although there is still some controversy concerning the actual mechanism of formation [13][17][26][27][28]. Fajardie et al. [26] studied Rh(Cl)/CeO2 catalysts and proposed two possible explanations to justify the high stability of the chloride ions in these systems after a high temperature reduction treatment in hydrogen: (i) a strong interaction of Cl - with Ce (III) ions formed during the reduction treatment (in this case, the chloride ions are 39 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). strongly bonded to the support surface, and could favor the formation of CeOCl species on the ceria surface [13]); (ii) the penetration of chloride ions into the lattice of reduced ceria to be accommodated into the oxygen vacancies generated during the reduction treatment. In this case, it could be expected the formation of CeOCl bulk entities. Apparently, above 523 K, the migration of chloride ions from the surface to the bulk oxygen vacancies is facilitated by the high ionic mobility. As chloride ions are larger than the oxide ions, the cubic cell of ceria is deformed upon chlorine incorporation to a tetragonal CeOCl arrangement. According to these authors, the incorporation of chlorine to Rh/CeO2 catalysts and the formation of CeOCl entities follow four steps (see Figure 3.5). For a reduction temperature below 523 K, Rh2O3 is reduced to Rh (0) in a first step. In a second step, the formation of surface oxygen vacancies takes place by ceria surface reduction with atomic hydrogen coming from the Rh (0) nanoparticles. Above 523 K, the chloride ions start to migrate to the bulk of the ceria support, these ions being incorporated into the oxygen vacancies created on the reduced ceria. Finally, the formation of CeOCl entities inhibits hydrogen migration to the core of the support particle, thus preventing the complete reduction of the ceria support. A similar mechanism was proposed by Kepinski et al. [13]. Figure 3.5. Mechanism proposed for the incorporation of chloride ions into the ceria lattice and the formation of CeOCl phase by Fajardie et al. [26]. Theoretical calculations [13] have shown that the energy of oxygen vacancy formation on the surface of CeO2 highly depends on the crystallographic structure; it is three times lower on (110) than on (111), the last one being equal to the energy of the vacancy formation at the bulk. A reduction treatment at low temperatures will favor the reduction of (110) faces in such a way that every second row of O2- ions in the (110) surface (showed as a dark blue circle in the Figure 3.6, second line) could be replaced by chloride ions. After the 40 Chapter 3 complete rearrangement of all the atoms (chloride ions (0.181 nm) are much larger than oxide ions (0.135 nm)), the formation of CeOCl (010) entities is possible (see Figure 3.6). Figure 3.6. Structure relationship between CeO2 (110) and CeOCl (010) surfaces [13]. It is interesting to mention that, according to this mechanism, the presence of noble metal is not essential for the formation of CeOCl species. However, the hydrogen spillover phenomena´s facilitates the surface reduction at low temperature and the formation of CeOCl. Finally, Force et al. and Bernal et al. [27][28] suggested that the incorporation of chloride ions is based on the surface exchange of OH- by Clions. During the reduction treatment of Rh/CeO2 catalysts, atomic hydrogen spilt over the support favors the formation of surface OH- groups. These OHgroups are expected to be progressively removed with temperature, with the subsequent formation of anion vacancies. Interestingly, the elimination of hydroxyl groups is favored at a lower reduction temperature for chlorinated catalysts, thus suggesting a destabilization of hydroxyl groups by chlorine species by a OH- -Cl- exchange mechanism. The scheme of the suggested reaction mechanism is shown in the Figure 3.7. Chlorine free catalyst Chlorine catalyst Rh O2- [ ] O2Ce4+ Ce3+ Cl[] Rh Rh O2- O2- O2- Ce4+ Ce4+ O2- [ ] O2- - H2 O Ce4+ Ce3+ + ½ H2 H+ Rh OH- Cl- O2- O2- O2Ce4+ Ce3+ Figure 3.7. Scheme for the mechanism proposed for the incorporation of chlorine ions into the lattice ceria suggested by Force [27]. 41 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). At this point it is interesting to add that all the mechanisms cited could take place in our sample, being difficult to determine exactly which one is the predominant one. 3.5. X-ray photoelectron spectroscopy analysis (XPS). The surface composition of the catalysts and the oxidation state of cerium were determined by XPS. Figure 3.8 (a) and (b) show the Ce 3d XPS spectra obtained with catalysts Pt(N)/CeO2 and Pt(Cl)/CeO2, respectively, both fresh and after an in situ reduction treatment at 523 and 773 K. The spectra for the Ce 3d level have been studied by different authors, and their interpretation is not straightforward [17][23][29][30][31]. The complexity of the Ce 3d spectra, which was first resolved by Burroughs et al. [31], is due to the hybridization between the Ce 4f levels and the O 2p states. The two sets of spin-orbital multiples, corresponding to the 3d3/2 and 3d5/2 contributions are labeled u and v, respectively, and up to four peaks for each contribution can be obtained by a curve fitting analysis. The peaks labeled v and v´´ have been assigned to a mixing of Ce 3d9 4f2 O 2p4 and Ce 3d9 4f1 O 2p5 Ce (IV) final states, and the peak denoted v´´´ corresponds to the Ce 3d9 4f0 O 2p6 Ce (IV) final state. On the other hand, lines v and v´ are assigned to the Ce 3d9 4f2 O 2p5 and the Ce 3d9 4f1 O 2p6 of Ce (III). The same assignation can be applied to the u structures, which corresponds to the Ce 3d3/2 levels. 0 XP spectra allow the determination of the percentage of Ce (III) present in the catalyst surface, together with the oxidation state of the different species as a function of the reduction temperature. Previous studies described in the literature have reported different approaches to evaluate the degree of CeO 2 reduction by XPS. As a first approach, some authors have used the contribution of the u´´´ peak to the total Ce 3d region to calculate the total amount of Ce (IV) in the sample [32][33][34]. However, it has been shown that this approach leads to erroneous quantitative results [35]. The second approach takes into consideration the relative intensity of the u0 (v0) and u´(v´) peaks, as representative of Ce (III), in the total Ce 3d region [36][37][38]. In this way, the degree of ceria reduction can be calculated, after deconvolution of the experimental spectra, by the ratio between the sum of the intensities of the u0, u´, v0, and v bands and the sum of the intensities of all the bands, Equation 3.1, [29][30][31]. (Equation 3.1) 42 Chapter 3 u´´´ (a) v v0 v´ v´´ u v´´´ u0 u´ u´´ Intensity, a.u. Fresh RT 523 K RT 773 K 880 890 900 910 920 Binding energy, eV u´´´ (b) v v0 v´ u0 v´´ v´´´ u u´ u´´ Intensity, a.u. Fresh RT 523 K RT 773 K 880 890 900 910 920 Binding energy, eV Figure 3.8. XPS spectra of Ce 3d region for the Pt(N)/CeO2 (a) and Pt(Cl)/CeO2 (b) catalysts both fresh and with the reduced temperature (RT) at 523 and 773 K. The XP spectra obtained for the two catalysts after different reduction treatments are plotted in Figure 3.9, and the data extracted from them are reported in Table 3.2. Interestingly, there is a certain amount of Ce (III) already in the fresh (calcined) catalysts, i.e. 35 and 36 % of Ce (III) for the Cl-free and Cl-containing catalyst, respectively. The presence of Ce (III) in the calcined catalyst has been attributed to the high energy of the X-ray beam, 43 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). which can produce the partial reduction of Ce (IV) ions during the XPS analysis [17][29][34]. A similar behaviour has been reported in the literature by Francisco et al. for CeTiOCu catalysts [37]. It is well known that one of the parameters that affect the photo-reduction of CeO2 during the XPS analysis is its crystallinity, in such a way that amorphous cerium oxide is reduced more extensively than crystalline cerium oxide [37]. However, taking into account that the same support has been used for the preparation of the two Pt/CeO 2 catalysts described in this chapter, and that the XPS analysis has been performed under the same experimental conditions, then it can be assumed that Ce (IV) photo-reduction due to the X-ray beam should be similar for both catalysts, the observed differences among them being only attributed to their distinctive chemical composition. Data in Table 3.2 show that the extent of Ce (IV) reduction increases after a reduction treatment at 523 K. The percentage of Ce (III) in these samples is close to 41 % and 38%, for the chlorine-free and the chlorinated catalyst, respectively. Interestingly, these values remain mainly unaffected after a further increase in the reduction temperature (up to 773 K) for both catalysts. These results are not in agreement with previous data from our group [17][29], where a higher amount of Ce (III) in the Pt(Cl)/CeO2 catalyst after a high temperature reduction treatment was detected. This fact was tentatively attributed to the presence of chlorine and, more specifically, to the formation of CeOCl species. Le Normand et al. [39] described the formation of the oxychloride species on a Pd(Cl)/CeO2 catalyst after a reduction treatment at 673 K. According to the authors, no definitive changes were observed by XRD and XPS analysis, the only evidence of a structural modification being the Cl/Ce molar ratio close to one, but just for low ceria content. In this context, Table 3.2 reports the Cl/Ce ratios for the Pt(Cl)/CeO2 catalyst in the fresh and reduced states. Taking into account the Cl/Ce ratio after the reduction treatment at 773 K, the value of 0.13 is quite different from the value of 1 reported in the literature [39]. However, due to the low chlorine content in this catalyst (because of the low platinum loading), it would be reasonable to expect the formation of CeOCl microphases just on a small fraction of the ceria surface. The binding energies of the Ce u´´´ peak are also reported in Table 3.2. All catalysts exhibit a value close to 917.2 eV, in close agreement with the literature [37]. Furthermore, no significant changes are observed due to the reduction temperature or the presence of chloride ions. 44 Chapter 3 50 Red. 523 K % Ce (III) 40 Red. 773 K Fresh 30 20 10 0 Reduction temperature Figure 3.9. % Ce (III) as a function of the reduction temperature ( ) Pt(N)/CeO2 and ( ) Pt(Cl)/CeO2 catalyst. Table 3.2. Catalyst characterization by XPS. Catalyst Red. Temp., K Ce (III), % Cl/Ce BE Ce u´´´, eV Pt(N)/CeO2 Fresh 35 --- 916.8 523 41 --- 917.0 773 39 --- 917.5 Fresh 36 0.13 916.7 523 38 0.19 916.6 773 36 0.13 916.9 Pt(Cl)/CeO2 The XP spectra of the Pt 4f level in the Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, both fresh (calcined) and in situ reduced at 523 K and 773 K, are plotted in Figure 3.10 (a) and (b), respectively. The overall spectrum of the Pt 4f band appears as the sum of two broad bands corresponding to levels 4f7/2 (at lower binding energies) and 4f5/2 (at higher binding energies). The Pt 4f7/2 band is deconvoluted in two components, corresponding to Pt (II) (around 72.7 eV) 45 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). and Pt (0) (around 70.4 eV) species. In the case of the Pt(N)/CeO2 catalyst (Figure 3.10 (a)), it was possible to observe that both, the fresh sample and that reduced at 523 K, presented two peaks centred at binding energies corresponding to a considerable amount of Pt (II) in different environments. However, after the reduction treatment at higher temperature, 773 K, platinum is mainly in the metallic state. This result indicates that the chlorine-free catalyst may be more difficult to reduce at low temperature. It is interesting to add that the same behaviour was not observed for the Pt(Cl)/CeO2 catalyst, Figure 3.10 (b). In this case, Pt (0) was detected in the samples reduced at 523 K and 773 K, as well as Pt (II) in both cases. This results show that the presence of chlorine difficulty the platinum reduction at high temperature. 46 Chapter 3 72.6 eV (a) 75.9 eV 73.8 eV 77.1 eV Intensity, a.u. Fresh 72.7 eV 74.2 eV 76.1 eV 77.2 eV RT 523K 71.6 eV 74.9 eV RT 773K 70 72 74 76 78 80 Binding energy, eV 72.7 eV (b) 75.4 eV Intensity, a.u. Fresh 72.9 eV 71.6 eV 74.9 eV 76.0 eV RT 523K 71.6 eV 74.9 eV 72.9 eV 76.0 eV RT 773K 70 72 74 76 78 80 Binding energy, eV Figure 3.10. XPS results of Pt 4f of the Pt(N)/CeO2 (a) and Pt(Cl)/CeO2 (b) catalysts, fresh and reduced in situ at 523 K and 773 K. 47 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). 3.6. Temperature-programmed desorption experiments of CO/CO2 (CO/CO2TPD). In order to characterize the oxygen mobility in the Pt/CeO2 catalysts, both in the presence of chlorine and in the Cl-free sample, an indirect determination has been carried out, the temperature-programmed oxidation of previously adsorbed CO. The amount of CO desorbed, together with the amount of CO2 formed, upon oxidation with oxygen from the CeO2 support, were monitored by on-line mass spectrometry. CO does not adsorb readily on ceria, but strongly chemisorbs on the noble metal particles [1]. In this case, the nature of the ceria support controls the ratio of CO adsorbed on the metal, in part through oxygen transfer between the ceria and the metal particle and also by other interactions between the metal and the support. There are two important manifestations of these interactions. The first one is the well-known ability of ceria to supply oxygen to oxidize CO to CO2, i.e. the oxygen storage capacity of ceria; the second one is that CO can be dissociated on the metal particles, and the extent of the dissociation depends on the extent of ceria reduction [1]. The CO2 and CO desorption profiles obtained during the TPD analysis are shown in Figure 3.11 (a) and (b), respectively. As it can observed, the CeO2 support does not adsorb CO and, consequently, does not produce CO2 in the temperature range analyzed. This observation demonstrates the importance of the Pt nanoparticles to chemisorb and oxidize CO to CO2. In fact, CO adsorption on the ceria support preferably generates formates and carbonates through surface reactions with the –OH groups from the support [40]. As it can be observed, the amount of CO desorbed is 10 times lower that the amount of CO2 produced, thus indicating that in both cases nearly all the CO is being oxidized to CO2. However, a close inspection of the CO2 desorption profile shows that the amount of CO2 formed is larger in the Cl-free catalyst. Several authors have used CO-TPD for the characterization of CeO2-based catalysts [40][41][42][43]. In the case of gold catalysts, two CO2 desorption peaks were reported; the first one, around 433 K, is assigned to the oxidation of adsorbed species over noble metal nanoparticles, and the second peak, near 773 K, is attributed to the decomposition of carbonate species on the support [44]. In the present work, the incorporation of Pt nanoparticles in the catalyst surface gives rise to a CO2 desorption peak at around 380 K for both catalysts, independent of the presence or absence of chlorine. Ribeiro et al. [44] have proposed two mechanisms to justify the desorption of CO2: first, a 48 Chapter 3 CO disproportionation reaction on the Pt surface giving rise to CO2 and C(s) as products, as described in Equation 3.2. Carbon deposition is a well-known deactivation mechanism, which causes the loss of metal-support interactions and leads to the covering of the catalytic surface, which in turn hinders reactant adsorption on active sites. (Equation 3.2) Secondly, these authors proposed that CO2 could be formed by the oxidation reaction of CO adsorbed in metal-support centers with oxygen coming from the support, forming CO2 and leaving an oxygen vacancy, as shown in Equation 3.3. (Equation 3.3) Previous studies on Au/TiO2 catalysts described in the literature have suggested the adsorption of CO on gold nanoparticles and the reaction with lattice oxygen as the mechanism for CO2 formation at low temperatures [45]. Moreover, in the case of Au/ZrO2 catalysts, two CO2 desorption peaks were observed, the first one at 393 K and the second one at 573 K. The first peak was due to CO disproportionation, Equation 3.2, but the second peak was related to the decomposition of carbonate species on the support surface [46]. Isotopic studies on Rh/CeO2 catalysts carried out by Putna et al. [41] demonstrated that oxygen atoms resulting from CO dissociation quickly exchange with oxygen coming from the ceria lattice. From Figure 3.11 (a) it is clear that the presence of chlorine affects the formation of CO2. In addition to the main peak at 380 K, there is a high temperature shoulder for both catalysts, this contribution being more evident in the chlorine-free catalyst. The low temperature peak (main contribution) must be associated to CO oxidation on the Pt nanoparticles (by either equation 3.2 or equation 3.3) whereas the high temperature shoulder must be attributed to carbonate decomposition. The greater amount of CO2 formed in the absence of chlorine (976.3 μmol CO2·g-1catalyst versus 273.3 μmol CO2·g-1catalyst), demonstrates that the presence of chlorine inhibits the formation of carbonates, while the presence of CeOCl species prevents oxygen mobility. On the other hand, the CO desorption profiles for both catalysts are very similar, Figure 3.11 (b), the amount of CO desorbed being 0.042 mmol CO·g-1catalyst and 0.034 mmol CO·g-1catalyst for the chlorine-free and the chlorinated catalyst, respectively. The presence of a wide desorption peak demonstrates the heterogeneity of the adsorption sites. This heterogeneity 49 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). suggests the presence of different energies for CO desorption, which indirectly reflects the presence of a broad Pt particle size distribution [47]. Two peaks can be differentiated in the CO desorption profile, one at low temperatures (473533 K) and another one at high temperatures (673-773 K) [43]. CO desorption at low temperature is associated with the linear CO adsorption over small Pt particles, while desorption at high temperature can be attributed to bridge bonded CO species, or CO species adsorbed in inaccessible surface sites where higher temperatures are required for desorption [47] and/or to the decomposition of carbonates. In this work, the Pt(N)/CeO2 catalyst exhibits a slightly wider CO desorption profile compared to the Pt(Cl)/CeO 2 catalyst, thus suggesting a slight heterogeneity in the metal particle size in the former. This observation will be confirmed later on by infrared experiments. 50 Chapter 3 (a) -1 0.0001 mmol CO2·s ·g -1 CeO2 CO2 desorption, a.u. Pt(N)/CeO2 Pt(Cl)/CeO2 300 350 400 450 500 550 600 650 700 750 Temperature, K (b) -1 0.00001 mmol CO·s ·g -1 CeO2 Pt(N)/CeO2 CO desorption, a.u. Pt(Cl)/CeO2 300 350 400 450 500 550 600 650 700 750 Temperature, K Figure 3.11. CO2 (a) and CO (b) desorption profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K. 51 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). Table 3.3. CO/CO2-TPD characterization of Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts. Catalyst Red. Temp., K µmol CO·g-1 cat. µmol CO2·g-1 cat. CeO2 523 7.9 56.1 Pt(N)/CeO2 523 42.2 976.3 Pt(Cl)/CeO2 523 34.0 273.3 3.7. Catalytic behaviour in the PROX reaction. 3.7.1. CO oxidation in the presence of hydrogen followed by gas chromatography: Effect of the reduction and reaction temperature. The reaction profiles in terms of CO conversion and selectivity to CO 2 for the CeO2 support, and the Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, at different reaction and reduction temperatures, are shown in Figure 3.12 and Figure 3.13 (gas mixture feed: 2% CO, 2% O2, 20% H2 balanced in He). The light-off curves in Figure 3.12 show the influence of the reduction temperature in the CO conversion for the different catalysts prepared. With regard to the influence of the reaction temperature in the catalytic activity it is possible to observe that both catalysts exhibit an important difference in the CO conversion with an increase in the reaction temperature. In the case of the chlorine-free catalyst there is a gradual increase in the CO conversion with temperature. On the contrary, the chlorinated catalyst exhibits a sharp increase in the CO conversion at 353 K, reaching a final conversion value similar to its counterpart. This behaviour could be associated to a different reaction mechanism taking place in each one of these catalysts. Details about possible mechanism would be reported later on. Interestingly, both catalysts exhibit a decrease in the CO conversion and selectivity to CO2 for reaction temperatures above 400 K. At these high temperatures the oxidation of H2 to H2O is more favored than the oxidation of CO to CO2.[2][7][19][48]. However, the effect of CO2 present in the reaction feed cannot be ruled out for the loss on the catalytic activity. Mariño et al. proposed the formation of carbonates due to CO2 adsorption on the ceria support as responsible of the observed behaviour in the catalytic activity [6]. 52 Chapter 3 Concerning the effect of the Pt nanoparticles, it can be observed that the support alone is practically inactive in the range of temperatures studied, independently of the reduction temperature used. This observation is in close agreement with previous analysis described in the literature [15][16]. Concerning the Pt-based catalysts, important changes in the catalytic activity are observed as a function of the reduction temperature and the precursor used. There is an increase in the catalytic activity in the temperature range between 320 K and 380 K for both catalysts, up to a conversion value close to 90%. A close inspection to these data shows that the chlorine-free catalyst presents a higher activity compared to the chlorinated catalyst, at least at low temperatures (333 K). The effect of the metal precursor was more pronounced after a reduction treatment at high temperature. A similar behaviour was observed by Ko et al. [49] for Pd-Co/YSZ catalysts. In this sense, whereas an increase in the reduction temperature to 773 K is beneficial for the reaction process on the Pt(N)/CeO2 catalyst, i.e. there is a slight improvement in the catalytic activity at low temperature, the same variation in the reduction temperature is detrimental for the Pt(Cl)/CeO2 catalyst. In accordance with the XPS results described above in Figure 3.8, an increase in the reduction temperature must give rise to an increase in the amount of oxygen vacancies by reduction of Ce (IV) to Ce (III). Apparently, those oxygen vacancies at the metal-support interface favor the distortion of the CO molecule and provide the active sites for the oxidation to CO2. On the contrary, in the chlorinated catalyst, chlorine inhibits the formation of those oxygen vacant centers due to the formation of CeOCl surface species [17][50][51]. This process is favored at high reduction temperatures. Complete O2 conversion (not shown) was reached at 413 K for both catalysts reduced at 523 K. However, in the case of a reduction treatment at 773 K, complete O2 conversion is observed at 433 K for the chlorine-free catalyst whereas it shifts to 413 K for the chlorinated catalyst. The selectivity to CO2 in the range of high CO conversion (~ 380-400 K) was around 43-53 % for both catalysts (see Figure 3.13). 53 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). 100 (a) CO conversion, % 80 60 Pt(N)/CeO2 Pt(Cl)/CeO2 40 CeO2 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 (b) CO conversion, % 80 60 Pt(N)/CeO2 40 Pt(Cl)/CeO2 CeO2 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K Figure 3.12. CO oxidation profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K (a) and at 773 K (b). 54 Chapter 3 100 (a) CO2 selectivity, % 80 60 40 20 Pt(N)/CeO2 Pt(Cl)/CeO2 CeO2 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 (b) CO2 selectivity , % 80 60 40 20 Pt(N)/CeO2 Pt(Cl)/CeO2 0 300 CeO2 320 340 360 380 400 420 440 460 480 Temperature, K Figure 3.13. CO2 selectivity profiles for CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K (a) and at 773 K (b). 55 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). 3.7.2. CO oxidation in the presence of hydrogen followed by gas chromatography: Isothermal experiments. In order to illustrate better the effect of the reaction temperature and to understand the differences in catalytic activity among the different catalyst, two isothermal experiments were carried out at 333 K and 353 K with the chlorine-containing and the chlorine-free catalysts, both reduced at 523 K. The same tendency with respect to CO conversion was observed in the isothermal experiments, Figure 3.14, compared to the behaviour described in Figure 3.12. At low temperature (333 K), the chlorinated catalyst exhibits a poor catalytic activity (around 2% conversion) which remains constant with time on stream. On the contrary, and in accordance with Figure 3.12, the chlorine-free catalyst exhibits a large catalytic activity (up to 73 % conversion) which is accompanied by a large deactivation during the first minutes of the reaction down to a steady state activity at around 12% conversion. The high catalytic activity, together with the large deactivation observed in the chlorinefree catalyst, clearly shows the presence of a different reaction mechanism in the absence of chlorine and at low temperatures. More probably, this reaction mechanism involves surface species which are consumed during the first stages of the reaction. A completely different scenario occurs at a slightly higher temperature (353 K). At this temperature, both catalysts exhibit a high catalytic activity (around 75-85% conversion), which remains more or less stable with time on stream. The mechanism for the CO oxidation over reducible metal oxides catalyst was proposed by Mars and Van Krevelen [2][7][40][52][53]. In this mechanism CO is adsorbed in the surface of the noble metal and is activated by labile oxygen coming from the support. CO and H2 compete for the same adsorption site but, at low temperature, the CO adsorption is favored. The high catalytic activity observed at low temperature on the Pt(N)/CeO2 catalyst compared to its chlorinated counterpart clearly reflects a different mechanism depending on the presence or absence of chlorinated species, most probably associated with the support. Ayastuy et al. observed a similar divergence in the catalytic activity of Pt catalysts supported on Al2O3 and CeO2 [2]. In this study the catalytic activity of the Pt/CeO2 catalyst was larger than that of the Pt/Al2O3 catalyst, these differences being associated to the different reaction mechanisms taking place in the different catalysts. In the case of Al2O3, the CO oxidation reaction took place through the competitive Langmuir-Hinshelwood mechanism, where oxygen and CO compete with hydrogen for the active sites. In the case of CeO2, the mandatory reaction mechanism was the non- 56 Chapter 3 competitive Mars-Van Krevelen, in which there is an important participation of the oxide support. In the present work, the high CO conversion for the chlorine-free catalyst at low temperature must be attributed to the availability of active sites/species in the oxide support, which are blocked or absent when chlorine is present. Furthermore, the irreversible consumption of these surface species (more probably –OH species) favoring the catalytic process at low temperature would explain the fast deactivation observed in the initial steps of the reaction. A description of the different hypothesis to explain this behaviour will be discussed in the subsequent section. 100 80 CO convertion, % Pt(N)/CeO2_353K 60 Pt(Cl)/CeO2_353K 40 20 Pt(N)/CeO2_333K Pt(Cl)/CeO2_333K 0 0 40 80 120 160 200 240 Time, min Figure 3.14. CO conversion for Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts, reduced at 523 K and reaction temperature at 333 K and 353 K. 3.7.3. CO oxidation in the presence of hydrogen followed by gas chromatography: Effect of feed composition. Another factor that can influence the reaction mechanism when it is working with oxide supports is the feed composition, i.e. the λ value (λ = 2[O2]/[CO]). The λ value has been modified in this study by increasing the O2 content in the reaction feed (2% CO, 0.6-2% O2, 20% H2 balanced in He). The evolution of the CO and O2 conversion profiles together with the CO2 selectivity for the Pt(N)/CeO2 catalyst reduced at 523 K, and at a reaction temperature of 353 K, can be observed in Figure 3.15. 57 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). As it can be seen, the CO conversion strongly depends on the λ value. Using an oxygen content above the stoichiometric value (λ = 1), i.e. when there is an excess of oxygen, both the CO and H2 oxidation reactions are favored. However, the effect of this excess oxygen is more pronounced for the hydrogen oxidation reaction, i.e. there is in general a decrease in the selectivity to CO2 with increasing the oxygen content. It must be kept in mind that ceria can act as an oxygen buffer. As a result, the oxygen concentration over the catalyst would virtually be constant up to a certain oxygen inlet concentration, when the maximum oxygen storage capacity (OSC) of ceria is exceeded [6]. This result is in agreement with the values reported in literature [2][7][9][40], which showed a similar dependence of the CO oxidation reaction with the λ value. Mariño et al. [7] studied the influence of the gas composition in platinum and iridium catalysts. For both systems the CO and H2 oxidation raise with an increase in the value, while the selectivity towards CO2 formation fall down. Wootsch et al. [51] also observed an increase of selectivity with the decrease of λ values on Pt/Al2O3 and Pt/CeO2 catalysts. 100 80 % 60 40 20 XCO XO2 SCO2 0 0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.0 2[O2]/[CO] Figure 3.15. Preferential CO oxidation on the Pt(N)/CeO2 catalyst, reduced at 523 K; reaction temperature at 353 K; feed composition: 2% CO, 0.6-2% O2, 20% H2 and He as a balance. 58 Chapter 3 3.7.4. CO oxidation in the presence of hydrogen followed by operando DRIFT spectroscopy: Effect of the reaction temperature. In order to analyze in detail the different steps taking place in the course of the catalytic reaction, both Pt/CeO2 catalysts have been analyzed by operando DRIFTS. The profiles obtained in the DRIFTS cell for CO oxidation are shown in Figure 3.16 (a), (b) and (c) for the CeO2, Pt(N)/CeO2 and Pt(Cl)/CeO2, respectively. DRIFTS experiments show the presence of formate and carbonate bands in the range between 1570-1200 cm-1, in accordance with earlier observations [9][40][50][54][55][56]. Interestingly, carbonate and formate bands are very similar (in magnitude) on the CeO2 support and on the Pt(Cl)/CeO2 catalyst, whereas they are much more intense for the chlorine-free catalyst, in accordance with the CO2-TPD results described in Figure 3.11. As it can be seen in Figure 3.16, these bands are different in both catalysts. The chlorinefree catalyst shows bands at 1567 cm-1, 1547 cm-1, 1462 cm-1, 1369 cm-1 and 1292 cm-1, attributed to bidentate, unidentate and polydentate carbonate, and also formate. On the contrary, the chlorinated catalyst shows bands at 1462 cm-1 and 1362 cm-1, corresponding to polydentate carbonate [9][40][52][54][55]. The presence of formate was identified mainly by peaks at 2926 cm-1 and 2840 cm-1, which are characteristic of –CH stretching vibrations, these bands being more pronounced for the Cl-free catalyst. According to these observations, the presence of chlorine hinders the formation of surface formates. Furthermore, it can be observed in both catalysts the presence of bands in the region between 3000 cm-1 and 3500 cm-1, assigned to surface hydroxyl groups (-OH) and water molecules adsorbed on the support. Interestingly, during the course of the PROX reaction, an increase in the reaction temperature for the Cl-free catalyst gives rise to a decrease in the signals attributed to water and hydroxyls groups (bands at 3640 cm-1, 3511 cm-1 and ~ 3180 cm-1), this decrease being very sharp in the reaction temperature range 313-333 K. Furthermore, an increase in reaction temperature gives rise to a significant decrease in the intensity of the carbonate bands at 1567 cm-1 and 1292 cm-1. For the chlorinated catalyst a slight decrease in the surface –OH groups or carbonates was also observed. The differences between the DRIFT spectra for both catalysts can be related with the differences observed in catalytic activity. As described in the literature [9][55][57], the surface -OH groups could facilitate the formation of carbonate species by reaction with CO. Fottinger et al. [55] suggested that the formation of carbonates could be associated with two models, the first one 59 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). being related with dissociation of CO on the noble metal followed by the reaction of CO2 with the support to form the surface carbonates, and the second one being related with the direct reaction between CO and -OH groups of the support, followed by CO2 reaction with additional -OH groups. At 333 K, the Cl-free catalyst presents a high catalytic activity and a large deactivation with time on stream (Figure 3.14). Initially, CO can react with -OH surface groups of the support to form carbonates and formates until total saturation; then, the reaction could move towards Pt surface sites, generating a constant activity. Shido et al. [58] studied Rh/CeO2 in WGS reactions and observed the formation of bidentate formates from CO and surface -OH groups on cerium. Daté et al. [11] studied the influence of humidity on the CO oxidation reaction on gold catalysts prepared on different supports. According to these authors, the reaction mechanism depends on the nature of the support and on the presence of moisture; moisture improves the reaction activity due to the involvement of -OH group as intermediates. Xu et al. [59] also studied the reaction mechanism of WGS and PROX reactions. In this case, CO2 formation occurred through the reaction between adsorbed CO and surface -OH groups (COads + OHsurf) taking place at Pt-oxide interface sites at low temperature. Graf et al. [60] determined that the reactivity of hydroxyl groups on Pt catalysts for the WGS reaction is associated with the formate formation by mono-coordinated hydroxyls. The existence of CO species adsorbed on the support and on the Pt nanoparticles can be followed by bands in the range 2240-1860 cm-1 (Figure 3.17). Peaks at 2172 cm-1 and 2116 cm-1 are due to CO adsorbed on Ce (IV) and Ce (III) sites, respectively, and/or CO from the gas phase. The appearance of these peaks is an indication of the partial reduction of the support. Peaks at 2070 cm-1 and 2052 cm-1 in the case of Cl-containing catalyst and at 2032 cm-1, in the case of Cl-free catalyst were assigned to CO species adsorbed on Pt. The presence of this band at lower wavenumbers in the chlorine-free catalyst could be associated with the presence of small nanoparticles together with the presence of defect sites, i.e. oxygen vacancies, at the metal-support interface able to tilt CO adsorption [61]. On the contrary, the peak at 2070 cm -1 in the chlorinated catalyst could indicate the presence of metal atoms in less dense close packed terraces, e.g. 100 faces; whereas the peak at ~ 2052 cm-1 could be associated with the presence of Pt atoms in defect sites (in steps and corners). The presence of the band at 2032 cm-1 anticipates the presence of defect sites able to activate the CO molecule on the chlorine-free catalyst, these sites being possible candidates to promote the CO oxidation reaction. Badri et al. [50] also observed a similar shift in the CO band induced by chlorine species. In 60 Chapter 3 agreement with these results, this shift was due to the formation of an active electronegative species by chlorine. The characteristics bands for the vibration of CO in the gas phase are assigned in the range 2120-2170 cm-1 [9][54]. Close to this region bands corresponding to CO adsorbed on sites belonging to a CeOCl phase, where cerium is reduced to Ce (III), can be found. They appear at around 2175 cm-1 [50]; therefore, they can difficult to identify due to overlap. Furthermore, and in agreement with the CO desorption profile, it is interesting to mention that the Pt(N)/CeO2 catalyst presents a wider Pt-CO desorption profile than the Cl-free catalyst, this showing the higher surface heterogeneity for the former catalyst. 61 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). (a) (b) KM, a.u. KM, a.u. 473 K 313 K 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm 4000 3500 3000 2500 2000 1500 1000 -1 Wavenumbers, cm -1 KM, a.u. (c) 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm -1 Figure 3.16. DRIFT spectra obtained during CO oxidation under 2% CO, 10% air, 20% H2 and balance N2 feed with catalysts reduced at 523 K: CeO2 (a), Pt(N)/CeO2 (b) and Pt(Cl)/CeO2 (c). The initial temperature was 313 K and it was increased by 20 K. 62 Chapter 3 2032 cm -1 KM, a.u. Pt(N)/CeO2 2052 cm 2070 cm -1 -1 Pt(Cl)/CeO2 2250 2200 2150 2100 2050 Wavenumbers, cm 2000 1950 1900 -1 Figure 3.17. DRIFTS spectra of CO adsorbed species on the Pt(N)/CeO2 and Pt(Cl)/CeO2 catalysts during PROX reaction at 313 K. It is interesting to mention that the changes observed in the surface chemistry of the Cl-free catalyst by FTIR after an increase in the reaction temperature from 313 K to 333 K (Figure 3.16), fit with the results obtained in the light-off curves for the PROX reaction (Figure 3.14), (in both cases the catalysts were reduced at 523 K). These observations suggest that the high activity obtained at low temperature (333 K) by the Cl-free catalyst must be attributed to the participation of the support in the reaction process. Apparently, the Pt(N)/CeO2 catalyst presents surface hydroxyl species capable of participating in the reaction process at low temperature following Equation 3.4. Moreover, some authors [62][63][64] justify that the PROX reaction generates a -HCOO intermediate by reaction between CO and -OH groups. (Equation 3.4) This hypothesis can be confirmed performing reaction studies at constant temperature during several hours (Figure 3.14). Whereas the chlorinated catalyst shows almost no activity, the Cl-free catalyst shows an initially high activity (CO conversion about 75%), together with a high deactivation (a 13% decrease in conversion) after 2 h reaction at 333 K. On the contrary, the CO oxidation reaction performed at a higher temperature (353 K) proceeded with high conversion for both catalysts (~ 80%), which remained constant with 63 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). reaction time. Therefore, these observations clearly demonstrate that the high catalytic activity of Pt(N)/CeO2 at low temperature (333K), compared with the chlorinated catalyst, can be due to the presence of reactive -OH species on the surface of the support, which react to generate CO2 and H2O. The presence of a limited amount of surface -OH groups on the catalyst could justify the limited activity of this catalyst at 333 K compared to the same behaviour at 353 K. In this regard, it is expected that at 353 K the reaction occurs in both catalysts on the platinum nanoparticles, without the involvement of surface -OH species from the support, i.e., reaction between adsorbed CO and oxygen from the metal-support interface sites. 4. Conclusions. In this work, two catalysts prepared using different metal precursors (in the presence and absence of chlorine) were evaluated in the preferential CO oxidation reaction in the presence of H2. From the obtained results it was possible to conclude that the Cl-free catalyst shows better activity at low temperature (333 K) than the chlorinated catalyst. At temperatures above 373K, the CO oxidation reaction occurred via the same mechanism in both catalysts (interfacial reaction centers between CO adsorbed on Pt and oxygen from the support). However, at low temperatures, the presence of a second reaction mechanism in the Cl-free catalyst was observed. This mechanism appears to involve the participation of -OH groups from the support, with the corresponding consumption of CO and subsequent CO2 formation. It has been possible to confirm this hypothesis by (i) DRIFTS studies under reaction conditions, in which a drastic drop in the hydroxyl signal after an increase in reaction temperature from 313 K to 333K was observed and, (ii) reaction studies at constant temperature, which showed a high deactivation with the formation of CO2, due to the limited amount of available -OH surface groups to reacted with CO. 5. References. [1] A. Trovarelli, Catalysis by ceria and related materials, 2ª Ed. (2002) London. [2] J.L. Ayastuy, A. Gil-Rodriguez, M.P. González-Marcos, M.A. Gutiérrez-Ortiz, International J. Hydrogen Energy, 31 (2006) 2231-2242. [3] H. Vidal, J. Kaspar, M. Pijolat, G. Colon, S. Bernal, A. Cordón, V. Perrichon, F. Fally, Appl. Catal. B: Env., 27 (2000) 49-63. [4] E. Mamontov, T. Egami, R. Brezny, M. Koranne, S. Tyagi, J. Phys. Chem. B, 104 (2000) 11110-11116. 64 Chapter 3 [5] C. Larese, M. López Granados, R. Mariscal, J.L.G. Fierro, P.S. Lambrou, A.M. Efstathiou, Appl. Catal. B: Env., 59 (2005) 13-25. [6] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 58 (2005) 175-183. [7] F. Mariño, C.Descorme, D. Duprez, Appl. Catal B: Env., 54 (2004) 59-66. [8] W. Li, F.J. Gracia, E.E. Wolf, Catal. Today, 81 (2003) 437-447. [9] O. Pozdnyakova, D. Teschner, A. Wootsch, J. Kröhnert, B. Steinhauer, H. Sauer, L. Toth, F.C. Jentoft, A. Knop-Gericke, Z. Paál, R. Schlögl, J. Catal., 237 (2006) 1-16. [10] E. Quinet, L. Piccolo, F. Morfin, P. Avenier, F. Diehl, J. Catal., 268 (2009) 384-389. [11] M. Daté, M. Okumura, S. Tsubota, M. Haruta, Angew. Chem. Ind. Ed., 43 (2004) 2129-2132. [12] M. Abid, R. Touroude, Catal. Letters, 69 (2000) 139-144. [13] L. Kepinski, J. Okal, J. Catal., 192 (2000) 48-53. [14] A. Sepúlveda-Escribano, F. Coloma, F. Rodríguez-Reinoso, J. Catal., 178 (1998) 649–657. [15] I. Dobrosz-Gómez, I. Kocemba, J.M. Rynkowski, Appl. Catal. B: Env., 83 (2008) 240-255. [16] M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today, 68 (2001) 53-61. [17] J. Silvestre-Albero, F. Coloma, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Appl. Catal. A: Gen., 304 (2006) 159-167. [18] H.S. Roh, H.S. Potdar, K.W. Jum, S.Y. Han, J.W. Kim, Catal. Letters, 93 (2004) 203207. [19] J.L. Ayastuy, M.P. González-Marcos, A. Gil-Rodríguez, J.R. González-Valesco, M.A. Gutiérrez-Ortiz, Catal. Today, 116 (2006) 391-399. [20] G. Avgouropoulos, M. Manzoli, F. Boccuzzi, T. Tabakova, J. Papavasiliou, T. Ioannides, V. Idakiev, J. Catal., 256 (2008) 237-247. [21] H. Sakurai, T. Akita, S. Tsubota, M. Kiuchi, M. Haruta, Appl. Catal. A: Gen., 291 (2005) 179-187. [22] P. Fornasiero, G. Balducci, R. Di Monte, J. Kaspar, V. Sergo, G. Gubitosa, A. Ferrero, M. Graziani, J. Catal., 164 (1996) 173-183. [23] S. Ricote, G. Jacobs, M. Milling, Y. Ji, P.M. Patterson, B.H. Davis, Appl. Catal. A: Gen., 303 (2006) 35-47. [24] G. Jacobs, L. Williams, U. Graham, G.A. Thomas, D.E. Sparks, B.H. Davis, Appl. Catal. A: Gen., 252 (2003) 107-118. [25] J.C. Serrano-Ruiz, G.W. Huber, M.A. Sánchez-Castillo, J.A. Dumesic, F. RodríguezReinoso, A. Sepúlveda-Escribano, J. Catal., 241 (2006) 378–388. [26] F. Fajardie, J.F. Tempere, J.M. Manoli, G. Djega-Mariadassou, G. Blanchard, J. Chem. Soc. Faraday Trans., 94 (1998) 3727-3735. [27] C. Force, J.P. Belzunegui, J. Sanz, A. Martínez-Arias, J. Soria, J. Catal., 197 (2001) 192-199. [28] S. Bernal, J.J. Calvino, G.A. Cifredo, J.M. Rodríguez-Izquierdo, J. Phys. Chem., 99 (1995) 11794-11796. [29] J. Silvestre-Albero, F. Rodríguez-Reinoso, A. Sepúlveda-Escribano, J. Catal., 210 (2002) 127-136. 65 Effect of the metal precursor on the catalytic behaviour of Pt/CeO2 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). [30] F. Zhang, P. Wang, J. Koberstein, S. Khalid, S.W. Chan, Surface Science, 563 (2004) 74-82. [31] R. Leppelt, B. Schumacher, V. Plzak, M. Kinne, R.J. Behm, J. Catal., 244 (2006) 137152. [32] J.Z. Shyu, K. Otto, W.L.H. Watkins, G.W. Graham, R.K. Belitz, H.S. Gandhi, J. Catal., 114 (1988) 23-33. [33] J.Z. Shyu, W.H. Weber, H.S. Gandhi, J. Phys. Chem., 92 (1988) 4964-4970. [34] F.B. Noronha, E.C. Fendley, R.R. Soares, W.E. Alvarez, D.E. Resasco, Chem. Eng. J., 82 (2001) 21-31. [35] A. Kotani, T. Jo, J.C. Parlebas, Adv. Phys., 37 (1989) 37-85. [36] A. Laachir, V. Perrichon, A. Badri, J. Lamotte, E. Catherine, J.C. Lavalley, J. El Fallal, L. Hilaire, F. Le Normand, E. Quéméré, G.N. Sauvion, O. Touret, J. Chem. Soc. Faraday Trans., 87 (1991) 1601-1069. [37] M.S.P. Francisco, V.R. Mastelaro, P.A.P. Nascente, A.O.A. Florentino, J. Phys. Chem. B, 105 (2001) 10515-10522. [38] B. Ernst, L. Hilaire, A. Kiennemann, Catal.Today, 50 (1999). 413-427. [39] F. Le Normand, L. Hilaire, K. Kili, G. Krill, G. Maire, J. Phys. Chem., 92 (1988) 2561–256831. [40] D. Teschner, A. Wootsch, O. Pozdnyakova-Tellinger, J. Kröhnert, E.M. Vass, M. Hävecker, S. Zafeiratos, P. Schnörch, P.C. Jentoft, A. Knop-Gericke, R. Schlögl, J. Catal., 249 (2007) 318-327. [41] E.S. Putna, R.J. Gorte, J.M. Vohs, G.W. Graham, J. Catal., 178 (1998) 598-603. [42] P. Thormählen, M. Skoglundh, E. Fridell, B. Andersson, J. Catal., 188 (1999) 300310. [43] R.K. Herz, D.F. Mc Cready, J. Catal., 81 (1983) 358-368. [44] N.F.P. Ribeiro, F.M.T. Mendes, C.A.C. Perez, M.M.V.M. Souza, M. Schmal, Appl. Catal. A: Gen., 347 (2008) 62-71. [45] M. Haruta, S. Tsubota, T. Kobayashi, H. Kageyama, M.J. Genet, B. Delmon, J. Catal., 144 (1993) 175-192. [46] P. Konova, A. Naydenov, C. Venkov, D. Mehandjiev, D. Andreeva, T. Tabakova, J. Mol. Catal. A, 213 (2004) 235-240. [47] R. Padilla, M. Benito, L. Rodriguéz, A. Serrano-Lotina, L. Daza, J. of Power Sources, 192 (2009) 114-119. [48] Z. Lendzion-Bielun, M.M. Bettahar, S. Monteverdi, D. Moszynski, U. Narkiewicz, Catal. Letters, 134 (2010) 196-203. [49] E.Y. Ko, E.D. Park, H.C. Lee, D. Lee, S. Kim, Angew. Chem., 46 (2007) 734-737. [50] A. Badri, C. Binet, J.C. Lavalley, J. Phys. Chem., 100 (1996) 8363-8368. [51] A. Wootsch, C. Descorme, D. Duprez, J. Catal., 225 (2004) 259-266. [52] A. Martínez-Arias, A.B. Hungría, M. Fernández-García, J.C. Conesa, G. Munuera, J. Power Sources, 151 (2005) 32-42. [53] A. Honés, A.B. Hungría, P. Bera, A. López Cámara, M. Fernández-García, A. Matínez-Arias, L. Barrio, M. Estrella, G. Zhou, J.J. Fonseca, J.C. Hanson, J.A. Rodriguez, J. Am. Chem. Soc., 132 (2010) 34-35. [54] C. Binet, M. Daturi, J.C. Lavalley, Catal. Today, 50 (1999) 207-225. 66 Chapter 3 [55] K. Föttinger, R. Schlögl, G. Rupprechter, Chem. Commun., (2008) 320-322. [56] P. Bera, A. Hornés, A.L. Cámara, A. Matínez-Arias, Catal. Today, 155 (2010) 184191. [57] H. Tanaka, M. Kuriyama, Y. Ishida, S.I. Ito, T. Kubota, T. Miyao, S. Naito, K. Tomishige, K. Kunimori, Appl. Catal. A: Gen., 343 (2008) 125-133. [58] T. Shido, Y. Iwasawa, J. Catal., 141 (1993) 71-81. [59] L. Xu, Y. Ma, Y. Zhang, Z. Jiang, W. Huang, J. Am. Chem. Soc., 131 (2009) 1636616367. [60] P.O. Graf, D.J.M. de Vlieger, B.L. Mojet, L. Lefferts, J. Catal., 262 (2009) 181-187. [61] P. Concepción, A. Corma, J. Silvestre-Albero, V. Franco, J.Y. Chane-Ching, J. Am. Chem. Soc., 126 (2004) 5523-5532. [62] K.I. Tanaka, M. Shou, Y. Yuan, J. Phys. Chem. C, 114 (2010) 16917-16923. [63] K.I. Tanaka, M. Shou, H. He, X. Shi, X. Zhang, J. Phys. Chem. C, 113 (2009) 1242712433. [64] A.B. Mhadeshwar, D.G. Vlachos, J. Phys. Chem. B, 108 (2004) 15246-15258. 67 68 METAL DOPING EFFECT Abstract. An important effect of doping ceria with a foreign cation is the increase of the number of surface defects (oxygen vacancies) and, consequently, of its oxygen storage capacity. In the following two chapters, the effect of ceria doping with two different cations, Y (III) and Nb (V), on the catalytic behaviour of Pt/doped-CeO2 in the preferential oxidation of CO in the presence of H2 will be studied. The presentation of the results obtained in this study will be divided in two chapters, the first one, Chapter 4, devoted to the effect of the presence of yttrium cations in the ceria support and the next one, Chapter 5, dedicated to the effect of doping with Nb (V). 70 CHAPTER 4 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. Abstract. This chapter reports a study on the effect of yttria in the catalytic behaviour of Pt/CeO2-Y2O3 catalysts in the preferential oxidation of CO in the presence of H2 (PROX). The catalysts have been prepared using [Pt(NH3)4](NO3)2 as Pt precursor and xCeO2-(1-x)Y2O3 supports with x = 1, 0.9, 0.7, 0.4 and 0. An important effect of the presence of the trivalent Y (III) cations is the increase of the oxygen storage capacity of the support through the generation of a larger number of defects (oxygen vacancies). In this study, the effects of the yttrium content in the support and of the reduction temperature on the catalytic behaviour have been determined. The results show that these parameters strongly affect the catalytic activity. Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 1. Introduction. Ceria-containing mixed oxides have attracted much attention as oxidation catalysts due to their redox properties and high oxygen storage capacity (OSC) [1][2]. A great effort has been dedicated to study the roles of ceria in these systems. Thus, ceria provides surface active sites and acts as an oxygen/transport medium by shifting between Ce (III) and Ce (IV) under reductive and oxidizing conditions, respectively [1][3][4][5]. These redox properties can be strongly enhanced when Ce (IV) cations in the fluorite-type lattice are replaced with foreign cations, with different radius and/or charge, due to an increased oxygen ion mobility favoured by the formation of lattice defects and oxygen vacancies. Many efforts have been addressed to the preparation of these mixed oxides, which are potentially useful as sensors, and catalysts for oxidation reactions, among other applications [4]. The goal at this point is to decrease the temperature required for O2 to diffuse through the catalyst, what could favour the catalytic efficiency. However, further development of these materials requires detailed information on their structural features and, above all, a precise knowledge of the role of their various components and the influence of the preparation procedure on their redox behaviour. The importance of zirconium addition to ceria catalysts in order to improve the OSC, redox properties, thermal resistance and supported metal dispersion [2][6], resulting in a better performance in CO oxidation, has been reported in the literature [3]. The improved behaviour observed, when Ce (IV) was replaced with zirconium, in ceria catalysts, to be used as a support in catalytic oxidation reactions, is attributed to the better thermal stability as well as to the enhancement of the oxygen storage capacity [2][3]. Roh et al. [5] used a Pt/CeZrO2 catalyst for the preferential CO oxidation at low temperature. The higher CO conversion obtained was justified as due to the higher OSC. It has been reported that the cubic phase of Ce-ZrO2 has more OSC and is more easily reducible than the tetragonal phase [7][8]. Furthermore, some authors have shown that the presence of zirconium must be associated with structural defects and high oxygen mobility [9][10][11]. In fact, Fornaciero et al. [10] showed that the decrease of the unit cell volume upon cerium substitution by zirconium favours the formation of defects. As it has been shown, the OSC is increased by doping with tetravalent cations such as zirconium. Moreover, high ionic conductivities are achieved by doping ceria with trivalent cations as lanthanum, samarium, gadolinium, and yttrium [12][13][14]. Steele et al. [15] have reported that the aliovalence 72 Chapter 4 substitution in CeO2 lattice must give a rise to the creation of oxygen vacancies. Llieva et al. [16] studied different rare earth modified ceria supports in CO oxidation catalysts, and they showed that the catalysts containing yttrium were the most promising ones. Furthermore, it is interesting to add that the proportion of yttrium doping in the ceria lattice could benefit the catalytic activity by Y (III) surface enrichment that hinders crystallite growth and favours the proportion of oxygen vacancies [17]; in other words, the proportion of yttrium substitution in the ceria lattice can affect the CO oxidation activity through the creation of oxygen vacancies to different extents. With this in mind, this work evaluates the catalytic activity of Pt/xCeO2-(1-x)Y2O3 catalysts, with x = 1, 0.9, 0.7, 0.4 and 0, as well as the influence of the Ce/Y ratio in the CO PROX reaction. 2. Experimental. 2.1. Catalysts preparation and characterization. A series of yttrium-doped ceria supports were prepared by the urea precipitation method. The appropriate amounts of cerium nitrate (Aldrich, 99 %), yttrium nitrate (Aldrich, 99.9 %) and urea (Fluka, 98 %) needed to obtain different xCeO2-(1-x)Y2O3 supports, with x = 1, 0.9, 0.7, 0.4 and 0, were dissolved in 400 ml of ultra-pure water. The solutions were heated at 363 K with constant stirring during 11 h. Finally, some ammonium hydroxide solution was added dropwise to complete the precipitation. The solids obtained were separated by filtration, washed with ultra-pure water, and dried at 383 K overnight. Finally, they were calcined in air at 773 K for 4 h, with a heating rate of 3 K·min−1. Different Pt/xCeO2-(1-x)Y2O3 catalysts were prepared by the wetness impregnation method. The support was impregnated with an aqueous solution of [Pt(NH3)4](NO3)2 (Aldrich, 99.9 %) as metal precursor, with the appropriate amount to achieve a 1 wt.% Pt loading. Afterwards, the samples were dried at 383 K overnight, and calcined in air at 773 K for 2 h, with a heating rate of 3 K·min−1. The prepared materials were characterized by different techniques: N 2 adsorption at 77 K, XRF, ICP-OES, XRD, SEM, TEM, H2-TPR, Raman spectroscopy, XPS and CO2/CO-TPD. Experimental details and equipment used were described in Chapter 2. 73 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 2.2. Catalytic behaviour. In a first stage, the catalytic behaviour of the catalysts in the PROX reaction was determined as a function of reaction temperature (303-473 K) at atmospheric pressure, under a gas flow (50 cm3·min−1) containing 20% H2, 2% CO, 0.6-2% O2 and He as a balance (GHSV = 17000 h-1). Previously, the catalysts were reduced in situ at two temperatures, 523 K and 773 K. Reaction products were monitored by online gas chromatography. In order to analyze in detail the process taking place in the course of the catalytic reaction, the reaction tests were also followed by diffuse reflectance infrared Fourier transformed spectroscopy (DRIFTS). The reaction oxidation experiments were carried out at temperature controlled conditions (303-473 K), at atmospheric pressure under a gas flow (40 cm3·min−1) containing 20% H2, 2% CO, 10% O2 air and N2 as a balance (GHSV = 17000 h-1). Experimental details, equipment used and calculation of selectivity and CO and O2 conversions were described in the Chapter 2. 3. Results and discussion. 3.1. Textural and metal loading characterization. Table 4.1 reports the actual Pt loading in the catalysts, as well as the relative CeO2 and Y2O3 content in the supports, determined by XRF and ICPOES. The oxide compositions cover a wide range, from pure ceria to pure yttrium. Hereinafter, samples will be labelled with the nominal composition, which in all cases differs only slightly from the actual one. The BET surface areas that were obtained for the supports are also reported in Table 4.1. It is interesting to observe the influence of the ceria relative content in the surface area. A strong decrease of surface area with increasing the yttrium content is observed. Serrano-Ruiz et al. [8] observed the same behaviour in CeZrO2 supported catalysts. Lingyun et al. [18] observed an increase of surface area in CexY1-xO washcoats with a decrease of yttrium content. She Yusheng et al. [19] studied yttrium doping in CuO/CeO2 catalysts for WGS reaction. They observed a variation of the surface area with the yttrium content. Initially, the surface area increases for a low yttrium content, but then it decreases afterwards. The authors attributed this observation to the agglomeration of copper oxide and ceria, which was prevented by an appropriate amount of yttrium dispersed spontaneously onto the ceria surface. 74 Chapter 4 Table 4.1. Characterization of Pt/xCeO2-(1-x)Y2O3 catalysts. Catalyst Pt loading, wt.% CeO2, relative content, % Y2O3, relative content, % SBET, m2·g-1 (a) x=1 1.0 100 0 110 x = 0.9 0.9 87 13 105 x = 0.7 1.2 73 27 90 x = 0.4 1.0 40 60 8 x=0 1.6 0 100 7 (a) BET superficial area of the support. 3.2. X-ray diffraction characterization. The structure of the oxide supports was determined by X-ray diffraction. The XRD patterns of the Pt/xCeO2-(1-x)Y2O3 catalysts are presented in Figure 4.1. The XRD profiles show the six main characteristic peaks for the fluorite – type structure of CeO2 [3][5][20][21]. However, their relative intensities progressively decrease and become broader with an increase of the yttrium content, i.e. there is a decrease of cristallinity after yttrium incorporation. In the case of cerium-yttrium binary oxide systems, the crystal structure depends on the Ce/Y proportion. The earlier version of the phase diagram of the cerium-yttrium system was derived by Gschneidner and Calderwood [22]. It is believed that there are five solution phases: liquid, body-centred cubic (bcc), hexagonal close-packed (hcp), face-centred cubic (fcc) and double-c hexagonal close-packed (dhcp). Upon calcination at 723 K, the fcc phase (γCe) transforms into the dhcp phase (βCe) and into the hpc phase (αY) with an increase of the yttrium content [22][23]. It is interesting to add that any evidence for extra peaks due to non-incorporated Y2O3 phase was not be detected by XRD (Figure 4.1). This fact could be justified or due to the efficient incorporation of the doping cations in the ceria lattice, and/or because the diffraction peaks of the Y2O3 phase are very close to those of CeO2, as suggested by same authors [18][24][25]; however, it is known that the yttrium incorporation could favours the oxygen storage capacity of the support. Thus, XRD analysis of the modified ceria solids confirms that the fluorite-type structure of ceria is preserved, although there is a loss of crystallinity by incorporation of yttrium. Although the segregation of phases is not directly deduced from the XRD patterns, the possibility of the existence of YOx patches on the ceria surface, 75 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. without forming a solid solution, cannot be ruled out, mainly at high yttrium loadings. The same conclusion was reported by Atribak et al. [17]. CeO2 x=0 Intensity, a.u. x = 0.4 x = 0.7 x = 0.9 x=1 20 30 40 50 60 70 80 2 Figure 4.1. X-rays difractograms of Pt/xCeO2-(1-x)Y2O3 catalysts (x = 1, 0.9, 0.7, 0.4 and 0). No diffraction peaks attributed to Pt could be identified in Figure 4.1, what is an indication of a high metal dispersion, i.e. small Pt crystallites. The sizes of the oxide support crystallites have been determined by using the Scherrer’s equation (Equation 2.5). The results obtained for the different samples are listed in Table 4.2. It is possible to appreciate a gradual decrease of the ceria crystal size (from 17 to 7 nm) with increasing the yttrium content. Moreover, it is observed a decrease in the lattice constant, calculated on the basis of the (111) plane of ceria, with the increase of yttrium content (Table 4.2). In this case Equation 2.6 was used considering the ceria cubic phase [26]. This decrease is a consequence of the replacement of Ce (IV) (0.097 nm ionic radium) with larger Y (III) (0.101 nm ionic radium) in the solid solution [17][27][28][29][30]. This fact supports that yttrium is incorporated in the ceria lattice. Rey et al. [31] observed the same behaviour in a study of lattice parameters of yttria-doped ceria. 76 Chapter 4 Table 4.2. Crystallite size and lattice constant of the xCeO2-(1-x)Y2O3 supports. Catalyst Crystallite size, nm (a) Lattice constant, nm x=1 17 0.5420 x = 0.9 10 0.5419 x = 0.7 8 0.5404 x = 0.4 5 0.5380 x=0 -- -- (a) Determinated by Scherrer´s equation. 3.3. Raman characterization of catalysts. To further confirm the crystalline phases present in the Pt/xCeO2-(1-x)Y2O3 catalysts, Raman spectroscopy analysis were carried out. The obtained spectra are shown in Figure 4.2. Ceria crystallizes in the cubic fluorite-type lattice and belongs to the Oh5 (Fm3m) space group, that posses a structure with six opticalphoton branches, and three zone center frequencies at 272 cm-1, 465 cm-1 and 595 cm-1. These frequencies are ascribed to the doubly degenerated TO mode, the triple degenerated Raman active mode and the non-degenerate LO mode, respectively [32]. Figure 4.2 (a) shows the Raman spectra of the oxides. It is possible to observe a feature band, centred at about 462 cm-1, corresponding to the CeO2 Raman mode F2g of the fluorite-type structure [18][24][17][33][34], which can be viewed as a symmetric breathing mode of the oxygen atoms around cerium ions [12][33]. It is interesting to note the decrease of the intensity of this band with the increase of the yttrium content due to the framework deformation, in accordance with XRD. It has been reported that this deformation, induced by doping, favours the oxygen mobility [35]. The evidence of the yttrium incorporation in the lattice, of the prepared supports, is given by the shift and width observed in the band at 461 cm -1. The incorporation of ions into the ceria lattice could induce it to distort and to influence the polarizability of the symmetrical stretching vibracional mode, and this could result in a shift of this band. The same behaviour has been observed by others authors [19][17][36][37][38]. In addition, it is possible to observe in Figure 4.2 (a) a band located at 540–620 cm-1, which is less pronounced for low yttrium contents. However, in the case of the sample with x = 4 this band was too much marked. This band 77 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. could be attributed to the LO vibration mode of the CeO2, which appears as a result of the relaxation of its symmetry rules [32] and the generation of oxygen vacancies [19][29][33][34]. Moreover, in the case of the catalyst with x = 0.4, the decrease of the intensity of the band at 462 cm-1 with a parallel increase of the band at 607 cm-1 may be due to the formation of a new phase, hexagonal closepacked, as it has been shown in the cerium-yttrium binary system phase diagram [22]. The band at 362 cm-1 is characteristic of the Y2O3 phase [18][24][39][40][41]. It is interesting to add that this band was observed only in the Raman spectra corresponding to the catalyst, Figure 4.2 (b). This fact may be related to the calcination treatment used after platinum impregnation, which could favour the crystallinity, fact that could facilitate the intensity of the bands in the Raman spectra. This band is vanished for the CeO2-Y2O3 solids, likely because of the incorporation of yttrium into the CeO2 crystal lattice. This fact is in agreement with XRD results. Solid solution systems of the rare earth trivalent and tetravalent metals could be present in homogeneous regions, with a fluorite structure form, with the proportion of 60 % of the trivalent form [42], favouring the formation of a solid-solution. In this case, yttrium could be included in the rare earth group due to the similarity with these elements by the higher atomic number. 78 (a) 462 cm -1 Intensity, a.u. Chapter 4 x=0 x = 0.4 x = 0.7 461 cm -1 x = 0.9 x=1 Intensity, a.u. 410 420 430 440 450 460 470 Raman shift, cm 460 cm 480 490 500 510 -1 -1 x=0 x = 0.4 x = 0.7 x = 0.9 x=1 200 300 400 500 600 700 Raman shift, cm 800 900 1000 -1 Intensity, a.u. (b) 362 cm -1 x=0 610 cm -1 x = 0.4 x = 0.7 x = 0.9 x=1 200 300 400 500 600 700 Raman shift, cm 800 900 1000 -1 Figure 4.2. Raman spectra of xCeO2-(1-x)Y2O3 (a) and Pt/xCeO2-(1-x)Y2O3 (b) solids. 3.4. SEM/EDS – Chemical mapping catalysts characterization. Chemical mapping was used to analyses the distribution of cerium and yttrium on the catalysts surface. Figure 4.3, Figure 4.4 and Figure 4.5 exhibit 79 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. SEM micrographs corresponding to Pt/0.9CeO2-0.1Y2O3, Pt/0.7CeO2-0.3Y2O3 and Pt/0.4CeO2-0.6Y2O3 catalysts, showing the cerium and yttrium distribution. In Figure 4.3 it is interesting to observe the change of the morphology with the increase of the yttrium proportion. For low yttrium contents, the support presents a needle shape. However, with the increase of the doping metal it is possible to observe a change of morphology from needle to spherical and the formation of agglomerated support particles. The same behaviour has been observed by TEM as will be shown later on in this chapter. From the SEM-chemical mapping Ce and Y analysis, a good distribution of these metals on the catalysts can be observed. It is also found that the intensity of Y obviously increases when more Y2O3 is present, as expected. Therefore, it is suggested that yttrium is well-distributed over the Pt/xCeO2-(x-1)Y2O3 catalysts series, in accordance with DRX and Raman results. (a) (b) (c) Figure 4.3. SEM images for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO2-0.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). (a) (b) (c) Figure 4.4. SEM-chemical mapping Ce analysis (red), for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO2-0.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). 80 Chapter 4 (a) (b) (c) Figure 4.5. SEM-chemical mapping Y analysis (green), for the samples Pt/0.9CeO2-0.1Y2O3 (a), Pt/0.7CeO2-0.3Y2O3 (b) and Pt/0.4CeO2-0.6Y2O3 (c). 3.5. Catalyst characterization by transmission electron microscopy (TEM). The images obtained by TEM for the Pt/xCeO2-(1-x)Y2O3 catalysts, with x = 1, 0.9, 0.7, 0.4 and 0, are shown in Figure 4.6. It is possible to observe a decrease of crystallinity with yttrium addition. This result is in agreement with XRD analysis. In the case of the catalyst with x = 0.4 it is possible to appreciate a heterogeneous particle size distribution, with the presence of crystalline and shapeless domains. This observation justifies the presence of the peaks in the XRD patterns and likely the new peak observed in the Raman spectra. Ou et al. [43] observed, using detailed TEM studies, a large lattice distortion with addition of yttrium. It was suggested that these lattice distortion imperfections were induced by small clusters of dopant cations. Furthermore, the Pt particle size distribution could not be calculated due to the high Pt dispersion, in closed agreement with XR diffraction. Some small Pt nanoparticles (indicated by a white circle) could be observed, except for Pt/0.4CeO2-Y2O3 and Pt/Y2O3, i.e. a very low Pt dispersion which can be due to a lower metal-support interaction when using Y2O3 as a support. Anyway, the presence of Pt was confirmed by EDS. The same behaviour has been found in gold catalysts [44][45]. 81 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. (c) (b) (a) 5 nm (d) 5 nm (e) Figure 4.6. TEM images of Pt/xCeO2-(1-x)Y2O3 catalysts, x = 1 (a), x = 0.9 (b), x = 0.7 (c), x = 0.4 (d) y x = 0 (e). 3.6. Catalysts characterization by temperature-programmed reduction with H2 (H2-TPR). The reducibility of the catalysts was studied by using temperatureprogrammed reduction techniques. H2-TPR profiles (H2 consumption) for xCeO2-(1-x)Y2O3 supports and Pt/xCeO2-(1-x)Y2O3 catalysts, with x = 1, 0.9, 0.7, 0.4 and 0, are shown in Figure 4.7 (a) and (b), respectively. The TPR profile for the pure ceria support exhibits two peaks, one at 760 K and another one at 1050 K, Figure 4.7 (a). These peaks are attributed to surface and bulk reduction, respectively [44][46][47][48]. Identical profiles were obtained with the supports with low yttrium content. However, the reduction peak attributed to bulk reduction decreases in intensity with increasing the yttrium loading. This result suggests that the reduction peak at low temperature could not be ascribed only to the removal of oxygen surface, but also to the reduction of bulk oxygen to some extent. This is in agreement with the results obtained by Atribak et al. [17]. It is speculated that the reduction of the bulk lattice oxygen in the solid solution become easier because of the structural distortion derived from the replacement of Ce (IV) with Y (III). The defects generated by the incorporation of yttrium in the ceria lattice could favour the migration of bulk oxygen to the surface. In summary, the structural distortion facilitates the 82 Chapter 4 migration of bulk species [33]. This result is consistent with those obtained from Raman analysis, and implies that the formation of the solid solution could promote the reduction of the Ce (IV) species. However, for high Y content (x = 0.4), the reduction profile was similar to that obtained with the pure yttrium oxide support. The addition of platinum to the ceria support produced an important change in the ceria surface reduction temperature, as evidenced by the shift of the reduction peak towards lower temperatures [44][49] (Figure 4.7). However, in the case of the Pt/Y2O3 catalyst the metal addition did not favoured the reducibility at low temperatures. In this point it is interesting to add that the addition of Y (III) clearly facilitates Ce (IV) reduction. Thus, it was possible to observe that the reduction peaks were shifted to lower temperatures in the catalysts, as compared with the supports. However, all the catalyst with Y in the support presented a further peak shift at lower temperatures, compared with the Pt/CeO2 catalyst. Moreover, the shape of these peaks was also different than those for the Pt/CeO2 catalyst. For the pure ceria-supported catalyst, a broad peak of hydrogen consumption at low temperature was obtained, which could be deconvoluted into two contributions, at 575 K and 610 K. This broad reduction peak includes the reduction of surface ceria in close contact with the metal, together with the reduction of platinum species [21]. However, in the case of the Y-containing ceria catalysts, a wide peak was observed between 470-620 K, and another one at 680 K, except in the catalyst with the highest yttrium content. The presence of these two peaks could be related with different reducible species; in this case, the peak at lowest temperature is the reduction of ceria in close contact with the platinum particles, and the peak at highest temperature corresponds to the reduction of carbonates on the ceria surface, these carbonates becoming more stables with the addition of yttrium. In the case of the highest yttrium content, x = 0.4, the catalyst presented two peaks; one at 505 K, assigned to ceria reduction, and another one at a higher temperature, 885 K, corresponding to Y2O3. The yttrium oxides could be reduced at temperatures about 773 K, very similar to the literature data [25][50]. Therefore, it seems clear from these TPR results that in all catalysts that contain cerium, except for x = 0.4, the reduction treatment at 773 K was enough to produce the surface reduction of ceria and, consequently, the creation of oxygen vacancies. On the other hand, the reduction at low temperature (523 K) will affect each catalyst to a different extent. Furthermore, this fact could justify the low activity shown by the catalyst with high yttrium 83 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. content and pure yttria, as these both catalysts presented a similar reduction profile in the TPR experiments. (a) -1 907 K -1 0.002 mmol H2· s ·g H2 consumption, a.u. x=0 907 K x = 0.4 690 K 815 K x = 0.7 800 K 665 K x = 0.9 760 K 1050 K x=1 400 600 800 1000 1200 Temperature, K (b) -1 -1 H2 consumption, a.u. 0.001 mmol H2.·s ·g x=0 x = 0.4 carbonates Pt-Ce x = 0.7 x = 0.9 x=1 400 600 800 1000 1200 Temperature, K Figure 4.7. TPR profiles for xCeO2-(1-x)Y2O3 (a) and Pt/xCeO2-(1-x)Y2O3 (b), with x = 1, 0.9, 0.7, 0.4 and 0. 84 Chapter 4 3.7. Catalyst characterization by X-ray photoelectron spectroscopy (XPS). The surface composition of the Pt/xCeO2-(1-x)Y2O3 catalysts was analyzed by XPS, after calcination at 773 K. The most interesting results obtained are summarized in Table 4.3. As it can be seen, the binding energy of the Y 3d5/2 level was similar for all the catalysts, within the precision limits of the measurement, at around 156.6 eV (typical binding energy for Y 3d5/2 [Y2O3]) [51][52]. However, a shift of the position of the O 1s band towards lower binding energies was observed as the yttrium loading increased. In accordance with the literature, the O 1s XPS spectra are fitted with three peaks contributions. One peak at BE = 528.8–529.0 eV may belong to lattice oxygen O2 in solid solutions [53], another one at BE = 531.0 eV can be ascribed to adsorbed oxygen or hydroxyl groups [53] and the last one at 532.4 eV that could be attributed to -OH groups [54], carbonate -CO2 species [55] or to the lack of structural homogeneity at the grain boundaries of CeO2 particles [56]. In the case of the solid solution oxides, Figure 4.8, a higher O 1s binding energy of the lattice oxygen in solid solutions was observed for higher ceria content (x = 0.9), followed by a decrease of O 1s binding energy with the increase of the yttrium content. This result can be explained in terms of the structural properties. The oxide symmetry formed favours the oxygen diffusion thorough the lattice due to an adequate size of the channel for oxygen migration and a decrease of the binding energy that would be expected as the yttrium content increase. Table 4.3. XPS characterization of Pt/xCeO2-(1-x)Y2O3 catalysts calcined at 673 K. Catalyst BE O 1s, eV BE O 1s, eV BE O 1s, eV BE Y 3d5/2, eV x=1 529.1 531.5 --- --- x = 0.9 529.6 531.7 532.8 157.3 x = 0.7 528.8 531.1 532.1 156.7 x = 0.4 527.8 529.6 532.0 157.0 x=0 528.7 530.0 532.0 156.9 85 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 529.1 eV 531.5 eV x=1 529.6 eV 531.7 eV 532.8 eV Intensity, a.u. x = 0.9 531.1 eV 528.8 eV 532.1 eV x = 0.7 532.0 eV 529.6 eV 527.8 eV x = 0.4 530.0 eV 532.0 eV 528.7 eV x=0 524 525 526 527 528 529 530 531 532 533 534 535 536 Binding Energy, eV Figure 4.8. XPS results of O 1s of fresh catalysts, calcined at 773 K. The chemical state of cerium ions in the catalysts after the different reduction treatments was also studied by XPS. The relative amounts of Ce (III) in the catalysts after the various reduction treatments are plotted in Figure 4.9 as a function of the yttrium content. It can be seen that, in all cases, there is a certain amount of Ce (III) even in the fresh catalysts, as shown before in Chapter 3, this fact being assigned to the partial reduction of Ce (IV) ions during the XPS experiments [57][58]. One parameter that strongly affects the photo-reduction of CeO2 during XPS analysis is its crystallinity, in such a way that amorphous cerium oxide samples are reduced more extensively than crystalline materials [59]. Taking into account that the supports have been prepared in a similar way, and that the XRD patterns indicate a similar degree of crystallinity, it can be assumed that the reducibility of Ce (IV) in the catalysts, after calcination, was mainly affected by the oxide composition. As expected, the relative amount of Ce (III) increases with the reduction temperature but, as shown in Figure 4.9, there was a similar trend after the different treatments. In the fresh samples, the relative amount of Ce (III) increased for low yttrium contents, x = 0.9, and then remained nearly unchanged. In the case of the reduced samples, the relative amount of Ce (III) is maximum for x = 0.9, then decreases for x = 0.7, and then, increases slightly with increasing the yttrium content. These results are in agreement with H2TPR. 86 Chapter 4 50 40 % Ce(III) 30 20 10 Fresh Red. 523 K Red. 773 K 0 0.0 0.2 0.4 0.6 Yttrium content, % Figure 4.9. Relative amount of surface Ce (III) (%) in Pt/xCeO2-(1-x)Y2O3 catalysts, as function of the yttrium content, after reduction treatments. 3.8. Catalysts characterization by temperature-programmed desorption of CO2 and CO (CO2/CO-TPD). The surface chemistry of the Pt/xCeO2-(1-x)Y2O3 catalysts was also characterized by temperature-programmed desorption experiments of CO2 and CO from the samples previously saturated with CO. The CO2 desorption profiles usually show two main peaks: the first one, at low temperature, is attributed to the oxidation of CO species adsorbed on the metal nanoparticles; the second peak, at higher temperature, is assigned to decomposition of the carbonate species formed on the supports [60][61]. The CO2 desorption profiles obtained with the catalysts reduced at 523 K are shown in Figure 4.10 (a). It can be seen that the presence of yttrium in the support favours the formation of CO2 at low temperature. However, it is interesting to add that all catalysts doped with yttrium showed less CO2 formation than Pt/CeO2. This is in agreement with the PROX results, as it will be shown below. At this point, it is interesting to note that the Raman, H2-TPR, XPS and CO2-TPD results are in all agreement: the addition of yttrium to the support facilitates the oxygen mobility. 87 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. The CO desorption profiles are shown in Figure 4.10 (b). It can be seen that the presence of yttrium in the supports hinders the evolution of CO. This fact could be related to the retention capacity of CO showed by the catalyst or, more likely, with the low adsorption capacity of these samples due to the presence of carbonates in the catalyst surface, as it has been shown in the TPR results. 88 Chapter 4 0.0001 mmol CO2·g x=1 x = 0.9 x = 0.7 x = 0.4 x=0 -1 CO2 desorption, a.u. (a) 300 350 400 450 500 550 600 650 700 750 Temperature, K 0.00001 mmol CO·g -1 x=1 x = 0.9 x = 0.7 x = 0.4 x=0 CO desorption, a.u. (b) 300 350 400 450 500 550 600 650 700 750 Temperature, K Figure 4.10. CO2 and CO desorption profiles for Pt/xCeO2-(1-x)Y2O3 catalysts (x = 1, 0.9, 0.7, 0.4, 0) reduced at 523 K (a) and (b) respectively. 89 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 3.9. Catalytic behaviour. 3.9.1. CO oxidation monitored by gas chromatography: effect of the reaction and reduction temperature. The reaction profiles in terms of CO conversion and CO 2 selectivity for the Pt/xCeO2-(1-x)Y2O3 catalysts, at different reaction temperatures and reduction treatments, with a gas feed containing 2% CO, 2% O2, 20% H2 and He as balance, are shown in Figure 4.11 and Figure 4.12, respectively. The light-off curves in Figure 4.11 show the influence of the presence of yttrium in the support and of the reduction temperature in the CO oxidation behaviour. As it can be observed in Figure 4.11 (a) the catalytic activity is affected by yttrium incorporation. Catalysts with x ≤ 0.7 present a similar trend. The catalytic activity passes through a maximum, at 373 K, close to 90-93% of conversion, and then decreases with the increase of the temperature. The decrease of the CO conversion at high temperatures could be associated with the WGS reverse reaction or with the competition between H2 and CO oxidation. After a reduction treatment at 523 K, all the doped catalysts present a lower CO conversion than the catalyst with the pure ceria support. This result is in agreement with the CO2/CO-TPD results, item 3.8, where all the doped catalysts presented a lower CO oxidation capacity (lower CO2 desorption) than the Pt/CeO2 catalysts. Furthermore, the catalyst with x = 0.4 and Pt/Y2O3 presented a much lower CO conversion. These results are in accordance with the TPR results, which showed that these catalysts present carbonate groups in the surface. As it has been shown in Chapter 3, the surface groups in the catalysts affect the catalytic activity. In this case, the presence of surface carbonates could influence the catalytic activity at low temperature, due to a higher stability present by these groups, with the increase of yttrium proportion. Another analysis concerns how the yttrium addition affects the catalytic activity after an increase in the reduction temperature, Figure 4.11 (b). After a reduction treatment at 773 K the catalytic activity slightly increases, with a CO conversion of 93% in the temperature range 340-380 K. Apparently, the oxygen vacancies created upon the reduction treatment at high temperature, in the metal-support inter-phase, favour a distorted adsorption of CO [62] and favours oxidation to CO2. This effect of the reduction temperature in the CO oxidation activity has been previously reported in the literature for Pt-CO catalysts supported on yttrium-doped zirconia [63]. 90 Chapter 4 F. Dong et al. [64] investigated the OSC performance of Pt/CeO2-ZrO2-Y2O3 (CZY) catalysts, and they observed that higher oxygen mobility was presented due to the homogeneous structure of the CZY oxide, which was very important for the catalytic performance. Furthermore, these authors also demonstrated the promoter role of Pt in the OSC, which increased with decreasing the size of the platinum particles dispersed on the CZY support. As it has been reported in the literature [65][66][67], the support surface provides releasable lattice oxygen for the oxidation of CO adsorbed on the metal surface. Taking this in mind, the Ce (IV)/Ce (III) reversible redox process on the support surface can be an important rate limiting step for this reaction. G. Xiao et al. [12] studied the CO oxidation in cerium doped with lanthanum, zirconium, yttrium, tin and praseodymium, and observed a negative effect for CeYO, CeLaO and CeZrO. This fact was justified by the presence of doping cations with a stable valence state that partially suppressed the Ce (IV)/Ce (III) conversion and hindered the dynamic OSC of ceria. Figure 4.12 (a) and (b) showed the CO2 selectivity for the catalyst series reduced at 523 K and at 773 K, respectively. It is possible to observe that the CO2 selectivity in the temperature range where high CO conversions were achieved was around of 43-53 %, depending on the catalyst (Figure 4.12) 91 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 100 80 CO conversion, % (a) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 60 40 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 (b) CO conversion, % 80 60 40 x=1 x = 0.9 x = 0.7 x = 0.4 x=0 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K Figure 4.11. CO oxidation light-off curves for Pt/xCeO2-(1-x)Y2O3 catalysts, reduced at 523 K (a) and at 773 K (b). 92 Chapter 4 100 (a) CO2 selectivity, % 80 60 40 x=1 x = 0.9 x = 0.7 x = 0.4 x=0 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 (b) CO2 selectivity, % 80 60 40 x=1 x = 0.9 x = 0.7 x = 0.4 x=0 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K Figure 4.12. CO2 selectivity profiles for Pt/xCeO2-(1-x)Y2O3 catalysts, reduced at 523 K (a) and at 773 K (b). 93 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. 3.9.2. CO oxidation monitored by gas chromatography: effect of the feed composition. Another fact that may affect the reaction mechanism is the composition of the gas feed, determined by the λ value (λ = 2[O2]/[CO]). This effect has been studied by increasing the O2 content in the gas feed during the oxidation reaction, using a feed of 2% CO, 0.6-2% O2, 20% H2 balanced with He, with the Pt/0.7CeO2-0.3Y2O3 catalyst reduced at 523 K and at a reaction temperature of 353 K. The evolution of CO and O2 conversions and CO2 selectivity with λ are plotted in Figure 4.13. It can be seen that the increase of the O2 concentration in the feed affects neither the CO conversion nor the CO2 selectivity. 100 XCO XO2 SCO2 80 % 60 40 20 0 0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.0 , 2[O2]/[CO] Figure 4.13. CO preferential oxidation on Pt/0.7CeO2-0.3Y2O3 catalyst, reduced at 523 K, with the reaction temperature at 353 K; gas feed composition: 2% CO, 0.6-2% O2, 20% H2 and balanced He. 3.9.3. CO oxidation monitored by operando DRIFT spectroscopy: effect of the reaction temperature. In order to analyze in detail the mechanism taking place in the course of the catalytic reaction, operando DRIFTS analysis has been performed. The profiles obtained in the DRIFTS cell for the CO oxidation reaction are shown in Figure 4.14 (a) and (b), for Pt/CeO2 and Pt/0.7CeO2-0.3Y2O3, respectively. For both catalysts, the presence of bands in the region between 3000 cm-1 and 3500 cm-1 attributed to surface hydroxyl groups (-OH) and water molecules 94 Chapter 4 adsorbed on the support can be appreciated. During the PROX reaction, it was observed that an increase of the reaction temperature resulted in a decrease of the signal of water and hydroxyl groups (bands at 3640 cm -1, 3511 cm-1 and ~ 3180 cm-1), with a very sharp decrease from 313 K to 343 K. As it has been shown in Chapter 3, some authors have reported that the presence of surface -OH groups could facilitate the formation of carbonates by the reaction between CO and –OH groups [68][69][70]. The catalyst prepared with the nitrate precursor presented labile hydroxyl species capable of participating in the reaction process, at low temperature (see Chapter 3). The participation of these species in the formation of carbonates could justify the decrease of band corresponding to -OH groups. The presence of CO species adsorbed on the support and on the catalyst surface can be appreciated in a range between 2240-1860 cm-1. Peaks at 2180-2175 cm-1 and 2116-2109 cm-1, assigned CO adsorbed on Ce (IV) and CO adsorbed on Ce (III), respectively, and/or to CO in the gas phase, are present. This fact is an indication that the support is partially reduced. The peaks at 2032 cm-1 and 2028 cm-1 for the Pt/CeO2 and Pt/0.7CeO2-0.3Y2O3 catalysts, respectively, are assigned to CO adsorbed on metallic Pt [66][68]. Both peaks present a very similar sharp shape, which could indicate that Pt presents a comparably dispersion in both catalysts. Furthermore, DRIFTS experiments demonstrated the presence of bands due to formates and carbonates between 1570-1040 cm-1, in agreement with earlier observations [68][69][71][72][73][74], together with specific bands corresponding to carbonates, carboxylates or formates, depending of the catalyst used. In the case of the Pt/CeO2 catalyst, Figure 4.14 (a), it was possible to observe the presence of bands characteristic of unidentate carbonates (bands at 1549 cm-1, 1298 cm-1 and 1043 cm-1), bidentate carbonates (bands at 1562 cm-1, 1298 cm-1 and 1061 cm-1), polydentate carbonates (bands at 1464 cm-1, 1359 cm-1 and 1061 cm-1), and formate [68][72][74][75]. The presence of formates was identified mainly by peaks at 2926 cm-1 and 2840 cm-1, which are characteristic of the –CH stretching vibration, and by peaks at 1560 cm-1 and 1384-1371 cm-1, attributed to symmetric and anti-symmetric bending vibrations of carbonate groups, namely γas (-OCO) and γs (-OCO), respectively [76][77]. It is interesting to add that it was observed, for the Pt/CeO2 catalyst, a decrease of the characteristic bands of carbonates and formates with the increase of the reaction temperature, to 313 K from 333 K. In the case of Pt/0.7CeO2-0.3Y2O3, characteristics bands principally of carbonate unidentate (bands at 1516 cm-1, 1379 cm-1 and 1073 cm-1) [68][72][74][75] were observed. Furthermore, in this case it was not possible to appreciate an important 95 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. decrease of referent bands. Comparing the DRIFTs results with the PROX results described above, it is possible to appreciate that, somehow, the catalysts act in different ways depending on the presence or absence of yttrium in the catalyst and on the different type of surface groups. Additionally, it is interesting to add that, as it has been suggested by some authors [76][78], the formates surface could behave as intermediates involved in the CO conversion mechanism. This fact could be an indication of the improved catalytic activity of the Pt/CeO2 catalyst in comparison with the Pt/0.7CeO2-0.3Y2O3 catalyst due to the presence of a higher amount of formates groups in the first one. In other words, it was appreciated that, by one hand, the presence of formate and bidentate carbonates could favour the CO oxidation on the Pt/CeO2 catalyst, and on the other hand, the presence of unidentate carbonates could affect negatively the catalytic activity of the yttrium modified systems. These results confirm the effect of yttrium in the catalytic behaviour of the studied samples. (b) (a) KM, a.u. KM, a. u. 473 K 313 K 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm -1 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm -1 Figure 4.14. DRIFT spectra obtained in the CO oxidation under 2% CO, 10% air, 20% H2 and N2 as balance gas feed for Pt/CeO2 (a) and Pt/0.7CeO2-0.3Y2O3 (b) reduced at 523 K. The starting reaction temperature was 313 K, and it was increased by 20 K steps from bottom to top. 96 Chapter 4 4. Conclusions. A series of Pt catalysts prepared with supports containing different proportions of ceria and yttria were evaluated in the CO PROX reaction. From the obtained results it was possible to conclude that addition of Y (III) to the ceria support facilitates the Ce (IV) reduction and, as a result, the oxygen mobility of the support. However, the solid solution oxide formation was hindered at higher yttrium concentrations. It was observed the presence of more stable surface carbonates on the surface of these catalysts, and this fact could justify their lower catalytic activity, mainly for high yttrium contents, as compared to the catalyst containing pure ceria as support. 5. References. [1] A. Trovarelli, C. de Leitenburg, M. Boaro, G. Dolcetti, Catal. Today, 50 (2000) 353367. [2] A. Trovarelli, Catal. Rev. Sci. Eng., 38 (1996) 439-520. [3] M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today, 68 (2001) 53-61. [4] A. Trovarelli, F. Zamar, J. Lorca, C. Leitenburg, G. Dolcetti, J.T. Kiss, J. Catal., 169 (1997) 490-502. [5] H. Roh, H.S. Potdar, K. Jun, S.Y. Han, J. Kim, Catal. Letters, 93 (2004) 203-207. [6] J. Kaspar, P. Fornasiero, M. Graziani, Catal. Today, 50 (1999) 285-298. [7] S. Rossignol, Y. Madier, D. Duprez, Catal. Today, 50 (1999) 261-270. [8] J.C. Serrano-Ruiz, J. Luettich, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, J. Catal., 241 (2006) 45-55. [9] C. Descorme, Y. Madier, D. Duprez, J. Catal., 196 (2000) 167-173. [10] P. Fornasiero, R. Di Monte, G.R. Rao, J. Kaspar, S. Meriani, A. Trovarelli, M. Graziani, J. Catal., 151 (1995) 168-177. [11] H. Vidal, S. Bernal, J. Kaspar, M. Pijolat, V. Perrichon, G. Blanco, J.M. Pintado, R.T. Baker, G. Colon, F. Fally, Catal. Today, 54 (1999) 93-100. [12] G. Xiao, S. Li, L. Chen, Microp. Mesop. Materials, 120 (2009) 426-431. [13] D. Wattanasiriwech, S. Wattanasrriwech, J. Mater. Sci., 43 (2008) 6473-6479. [14] J.V. Herle, T. Horita, T. Kawada, N. Sakai, H. Yokokawa, M. Dokiya, J. Europ. Ceram., Soc. 16 (1999) 961-973. [15] B.C.H. Steele, J.M. Floyd, Proc. Br. Ceram. Soc., 19 (1971) 55-76. [16] L. Llieva, G. Pantaleo, I. Ivanov, R. Zanella, A.M. Venezia, D. Andreeva, International J. Hydrogen Enegy, 34 (2009) 6505-6515. [17] I. Atribak, A. Bueno-López, A. García-García, J. Molecular Catal. A: Chemical, 300 (2009) 103-110. [18] J. Lingyun, H. Mai, L. Jiqing, L. Mengfei, G. Libiao, H. Jun, J. Rare Earths, 26 (2008) 614-618. 97 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. [19] S. Yusheng, L. Lei, Z. Yingying, L. Xingyi, Z. Qi, W. Kemei, J. Rare Earths, 27 (2009) 411-417. [20] I. Dobrosz-Gómez, I. Kocemba, J.M. Rynkowski, Appl. Catal. B: Env., 83 (2008) 240-255. [21] J. Silvestre-Albero, F. Coloma, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Appl. Catal. A: Gen., 304 (2006) 159-167. [22] K.A. Gschneidner, F.W. Calderwood, Bulletin of Alloy Phase Diagrams, 3 (1982) 192-194. [23] F.G. Meng, L.B. Liu, H.S. Liu, Z.P. Jin, Computer Coupling of Phase Diagrams and Thermochemistry, 30 (2006) 323-325. [24] M.F. Luo, M. He, Y.L. Xie, P. Fang, L.Y. Jin, Appl. Catal. B: Env., 69 (2007) 231-218. [25] G.B. Sun, K. Hidajat, X.S. Wu, S. Kawi, Appl. Catal. B: Env., 81 (2008) 303-312. [26] M.R. Gallego, La difracción de los rayos X, Edición Alambra (1982). [27] J.B. Wang, S.Z. Hsiao, T.J. Huang, Appl. Catal. A: Gen., 246 (2003) 197-211. [28] K. Krishna, A. Bueno-López, M. Makkee, J.A. Moulijn, Appl. Catal. B: Env., 75 (2007) 189–200. [29] P. Singh, M.S. Hegde, J. Solid State Chemistry, 181 (2008) 3248-3256. [30] J. Kimpton, T.H. Randle, J. Drennan, Solid State Ionics, 149 (2002) 89– 98. [31] J.F.Q. Rey, E.N.S. Muccillo, J. Europ. Ceram. Soc., 24 (2004) 1287-1290. [32] X.-M. Lin, L.-P. Li, G.-S. Li, W.-H. Su, Mater. Chem. Phys., 69 (2001) 236. [33] Q. Wu, J. Chen, J. Zhang, Fuel Processing Technology, 89 (2008) 993-999. [34] S.T. Aruna, V.K. William Grips, V. Exhil Selvi, K.S. Rajam, J. Appl. Electrochem., 37 (2007) 991-1000. [35] P. Vidmar, P. Fornasiero, J. Kaspar, G. Gubitosa, M. Graziani, J. Catal., 171 (1997) 160-168. [36] J. Li, Y. Han, Y. Zhu, R. Zhou, Appl. Catal. B: Env., 108-109 (2011) 72-80. [37] J.R. McBride, K.C. Hass, B.D. Poindexter, W.H. Weber, J. Appl. Phys., 76 (1994) 2435-2441. [38] D. Gamarra, G. Munuera, A.B. Hungría, M. Fernández-García, J.C. Conesa, P.A. Midgley, X.Q. Wang, J.C. Hanson, J.A. Rodriguéz, A. Martínez-Arias, J. Phys. Chem. C, 111 (2007) 11026-11038. [39] A. Ubaldini, M.M. Carnasciali, J. Alloys and Compounds, 454 (2008) 374-378. [40] M. Yashima, J.H. Lee, M. Kakihana, M. Yoshimura, J. Phys. Chem. Solids, 58 (1997) 1593-1597. [41] Y. Repelin, C. Proust, E. Husson, J.M. Beny, J. Solid State Chemistry, 118 (1995) 163-169. [42] J.D. McCullough, J.D. Britton, J. Am. Chem. Soc., 74 (1952) 5225-5227. [43] D.R. Ou, T. Mori, F. Yei, M. Takahashi, J. Zou, J. Drennan, Acta Materialia, 54 (2006) 3737-3746. [44] G. Avgouropoulos, M. Manzoli, F. Boccuzzi, T. Tabakova, J. Papavasiliou, T. Ioannides, V. Idakiev, J. Catal., 256 (2008) 237-247. [45] H. Sakurai, T. Akita, S. Tsubota, M. Kiuchi, M. Haruta, Appl. Catal. A: Gen., 291 (2005) 179-187. 98 Chapter 4 [46] J.L. Ayastuy, M.P. González-Marcos, A. Gil-Rodríguez, J.R. González-Valesco, M.A. Gutiérrez-Ortiz, Catal. Today, 116 (2006) 391-399. [47] P. Fornasiero, G. Balducci, R. Di Monte, J. Kaspar, V. Sergo, G. Gubitosa, A. Ferrero, M. Graziani, J. Catal., 164 (1996) 173-183. [48] S. Ricote, G. Jacobs, M. Milling, Y. Ji, P.M. Patterson, B.H. Davis, Appl. Catal. A: Gen., 303 (2006) 35-47. [49] J.C. Serrano-Ruiz, G.W. Huber, M.A. Sánchez-Castillo, J.A. Dumesic, F. RodríguezReinoso, A. Sepúlveda-Escribano, J. Catal., 241 (2006) 378–388. [50] F.B. Passos, E.R. Oliveira, L.V. Matto, F.B. Noronhe, Catal. Lett., 110 (2006) 261-267. [51] C.D. Wagner, W.M. Riggs, L.E. Davis, J.F. Moudelr, G.E. Muilenberg, Handbook of X-ray photoelectron spectroscopy, Perkin-Elmer, Eden Prairie (1979) 98. [52] M.D. Ulrich, J.E. Rowe, D. Niu, G.N. Parsons, J. Vac. Sci. Technol. B, 21 (2003) 17921797. [53] X. Wang, G. Lu, Y. Guo, Y. Xue, L. Jiang, Y. Guo, Z. Zhang, Catal. Today, 126 (2007) 412–419. [54] J.P. Holgado, G. Munuera, J.P. Espinós, A.R. González-Elipe, Appl. Surface Science, 158 (2000) 164–171. [55] E. Papparazzo, Surf. Sci. Lett., 234 (1990) L253–L258. [56] G. Rama-Rao, T. Shripathi, J. Electron Spectrosc. Relat. Phenom., 87 (1997) 121-128. [57] M.S.P. Francisco, V.R. Mastelaro, P.A.P. Nascente, A.O.A. Florentino, J. Phys. Chem. B., 105 (2001) 10515-10522. [58] B.M. Reddy, A. Khan, Y. Yamada, T. Kobayashi, S. Loridant, J.-C. Volta, J. Phys. Chem. B., 107 (2003) 11475-11484. [59] P.W. Park, J.S. Ledford, Langmuir, 12 (1996) 1794-1799. [60] A. Trovarelli, Catalysis by ceria and related materials, 2ª Ed. (2002) London. [61] N.F.P. Ribeiro, F.M.T. Mendes, C.A.C. Perez, M.M.V.M. Souza, M. Schmal, Appl. Catal. A: Gen., 347 (2008) 62-71. [62] P. Concepción, A. Corma, J. Silvestre-Albero, V. Franco, J.Y. Chane-Ching, J. of Am. Chem. Soc., 126 (2004) 5523-5532. [63] E.Y. Ko, E.D. Park, H.C. Lee, D. Lee, S. Kim, Angew. Chem., 46 (2007) 734-737. [64] F. Dong, T. Tanabe, A. Suda, N. Takahashi, H. Sobukawa, H. Shinjoh, Chemical Engineering Science, 63 (2008) 5020-5027. [65] K. Ramesh, L.W. Chen, F.X. Chen, Y. Liu, Z. Wang, Y.F. Han, Catal. Today, 131 (2008) 477-482. [66] R. Cracium, B. Nentwick, K. Hadjiivanov, H. Knözinger, Appl. Catal. A: Gen., 243 (2003) 67-79. [67] L.M. Molina, B. Hammer, Phys. Rev. B., 69 (2004) 155424-22. [68] O. Pozdnyakova, D. Teschner, A. Wootsch, J. Kröhnert, B. Steinhauer, H. Sauer, L. Toth, F.C. Jentoft, A. Knop-Gericke, Z. Paál, R. Schlögl, J. Catal., 237 (2006) 1-16. [69] K. Föttinger, R. Schlögl, G. Rupprechter, Chem. Commun., (2008) 320-322. [70] H. Tanaka, M. Kuriyama, Y. Ishida, S.I. Ito, T. Kubota, T. Miyao, S. Naito, K. Tomishige, K. Kunimori, Appl. Catal. A: Gen., 343 (2008) 125-133. 99 Preferential CO oxidation (PROX) on Pt/CeO2-Y2O3 catalysts. [71] D. Teschner, A. Wootsch, O. Pozdnyakova-Tellinger, J. Kröhnert, E.M. Vass, M. Hävecker, S. Zafeiratos, P. Schnörch, P.C. Jentoft, A. Knop-Gericke, R. Schlögl, J. Catal., 249 (2007) 318-327. [72] C. Binet, M. Daturi, J.C. Lavalley, Catal. Today, 50 (1999) 207-225. [73] A. Badri, C. Binet, J.C. Lavalley, J. Phys. Chem., 100 (1996) 8363-8368. [74] P. Bera, A. Hornés, A.L. Cámara, A. Matínez-Arias, Catal. Today, 155 (2010) 184191. [75] A. Martínez-Arias, A.B. Hungría, M. Fernández-García, J.C. Conesa, G. Munuera, J. Power Sources, 151 (2005) 32-42. [76] P.O. Graf, D.J.M. de Vlieger, B.L. Mojet, L. Lefferts, J. Catal., 262 (2009) 181-187. [77] H. Zou, S. Chen, Z. Liu, W. Lin, International J. of Hydrogen Energy, 34 (2009) 9324-9333. [78] G. Jacobs, L. Williams, U. Graham, D. Sparks, B.H. Davis, J. Phys. Chem. B, 107 (2003) 10398-10404. 100 CHAPTER 5 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalysts. Abstract. This chapter reports the effect of niobium addition to a series of Pt/CeO2 catalysts in the preferential CO oxidation reaction. The catalysts have been prepared using [Pt(NH3)4](NO3)2 as the metal precursor and xCeO2-(1-x)Nb2O5 mixed oxides as supports, where x = 1, 0.9, 0.7, 0.4 and 0. The main objective of this chapter is to ascertain the effect of the doping cation in the chemical properties of the support and on the catalytic behaviour of these systems when they are used as supports of Pt nanoparticles. The influence of the reduction temperature and the niobium content was evaluated. Incorporation of niobium in the formulation of Pt/CeO2 catalysts favors the catalytic activity and selectivity. 130 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. 1. Introduction. One of the most intriguing aspects of ceria-based catalysts is that their properties strongly depend on the pre-treatment conditions used and on the exact composition of the oxide. In this sense, it is known that the oxygen storage capacity (OSC) of pure ceria is inhibited when these systems are used in high temperature applications, e.g. automotive applications. In order to overcome this drawback, the stabilization of ceria by incorporation of a second metal, e.g. zirconia, is mandatory [1]. The large number of applications of CeO2 are based on its interesting properties such as: (i) the crystal size can be tailored by modifying the synthesis conditions [2], (ii) the reducibility of CeO2 can be altered by incorporation of others metals (e.g. Ce-Zr) due to solid solution formation [1], (iii) the presence of defect sites modifies the reduction properties [3], and (iv) the ability of cerium to be in either the (III) or (IV) oxidation states can be used in industrial processes (catalytic processes). Furthermore, it is known that the ionic conductivity of ceria is enhanced by doping with other rare-earth cations. Moreover, it depends on the ionic radius of the doping cation [4] and the effect that this radius has on distorting the lattice structure [5]. O’Connell et al. [6] suggested that the anion vacancies produced by the introduction of M (III) ions into the ceria lattice may enhance the catalytic activity. It is known that doping with other ions could lead to enhanced activity for different reasons. For example, in the case of M (V) ions like niobium, one might be able to introduce extra oxygen anions that would be more easily removed [7]. Niobium-based materials are effective catalysts in several applications, e.g. pollution abatement [8], selective oxidation [9], hydrocarbon conversion reactions [7], hydrogenation and dehydrogenation [10], photochemistry and electrochemistry [11][12] and polymerization among others [13]. The number of references in the literature concerning niobium catalysts have been steadily increasing over the last two decades, what reflects the growing interest in this area of research [13][14][15]. A major application of niobium-based catalysts has been in the area of oxidation reactions, due to the redox properties of niobium oxide catalysts. These catalysts can be constituted either as twodimensional layer (surface niobia species supported in other oxides such as Al2O3), as bulk niobium oxide pure or modified with redox species (e.g. MnOx), or as a mixed oxide (solid solution) [14]. The surface niobia species are not stable on basic oxide supports such as magnesia [16] and bismuth oxide [17] due to the incorporation of the acidic Nb (V) into these supports as a result of a strong acid-base interaction. Niobia-doped ceria materials have 102 Chapter 5 shown a good tolerance to carbon deposition [9] and excellent properties as solid oxide fuel cell (SOFC) anodes [18]. However, more research is necessary in order to extent the improved performance of these systems for other applications [11]. For example the excellent electrical properties of niobiadoped ceria were already reported by Naik and Tien [12] and De Guire et al. [19]. Some authors have also studied niobia catalysts for the CO oxidation reaction. Guerrero et al. [20] studied the promoting effect of niobium supported on alumina in the PROX reaction. The results showed that at low niobium loading, Pt/alumina catalysts exhibited an increase in the CO oxidation activity and selectivity. On the contrary, Marques et al. [21] showed a low selectivity for Pt-Sn/Nb2O5 or Pt/Nb2O5 catalysts in the CO oxidation reaction in the presence of H2 which could be explained in terms of platinum modification by the niobia (strong metal-support interaction effect - SMSI) and tin presence (bimetallic effect). In this work the catalytic activity of Pt/xCeO2-(1-x)Nb2O5 catalysts, where x = 1, 0.9, 0.7, 0.4 and 0, will be evaluated in the CO oxidation reaction in the presence of H2, with special emphasis in the influence of the cerium/niobium ratio. 2. Experimental. 2.1. Catalysts preparation and characterization. A series of niobium-doped ceria supports were prepared by the urea precipitation method. An appropriate amount of cerium nitrate (Aldrich, 99 %) and ammonium niobate (V) oxalate hydrate (Aldrich, 99.99 %), together with urea (Fluka, 98 %), were dissolved in 400 ml of ultra-pure water to obtain different supports of composition xCeO2-(1-x)Nb2O5, with x = 1, 0.9, 0.7, 0.4 and 0. The mixture was heated at 363 K with constant stirring for 11 h. Finally, some ammonium hydroxide solution was added dropwise for complete precipitation. The solid obtained was separated by filtration, washed with ultra-pure water, and dried overnight at 383 K. Finally, the synthesized supports were calcined in air at 773 K for 4 h, with a heating rate of 3 K·min−1. Different Pt/xCeO2-(1-x)Nb2O5 catalysts were prepared by the wetness impregnation method. The support was impregnated with an aqueous solution of [Pt(NH3)4](NO3)2 (Aldrich, 99.9 %), as the metal precursor, in the appropriate amount to obtain a 1 wt.% Pt loading. Afterwards, the sample was dried at 383 K overnight, and it was calcined in air at 773 K for 2 h, with a heating rate of 3 K·min−1. 103 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. The synthesized materials were characterized by different techniques: N2 adsorption isotherms, XRF, ICP-OES, XRD, TEM, SEM, H2-TPR, Raman spectroscopy, XPS, CO2/CO-TPD and H2-TPD. Experiments details and equipment used were described in Chapter 2 of this PhD Thesis. 2.2. Catalytic behaviour. In a first step, the activity of the catalysts in the PROX reaction was measured in the temperature range 313-473 K at atmospheric pressure, under a gas flow (50 cm3·min−1) containing 20% H2, 2% CO, 0.6-2% O2 and He as a balance (GHSV = 17000 h-1). Previously to the oxidation reaction the catalysts were reduced at 523 K and 773 K under a flow of hydrogen (50 cm3·min-1). Reaction products were analyzed by online gas chromatography. In order to analyze in detail the different steps taking place in the course of the reaction, the catalytic activity was also followed in-situ using diffuse reflectance infrared Fourier transform spectroscopy (DRIFTS). The catalytic tests using DRIFTS were carried out under temperature controlled conditions (313-473 K) at atmospheric pressure under a gas flow (40 cm3·min−1) containing 20% H2, 2% CO, 10% air and N2 as a balance (GHSV = 17000 h-1). Experiment details, calculations for CO and O2 conversion as well as selectivity, equipment used and so on were described before in Chapter 2 of this PhD Thesis. 3. Results and discussion. 3.1. Textural and metal loading characterization. Table 5.1 reports the Pt loading as well as the relative CeO2 and Nb2O5 content in the supports, determined by ICP-OES and XRF. The oxides’ composition covers a wide range, from pure ceria to pure niobium. Hereinafter, samples will be labelled with the nominal composition, which in all cases differs only slightly from the actual composition. The BET surface area obtained for the supports is also included in Table 5.1. It is interesting to observe the influence of the niobium content in the textural properties. Thus, the surface area of the pure ceria support is 108 m2·g-1; then it passes through a minimum for a composition x = 0.9, 84 m2·g-1, and then it increases slightly with a further increase in the niobium content. This increase of the surface area could be justified by two facts: the incorporation of niobium into the ceria lattice could change the structure of the mixed oxide or, more likely, niobium addition hinders the formation of large ceria nanocrystals, i.e. niobia addition 104 Chapter 5 hinders the sintering of ceria crystals. A similar behaviour has been described in the literature for ceria supports after incorporation of a doping cation [20][22][23]. For example, Mei et al. [22] showed an increase in the surface area of ceria-based oxides after incorporation of yttrium (Ce70Zr30O materials). According to these authors, yttrium incorporation in ceria-zirconium solid solutions can enhance the thermal stability. This fact was attributed to yttrium segregation at crystal boundaries, making crystal agglomeration or sintering difficult. Guerrero et al. [20] also observed an increase in the surface area with niobium content on Pt/Nb-Al2O3 catalysts. Table 5.1. Characterization of Pt/xCeO2-(1-x)Nb2O5 catalysts. Catalyst Pt loading, wt.% CeO2, wt.% Nb2O5, wt.% SBET, m2·g-1 (a) x=1 1.0 100 0 108 x = 0.9 0.8 89 11 84 x = 0.7 0.8 72 28 114 x = 0.4 0.8 45 55 138 x=0 0.6 0 100 186 (a) BET surface area. 3.2. X-ray diffraction analysis. The structure of the different oxides was analysed by XRD. The XRD patterns of Pt/xCeO2-(1-x)Nb2O5 catalysts are presented in Figure 5.1. The XRD profiles show six main characteristic peaks attributed to the fluorite structure of ceria [24][25][26][27] (face centred cubic structure). The niobium doped ceria-based catalysts exhibited XRD profiles very similar to those observed for yttrium-doped ceria-based catalysts (see previous chapter). In any case, niobium incorporation gives rise to both a progressive decrease in the peak intensity together with a broadening of the main diffraction peaks. This observation may be attributed either to a decrease of the crystallinity or, more likely, to a decrease in the crystal size after niobium incorporation, in close agreement with textural properties described before. At this point it is interesting to highlight that, in general, only the characteristic peaks of CeO2 are observed, thus suggesting the formation of a true mixed oxide. Only for higher niobium contents (Pt/0.4CeO2-0.6Nb2O5 catalyst) additional peaks attributed to the hexagonal structure of niobium oxide could be observed 105 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. [28][29][30][31]. Chai et al. [29] remarked the formation of the pseudohexagonal Nb2O5 crystals on samples calcined at 773 K and 873 K, which are characterized by diffraction peaks at 2θ = 22.6º, 28.4º, 36.7º and 46.2º. It is well known that cerium niobate, CeNbO4+δ, has a monoclinic fergusonite structure at room temperature [7][32][33][34][35]. Studies on the structures of the CeNbO4+δ phases have been reported in the literature with data collected on samples heated under vacuum and in air [32][36][37][38][39]. These studies have clearly identified structural modifications with four regimes as a result of the incorporation of Nb in interstitial sites with the charge being balanced by the oxidation of some of the Ce (III) normally present to Ce (IV): (i) fully oxygen stoichiometric, i.e., O4, (ii) δ = 0.08, (iii) δ = 0.25 and (iv) δ = 0.33. Each phase has been reported as a monoclinic structure type. Another interesting feature of CeNbO4+δ is that it exhibits a phase change at approximately 1023 K in air to a tetragonal scheelite-type structure [32][33][38]. The fergusonite-like structure could be considered as intermediate between the fluorite and the scheelite structures, with monoclinic symmetry [33]. The XRD data showed in Figure 5.1 confirms ceria as the major crystalline phase, and any evidence for the fergusonite formation as a second phase was not present, at least for samples rich in ceria. However, the presence of these alloys and complex oxides cannot be ruled out, at least if they are below the detection limit of the XRD instrument. A similar effect has been observed by Packer et al. [35]. However, Ramírez-Cabrera et al. [7] did observe the fergusonite structure (CeNbO4) on niobium doped ceria materials. Furthermore, no diffraction peaks attributed to Pt could be identified for the catalysts in Figure 5.1, what can be due to the small Pt crystal size below the XRD sensibility. 106 Chapter 5 CeO2 Nb2O5 x=0 Intensity, a.u. x = 0.4 x = 0.7 x = 0.9 x=1 20 30 40 50 2 60 70 80 Figure 5.1. X-rays difractograms for Pt/xCeO2-(1-x)Nb2O5 catalysts, x = 1, 0.9, 0.7, 0.4 and 0. The average ceria crystal size obtained in the different catalysts after application of the Scherrer’s equation (Equation 2.5) is listed in Table 5.2. The results obtained resemble those reported in Chapter 4 for yttrium-doped ceriabased oxides. A gradual decrease in the ceria crystal size (from 17 nm to 6 nm) with an increase of niobium content can be clearly observed. This fact is in agreement with the textural properties described before, i.e. an increase of the BET surface area after a decrease in the crystal size. Furthermore, the results described in Table 5.2 show a slight variation of the lattice constant with an increase in the niobium content (calculated using Equation 2.6), based on the (111) plane and considering the ceria cubic phase [40]. For the niobium-doped ceria-based oxides, the slight change observed in the lattice parameters indicates that not all the niobium is substituting cerium atoms in the fluorite-type structure, i.e. the solid solution has not been fully formed. Since X-ray diffraction fails to show a change in the lattice parameters after niobium incorporation, the formation of a solid solution is unlikely [41], even though we could not detect a separate niobium oxide phase. In fact, the incorporation of niobium to the ceria structure would give a rise to a large lattice modification (the ionic radium of Ce (IV) (0.097 nm) is larger than Nb (V) (0.069 nm)), which is not observed in our case. For example, Santoro et 107 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. al. [33] reported a change in the structure of LaTaO4 systems due to the size of rare-earth cation incorporated. Table 5.2. Crystallite size and lattice constant of the xCeO2-(1-x)Nb2O5 support. Catalyst Crystallite size, nm (a) Lattice constant, nm x=1 17 0.5420 x = 0.9 10 0.5415 x = 0.7 8 0.5421 x = 0.4 6 0.5424 x=0 -- -- (a) Determinated by Scherrer´s equation. 3.3. Raman spectroscopy characterization. Raman spectroscopy experiments were carried out on the supports and the catalysts, in order to further analyze the possible formation of a solid solution and to confirm the phases present in each case (Figure 5.2 (a) and (b)). In the case of the Pt/0.4CeO2-0.6Nb2O5 catalyst, it was necessary to increase the acquisition time due to low band intensity, as it is shown in the inset of Figure 5.2 (b). In the case of the supports, Figure 5.2 (a), it is interesting to observe a decrease of the intensity of the band centred at about 462 cm-1, which corresponds to the fluorite-type structure of ceria [23][42][43][44], with an increase of the niobium content. This can be due to the deformation of the framework after niobium incorporation. Furthermore, this decrease is accompanied by a shift of this peak to 464 cm-1 in the case of catalysts with x = 0.9 and x = 0.7, and to 463 cm-1 in the case of the catalyst with x = 0.4, which can be attributed to the lattice distortion due to the incorporation of a smaller cation. Previous studies reported in the literature have shown that while oxide vacancies could be introduced in the ceria by doping with oxides of metal with lower oxidation state, as it has been discussed in Chapter 4 by the introduction of Y (III); the oxide vacancies of CeO2 may be removed by doping with oxides of higher valences, as Nb (V) [7][10][45][46]. Additionally, in the catalyst with a high niobium content, x = 0.4, it is possible to observe the presence of an additional band at 706 cm-1, characteristic of Nb2O5. This observation could suggest the formation of a solid solution for samples with low niobium 108 Chapter 5 content and the formation of two solid phases in the case of solids with high niobium content. This hypothesis would be in agreement with XRD results. Raman spectroscopy studies on Nb2O5 provide information about the Nb-O bond length and bond orders, since these parameters are directly related to the Nb-O vibration frequencies [47]. Terminal Nb=O bonds typically occur between 850-1000 cm-1 and Nb-O bonds usually occur between 500-700 cm-1 [14]. The band at 714 cm-1 is characteristic of the Nb2O5 phase. This band vanishes for niobium oxide doped with ceria, possibly because of cerium incorporated into the Nb2O5 crystal lattice. Furthermore, the presence of a band centred between 540–600 cm-1 is attributed, in the literature, to the LO vibration mode of the CeO2 which appears due to the relaxation of its symmetry rules [48] and the generation of oxygen vacancies [23][49][50][51]. In our case, this band is not very clear and, after the amplification of these spectra, a small band can be observed only on the pure support. This fact may indicate that the OSC is not favored in these materials. However, additional experiments are needed to confirm this observation. In the case of the catalysts, Figure 5.2 (b), the same behaviour is observed. The main peak of ceria shows a decrease in intensity together with a shift to lower wave numbers. Interestingly, new bands appear at 305 cm-1 and 800 cm-1 for catalysts with high niobium content (e.g. Pt/0.7CeO2-0.3Nb2O5) and an additional band at 630 cm-1 for the sample Pt/0.4CeO2-0.6Nb2O5. The assignment of these new bands is difficult at this point. However, it is interesting to mention that similar bands around e.g., 831 cm-1, have been reported in the literature for CuO/CeO2 catalysts treated with oxygen [52][53]. This band has been attributed to the presence of peroxide species (O22-) in ceria. Similar species could be responsible for our observations, although further analyses are required to achieve a conclusion. 109 (a) 462 cm Intensity, a.u. Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. -1 x=0 x = 0.4 x = 0.7 x = 0.9 x=1 410 420 430 440 450 460 470 Raman shift, cm Intensity, a.u. 714 cm 480 490 500 510 -1 -1 706 cm x=0 -1 x = 0.4 x = 0.7 x = 0.9 x=1 200 300 400 500 600 700 Raman shift, cm 800 (b) 714 cm 461 cm 305 cm 900 1000 -1 -1 -1 x=0 -1 x=0 -1 Intensity, a.u. Intensity, a.u. 630 cm x = 0.4 x = 0.7 x = 0.9 x=1 200 300 400 500 600 700 800 900 1000 -1 Raman shift, cm 800 cm x = 0.4 -1 x = 0.7 x = 0.9 x=1 200 300 400 500 600 700 Raman shift, cm 800 900 1000 -1 Figure 5.2. Raman spectra of xCeO2-(1-x)Nb2O5 supports (a) and Pt/xCeO2-(1-x)Nb2O5 catalysts (b). 110 Chapter 5 3.4. SEM/EDS – chemical mapping catalysts characterization. Chemical mapping was used to analyze the distribution of cerium and niobium on the catalysts’ surface. Figure 5.3, Figure 5.4 and Figure 5.5 show the SEM micrographs for the catalysts Pt/0.9CeO2-0.1Nb2O5, Pt/0.7CeO20.3Nb2O5 and Pt/0.4CeO2-0.6Nb2O5, respectively. In Figure 5.3 it is interesting to observe the changes in the morphology with the increase of niobium content, i.e. the catalyst shifts towards thin, needle shaped particles. It is also interesting to observe the decrease in the particle size after niobium incorporation, in close agreement with the textural properties described above. From the SEM-chemical mapping analysis of cerium and niobium (Figure 5.4 and Figure 5.5, respectively) it is possible to observe the good distribution of both metals in two of the catalysts evaluated (x = 0.9 and x = 0.7 catalysts). However, in the case of x = 0.4 it is possible to observe points richer in Nb2O5. It is interesting to mention that high niobia concentrations (rich areas) are present as agglomerated particles. This fact confirms the results obtained with XRD and Raman experiments, where the presence of two separate oxide phases in the catalyst containing high niobia content was observed. (a) (b) Figure 5.3. SEM images for the samples Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO2-0.6Nb2O5 (c). (a) (b) (c) Pt/0.9CeO2-0.1Nb2O5 (a), (c) Figure 5.4. SEM-chemical mapping Ce analysis (red), for the samples Pt/0.9CeO2-0.1Nb2O5 (a), Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO2-0.6Nb2O5 (c). 111 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. (a) (b) (c) Figure 5.5. SEM-chemical mapping Nb analysis (blue and green) for the samples Pt/0.9CeO2-0.1Nb2O5 (a), Pt/0.7CeO2-0.3Nb2O5 (b) and Pt/0.4CeO2-0.6Nb2O5 (c). 3.5. Transmission electron microscopy. TEM images for the Pt/xCeO2-(1-x)Nb2O5 catalysts, where x = 1, 0.9, 0.7, 0.4 and 0, are shown in Figure 5.6. The crystal size of the oxides could not be calculated due to a high crystal agglomeration. On the other hand, Pt particle size distribution could also not be calculated due to the high metal dispersion (small Pt nanoparticles, identified with a circle). This fact is in accordance with XRD results. However, the presence of Pt was confirmed by EDS. (b) (a) (c) 5 nm (d) (e) Figure 5.6. TEM images of Pt/xCeO2-(1-x)Nb2O5 catalysts, x = 1 (a), x = 0.9 (b), x = 0.7 (c), x = 0.4 (d) y x = 0 (e). 112 Chapter 5 3.6. Temperature-programmed reduction with hydrogen. The H2-TPR profiles for the xCeO2-(1-x)Nb2O5 supports and Pt/xCeO2-(1x)Nb2O5 catalysts, x = 1, 0.9, 0.7, 0.4 and 0, are shown in Figure 5.7 (a) and (b), respectively. Identical profiles to those of pure ceria were obtained for catalysts with low niobium content. There are always two peaks, the first one at 760 K and the second one at 1050 K [53][54][55][56] (Figure 5.7 (a)). However, niobium incorporation gives rise to a decrease in the amount of ceria reduction at high temperature (bulk reduction) together with a slight increase in the hydrogen consumption at low temperature. This result suggests that the reduction peak at low temperature could not be ascribed only to the reduction of platinum, but also to the reduction of the oxide surface. This result is consistent with the conclusions obtained from Raman analysis, implying the formation of a solid solution, thus promoting the reduction of Ce (IV) species. Interestingly, the sample with the highest niobium content (x = 0.4) presents an additional reduction peak at 1170 K, characteristic of Nb2O5, i.e. this catalyst exhibits the same reducibility behaviour than pure niobium oxide. It is interesting to mention at this point that addition of Pt to these catalysts facilitates the Ce (IV) reduction, as shown in Figure 5.7 (b). Compared to the Pt/CeO2 catalyst, in the presence of niobium there is always a shift in the low temperature reduction peaks. While in the pure ceria catalyst the hydrogen consumed, at low temperature, exhibits two contributions at 575 K and 610 K, the niobium-doped ceria catalysts show a large peak centred at around 350375 K. This broad hydrogen consumption peak includes the reduction of surface ceria in close contact with the metal particles, and it could also include the reduction of platinum species [27]. However, in the case of the Pt/Nb2O5 catalyst, this low temperature peak is mainly absent. Therefore, and considering one of the reduction temperatures that will be used later on in this study, it seems clear from these TPR results that in all doped catalysts the reduction treatment at 523 K is enough to produce the surface ceria reduction. Only in the pure ceria and pure niobia supported catalysts this temperature is not enough to produce any surface modification. 113 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. (a) x=0 H2 consumption, a.u. x = 0.4 x = 0.7 x = 0.9 x=1 400 600 800 1000 1200 Temperature, K (b) x=0 H2 consumption, a.u. 374 K x = 0.4 351 K x = 0.7 360 K x = 0.9 575 K 610 K x=1 400 600 800 1000 1200 Temperature, K Figure 5.7. TPR curves for (a) xCeO2-(1-x)Nb2O5 and (b) Pt/xCeO2-(1-x)Nb2O5, where x = 1, 0.9, 0.7, 0.4 and 0. 3.7. X-ray photoelectron spectroscopy. The surface composition of the Pt/xCeO2-(1-x)Nb2O5 catalysts was analyzed by XPS, after calcination at 773 K. Concerning the O 1s band (Table 5.3 and Figure 5.8) there is a progressive shift in the binding energy to higher values 114 Chapter 5 with niobium incorporation. For all samples, this band can be deconvoluted into two peaks. The lower binding energy peak may be ascribed to lattice oxygen species, O2- [57][58][59][60] whereas the other one may be assigned to less electron-rich oxygen species. Previous studies described in the literature have shown that these peaks can be attributed to different components: a peak at 530.6 eV could be assigned to adsorbed oxygen species, O22-/O1- [57][61], a peak at 531.6 eV comes from hydroxyl species, -OH [62] and probably from carbonate species, CO32- [63] (the C 1s spectra also showed a small component at 289.0 eV), and finally, a component at 533.1 eV that is assigned to molecular water adsorbed on the surface [62][64]. In the case of the ceria catalysts doped with niobium, a displacement to higher O 1s binding energy with the increase of the niobium content was observed, this effect being reversed for the pure niobia catalyst. This result can be explained in terms of structural properties. The significant increase of the O 1s binding energies of niobium could suggest that more covalent metal–oxygen bonds are established, with less electron rich oxygen species [65]. Table 5.3. XPS characterization of Pt/xCeO2-(1-x)Nb2O5 catalysts. Catalyst BE O 1s, eV BE O 1s, eV x=1 529.4 531.5 x = 0.9 530.1 532.0 x = 0.7 531.8 533.4 x = 0.4 535.5 537.2 x=0 529.7 531.8 115 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. x=0 Intensity, a.u. x = 0.4 x = 0.7 x = 0.9 x=1 526 528 530 532 534 536 538 540 Binding energy, eV Figure 5.8. XPS results of O 1s of different catalysts calcined at 773 K. The chemical state of cerium ions in the catalysts after the different reduction treatments was also studied by XPS. The relative amounts of Ce (III) in the catalysts after the different reduction treatments are plotted in Figure 5.9 as a function of the niobium content. It can be seen that, in all cases, there is a certain amount of Ce (III) even in the fresh catalysts. This fact is assigned to the partial reduction of Ce (IV) ions during the XPS experiments [66][67]. There was a similar trend after both reduction treatments. The relative amount of Ce (III) decreased with low niobium content, x = 0.9, and then it slightly increased with the rise of the niobium amount, mainly in the x = 0.7 sample. The surface Ce (III) concentrations were 39% and 35% for the Pt/CeO2 catalyst and the Pt/0.7CeO2-0.3Nb2O5 catalyst respectively, after reduction at 773 K. This means that the reducibility of Ce (IV) in the mixed oxide is lower than in the pure oxide. This may be related to the difficulty for the diffusion of Nb (V) ion into ceria by the substitution mechanism, and the hindering of the formation of oxygen vacancies. The substitution of Nb (V) by Ce (IV) in the niobium oxide network adds a negative charge which maybe makes up for an oxygen vacancy trapping one electron. However, the substitution of Ce (IV) by Nb (V) in the ceria network brings a positive charge which may be compensated by the formation of Ce (III) ions. Brayner et al. [68] observed the presence of Ce (III) ions from the rise of an absorption band near 650 nm in the UV spectra. Zhang et al. [69] 116 Chapter 5 showed the increase of Ce (III) concentration in a double layer CeO2/Nb2O5 thin film. It has been justified that the diffusion of Nb (V) from the CeO2/Nb2O5 interface takes place following this reaction, Equation 5.1: (Equation 5.1) In this case, the Nb (V) ion diffuses into the CeO2 thin film to replace Ce (IV). The same amount of Ce (IV) in CeO2 films will be reduced to Ce (III) due to the neutrality, whereas the concentration of Ce (III) ion in the CeO2/Nb2O5 thin film will be increased compared with the CeO2 thin film. 50 40 % Ce (III) 30 20 10 Fresh Red. 523 K Red. 773 K 0 0.0 0.2 0.4 0.6 Niobium content, % Figure 5.9. Relative amount of surface Ce (III) (%) in Pt/xCeO2-(1-x)Nb2O5 catalysts, as function of the niobium content, after reduction treatments. The XPS spectra corresponding to the Pt 4f7/2 level of the Pt/0.7CeO2-0.3Nb2O5 catalysts, in situ reduced at 523 K, are plotted in Figure 5.10. The overall spectrum appears as the sum of two broad bands corresponding to levels 4f7/2 (at lower binding energies) and 4f5/2 (at higher binding energies). The Pt 4f7/2 binding energy was 71.4 eV, which corresponds to metallic platinum species. In fact, the reduction treatment was enough to reduce all the PtOx present in the catalyst, as it has been shown by H2-TPR. 117 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. 71.4 eV Intensity, a.u. 74.6 eV 66 68 70 72 74 76 78 80 82 Binding energy, eV Figure 5.10. XPS results of Pt 4f of the Pt/0.7CeO2-0.3Nb2O5 catalysts, reduced at 523 K. 3.8. Catalyst characterization by temperature-programmed desorption of CO2 and CO (CO2/CO-TPD). The surface chemistry of the Pt/xCeO2-(1-x)Nb2O5 catalysts was also characterized by temperature-programmed desorption experiments of CO2 and CO from the samples previously saturated with CO. The CO2 desorption profiles obtained with the catalysts reduced at 523 K are shown in Figure 5.11 (a). It can be seen that the presence of niobium in the support hinders the formation of CO2 at low temperature. This fact may be related with a decrease of oxygen mobility of the support with niobium addition, in opposition with the results obtained by yttrium addition (Chapter 4). However, it is interesting to add that all catalysts doped with niobium showed less CO2 formation than Pt/CeO2. As the niobium-containing catalysts showed a high CO conversion at low temperatures, as it will be seen below in this chapter, the lower formation of CO2 could be due to the presence of a weaker interaction of this molecule with the support. The CO desorption profiles are shown in Figure 5.11 (b). It can be seen that the presence of niobium in the supports hinders the evolution of CO. This fact could be related to the lower retention capacity of CO showed by the catalyst 118 Chapter 5 due to the presence of carbonates in the catalyst surface, or, more likely, with the weak CO adsorption on the support. (a) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 -1 CO2 desorption, a.u. 0.0001 mmol CO2·g 300 350 400 450 500 550 600 650 700 750 Temperature, K (b) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 -1 CO desorption, a.u. 0.00001 mmol CO·g 300 350 400 450 500 550 600 650 700 750 Temperature, K Figure 5.11. CO2 and CO desorption profiles for Pt/xCeO2-(1-x)Nb2O5 catalysts reduced at 523 K, (a) and (b) respectively. 119 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. 3.9. H2-temperature-programmed desorption experiments. Temperature-programmed hydrogen desorption experiments were performed in order to characterize the thermal evolution of hydrogen chemisorbed on the Pt/xCeO2-(1-x)Nb2O5 catalysts, Figure 5.12. It was possible to observe the presence of a hydrogen desorption peak at low temperature, around of 400 K, which was much more intense for the Pt/0.9CeO2-0.1Nb2O5 and Pt/0.4CeO2-0.6Nb2O5 catalysts comparing with the others. It is known that hydrogen desorption on ceria starts at low temperature (373 K), and it is related with the presence of a dispersed noble metal [1][70]. Additionally, desorption peaks at slightly higher temperatures can be associated with a direct desorption reaction from the metal and with a back spillover process from the support. In this case, an overlapping between both processes seems to be unavoidable. The presence of this peak may be interpreted as due to a change in the desorption mechanism, associated with the presence of dispersed and small platinum nanoparticle. The metal back spillover mechanism, which mainly govern the desorption reaction, is much faster than the direct recombination of the hydrogen species chemisorbed on the support. Another interpretation could be associated with the weak capacity of the support to withhold hydrogen. Furthermore, it is interesting to add that a higher amount of water was formed on the Pt/0.7CeO2-0.3Nb2O5 catalyst than on its counterparts, with the peak at about 650 K (not shown). This peak is shifted to a lower temperature than in the case of Pt/0.9CeO2-0.1Nb2O5 and Pt/0.4CeO2-0.6Nb2O5 catalysts, at about 735 K. This fact may demonstrate the higher affinity for hydrogen oxidation and, consequently, the ability for water formation presented by this catalyst, and it can also justify the low catalytic activity shown by this catalyst after the reduction treatment at 773 K, as will be discussed below. 120 Chapter 5 x=1 x = 0.9 x = 0.7 x = 0.4 -1 H2 desorption, a.u. 0.00001 mmol H2.g 300 400 500 600 700 800 900 1000 1100 1200 Temperature, K Figure 5.12. H2 desorption profiles for Pt/xCeO2-(1-x)Nb2O5 catalysts reduced at 523 K. 3.10. Catalytic behaviour. 3.10.1. CO oxidation analysis using gas chromatography: effect of the reduction temperature. The reaction profiles in terms of CO conversion and CO2 selectivity for the Pt/xCeO2-(1-x)Nb2O5 catalysts, at different reaction and reduction temperatures, and using a gas mixture containing 2% CO, 2% O2, 20% H2 and He as balance, are shown in Figure 5.13 and Figure 5.14, respectively. The light-off curves in Figure 5.13 show the influence of the doping cation (niobium) and the reduction temperature in the CO oxidation reaction. In all cases, CO conversion passes through a maximum at 353 K, close to 93-95%, and then decreases with an increase in the reaction temperature. As it can be observed, the incorporation of niobium produces a slight improvement in the catalytic activity over the whole temperature range, i.e. all the catalysts containing ceria-niobia exhibit a better CO conversion compared to those with the pure oxides, both after a reduction treatment at low and at high temperature. However, this improvement is very small. Only the catalyst with x = 0.7 fails after a reduction treatment at high temperature, i.e. Pt/0.9CeO2-0.1Nb2O5 and Pt/0.4CeO2-0.6Nb2O5 catalysts presented a higher 121 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. catalytic activity after a reduction treatment at 773 K. It is known from the literature [71] that an increase in the reduction temperature becomes beneficial for the CO oxidation reaction, as observed for our catalysts, at least at low reaction temperature. At this point, it could be interesting to analyze why niobium incorporation produces an improvement in the CO conversion. As described before, XRD results showed the presence of peaks attributed to CeO2 and Nb2O5 phases in the Pt/0.4CeO2-0.6Nb2O5 catalyst, these observations being in close agreement with Raman characterization, i.e. this catalyst presents two separated phases. In any case, TPR analysis showed that the reduction treatment at 523 K was enough to produce the surface reduction of support, and consequently, to promote the creation of oxygen vacancies. Taking into account that previous studies described in the literature [72][73][74][75] have anticipated that the amount of CO adsorbed by the catalyst highly depends on the concentration of releasable lattice oxygen, the improved redox properties [Ce (IV)/Ce (III)] after niobium incorporation could be responsible of the improved oxidation properties. Guerrero et al. [20] studied the preferential oxidation of CO and showed a unique effect of niobium as a promoter of Pt/Al2O3 catalysts. The activity and selectivity increased for low niobium loadings on these systems. It is interesting to add that the PROX results are in agreement with the TPD results; in other words, the higher CO conversion observed for the Nbcontaining catalysts, at low temperature, can be associated not with the oxygen store capacity, but with the weak CO/CO2 adsorption on the support. The selectivity towards CO2 formation is very similar for all catalysts at higher reaction temperatures (30-50%), independently of the reduction temperature used. Only at low reaction temperatures the differences among the different catalysts are more pronounced (see Figure 5.14). At low reaction temperatures the niobium-doped catalysts exhibit an improved selectivity (8090%) compared to catalysts with the pure oxides. At this point it would be interesting to highlight the excellent behaviour of the Pt/0.7CeO2-0.3Nb2O5 catalyst, with a high CO conversion (85%) and a high selectivity (around 73-75%) after a reduction treatment at 523 K. 122 Chapter 5 100 (a) CO conversion , % 80 60 40 x=1 x = 0.9 x = 0.7 x = 0.4 x=0 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 CO conversion , % 80 (b) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 60 40 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K Figure 5.13. CO oxidation light-off curves for Pt/xCeO2-(1-x)Nb2O5 serie catalysts, reduced at 523 K (a) and at 773 K (b). 123 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. 100 (a) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 CO2 selectivity, % 80 60 40 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K 100 (b) x=1 x = 0.9 x = 0.7 x = 0.4 x=0 CO2 selectivity, % 80 60 40 20 0 300 320 340 360 380 400 420 440 460 480 Temperature, K Figure 5.14. CO2 selectivity profiles for Pt/xCeO2-(1-x)Nb2O5 serie catalysts, reduced at 523 K (a) and at 773 K (b). 124 Chapter 5 3.10.2. CO oxidation using gas chromatography: effect of feed composition. Another parameter analyzed was the influence of the feed composition in the reaction mechanism, evaluated by changing the λ value (λ = 2[O2]/[CO]), using a feed composition of 2% CO, 0.6-2% O2, 20% H2 balanced with He. The experimental results obtained for the sample Pt/0.7CeO2-0.3Nb2O5 reduced at 523 K, and with a reaction temperature of 353 K, are shown in Figure 5.15. The CO conversion highly depends of the λ value. As it can be observed, there is an increase in the catalytic activity with an increase in the O2 content. This increase is accompanied by a decrease in the selectivity towards CO2 formation, whereas the oxygen conversion remains unchanged. In other words, under oxygen rich conditions both CO and H2 oxidation are favored. These results are in agreement with previous studies reported in the literature [76][77][78][79][80], where a CO oxidation dependence with λ is reported. 100 80 % 60 40 20 XCO XO2 SCO2 0 0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.0 , 2[O2]/[CO] Figure 5.15. CO preferential oxidation on Pt/0.7CeO2-0.3Nb2O5 catalyst, reduced at 523 K and with the reaction temperature at 353 K, in the feed of 2% CO, 0.6-2% O2, 20% H2 and He as balance. 3.10.3. CO oxidation studies using operando DRIFT spectroscopy: effect of the reaction temperature. DRIFTS experiments have been performed in order to analyze in detail the different steps taking place in the course of the catalytic reaction. The results 125 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. obtained using DRIFTS will be compared with the catalytic measurements obtained using gas chromatography. Figure 5.16 shows the behaviour of Pt/CeO2 and Pt/0.7CeO2-0.3Nb2O5 catalysts during the CO oxidation reaction. The presence of bands in the region between 3000 cm-1 and 3500 cm-1 attributed to surface hydroxyl groups (-OH) and water molecules adsorbed on the support can be observed for both catalysts. Moreover, it is interesting to observe a decrease of the signals of water and hydroxyls groups (bands at 3640 cm-1, 3511 cm-1 and ~ 3180 cm-1), which is drastic from 313 K to 343 K during the PROX reaction. Furthermore, this decrease is more intense for the non-doped catalyst. CO adsorbed species on the catalyst surface appear in the 2240-1860 cm-1 region. Among them, peaks at 2182 cm-1 and 2102-2113 cm-1 can be ascribed to CO adsorbed on Ce (IV), CO adsorbed on Ce (III) and/or CO gas. This observation suggests the presence of support reduction processes at low temperature. Additional peaks at 2032 cm-1 and 2055 cm-1 can be assigned to CO adsorbed on Pt metal for Pt/CeO2 and Pt/0.7CeO2-0.3Nb2O5 catalysts, respectively [74][79]. The difference between both catalysts clearly suggests a different morphology for Pt nanoparticles depending on the support used. Interestingly, the Pt/CeO2 catalyst exhibits a decrease in the characteristic bands of bidentate carbonates at 1567 cm-1 and 1292 cm-1, and an increase of unidentate carbonates at 1547 cm-1. However, in the case of Pt/0.7CeO2-0.3Nb2O5, a decrease of bidentate carbonate bands and an increase of formate bands at 1364 cm-1 is observed [79][80][81][82][83][84][85][86][87]. These results suggest that both the oxide surface and the morphology of the Pt nanoparticles highly depend on the nature of the oxide support, presence or absence of niobium, this influencing the catalytic activity. Furthermore, these results confirm the observation of the H2-TPD results where the formation of smaller Pt particles it was suggested in the case of niobium-doped catalysts. 126 Chapter 5 (b) (a) KM, a.u. KM, a.u. 473 K 313 K 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm -1 4000 3500 3000 2500 2000 1500 1000 Wavenumbers, cm -1 Figure 5.16. DRIFT spectra obtained to CO oxidation under 2% CO, 10% air, 20% H2 and N2 as balance feed, reduced at 523 K, for Pt/CeO2 (a) and Pt/0.7CeO2-0.3Nb2O5 (b) the initial temperature was of 313 K and increase to each 20 K of bottom to top. 4. Conclusions. A series of Pt/CeO2-Nb2O5 catalysts were prepared using different proportions of ceria and niobium, and tested in the preferential oxidation of CO in the presence of hydrogen. With the results obtained it is possible to conclude that the presence of niobium in the support favors the CO conversion, yielding a higher catalytic activity and selectivity that can be explained as due to the weak CO support adsorption, as it has been observed by TPD studies. Moreover, it is interesting to add that the formation of a solid solution oxide is favored only at low niobium contents. 5. References. [1] A. Trovarelli, Catalysis by ceria and related materials, Imperial College Press, London (2002). [2] X. Wang, R.J. Gorte, J. Wagner, J. Catal., 212 (2002) 225-230. [3] E. Mamontov, T. Egami, J. Phys. Chem. B, 104 (2000) 11110-11116. [4] K. Eguchi, T. Setoguchi, T. Inoue, H. Arai, Solid State Ionics, 52 (1992) 165-172. 127 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. [5] H. Hayashi, R. Sagawa, H. Inaba, K. Kawamura, Solid State Ionics, 131 (2000) 281290. [6] M. O’Connell, M.A. Morris, Catal. Today, 59 (2000) 387-393. [7] E. Ramírez-Cabrera, A. Atkinson, D. Chadwick, Appl. Catal. B: Env., 36 (2002) 193206. [8] M. Casapu, A. Bernhard, D. Peitz, M. Mehring, M. Elsener, O. Kröcher, Appl. Catal. B: Env., 103 (2011) 79–84. [9] E. Ramírez-Cabrera, A. Atkinson, D. Chadwick, Solid State Ionics, 136–137 (2000) 825-831. [10] N. Laosiripojana, W. Sutthirsripok, P. Kim-Lohsoontorn, S. Assabumrungrat, International J. Hydrogen Energy, 35 (2010) 6747-6756. [11] K. Yashiroa, T. Suzukia, A. Kaimaia, H. Matsumotoa, Y. Nigaraa, T. Kawadaa, J. Mizusakia, J. Sfeirb, J. Vanherle, Solid State Ionics, 175 (2004) 341–344 [12] I.K. Naik, T.Y. Tien, J. Electrochem. Soc., 126 (1979) 562-566. [13] I.E. Wachs, Proc. Intern. Conf. Niobium Tantalum, (1989) 679. [14] I.E. Wachs, J.-M. Jehng, G. Deo, H. Hu, N. Arora, Catal. Today, 28 (1996) 199-205. [15] K. Tanabe, Catal. Today, 8 (1990) 1-11. [16] J.-M. Jehng, I.E. Wachs, J. Mol. Catal., 67 (1991) 369-387. [17] N. Arora. G. Deo, I.E. Wachs, A. Hirt, J. Catal., 159 (1996) 1-13. [18] J. Vanherle, R. Ihringer, J. Sfeir, N.M. Sammes, G. Tompsett, K. Kendall, K. Yamada, C. Wen, M. Ihara, T. Kawada, J. Mizusaki, A.J. McEvoy (Ed.), Proc. Forth European SOFC Forum, vol. 1, European Fuel Cell Forum, Switzerland, 2000, p. 251. [19] M.R. De Guire, M.J. Shingler, E. Dincer, Solid State Ionics, 52 (1992) 155-163. [20] S. Guerrero, J.T. Miller, E.E. Wolf, Appl. Catal. A: Gen., 328 (2007) 27-34. [21] P. Marques, N.F.P. Ribeiro, M. Schamal, D.A.G. Aranda, M.M.V.M. Souza, J Power Sources, 158 (2006) 504-508. [22] L. Mei, L. Zhaogang, H. Yanhong, W. Mitang, L. Hangquan, J. Rare Earths, 26 (2008) 357-361. [23] Q. Wu, J. Chen, J. Zhang, Fuel Processing Technology, 89 (2008) 993-999. [24] M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today, 68 (2001) 53-61. [25] H. Roh, H.S. Potdar, K. Jun, S.Y. Han, J. Kim, Catal. Letters, 93 (2004) 203-207. [26] I. Dobrosz-Gómez, I. Kocemba, J.M. Rynkowski, Appl. Catal. B: Env., 83 (2008) 240-255. [27] J. Silvestre-Albero, F. Coloma, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Appl. Catal. A: Gen., 304 (2006) 159-167. [28] M. Paulis, M. Martín, D.B. Soria, A. Díaz, J.A. Odriozola, M. Montes, Appl. Catal. A: Gen., 180 (1999) 411-420. [29] S.-H. Chai, H.-P. Wang, Y. Liang, B.-Q. Xu, J. Catal., 250 (2007) 342–349. [30] J. Li, G. Lu, K. Li, W. Wang, J. Li, G. Lu, K. Li, W. Wang, M. Casapu, A. Bernhard, D. Peitz, M. Mehring, M. Elsener, O. Kröcher, Appl. Catal. B: Env., 103 (2011) 79– 84. [31] I. Nowak, M. Ziolek, Chem. Rev., 99 (1999) 3603-3624. 128 Chapter 5 [32] R.J. Packer, P.A. Stuart, S.J. Skinner, J. of Solid State Chemistry, 181 (2008) 1445– 1455. [33] A. Santoro, M. Marenzio, R.S. Roth, D. Minor, J. Solid State Chemistry, 35 (1980) 167-175. [34] T. Negas, R.S. Roth, C.L. McDaniel, H.S. Parker, C.D. Olson, Mat. Res. Bull., 12 (1977) 1161-1171. [35] R.J. Paker, J. Barlow, A. Cott, S.J. Skinner, Solid State Ionics, 179 (2008) 1094-1100. [36] J.G. Thompson, R.L. Withers, J. of Solid State Chemistry, 143 (1999) 122-131. [37] S.J. Skinner, Y. Kang, Solid State Sciences, 5 (2003) 1475–1479. [38] E.V. Tsipis, C.N. Munnings, V.V. Kharton, S.J. Skinner, J.R. Frade, Solid State Ionics, 177 (2006) 1015-1020. [39] R.J. Cava, R.S. Roth, T. Negas, H.S. Parker, D.B. Minor, J. Solid State Chemistry, 40 (1981) 318-329. [40] M.R. Gallego. La difracción de los rayos X. Edición Alambra (1982). [41] S. Zhao, R.J. Gorte, Appl. Catal. A: Gen., 248 (2003) 9-18. [42] I. Atribak, A. Bueno-López, A. García-García, J. Molecular Catal. A: Chemical, 300 (2009) 103-110. [43] J. Lingyun, H. Mai, L. Jiqing, L. Mengfei, G. Libiao, H. Jun, J. Rare Earths, 26 (2008) 614-618. [44] M.F. Luo, M. He, Y.L. Xie, P. Fang, L.Y. Jin, Appl. Catal. B: Env., 69 (2007) 231-218. [45] M. Mogensen, N.M. Sammes, G.A. Tompsett, Solid State Ionics, 129 (2000) 63-94. [46] S. Raghavan, H. Wang, W.D. Porter, R.B. Dinwiddie, M.J. Mayo, Acta Mater., 49 (2001) 169-179. [47] F.D. Hardcastle, I.E. Wachs, Solid State Ionics, 45 (1991) 201-213. [48] X.-M. Lin, L.-P. Li, G.-S. Li, W.-H. Su, Mater. Chem. Phys., 69 (2001) 236-240. [49] S.T. Aruna, V.K. William Grips, V. Exhil Selvi, K.S. Rajam, J. Appl. Electrochem., 37 (2007) 991-1000. [50] F.G. Meng, L.B. Liu, H.S. Liu, Z.P. Jin, Computer Coupling of Phase Diagrams and Thermochemistry, 30 (2006) 323-325. [51] K. Krishna, A. Bueno-López, M. Makkee, J.A. Moulijn, Appl. Catal. B: Env., 75 (2007) 189–200. [52] A. Martínez-Arias, D. Gamarra, M. Fernández-García, X.Q. Wang, J.C. Hanson, J.A. Rodriguez, J. Catal., 240 (2006) 1–7. [53] J.L. Ayastuy, M.P. González-Marcos, A. Gil-Rodríguez, J.R. González-Valesco, M.A. Gutiérrez-Ortiz, Catal. Today, 116 (2006) 391-399. [54] P. Fornasiero, G. Balducci, R. Di Monte, J. Kaspar, V. Sergo, G. Gubitosa, A. Ferrero, M. Graziani, J. Catal., 164 (1996) 173-183. [55] S. Ricote, G. Jacobs, M. Milling, Y. Ji, P.M. Patterson, B.H. Davis, Appl. Catal. A: Gen., 303 (2006) 35-47. [56] G. Avgouropoulos, M. Manzoli, F. Boccuzzi, T. Tabakova, J. Papavasiliou, T. Ioannides, V. Idakiev, J. Catal., 256 (2008) 237-247. [57] N. Yamazoe, Y. Teraoka, T. Nakamura, Chem. Lett., 10 (1981) 1767-1780. [58] G.U. Kulkarni, C.N.R. Rao, M.W. Roberts, J. Phys. Chem. 99 (1995) 3310-3316. [59] A.F. Carley, M.W. Roberts, A.K. Santra, J. Phys. Chem. B, 101 (1997) 9978-9983. 129 Preferential CO oxidation (PROX) on Pt/CeO2-Nb2O5 catalyst. [60] [61] [62] [63] [64] [65] [66] [67] [68] [69] [70] [71] [72] [73] [74] [75] [76] [77] [78] [79] [80] [81] [82] [83] [84] [85] [86] [87] J.L.G. Fierro, L.G. Tejuca, Appl. Surf. Sci., 27 (1987) 453-457. L. Richter, S.D. Bader, M.B. Brodsky, Phys. Rev. B, 22 (1980) 3059-3064. J.L.G. Fierro, Catal. Today, 8 (1990) 153-174. T.H. Fleish, R.F. Hicks, A.T. Bell, J. Catal., 87 (1984) 398-413. L.G. Tejuca, A.T. Bell, J.L.G. Fierro, M.A. Peña, Appl. Surf. Sci., 31 (1988) 301-316. K. Musialskaa, E. Finocchiob, I. Sobczaka, G. Buscab, R. Wojcieszakc, E. Gaigneauxc, M. Zioleka, Appl. Catal. A: Gen., 384 (2010) 70–77. B.M. Reddy, A. Khan, Y. Yamada, T. Kobayashi, S. Loridant, J.-C. Volta, J. Phys. Chem. B., 107 (2003) 11475-11484. P.W. Park, J.S. Ledford, Langmuir, 12 (1996) 1794-1799. R. Brayner, D. Ciuparu, G.M. da Cruz, F. Fiévet-Vincent, F. Bozon-Verduraz, Catal. Today, 57 (2000) 261-266. Z. Zhang, X. Du, W. Wang, J. Vac. Sci. Technol. A, 18 (2000) 2928-2931. S. Bernal, J.J. Calvino, M.A. Cauqui, J.M. Gatica, C. Larese, J.A. Pérez Omil, J.M. Pintado, Catal. Today, 50 (1999) 175-206. E.Y. Ko, E.D. Park, H.C. Lee, D. Lee, S. Kim, Angew. Chem., 46 (2007) 734-737. F. Dong, T. Tanabe, A. Suda, N. Takahashi, H. Sobukawa, H. Shinjoh, Chemical Engineering Science, 63 (2008) 5020-5027. K. Ramesh, L.W. Chen, F.X. Chen, Y. Liu, Z. Wang, Y.F. Han, Catal. Today, 131 (2008) 477-482. R. Cracium, B. Nentwick, K. Hadjiivanov, H. Knözinger, Appl. Catal. A: Gen., 243 (2003) 67-79. L.M. Molina, B. Hammer, Phys. Rev. B., 69 (2004) 155424-22. J.L. Ayastuy, A. Gil-Rodriguez, M.P. González-Marcos, M.A. Gutiérrez-Ortiz, International J. Hydrogen Energy, 31 (2006) 2231-2242. F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 58 (2005) 175-183. F. Mariño, C.Descorme, D. Duprez, Appl. Catal B: Env., 54 (2004) 59-66. O. Pozdnyakova, D. Teschner, A. Wootsch, J. Kröhnert, B. Steinhauer, H. Sauer, L. Toth, F.C. Jentoft, A. Knop-Gericke, Z. Paál, R. Schlögl, J. Catal., 237 (2006) 1-16. D. Teschner, A. Wootsch, O. Pozdnyakova-Tellinger, J. Kröhnert, E.M. Vass, M. Hävecker, S. Zafeiratos, P. Schnörch, P.C.Jentoft, A.Knop-Gericke, R. Schlögl, J. Catal., 249 (2007) 318-327. C. Binet, M. Daturi, J.C. Lavalley, Catal. Today, 50 (1999) 207-225. A. Badri, C. Binet, J.C. Lavalley, J. Phys. Chem., 100 (1996) 8363-8368. K. Föttinger, R. Schlögl, G. Rupprechter, Chem. Commun., (2008) 320-322. P. Bera, A. Hornés, A.L. Cámara, A. Matínez-Arias, Catal. Today, 155 (2010) 184191. P.O. Graf, D.J.M. de Vlieger, B.L. Mojet, L. Lefferts, J. Catal., 262 (2009) 181-187. H. Zou, S. Chen., Z. Liu, W. Lin, International J. of Hydrogen and Energy, 34 (2009) 9324-9333. A. Martínez-Arias, A.B. Hungría, M. Fernández-García, J.C. Conesa, G. Munuera, J. Power Sources, 151 (2005) 32-42. 130 CAPÍTULO 6 Catalizadores de oro soportado en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. Abstract. In the present chapter, gold nanoparticles supported on 0.7CeO2-0.3MOx (M = Nb or Y) mixed oxides have been prepared, using HAuCl4 as a precursor. These catalysts have been evaluated in the preferential oxidation of CO in H2 excess after being characterized by N2 adsorption at 77 K, ICP-OES, XRD, XRF, TEM, XPS and H2-TPR. This study analyzes the effect of the support composition on the catalytic behaviour of supported gold nanoparticles. The results show that gold catalysts are more active than platinum-based catalysts in the title reaction. It has been reported in the literature that gold, in a highly dispersed form, is a good catalyst for low-temperature CO oxidation. Depending on the nature of the support and on the gold particle size, CO and H2 oxidations are affected in different forms. Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. 1. Introducción. Son muchos los catalizadores que se han evaluado en la oxidación preferencial de CO. Sin embargo, los basados en oro no han sido muy utilizados debido al valor relativamente alto de su primera energía de ionización [1][2]. Además, este aspecto viene acompañado por una baja actividad química superficial [3][4][5], que se refleja en una baja capacidad del oro para la adsorción de H2 y CO. Sin embargo, trabajos realizados por Haruta y col. en la década de los años 80 mostraron que nanopartículas de Au de pequeño tamaño (2-4 nm de diámetro), sí son efectivas para la oxidación de CO [4][6][7]. Estudios teóricos propuestos por Kandoi y col. [8] encontraron que el valor en la barrera de la energía de activación para la reacción de oxidación de CO sobre Au (111) es de 0,18 eV, mientras que para el Cu (111) y el Pt (111) es de 0,82 eV y 0,96 eV, respectivamente; por otro lado, la barrera para la formación del grupo -OH, primer paso en la oxidación del H2, es 0,90, 1,28 y 0,83 eV, respectivamente. Un modelo microcinético basado en parámetros derivados de cálculos de la teoría del funcional de densidad (DFT), sugiere que la selectividad en esta reacción viene determinada tanto por un aspecto cinético relacionado con la competencia de las reacciones de oxidación de las moléculas de CO y H2, como por el cubrimiento de estas especies sobre los sitios metálicos disponibles en la superficie. En este sentido, tanto el Au como el Cu son más selectivos que el Pt para la oxidación de CO a bajas temperaturas en presencia de H2. Factores como el tamaño de partícula del Au [9][10], su estado de oxidación [11][12][13], la naturaleza del soporte [14][15] y las características de la interfase entre las partículas de oro y el soporte afectan a la actividad catalítica en la oxidación de CO a bajas temperaturas. Esto hace que el comportamiento de los catalizadores de Au dependa de forma importante del método de preparación utilizado [16]. Afortunadamente, Haruta y col. [7][17] han desarrollado métodos alternativos de preparación para obtener partículas de Au altamente dispersas con el objetivo de estudiar sus aplicaciones catalíticas. Entre los sistemas catalíticos estudiados en la reacción PROX destacan aquellos en los que nanopartículas de Au se dispersan sobre determinados óxidos (TiO2, CeO2, Fe2O3). Estos materiales presentan una buena capacidad para eliminar el CO proveniente del reformado, mostrando una elevada velocidad de reacción y una buena selectividad a bajas temperaturas [18][19]. En este aspecto el CeO2 es un óxido atractivo, ya que favorece una alta dispersión metálica, promueve una alta actividad catalítica en la interfase metal-soporte, y facilita la conversión del CO por oxidación con oxígeno de la 132 Capítulo 6 red. En este sentido, estudios recientes han demostrado que nanopartículas de oro soportadas sobre CeO2 constituyen materiales eficientes para catalizar la reacción PROX, mostrando una elevada actividad y selectividad a bajas temperaturas [19][20][21][22]. Entre los diferentes estudios realizados para comprender el origen de la elevada actividad de los catalizadores de Au a bajas temperaturas, destacan las contribuciones de Jia y col. [23], en las que la elevada actividad de catalizadores Au/CeO2 se relaciona con la presencia de grupos hidroxílicos. Quinet y col. [24] han mostrado que la reacción de oxidación preferencial de CO en catalizadores de Au/Al2O3 está promovida por la formación del grupo -HOO como intermediario, mientras que Tanaka y col. [25] han reportado que la reacción PROX se produce a través de un intermedio -HCOO. Existen algunas discrepancias en relación a la naturaleza de los sitios activos de este tipo de catalizadores. Bond y Thompson [11] propusieron un modelo en el que los centros activos para la oxidación son los átomos de Au presentes en la interfase entre la partícula de oro y el óxido. Estos sitios, ubicados en la periferia de la partícula metálica, se encontrarían en estado oxidado e interaccionando con el soporte, mientras que el resto de la nanopartícula estaría formada por Au0. Así, la adsorción de CO se produciría preferentemente sobre los centros de Au0, mientras que su oxidación tendría lugar en la periferia sobre sitios de Au oxidado. Varios autores han concluido que la reacción de oxidación de CO se produce en la periferia de las partículas de oro, con implicación tanto de la fase metálica como del soporte [26][27][28]. La interfase entre las pequeñas partículas de Au y el soporte, junto con la disponibilidad de sitios defectuosos en esta interfase, son probablemente las características más importantes de los centros activos [29]. Este hecho da más peso al mecanismo propuesto por Bond y Thompson. Dada la elevada actividad de los catalizadores de Au soportados sobre CeO2, en el presente capítulo se evalúa la actividad catalítica de catalizadores de Au soportados sobre óxidos de cerio (CeO2) modificados con niobio o itrio (denominados Au/0,7CeO2-0,3Nb2O5 y Au/0,7CeO2-0,3Y2O3) con el objetivo de estudiar el efecto de la modificación del soporte de CeO2 en esta reacción. 2. Experimental. 2.1. Preparación y caracterización de los catalizadores. La serie de catalizadores de Au se preparó utilizando los soportes CeO2, 0,7CeO2-0,3Nb2O5 y 0,7CeO2-0,3Y2O3. Los soportes se prepararon por 133 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. precipitación con urea a 363 K durante 11 h. Los detalles del método de preparación se presentaron en los Capítulos 3, 4 y 5 de la presente Memoria, respectivamente. Los catalizadores fueron preparados por dos métodos: (i) impregnación a humedad incipiente e (ii) impregnación con exceso de disolución. Para los tres soportes se utilizó una disolución acuosa de HAuCl4 (Aldrich, 98,5 %) de concentración adecuada para obtener un 1% en peso de Au. En el caso de impregnación con humedad incipiente (i), se adicionó gota a gota y de forma homogénea la solución acuosa de HAuCl4 sobre el soporte, con agitación continua para homogeneizar lo mejor posible el sólido. En el caso de la impregnación con exceso de disolución (ii), inicialmente se preparó una suspensión del CeO2 en H2O a 333 K; posteriormente, se ajustó el pH entre 6,5-7,0 utilizando una disolución 0,16 M de Na2CO3. Una vez ajustado el pH, se adicionó gota a gota la disolución de HAuCl4, manteniendo constante la agitación y la temperatura. Durante este proceso, el pH se mantuvo constante entre 6,5-7,0. Después de 30 min. de agitación a temperatura constante, el precipitado formado se enfrió, lavó y filtró. Finalmente, los catalizadores obtenidos por ambos métodos se secaron en estufa a 383 K durante 12 h y se calcinaron a 473 K durante 30 min., utilizando para ello una corriente gaseosa compuesta por un 20% de O2 en He. En este punto cabe mencionar que ambos métodos de preparación fueron utilizados solamente para el catalizador Au/CeO2, mientras que para el resto de muestras (soportes dopados) se utilizó solamente el método de impregnación con exceso de disolución debido a los mejores resultados obtenidos con este método en cuanto a comportamiento catalítico (ver sección de actividad catalítica más adelante). Teniendo en cuenta estas premisas, todos los ensayos de caracterización descritos en adelante siempre serán aplicados a los catalizadores preparados por impregnación con exceso de disolución, salvo que se indique lo contrario. Las técnicas de caracterización empleadas para estudiar las propiedades físico–químicas de los catalizadores han sido adsorción de N2 a 77 K, difracción de rayos X (DRX), fluorescencia de rayos X (FRX), espectroscopía atómica de emisión por plasma de acoplamiento inductivo (ICP-EOS), microscopía electrónica de transmisión (TEM), reducción a temperaturaprogramada (RTP-H2) y espectroscopía fotoelectrónica de rayos X (XPS). 2.2. Ensayos catalíticos. El comportamiento catalítico de las muestras preparadas se analizó en experimentos de reacción a temperatura programada (313–473 K) a presión 134 Capítulo 6 atmosférica, utilizando una mezcla gaseosa compuesta por un 20% H2, 2% CO y entre 0,6-2% O2, balanceada en He. Los equipos experimentales empleados y las condiciones de medida han sido descritos en el Capitulo 2. Previamente a cada ensayo, los catalizadores fueron reducidos in situ a 473 K durante 1 h en flujo de H2 (50 ml·min-1). Los productos de reacción fueron analizados por cromatografía de gases. El método de cálculo utilizado para determinar la conversión de CO y O2, así como la selectividad, ha sido descrito en el Capitulo 2. 3. Resultados y discusión. 3.1. Caracterización textural y porcentaje metálica. En la Tabla 6.1 se muestran los valores de área superficial BET para los catalizadores, así como el contenido en los diferentes metales determinado por ICP-OES y FRX. Se puede apreciar que el contenido en oro de la serie preparada es ligeramente inferior al nominal (1%) indicando que una pequeña cantidad de oro no llega a incorporarse al respectivo soporte. También se observa que los catalizadores presentan un amplio intervalo de composiciones, de tal forma que, a partir de ahora, las muestras se nombrarán haciendo mención al contenido nominal, el cual, como se puede observar en la Tabla 6.1, solo difiere ligeramente del contenido real. Tabla 6.1. Contenido de Au de los catalizadores y composiciones molares y área superficial B.E.T. de los soportes. Contenido de Au, % en peso Contenido de CeO2, % Contenido de Nb2O5 o Y2O3, % SBET, m2.g-1 Au/CeO2 0,85 100 -- 108 Au/0,7CeO2-0,3Nb2O5 0,95 72 28 114 Au/0,7CeO2-0,3Y2O3 0,86 73 27 90 Catalizador (a) (a) Área superficial BET del soporte. 3.2. Caracterización de los catalizadores mediante DRX. En la Figura 6.1 se muestran los difractogramas de rayos X de los diferentes catalizadores. En el caso del catalizador soportado en el óxido puro, Au/CeO2, se observa la presencia de picos relacionados con la fase cúbica de la 135 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. estructura tipo fluorita del CeO2, asignados a los planos de difracción (111), (200), (220), (311), (222) y (400) a valores de 2θ de 28,520; 33,140; 47,580; 56,340; 59,250 y 69,280, respectivamente [30][31][32][33]. Por otro lado, en los difractogramas de los catalizadores con soportes dopados no se observa la presencia de picos correspondientes a Nb2O5 y Y2O3. Teóricamente, los picos de difracción correspondientes al oro metálico deben aparecer a valores de 2 de 38,210; 44,420; 64,630 y 77,620, siendo el primero de ellos asignado a la reflexión en el plano (111) de la estructura cúbica centrada en las caras del Au. [20][34]. Para el Au2O se encuentran picos de difracción a valores de 2 de 32,590; 35,300; 40,600; 53,960 y 60,030 y para Au2O3 a 25,660; 32,480; 32,700; 34,080; 35,360; 40,730 y 43,290 [35]. Sin embargo, para las muestras preparadas no se observan picos de difracción que correspondan a ninguna especie de oro, observación que puede ser atribuida a la alta dispersión de las nanopartículas de Au y/o a la baja carga de oro en estos sistemas. Estos resultados están de acuerdo con las observaciones de TEM, como se presentará a continuación. CeO2 Intensidad, u.a. Au/0,7CeO2-0,3Y2O3 Au/0,7CeO2-0,3Nb2O5 Au/CeO2 20 30 40 50 60 70 80 2 Figura 6.1. Difractogramas de rayos X de los catalizadores de Au/CeO2 y Au/0,7CeO2-0,3MO (M = Nb o Y). 3.3. Caracterización de los catalizadores mediante TEM. En la Figura 6.2 se muestran las imágenes obtenidas mediante TEM para los catalizadores Au/CeO2, Au/0,7CeO2-0,3Nb2O5 y Au/0,7CeO2-0,3Y2O3. El tamaño de partícula de los soportes no ha sido calculado por medio de esta 136 Capítulo 6 técnica (TEM) debido al elevado grado de aglomeración de los cristales de soporte, hecho que dificulta su determinación. Por otro lado, la distribución de tamaño de nanopartículas de oro también es difícil de cuantificar debido al elevado grado de dispersión (presencia de partículas muy pequeñas) y el débil contraste entre las nanopartículas del metal y el soporte. Sin embargo, la presencia de Au ha sido confirmada por EDS. Estudios descritos en la literatura confirman la dificultad en la detección de nanopartículas muy pequeñas de oro mediante TEM, siendo necesario el uso de otras técnicas como ADF-STEM (annular dark field-scanning transmission electron microscope) [36]. El débil contraste entre las partículas de Au en catalizadores soportados sobre CeO2 podría estar relacionado con la elevada densidad electrónica de estos dos metales [18][37][38][39]. (a) (b) (c) Figura 6.2. Imágenes de TEM de los catalizadores de Au/CeO2 (a), Au/0,7CeO2-0,3Nb2O5 (b) y Au/0,7CeO2-0,3Y2O3 (c). 3.4. Caracterización de los catalizadores mediante RTP-H2. El grado de reducibilidad de los catalizadores se ha determinado mediante experimentos de reducción a temperatura programada con hidrógeno (RTP-H2). Los perfiles de consumo de hidrógeno se presentan en la Figura 6.3. Como cabía esperar, hay importantes diferencias entre los perfiles de los catalizadores y los de los soportes. En el caso del soporte del CeO2 puro se observa la presencia de dos pico de reducción, uno a 760 K atribuido a la reducción del CeO2 superficial y otro a 1050 K debido a la reducción del CeO2 másico (bulk) [40][41][42]. En el caso de los soportes dopados, los perfiles de reducción a temperatura programada son similares a los de CeO2 puro. Los perfiles de consumo de hidrógeno de los catalizadores de Au muestran dos picos principales a bajas temperaturas. Está bien establecido que el consumo de hidrógeno a bajas temperaturas se debe a dos procesos [43][44]: (i) la reducción de las nanopartículas de Au obtenidas tras el tratamiento de calcinación (Au2O3 a Au (0)) y, (ii) la reducción superficial del CeO2. Además, 137 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. se puede observar una segunda región de consumo de H2 entre 620-750 K que, dependiendo del catalizador, está asociada con la reducción superficial del CeO2 que no está en contacto directo con las nanopartículas de oro [40][41][42]. Los perfiles de reducción obtenidos para los catalizadores de Au indican claramente que la presencia de oro promueve la reducción del soporte, como queda evidenciado por el desplazamiento del pico de reducción desde 690-820 K (en los soportes) a temperatura más bajas en los catalizadores. Este fenómeno se explica por la habilidad del metal para promocionar la reducción del CeO2 a través de un proceso de spillover de hidrógeno desde el metal al soporte. Dadas las características que presentan los perfiles de reducción de los catalizadores de Au, se puede destacar que aquellos que tienen óxidos dopados como soporte (Au/0,7CeO2-0,3Nb2O5 y Au/0,7CeO2-0,3Y2O3) muestran un primer pico de reducción a más bajas temperaturas en comparación con el catalizador soportado en óxido de cerio puro (Au/CeO2). El efecto del dopante en la reducibilidad del óxido se aprecia mejor en el primer intervalo de reducción, comprendido entre 300-520 K, para el catalizador dopado con niobio y hasta 590 K, para el caso del itrio. Esta disminución de la temperatura de reducción comparada con la del catalizador soportado sobre CeO2 puro indica que la presencia del dopante puede favorecer procesos redox a baja temperatura en estos catalizadores. Sin embargo, no se debe despreciar el hecho de que el catalizador dopado con itrio presenta un consumo inferior de hidrógeno en ese proceso de reducción a baja temperatura (156 μmol de H2 consumido por el catalizador Au/0,7CeO2-0,3Y2O3 frente a 618 μmol de H2 consumido para el Au/0,7CeO2-0,3Nb2O5). Si se consideran las especies de Au (III) y/o Au (I) como posibles especies presentes en los catalizadores tras la calcinación, el consumo de hidrógeno obtenido en los experimentos de reducción a temperatura programada debería ser menor del obtenido. Esta observación justifica el consumo de hidrógeno por parte del soporte. En el catalizador dopado con niobio se aprecia que las características redox de las nanopartículas de Au también se ven modificadas en comparación con el catalizador de CeO2 sin dopar. Sin embargo, ambos catalizadores presentan valores de consumo de hidrógeno muy próximos (618 μmol de H2 consumido para el catalizador Au/0,7CeO2-0,3Nb2O5 frente a 660 μmol de H2 consumido para el catalizador Au/CeO2). En resumen, la presencia de niobio en el CeO2 favorece la reducibilidad del oro. 138 Capítulo 6 0,0005 mmol H2·g -1 Au/0,7CeO2-0,3Y2O3 Consumo de hidrógeno, u.a. 360 K 300 Au/0,7CeO2-0,3Nb2O5 420 K 355 K 395 K 435 K Au/CeO2 400 500 600 700 800 900 1000 1100 1200 Temperatura, K Figura 6.3. Perfiles de reducción a temperatura programada (consumo de hidrógeno) de los catalizadores de oro. 3.5. Caracterización de Au/0,7CeO2-0,3Nb2O5 mediante XPS. La composición superficial del catalizador Au/0,7CeO2-0,3Nb2O5 ha sido determinada por XPS. La muestra fue reducida in situ con H2 a 473 K antes de llevar a cabo las medidas. Los resultados más relevantes se presentan en la Tabla 6.2. Como se puede observar, la energía de ligadura correspondiente al nivel Nb 3d5/2 está alrededor de 207,1 eV (energía de ligadura típica de Nb2O5). Además, la energía de ligadura para el pico u´´´ del Ce (IV) está próxima al valor encontrado en la literatura [45], alrededor de 917,2 eV. El porcentaje de Ce (III) fue del 37%. Es interesante resaltar que el porcentaje de Ce (III) presente en el catalizador de Au reducido a 473 K presenta un valor muy próximo al del catalizador de Pt soportado sobre el mismo soporte, 41%, como se presentó en el Capítulo 5. Esto indica que el porcentaje de Ce (III) formado depende, de manera general, más de la cantidad de metal presente en la superficie del soporte que de la naturaleza del metal soportado. 139 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. Tabla 6.2. Caracterización por XPS del catalizador Au/0,7CeO2-0,3Nb2O5 reducido a 473 K. Catalizador Au/0,7CeO2-0,3Nb2O5 EL Nb 3d5/2, eV 207,1 EL Ce u´´´, eV 916,5 % Ce (III) 37 En la Figura 6.4 se muestra, a modo de ejemplo, el espectro para la banda Au 4f obtenido con la muestra Au/0,7CeO2-0,3Nb2O5. El espectro global aparece como la suma de dos contribuciones que corresponden a los niveles 4f7/2 (a menores energías de ligadura) y 4f5/2 (a mayores energías de ligadura). Se ha publicado que los picos de XPS a 83,8 eV y 87,5 eV son debidos a especies de Au (0), y los picos a 84,6 eV y 88,2 eV se asignan a especies Au (I), mientras los picos a 86,5 eV y 90,1 eV corresponden a especies de Au (III) [19][26][35][37]. En el caso del catalizador Au/0,7CeO2-0,3Nb2O5 se puede apreciar la presencia de Au (0), picos a 83,3 eV y 87,0 eV. Como se puede observar estos valores de energía de ligadura se encuentran significantemente desplazados a respecto de las referencias citadas anteriormente. Estas diferencias son atribuibles a la alta dispersión del oro en la muestra, un parámetro que también afecta a la posición de los picos [9][45][46]. La identificación de las especies reducidas de oro por XPS es consistente con los perfiles de RTP-H2 obtenidos (Figura 6.3). 140 Capítulo 6 83,3 eV Intensidad, u.a. 87,0 eV 76 78 80 82 84 86 88 90 92 Energia ligadura, eV Figura 6.4. Espectros XPS para el nivel Au 4f en el catalizador Au/0,7CeO2-0,3Nb2O5 reducido a 473 K. 3.6. Comportamiento catalítico. 3.6.1. Oxidación preferencial de CO: efecto del método de preparación del catalizador. El primer estudio realizado ha sido el de la influencia del método de preparación de los catalizadores en su actividad catalítica. En concreto, se han comparado el método de impregnación con humedad incipiente (I) y el de impregnación con exceso de disolución. Estos análisis han sido realizados con el catalizador Au/CeO2. Los perfiles de oxidación de CO obtenidos se muestran en la Figura 6.5. Se puede observar que a pesar de que el catalizador preparado por el método de impregnación con humedad incipiente presenta una mejor selectividad hacia la formación de CO2, también muestra valores bajos de actividad, principalmente a temperaturas bajas. Este hecho puede estar relacionado con el efecto del tamaño de partícula en la reacción a bajas temperaturas. Las imágenes obtenidas de TEM para estos materiales indicaron que, mientras que en el catalizador preparado por el método de impregnación con exceso de disolución el oro está presente en forma de partículas pequeñas, el catalizador preparado por impregnación con humedad incipiente muestra partículas de tamaños superiores a 20 nm (fotos no mostradas). En definitiva, la reacción de oxidación de CO está favorecida a bajas temperaturas en 141 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. catalizadores de oro con pequeños tamaños de partícula, lo que está de acuerdo con datos reportados en la literatura [4][6][7][47][48]. A temperaturas de reacción superiores se observa, para ambos catalizadores, una elevada conversión de CO, lo que puede ser un indicio de que a temperaturas superiores no solo desaparece la influencia del tamaño del cristal de Au, sino que el soporte también ejerce un papel importante sobre el valor de actividad catalítica. En base a los resultados obtenidos, se decidió preparar el resto de catalizadores usando el método de impregnación con exceso de disolución. 142 Capítulo 6 100 (a) Conversión de CO, % 80 60 40 20 Au/CeO2 (I) 0 300 Au/CeO2 320 340 360 380 400 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 20 Au/CeO2 (I) 0 300 Au/CeO2 320 340 360 380 400 420 440 460 480 Temperatura, K Figura 6.5. Conversión de CO (a) y selectividad hacia a CO2 (b) para los catalizadores de oro reducidos a 473 K preparados por distintos métodos de preparación. 3.6.2. Oxidación preferencial de CO: efecto del soporte. La actividad catalítica de los tres catalizadores preparados por el método de impregnación con exceso de disolución en la reacción de oxidación 143 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. preferencial de CO se ha determinado mediante experimentos de reacción a temperatura programada. Los perfiles de conversión de CO, así como la selectividad hacia CO2, se muestran en la Figura 6.6 (a) y (b), respectivamente. Se puede apreciar que los catalizadores Au/0,7CeO2-0,3Nb2O5 y Au/CeO2 son los más activos. Ambas muestras presentan un comportamiento similar a bajas temperaturas, entre 313 K y 353 K, con un valor de conversión de aproximadamente 95 %, así como una ligera pérdida de actividad a temperaturas superiores a los 353 K. Sin embargo, el catalizador preparado utilizando el soporte dopado con itrio presenta una actividad mucho menor. En este catalizador se observa que la conversión de CO va aumentando con la temperatura de reacción hasta alcanzar un valor máximo del 85 % a 373 K, y luego disminuye a temperaturas superiores. El comportamiento observado en los experimentos de reacción a temperatura programada permite destacar algunos aspectos importantes en la actividad catalítica de los materiales evaluados. Por un lado, la adición del dopante en el soporte puede favorecer o no la actividad catalítica hacia la reacción deseada, dependiendo de la naturaleza (estado de oxidación) de la especie dopante. Se ha apreciado que la presencia de itrio en el soporte es perjudicial para la reacción, mientras que la adición de niobio favorece el proceso. Los resultados de reducción a temperatura programada mostraron que los dos catalizadores con el soporte dopado presentan una mejor reducibilidad (picos de reducción a menor temperatura). Sin embargo, el catalizador dopado con itrio presentaba una cantidad menor de hidrógeno consumido. Así, los catalizadores dopados con niobio presentan mejores propiedades redox, lo que podría estar relacionado con su eficiencia catalítica. Otra posibilidad que se debe considerar en el efecto de los diferentes dopantes sobre CeO2 es la formación de vacantes de oxígeno en el soporte, factor éste que también afectaría a la actividad catalítica. Una tercera posibilidad, ya considerada anteriormente, viene determinada por el tamaño de las nanopartículas de Au sobre los diferentes soportes utilizados. Finalmente, se observa que la selectividad hacia la formación de CO2 presenta un comportamiento opuesto al de la conversión. A bajas temperaturas es el catalizador modificado con itrio el que presenta una mayor selectividad. Sin embargo, la tendencia se invierte al aumentar la temperatura por encima de los 373 K. Este fenómeno, así como el de disminución de la conversión con la temperatura, se debe a la competencia de la reacción de oxidación de hidrógeno [40][49][50][51][52]. 144 Capítulo 6 Llieva y col. [53] estudiaron la actividad catalítica de catalizadores de oro soportados en óxido de cerio dopado con óxidos de hierro, de manganeso y de cobalto. Estos autores obtuvieron diferentes resultados de conversión de CO en función del soporte, la naturaleza del dopante y el método de preparación utilizado. Laguna y col. [54] observaron que la adición de hierro en catalizadores de Au soportados sobre óxido de cerio favorece la conversión de CO, principalmente a bajas temperaturas. Por su parte, Dobrosz-Gómez y col. [33] determinaron que la actividad catalítica en catalizadores de Au/CeZrO depende fuertemente de la relación Ce/Zr y de su reducibilidad, es decir, de la movilidad del oxígeno de red. 145 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. 100 (a) Conversión de CO, % 80 60 40 20 Au/CeO2 Au/0,7CeO2-0,3Nb2O5 0 300 Au/0,7CeO2-0,3Y2O3 320 340 360 380 400 420 440 460 480 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 20 Au/CeO2 Au/0,7CeO2-0,3Nb2O5 0 300 Au/0,7CeO2-0,3Y2O3 320 340 360 380 400 Temperatura, K Figura 6.6. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores de oro reducidos a 473 K utilizando un flujo de 20 % de H2, 2% de CO y O2 y He como balance. 146 Capítulo 6 3.6.3. Oxidación preferencial de CO: influencia de la temperatura de reducción. Los resultados mostrados en la Figura 6.6 claramente muestran que los tres catalizadores estudiados presentan perfiles de reducción totalmente diferentes a bajas temperaturas. Sobre esta base, se ha considerado conveniente realizar un estudio del comportamiento catalítico de las muestras reducidas a una temperatura inferior que la utilizada anteriormente (343 K vs. 473 K). Para ello se estudió la reacción de oxidación de CO en condiciones isotermas (343 K), con las muestras previamente reducidas a 343 K, utilizando una mezcla de gases compuesta por un 2 % de CO, 2 % de O2 y 20 % H2, balanceado en He. Las temperaturas de reducción y de reacción seleccionadas se basan en la menor temperatura de reducción obtenida en los experimentos de RTP-H2 para las muestras dopadas. Así, el catalizador de Au/CeO2 presenta un pico de reducción a temperaturas superiores a 343 K, lo que puede ser indicativo de que a esta temperatura todavía no se han reducido completamente las especies de Au presentes en el catalizador. Las Figura 6.7 (a) y (b) muestran respectivamente los perfiles de conversión de CO y de selectividad obtenidos en los ensayos catalíticos realizados. Independientemente de la temperatura de reducción, el catalizador de Au/0,7CeO2-0,3Y2O3 presenta una menor conversión de CO, como se mostró también en la Figura 6.6 (a). Por otro lado, no se observó ninguna diferencia en la actividad catalítica entre los otros dos catalizadores. Algo similar ocurre con los valores de selectividad a CO2 obtenidos. En este punto es interesante destacar que, en un primero momento, se esperaba que el catalizador Au/CeO2 fuera el menos activo de los tres tras la reducción a baja temperatura, dado que según los resultados de RTP a esta temperatura de reducción todavía las partículas de oro no deberían estar completamente reducidas. Sin embargo, los resultados han mostrado que es el catalizador Au/0,7CeO2-0,3Y2O3 el que sigue presentando una actividad más baja. Así, cabe concluir que este catalizador es el menos activo para la reacción, independientemente de la temperatura de reducción utilizada (en el rango utilizado), lo que puede estar relacionado con su capacidad para suministrar el oxígeno de red o, como otra posibilidad, con el tamaño de partícula metálica en este catalizador. Por último, resulta interesante destacar la elevada estabilidad, en términos de conversión y selectividad, de los catalizadores Au/CeO2 y Au/0,7CeO2-0,3Nb2O5 (no se observa desactivación con el tiempo). 147 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. 100 (a) Conversión de CO, % 80 60 40 20 Au/CeO2 Au/0,7CeO2-0,3Nb2O5 Au/0,7CeO2-0,3Y2O3 0 0 20 40 60 80 100 120 140 160 180 200 Tiempo, min 100 (b) Selectividad a CO2, % 80 60 40 20 Au/CeO2 Au/0,7CeO2-0,3Nb2O5 Au/0,7CeO2-0,3Y2O3 0 0 20 40 60 80 100 120 140 160 180 200 Tiempo, min Figura 6.7. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores de oro reducidos y en isotermos a 343 K. 148 Capítulo 6 3.6.4. Oxidación preferencial de CO: influencia de la temperatura de calcinación. Como ha sido mencionado inicialmente, hay varios factores que pueden afectar a la actividad catalítica en catalizadores basados en Au. Entre ellos se encuentran el tamaño de partícula del oro y su movilidad en el soporte (estabilidad frente a la sinterización), así como la química superficial (presencia de grupos -OH superficiales). El proceso de calcinación durante la preparación del catalizador puede modificar estos parámetros. Por ello, se consideró importante analizar el comportamiento catalítico de las muestras preparadas, sometidas a diferentes temperaturas de calcinación. En la Figura 6.8 se muestran los resultados de actividad catalítica para los tres catalizadores de Au calcinados a diferentes temperaturas. En primer lugar cabe señalar que la actividad catalítica del catalizador Au/CeO2 calcinado a 473 K y a 573 K es muy similar, sólo disminuyendo ligeramente a bajas temperaturas de reacción tras la calcinación a 773 K. Esta observación demuestra la elevada estabilidad térmica de las nanopartículas de Au cuando se utiliza el CeO2 como soporte. En el caso de los catalizadores dopados con óxido de niobio y óxido de itrio, el aumento de la temperatura de calcinación de 473 K a 773 K, afecta de forma mucho más acentuada al comportamiento catalítico, sobre todo a bajas temperaturas de reacción. El efecto es más importante en el caso del catalizador Au/0,7CeO2-0,3Y2O3. En principio, el fenómeno observado sería consecuencia de un aumento del tamaño de las nanopartículas de oro al aumentar la temperatura de calcinación, es decir, que la estabilidad térmica de las nanopartículas de Au disminuye en el orden CeO2 > 0,7CeO2-0,3Nb2O5 > 0,7CeO2-0,3Y2O3. Por lo tanto, se puede establecer que la menor actividad del catalizador Au/0,7CeO2-0,3Y2O3, calcinado a 473 K (Figura 6.6), está relacionada con un mayor tamaño de partícula (mayor movilidad) del Au sobre este soporte. En resumen, se puede asumir que la disminución de la actividad en el caso de los catalizadores de Au/0,7CeO2-0,3Y2O3 y Au/0,7CeO2-0,3Nb2O5 con el incremento de la temperatura de reacción puede estar relacionada con una mayor movilidad de las partículas del oro en el soporte y, por lo tanto, una mayor facilidad de sinterización que en el caso del catalizador Au/CeO2. Si se asume que la disminución de la actividad catalítica con la temperatura de calcinación se debe fundamentalmente a un mayor tamaño de partícula de Au, resulta evidente que el tamaño y la morfología de las nanopartículas soportadas depende en gran medida de la naturaleza del soporte (más estables sobre CeO2 puro frente a los óxidos dopados). 149 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. 100 (a) Conversión de CO, % 80 60 40 20 Au/CeO2_TC473 Au/CeO2_TC573 0 300 Au/CeO2_TC773 320 340 360 380 400 420 440 460 480 Temperatura, K 100 (b) Conversión de CO, % 80 60 40 Au/0,7CeO2-0,3Nb2O5_TC473 20 Au/0,7CeO2-0,3Nb2O5_TC573 Au/0,7CeO2-0,3Nb2O5_TC673 0 300 Au/0,7CeO2-0,3Nb2O5_TC773 320 340 360 380 400 Temperatura, K 150 420 440 460 480 Capítulo 6 100 (c) Conversión de CO, % 80 60 40 20 Au/0,7CeO2-0,3Y2O3 _TC473 Au/0,7CeO2-0,3Y2O3_TC573 0 300 Au/0,7CeO2-0,3Y2O3_TC773 320 340 360 380 400 420 440 460 480 Temperatura, K Figura 6.8. Conversión de CO para los catalizadores de Au/CeO2 (a), Au/0,7CeO2-0,3Nb2O5 (b) y Au/0,7CeO2-0,3Y2O3 (c) reducidos a 473 K y calcinados a distintas temperaturas (TC). 3.6.5. Oxidación preferencial de CO: influencia de la concentración de O2. Otro parámetro estudiado en la reacción de oxidación preferencial de CO ha sido la influencia de la concentración de O2 en el gas de reacción, determinada por el valor de λ (λ = 2[O2]/[CO]). El estudio se ha realizado mediante reacción a temperatura programada con una mezcla de gases que contiene 2 % de CO, 0,6-4 % de O2, 20 % H2 balanceada en He, con las muestras previamente reducidas a 473 K. Los perfiles de conversión de CO y de selectividad en función de la temperatura de reacción se muestran en las Figura 6.9, Figura 6.10 y Figura 6.11, para las muestras Au/CeO2, Au/0,7CeO2-0,3Nb2O5 y Au/0,7CeO2-0,3Y2O3, respectivamente. Como se puede apreciar en las diferentes figuras, tanto los valores de conversión de CO como de selectividad a CO2 dependen de forma ostensible del valor de λ. En general, la actividad catalítica aumenta al aumentar el contenido de O2 durante la reacción PROX. Paralelamente, este aumento en la actividad catalítica viene acompañado de una diminución en la selectividad a CO2. Así, con un exceso de oxígeno, en condiciones no estequiométricas de reacción, se favorece tanto la conversión de monóxido de carbono como la de hidrógeno. Diferentes estudios han encontrado la misma tendencia en cuanto a la dependencia de la reacción con el valor de λ, sobre diferentes catalizadores [50][51][55][56][57]. 151 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. Es interesante destacar que todas las curvas de light-off del catalizador Au/0,7CeO2-0,3Y2O3, obtenidas para las diferentes proporciones de oxígeno siguen la misma tendencia, es decir, presentan un valor más bajo de conversión de CO a bajas temperaturas en comparación con los otros dos catalizadores. Otra observación importante, que cabe analizar en esta etapa, es el efecto de utilizar condiciones reductoras y estequiométricas, con λ = 0,6 y λ = 1, respectivamente. Se puede apreciar que, en el caso del catalizador Au/0,7CeO2-0,3Nb2O5, un aumento en la concentración de oxígeno desde λ = 0,6 a λ = 1, produce un aumento de la conversión de CO del 45 % al 67 % a 313 K, sin que la selectividad se modifique de forma importante. Además, cuando se utilizan condiciones oxidantes (λ > 1), se observa una mejora de la conversión de CO y una disminución de la selectividad, debido a la competencia entre la oxidación del CO y la del hidrógeno. Esta mejora de la actividad catalítica no es ya muy evidente para valores muy elevados de λ. En este caso (λ > 1) se observó un aumento muy ligero de la conversión de CO, principalmente para el catalizador Au/CeO2. Se apreció un aumento del 95 % al 100 % de conversión de CO a 353 K, utilizando λ = 2 y λ = 4, respectivamente, junto con una bajada elevada de la selectividad hacia la formación de CO2 del 50 % al 25 %, en las mismas condiciones. Esto indica que el aumento de la concentración de oxígeno favorece la oxidación del CO y, también, del H2, siendo ese efecto proporcional muy diferente dependiendo del soporte y, por tanto, del catalizador utilizado. En la bibliografía se muestra que el CeO2 podría actuar como un regulador de oxígeno, de forma que estabiliza en cierta forma el valor de λ cuando las condiciones no son estequiométricas. Sin embargo, este efecto estabilizador es temporal si no varía la composición de la corriente gaseosa de alimentación [58]. 152 Capítulo 6 100 (a) Conversión de CO, % 80 60 40 20 0 300 = 0,6 =1 =2 =3 =4 320 340 360 380 400 420 440 460 480 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 20 0 300 = 0,6 =1 =2 =3 =4 320 340 360 380 400 Temperatura, K Figura 6.9. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores de Au/CeO2 con distintas concentraciones de O2. 153 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. 100 (a) Conversión de CO, % 80 60 40 20 0 300 = 0,6 = 1 = 2 = 4 320 340 360 380 400 420 440 460 480 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 20 0 300 = 0,6 = 1 = 2 = 4 320 340 360 380 400 Temperatura, K Figura 6.10. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores de Au/0,7CeO2-0,3Nb2O5 con distintas concentraciones de O2. 154 Capítulo 6 100 (a) Conversión de CO, % 80 60 40 20 0 300 =1 =2 =4 320 340 360 380 400 420 440 460 480 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2 , % 80 60 40 20 0 300 =1 =2 =4 320 340 360 380 400 Temperatura, K Figura 6.11. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores de Au/0,7CeO2-0,3Y2O3 con distintas concentraciones de O2. 4. Conclusión. Se han preparado tres catalizadores de Au utilizando óxido de cerio puro y óxidos mixtos de cerio-niobio y cerio-itrio como soportes. Los perfiles de DRX 155 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. indican que el método utilizado para la preparación de los soportes da lugar a disoluciones sólidas cerio-niobio y cerio-itrio. Los resultados de reducción a temperatura programada permiten concluir que la adición del oro favorece la reducibilidad de los catalizadores, y que este efecto fue menor en el catalizador con el soporte dopado con itrio. Los resultados obtenidos para la actividad catalítica han mostrado que la conversión de CO está fuertemente influenciada por la concentración de oxígeno en el flujo gaseoso de alimentación, de forma que elevadas concentraciones de oxígeno favorecen la conversión de CO, con un consiguiente descenso en la selectividad. Además, se observó que el catalizador Au/0,7CeO2-0,3Nb2O5 presenta mejores resultados para la conversión de CO que el catalizador Au/0,7CeO2-0,3Y2O3. Esta observación está relacionada con un mayor tamaño de las nanopartículas de oro en el catalizador dopado con itrio, posiblemente debido a una mayor movilidad de las nanopartículas en este soporte (menor interacción metalsoporte). 5. Referencias. [1] [2] [3] [4] [5] [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] B. Hammer, J.K. Norskov, Nature, 376 (1995) 238-240. G. Bond, Gold Bull, 41 (2008) 235-241. G.J. Hutchings, M. Brust, H. Schmidbaur, Chem. Soc. Rev., 37 (2008) 1759-1765. A. Stephen, K. Hashmi, G.J. Hutchings, Angew. Chem. Int. Ed., 45 (2006) 7896-7936. C. Galletti, S. Fiorot, S. Specchia, G. Saracco, V. Specchia, Chem. Eng J., 134 (2007) 45-50. M. Haruta, T. Kobayashi, H. Sano, N. Yamada, Chem. Lett., 16 (1987) 405-408. M. Haruta, Gold Bull., 37 (2004) 27-36. S. Kandoi, A.A. Gokhale, L.C. Grabow, J.A. Dumesic, M. Marvikakis, Catal. Lett., 93 (2004) 93-100. B. Schumacher, V. Plzak, K. Kinne, R.J. Behm, Catal. Lett., 89 (2003) 109-114. G.R. Bemwenda, S. Tsubota, T. Nakamura, M. Haruta, Catal. Lett., 44 (1997) 83-87. G.C. Bond, D.T. Thompson, Gold Bull., 33 (2000) 41-51. A.M. Venezia, G. Pantaleo, A. Longo, G. Di Carlo, M.P. Casaletto, F.L. Liotta, G. Deganello, J. Phys. Chem. B, 109 (2005) 2821-2827. L. Delannoy, N. Weither, N. Tsapatsaris, A.M. Beesley, L. Nchari, L.M. Schroeder, C. Louis, Top. Catal., 44 (2007) 263-273. S. Arii, F. Mortin, A.J. Renouprez, J.L. Rousset, J. Am. Chem. Soc., 126 (2004) 11991205. A. Beck, A. Horváth, Gy. Stefler, R. Katona, O. Geszti, Gy. Tolnai, L.F. Liotta, L. Guczi, Catal. Today, 139 (2008) 180-189. A. Wolf, F. Schüth, Appl. Catal. A: Gen., 226 (2002) 1-13. H. Sakurai, M. Haruta, Appl. Catal. A: Gen., 127 (1995) 93-105. G. Yi, H. Yang, B. Li, H. Lin, K-I Tanaka, Y. Yuan, Catal. Today, 157 (2010) 83-88. 156 Capítulo 6 [19] W. Deng, J. de Jesus, H. Saltsburg, M. Flytzani-Stephanopoulos, Appl. Catal. A: Gen., 291 (2005) 126-135. [20] L.F. Liotta, G. Di Carlo, G. Pantaleo, A.M. Venezia, Catal. Today, 158 (2010) 56-62. [21] J. Guzman, S. Carrettin, J.C. Fierro-Gonzalez, Y. Hao, B.C. Gates, A. Corma, Angew. Chem. Int. Ed., 44 (2005) 4778-4781. [22] J. Guzman, S. Carrettin, A. Corma, J. Am. Chem. Soc., 127 (2005) 3286-3287. [23] M. Jia, Y. Shen, C. Li, Z. Bao, S. Sheng, Catal. Lett., 99 (2005) 235-239. [24] E. Quinet, F. Morfin, G. Diehl, P. Avenier, V. Caps, J.L. Rousset, Appl. Catal. B: Env., 80 (2008) 195-201. [25] K. Tanaka, M. Shou, H. He, X. Shi, X. Zhang, J. Phys. Chem. C, 113 (2009) 1242712433. [26] R. Leppelt, B. Schumacher, V. Plzak, M. Kinne, R.J. Behm, J. Catal., 244 (2006) 137152. [27] Q. Fu, H. Saltsburg, M. Flytzani-Stephanolopoulos, Appl. Catal. B: Env., 56 (2005) 57-68. [28] M. Manzoli, F. Boccuzzi, A. Chiorino, F. Vindigni, W. Deng, M. FlytzaniStephanolopoulos, J. Catal., 245 (2007) 308-315. [29] M. Comotti, C. Della Pina, R. Matarrese, M. Rossi, Angew. Chem. Int. Ed., 43 (2004) 5812-5815. [30] Q. Wu, J. Chen, J. Zhang, Fuel Processing Technology, 89 (2008) 993-999. [31] M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today, 68 (2001) 53-61. [32] H. Roh, H.S. Potdar, K. Jun, S.Y. Han, J. Kim, Catal. Letters, 93 (2004) 203-207. [33] I. Dobrosz-Gómez, I. Kocemba, J.M. Rynkowski, Appl. Catal. B: Env., 83 (2008) 240-255. [34] G. Avgouropoulos, M. Manzoli, F. Boccuzzi, T. Tabakova, J. Papavasiliou, T. Ioannides, V. Idakiev, J. Catal., 256 (2008) 237-247. [35] N.F.P. Ribeiro, F.M.T. Mendes, C.A.C. Perez, M.M.V.M. Souza, M. Schmal, Appl. Catal. A: Gen., 347 (2008) 62-71 [36] H. Sakurai, T. Akita, S. Tsubota, M. Kiuchi, M. Haruta, Appl. Catal. A: Gen., 291 (2005) 179–187. [37] T. Yun-Bao, L. Jin-Yong, M. Ming, W. Gang, H. Jun-Jun, International J. Hydrogen Energy, 34 (2009) 3743-3754. [38] T. Akita, M. Okumura, K. Tanaka, M. Kohyama, S. Tsubota, M. Haruta, J. Electron Microscopy, 54 (2005) i81-i85. [39] T. Akita, M. Okumura, K. Tanaka, M. Kohyama, M. Haruta, Catal. Today, 117 (2006) 62-68. [40] J.L. Ayastuy, M.P. González-Marcos, A. Gil-Rodríguez, J.R. González-Valesco, M.A. Gutiérrez-Ortiz, Catal. Today, 116 (2006) 391-399. [41] P. Fornasiero, G. Balducci, R. Di Monte, J. Kaspar, V. Sergo, G. Gubitosa, A. Ferrero, M. Graziani, J. Catal., 164 (1996) 173-183. [42] S. Ricote, G. Jacobs, M. Milling, Y. Ji, P.M. Patterson, B.H. Davis, Appl. Catal. A: Gen., 303 (2006) 35-47. 157 Catalizadores de oro soportados en CeO2 dopado con niobio o itrio para la oxidación preferencial de CO en presencia de H2. [43] T. Tabakova, F. Boccuzzi, M. Manzoli, J.W. Sobczak, V. Idakiev, D. Andreeva, Appl. Catal. A: Gen., 298 (2006) 127–143. [44] D. Andreeva, V. Idakiev, T. Tabakova, L. Ilieva, P. Falaras, A. Bourlinos, A. Travlos, Catal. Today, 72 (2002) 51–57. [45] M.S.P. Francisco, V.R. Mastelaro, P.A.P. Nascente, A.O.A. Florentino, J. Phys. Chem. B, 105 (2001) 10515-10522. [46] E.R. Sánchez, Catalizadores de Oro soportado sobre óxidos mixtos de tipo Ce-Zr. Influencia de las condiciones de pre-tratamiento sobre su actividad en la oxidación de CO, Tesis de doctorado, Universidad de Cádiz (2011). [47] Y-B. Tu, J-Y. Luo, M. Meng, G. Wang, J-J. He, International J. Hydrogen Energy, 34 (2009) 3743-3754. [48] N.F.R. Ribeiro, R.P.F. Bonfin, M.M.V.M. Souza, M. Schmal, J. Power Sources, 195 (2010) 7386-7390. [49] Z. Lendzion-Bielun, M.M. Bettehar, S. Monteverdi, D. Mosynski, U. Narkiewicz, Catal. Lett., 134 (2010) 196-203. [50] J.L. Ayastuy, A. Gil-Rodriguez, M.P. González-Marcos, M.A. Gutiérrez-Ortiz, International J. Hydrogen Energy, 31 (2006) 2231-2242. [51] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 58 (2005) 175-183. [52] H. Imai, M. Daté, S. Tsubota, Catal. Lett., 124 (2008) 68-73. [53] L. Llieva, G. Pantaleo, I. Ivanov, A. Maximova, R. Zanella, Z. Kaszkur, A.M. Vanezia, D. Andreeva, Catal. Today, 158 (2010) 44-55. [54] O.H. Laguna, M.A. Arzamendi, L.M. Gandía, F. Romero-Sarria, J.A. Odriozola, Catal. Today, 157 (2010) 155-159. [55] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 54 (2004) 59-66. [56] O. Pozdnyakova, D. Teschner, A. Wootsch, J. Kröhnert, B. Steinhauer, H. Sauer, L. Toth, F.C. Jentoft, A. Knop-Gericke, Z. Paál, R. Schlögl, J. Catal., 237 (2006) 1-16. [57] D. Teschner, A. Wootsch, O. Pozdnyakova-Tellinger, J. Kröhnert, E.M. Vass, M. Hävecker, S. Zafeiratos, P. Schnörch, P.C. Jentoft, A. Knop-Gericke, R. Schlögl, J. Catal., 249 (2007) 318-327. [58] A. Yee, S.J. Morrison, H. Idriss, J. Catal., 191 (2000) 30-45. 158 CAPÍTULO 7 Catalizadores de cobre soportados sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. Abstract. This chapter describes a study on copper-based catalysts supported on niobium-doped ceria in the preferential oxidation of CO in excess H2. The catalysts have been characterized by ICP-EOS, XRD, Raman, TEM, and H2TPR. The effects of the copper loading and of the amount of niobium added to the supports have been evaluated. It has been shown that these catalysts show high activity and selectivity in the title reaction. Furthermore, copper-based catalysts have relatively low price compared to platinum and gold-based catalysts. 176 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. 1. Introducción. El proceso denominado PROX es uno de los métodos más prometedores para la eliminación de CO en la corriente de alimentación de las pilas de combustible. Este proceso se puede llevar a cabo en dos intervalos de temperatura: (i) a bajas temperaturas, valores próximos a la temperatura de la pila de combustible (353–373 K), o (ii) a temperaturas más elevadas, valores cercanos a la temperatura de la unidad de reformado (523-573 K) [1]. De esta forma, y en función de la temperatura de trabajo, los catalizadores para esta reacción se pueden dividir básicamente en catalizadores compuestos por metales nobles y catalizadores basados en óxidos puros/óxidos mixtos, todos ellos soportados en distintos materiales. En este sentido, los catalizadores basados en Cu-CeO2 han generado mucha expectativa en la reacción de oxidación preferencial de CO debido a su fácil disponibilidad, su bajo coste y su elevada actividad [1][2][3]. La particular actividad de estos catalizadores, en términos de conversión de CO, se debe principalmente a sus propiedades redox en los sitios interfaciales entre el metal y el soporte [2][4][5][6][7]. En otras palabras, las propiedades redox del óxido de cobre, de manera general, dependen en mayor o menor medida de su interacción con el óxido de cerio. Adicionalmente, la presencia de óxido de cobre favorece la capacidad de almacenamiento de oxígeno (OSC) y la estabilidad térmica del óxido de cerio [8][9]. En este sentido, es conocido que el óxido de cobre bien disperso sobre el óxido de cerio se reduce a temperaturas inferiores, lo que favorece la adsorción de CO [10][11][12]. Hay varios factores que pueden afectar a las propiedades catalíticas de estos materiales: el método de preparación, la temperatura de calcinación y el contenido metálico [13][14][15]. Liu y col. [14] han investigado la influencia de distintos métodos de preparación para los catalizadores de cobre-cerio (coprecipitación, efecto del quelato, método del ácido cítrico y fase crítica), estableciendo que el método “efecto del quelato” es el que ofrece los mejores resultados, es decir, favorece la formación de defectos en el óxido de cerio y, consecuentemente, produce un efecto sinérgico entre el ciclo Cu (I)/Cu (II) y el Ce (III)/Ce (IV). Otro estudio realizado por Martínez-Arias y col. [15] sobre catalizadores de cobre-óxido de cerio preparados por el método de impregnación con humedad incipiente sugiere un modelo para el proceso redox que tiene lugar en estos catalizadores. En una primera etapa se reduce el óxido de cobre presente en las posiciones interfaciales con el óxido de cerio, promoviendo la reducción de este último. En este caso, la re-oxidación es generalmente fácil. En una segunda etapa, la reducción incluye primero al 160 Capítulo 7 cobre, y se extiende hacia el óxido de cerio en posiciones más lejanas de la interfase. En este caso la re-oxidación se lleva a cabo primeramente en el cerio que se encuentra lejos de la interfase, mientras que la oxidación del cobre se produce más tarde y se amortigua un poco por la estabilización de un estado reducido de cobre (Cu (I)) durante el ciclo redox. El comportamiento redox de los óxidos de cerio puede modificarse por la incorporación de otros elementos a la red, es decir, por la formación de un óxido mixto. En este sentido, varios autores han estudiado el efecto de la adición de un agente dopante en catalizadores de CuO/CeO2 sobre la actividad catalítica de estos sistemas en la reacción de oxidación de CO [3][12][13][16][17][18][19][20]. Estos estudios demuestran que la adición de un dopante puede favorecer la reacción PROX. Así, Chen y col. [17] observaron que proporciones apropiadas de Zr incorporado en la red del CeO2 favorecen tanto la movilidad de oxígeno como la actividad catalítica para la oxidación de CO. Estos autores proponen que la oxidación de CO está favorecida, principalmente, por el efecto sinérgico entre el óxido de cobre y el óxido de cerio. De esta forma, proponen un mecanismo redox en la interfase entre el soporte y el óxido de cobre [17]. La incorporación de un segundo catión metálico en el soporte puede favorecer la reducción-oxidación del CuO y CeO2, seguida de la interacción del CO/O2, y generar Ce (III) y Cu (I) junto con vacantes de oxígeno (VO) en la interfase entre del óxido de cobre y el soporte (Ecuación 7.1). A su vez, se crean especies carbonilo al contacto del CO con las especies de Cu (I) (Ecuación 7.2). Ce4+_O2-_Cu2+ + CO Ce3+_VO_Cu1+ + CO Ce3+_VO_Cu1+ + CO2 Ce3+_VO_Cu1+_CO (Ecuación 7.1) (Ecuación 7.2) El siguiente paso es la formación de un intermediario, un superóxido (O2-), mediante la adsorción de una molécula de oxígeno en el sitio vacante (Ecuación 7.3). Ce3+_VO_Cu1+_CO + O2 Ce4+_O2-_Cu1+_CO (Ecuación 7.3) Estas especies formadas pueden ser activas en la reacción de oxidación de CO (Ecuación 7.4), o pueden ser transformadas en O22- debido a la desorción de CO y la oxidación del Cu (I) (Ecuación 7.5). Ce4+_O2-_Cu1+ + CO Ce4+_O2-_Cu2+ + CO2 (Ecuación 7.4) Ce4+_O2-_Cu1+_CO Ce4+_O22-_Cu2+ + CO (Ecuación 7.5) 161 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. Finalmente, el peróxido se desvincula y el oxígeno migra a una vacante vecina, según la Ecuación 7.6. Ce4+_O22-_Cu2+ + Ce3+_VO_Cu1+_CO 2 Ce4+_O2-_Cu2+ + CO2 (Ecuación 7.6) Sin embargo, la adición de un dopante también puede ser perjudicial para la actividad catalítica, como observaron Ratnasamy y col. [12], quienes encontraron valores inferiores de conversión en CO para catalizadores dopados con Zr en comparación con los catalizadores donde se utilizó CeO2 puro como soporte. En este capítulo se describe la preparación de una serie de catalizadores de CuO soportados en óxidos mixtos xCeO2-(1-x)Nb2O5 (x= 1; 0,9; 0,7 y 0,4), utilizando diferentes proporciones de agente dopante. El objetivo es estudiar la influencia del agente dopante, así como las propiedades del cobre sobre la reacción de oxidación selectiva de CO. La idea de utilizar el óxido de niobio como dopante ha sido planteada con el objeto de evaluar la eficiencia catalítica de estos catalizadores, cuyo coste es inferior al que presentan aquellos que utilizan óxido de cerio puro como soporte. Cabe mencionar que en este capítulo no han sido estudiados los catalizadores soportados sobre óxido de cerio dopado con itrio, ya que estos soportes no favorecen la actividad catalítica incluso cuando se utiliza óxido de cobre como especie activa, en coherencia con los resultados anteriores obtenidos con platino y oro. 2. Experimental. 2.1. Preparación y caracterización de los catalizadores. La serie de catalizadores de cobre se preparó utilizando como soporte óxido de cerio dopado con niobio en diferentes proporciones, xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4). El soporte ha sido preparado por precipitación con urea a 363 K durante 11 h. Los detalles de la preparación de los soportes se encuentran en el Capítulo 5. Los catalizadores se prepararon por impregnación con humedad incipiente de los soportes citados anteriormente, utilizando disoluciones acuosas de Cu(NO3)2·3H2O (Panreac, 99,999%) de concentración adecuada para obtener catalizadores con 4 y 8 % en peso de cobre. Tras la impregnación, los catalizadores se secaron en estufa a 383 K durante 12 h y se calcinaron a 723 K durante 4 h. Los materiales obtenidos han sido caracterizados mediante diferentes técnicas, tales como DRX, ICP-OES, espectroscopía Raman, TEM y RTP-H2. 162 Capítulo 7 2.2. Ensayos catalíticos. Para analizar el comportamiento catalítico de las muestras en la reacción de oxidación de CO se llevaron a cabo experimentos de reacción a temperatura programada (313–473 K) y a presión atmosférica, utilizando una mezcla gaseosa de alimentación que contenía 20% H2, 2% CO, 2% O2 y balance con He. Antes de iniciar los experimentos, los catalizadores fueron tratados in situ a 313 K durante 10 minutos en un flujo de 10% de O2 en He (50 ml·min-1). Los productos de reacción fueron analizados por cromatografía de gases, utilizando detectores TDC y FID. La forma de cálculo utilizada para determinar la conversión de CO y O2, así como la selectividad, ha sido descrita en el Capitulo 2. 3. Resultados y discusión. 3.1. Caracterización textural y porcentaje metálico. En la Tabla 7.1 se muestran los valores obtenidos para la superficie específica BET de los soportes, y el porcentaje de cobre en cada catalizador determinado por ICP-EOS. Se puede observar inicialmente una disminución del área superficial para el soporte con bajo contenido de niobio, seguido de un aumento de la misma para proporciones más elevadas. Este resultado puede indicar que, de alguna manera, la adición de niobio modifica la estructura del óxido de cerio. Además, los resultados de ICP-EOS indican que los valores obtenidos para el contenido de cobre en cada catalizador fueron muy próximos a los valores nominales. Tabla 7.1. Área superficial BET del soporte y contenido de cobre (% en peso) de los catalizadores. Catalizador SBET, m2·g-1 (a) Contenido de Cu, % en peso 8Cu/CeO2 108 7,9 4Cu/CeO2 108 3,9 4Cu/0,9CeO2-0,1Nb2O5 84 3,9 4Cu/0,7CeO2-0,3Nb2O5 114 3,9 4Cu/0,4CeO2-0,6Nb2O5 138 3,9 (a) Área superficial BET del soporte. 163 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. 3.2. Caracterización de los catalizadores mediante DRX. En la Figura 7.1 se muestran los difractogramas de rayos X de los diferentes catalizadores estudiados. Se observa la presencia de picos relacionados con la fase cúbica de la estructura tipo fluorita del óxido de cerio, asignados a los planos de difracción (111), (200), (220), (311), (222) y (400) [21][22][23][24]. Además, se puede apreciar la presencia de picos correspondientes a la estructura hexagonal del óxido de niobio [25][26][27][27][28] en el caso de los soportes con proporciones elevadas de dopante, hecho que indica la presencia de fases aisladas de óxido (no hay formación de un óxido mixto). Adicionalmente, en los difractogramas puede apreciarse una progresiva disminución de la intensidad y un aumento de la anchura de los picos en relación con el pico principal (111) del óxido de cerio con la adición de dopante. Esta observación indica por un lado la pérdida de cristalinidad, y por otro lado, una disminución del tamaño del cristal. Se puede observar también la presencia de picos correspondientes a óxido de cobre (2 θ = 35,5º y 38,7º [29][30]), principalmente para el catalizador con un mayor porcentaje de óxido de cobre, mientras que para el resto de catalizadores no se ha detectado la presencia del mismo. La ausencia de picos correspondientes a óxido de cobre en los catalizadores con baja carga puede ser atribuido a la presencia de óxido de cobre amorfo, o a la presencia de una buena dispersión superficial del óxido de cobre, hecho que dificultaría la detección mediante esta técnica, de acuerdo con la literatura [19][31]. 164 Capítulo 7 CeO2 Nb2O5 CuO 4Cu/0,4CeO2-0,6Nb2O5 Intensidad, u.a. 4Cu/0,7CeO2-0,3Nb2O5 4Cu/0,9CeO2-0,1Nb2O5 4Cu/CeO2 8Cu/CeO2 20 30 40 50 60 70 80 2 Figura 7.1. Difractogramas de rayos-X de los catalizadores de 8Cu/CeO2 y 4Cu/xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4). 3.3. Caracterización de los catalizadores mediante espectroscopía Raman. Los espectros Raman para los soportes y los catalizadores de cobre se muestran en la Figura 7.2 (a) y (b), respectivamente. Se puede apreciar que los espectros correspondientes a los soportes muestran una disminución de la intensidad de la banda debida al modo activo F2g de la estructura tipo fluorita del óxido de cerio, a 462 cm-1, al tiempo que se puede observar una banda débil, en torno a los 540-600 cm-1, que puede ser atribuida a vacantes de oxígeno debido a la sustitución de Ce (IV) por iones de diferente tamaño [32]. Además, se observa un pequeño desplazamiento que puede estar relacionado con la distorsión de la red debida a la incorporación del niobio en la red del óxido de cerio. Este hecho puede ser indicativo de que el niobio se incorpora a la estructura del óxido de cerio, formando un óxido mixto. Por último, es interesante mencionar que en el caso del catalizador con una elevada proporción de niobio, x = 0,4, se observa la presencia de una banda a 706 cm-1 que puede ser característica a la fase Nb2O5. La aparición de esa banda, junto con la disminución de la banda a 462 cm-1, indicaría que en este caso o bien no se forma el óxido mixto o, más probablemente, parte del niobio se encuentra segregado como Nb2O5. 165 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. En el caso de los catalizadores se apreciaron las mismas bandas observadas en los espectros de los soportes y, adicionalmente, nuevas bandas a 310 cm-1 y a 800 cm-1 en el caso de los catalizadores dopados con niobio. Algunos autores [33][34] observaron la presencia de una banda a 831 cm-1 en catalizadores de CuO/CeO2 tras un tratamiento con oxígeno. Esta banda ha sido relacionada con la formación de especies peróxido (O22-) en el óxido de cerio. Sin embargo, en el caso de los catalizadores estudiados en este capítulo no se ha hecho un pre tratamiento de la muestras con oxígeno, por lo que se descarta esta posibilidad. Por lo tanto, la presencia de esta banda puede estar relacionada con la interacción entre el metal y el soporte. Paralelamente, no se observó la presencia de bandas características del óxido de cobre a 290 cm-1, 340 cm-1 y 630 cm-1 [32][33][34], lo que sugiere que éste está bien disperso en la superficie del catalizador, de acuerdo con los resultados obtenidos por DRX. 166 Capítulo 7 CeO2 0,9CeO20,1Nb2O5 0,7CeO20,3Nb2O5 Intensidad, u.a. 0,6CeO20,4Nb2O5 -1 462 cm (a) CeO2 0,9CeO2-0,1Nb2O5 0,7CeO2-0,3Nb2O5 410 420 430 440 450 460 470 490 500 0,4CeO2-0,6Nb2O5 510 Intensidad, u.a. Raman shift, cm 480 -1 200 -1 706 cm 300 400 500 600 700 Desplazamiento Raman, cm 800 900 1000 -1 (b) 4Cu/CeO2 4Cu/0,9CeO2-0,1Nb2O5 4Cu/0,7CeO2-0,3Nb2O5 -1 4Cu/0,4CeO2-0,6Nb2O5 Intensidad, u.a. 310 cm 200 -1 706 cm 300 400 500 600 -1 800 cm 700 Desplazamiento Raman, cm 800 900 1000 -1 Figura 7.2. Espectros Raman de los catalizadores de Cu/xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4). 3.4. Caracterización de los catalizadores mediante TEM. En la Figura 7.3 se muestran las imágenes de los catalizadores 8Cu/CeO2 y 4Cu/xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4) obtenidas mediante TEM. Todas las 167 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. partículas de CuO están bien dispersas y presentan una forma esférica. El tamaño de partícula de los catalizadores no ha sido calculado debido al elevado grado de aglomeración, el cual dificulta su determinación. Además, la distribución del tamaño de partícula de óxido de cobre ha sido difícil de determinar debido a su elevado grado de dispersión y por la presencia de tamaños de partículas muy pequeños. Excepto para el caso del catalizador con alto contenido en cobre (8 %), donde se observa la presencia de partículas muy grandes de óxido de cobre, aproximadamente de 100 nm, aglomeradas en puntos específicos (Figura 7.3 (b)). Este resultado concuerda con los datos obtenidos con DRX. Además, algunos autores sugieren que la difícil detección del mismo, en las imágenes TEM, puede estar relacionada con la incorporación de éste en el soporte, ya que se pueden tornar invisibles en la superficie. [18]. (a) (b) (c) (e) (f) 2 nm (d) 2 nm Figura 7.3. Imágenes de TEM de los catalizadores de 8Cu/CeO2 (a,b), 4Cu/CeO2 (c), 4Cu/0,9CeO2-0,1Nb2O5 (d), 4Cu/0,7CeO2-0,3Nb2O5 (e) y 4Cu/0,4CeO2-0,6Nb2O5 (f). 3.5. Caracterización de los catalizadores mediante RTP-H2. La reducibilidad de los catalizadores se ha determinado mediante la técnica de reducción a temperatura programada con hidrógeno (RTP-H2). Los perfiles de reducción se presentan en la Figura 7.4. La curva de reducción del CeO2 muestra dos picos, uno a 760 K atribuido a la reducción superficial del óxido, y otro a 1050 K debido a la reducción del interior de las partículas (másica) 168 Capítulo 7 [35][36][37]. En este caso solo se presentaron los perfiles hasta una temperatura de 650 K, puesto que es el intervalo donde aparecen los picos con mayor interés en esta etapa. Es conocido que el efecto de la interacción sinérgica entre el óxido de cobre y el óxido de cerio favorece la reducción de las especies de cobre en la superficie del óxido de cerio. Generalmente, el perfil de reducción del óxido de cobre puede estar asociado con diferentes especies de Cu-O: (i) la presencia de especies Cu (II) altamente dispersas que pueden interaccionar fuertemente con el soporte; (ii) débil interacción magnética entre iones de Cu (II) cercanos; (iii) pequeños clústeres bi- y tri-dimensionales sin estructura regular; (iv) grandes agregados tridimensionales con propiedades idénticas al óxido de cobre puro [13][18][37]. Para las muestras estudiadas en este capítulo se observó la presencia de diferentes especies de Cu susceptibles de sufrir procesos de reducción, con la aparición de varios picos de consumo de hidrógeno. Además, es interesante observar que la presencia o no de estas especies de cobre no afecta a la actividad catalítica de estos catalizadores, como se verá más adelante en el presente capítulo. La presencia de dos o tres picos de reducción bien definidos indica una gran heterogeneidad superficial en la muestra, debida a la presencia de diferentes especies de cobre reducibles. Estudios descritos en la literatura demuestran que la reducción del CuO puro se produce a 623 K [13]. La interacción cerio/cobre queda evidenciada por la presencia de procesos de reducción característicos del sistema CuO-CeO2 localizados a temperaturas inferiores a la correspondiente reducción del CuO puro. La temperatura de reducción también está influenciada por el tamaño de cristal del óxido metálico [19][38][39], de forma que cuanto menor sea el tamaño de cristal, menor será la temperatura de reducción de los óxidos debido al mayor contacto o interacción con el soporte [38][39]. En este sentido, se observa que en la serie de xCeO2-(1-x)Nb2O5 el tamaño de los cristales de cobre es bastante homogéneo, ya que presentan valores de temperatura de reducción muy próximos. Este resultado está de acuerdo con los difractogramas de rayos X, donde no se observó la presencia de picos correspondientes al óxido de cobre en los catalizadores con baja proporción del mismo, y con las imágenes TEM, en las que tampoco fue posible apreciar la presencia de cristales de óxido de cobre. 169 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. 4Cu/0,4CeO2-0,6Nb2O5 Intensidad, u.a. 4Cu/0,7CeO2-0,3Nb2O5 4Cu/0,9CeO2-0,1Nb2O5 4Cu/CeO2 8Cu/CeO2 300 350 400 450 500 550 600 650 Temperatura, K Figura 7.4. Perfiles de reducción a temperatura programada de los catalizadores de cobre. 3.6. Comportamiento catalítico. 3.6.1. Oxidación preferencial de CO: influencia del porcentaje de cobre. La primera variable estudiada en condiciones de reacción fue la influencia del contenido de cobre. Para ello se utilizaron los catalizadores con un 8 % y un 4 % en peso de cobre soportados sobre óxido de cerio puro. Los perfiles de conversión de CO y de selectividad en función de la temperatura se muestran en la Figura 7.5 (a) y (b), respectivamente. Se puede apreciar que, independiente de la carga de cobre, los dos catalizadores estudiados presentan valores de conversión de CO así como de selectividad muy próximos. Por ello, se decidió utilizar catalizadores con un 4 % de cobre en peso para el estudio del efecto del soporte. La similitud en el comportamiento de ambos catalizadores está en coherencia con los resultados obtenidos por RTP-H2, donde se apreciaron procesos de reducción (especies en superficie) muy similares para ambos catalizadores (Cu/CeO2 con 8 % y 4 % en peso). En el caso del catalizador con un elevado porcentaje de cobre (8 %) aparece un tercer pico de reducción a elevada temperatura, atribuible a la reducción másica del óxido de cobre y que, aparentemente, no afecta a los resultados de actividad tras reducción a baja temperatura. 170 Capítulo 7 100 (a) Conversión de CO, % 80 60 40 20 4Cu/CeO2 0 300 8Cu/CeO2 320 340 360 380 400 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 20 4Cu/CeO2 0 300 8Cu/CeO2 320 340 360 380 400 420 440 460 480 Temperatura, K Figura 7.5. Conversión de CO (a) y selectividad a CO2 (b) para los catalizadores con 8 % y 4 % en peso de cobre. 171 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. 3.6.2. Oxidación preferencial de CO: estudio de la influencia de la proporción de cerio y niobio en el soporte. Como una segunda etapa, se estudió la oxidación preferencial de CO con la serie de catalizadores soportados sobre xCeO2-(1-x)Nb2O5, con el objetivo de estudiar el efecto de la proporción de niobio en el soporte sobre la actividad catalítica. Los resultados de actividad catalítica y selectividad se muestran en la Figura 7.6 (a) y (b), respectivamente. Como se puede apreciar, independientemente de la relación Ce/Nb, los catalizadores presentan una elevada conversión de CO, con valores equiparables a los del catalizador con el soporte de óxido de cerio puro. Prácticamente todos los catalizadores presentan una conversión de CO del 100% y con valores de selectividad mayores del 96% a 413 K. Es interesante observar una pérdida de la selectividad con el aumento de la temperatura de reacción, lo que indica que a elevadas temperaturas de reacción se favorece también la reacción de oxidación de hidrógeno. Wu y col. [18] estudiaron la oxidación de CO en catalizadores de cobre soportados sobre óxido de cerio dopado con óxido de titanio. Estos autores observaron una elevada actividad que puede estar relacionada con la presencia del dopante. La adición del TiO2 favorece el aumento del área superficial, disminuye el tamaño de partícula del soporte y favorece la dispersión del óxido de cobre. Así, la fuerte interacción superficial metalsoporte favorece la actividad catalítica. Zou y col. [3][40] observaron que el pre-tratamiento con un 20% de oxígeno favorece la conversión de CO, debido a la formación de especies Cu (I)/Cu (II) y CuO activadas en la superficie del catalizador. Todos los catalizadores de cobre soportados sobre ceria dopada con niobio presentan el mismo perfil de conversión de CO que el catalizador con el soporte no dopado. Esta tendencia está de acuerdo con los resultados obtenidos de caracterización por reducción a temperatura programada, difracción de rayos X, TEM y espectroscopía Raman. De hecho, es interesante indicar que en el caso del catalizador 4Cu/0,4CeO2-0,6Nb2O5 se observó un perfil distinto de selectividad a la formación de CO 2, de forma que el catalizador es menos selectivo a temperaturas más elevadas, y esto puede estar relacionado con la presencia de óxido de niobio segregado, tal y como se observó en los análisis de espectroscopía Raman. 172 Capítulo 7 100 (a) Conversión de CO, % 80 60 40 4Cu/CeO2 4Cu/0,9CeO2-0,1Nb2O5 20 4Cu/0,7CeO2-0,3Nb2O5 4Cu/0,4CeO2-0,6Nb2O5 0 300 320 340 360 380 400 420 440 460 480 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 4Cu/CeO2 20 4Cu/0,9CeO2-0,1Nb2O5 4Cu/0,7CeO2-0,3Nb2O5 0 300 4Cu/0,4CeO2-0,6Nb2O5 320 340 360 380 400 420 440 460 480 Temperatura, K Figura 7.6. Conversión de CO (a) y selectividad a CO2 (b) para la serie 4Cu/xCeO2-(1-x)Nb2O5 (x = 1; 0,9; 0,7 y 0,4). 4. Conclusiones. Se prepararon diferentes catalizadores de cobre soportado sobre una serie de óxido de cerio dopado con niobio. El primer estudio realizado fue el de la influencia del porcentaje de cobre en la actividad catalítica. Los resultados 173 Catalizadores de cobre soportado sobre CeO2 dopado para la reacción de oxidación preferencial de CO en presencia de H2. obtenidos demostraron que, independiente de la proporción de cobre, 4 % u 8% en peso, ambos catalizadores presentaron los mismos resultados de conversión de CO. El estudio del efecto de la relación Ce/Nb en los soportes permite concluir que todos los catalizadores preparados presentaron valores de conversión de CO y de selectividad a CO2 muy similares. Sólo el catalizador con mayor contenido en Nb en el soporte presentaba una mayor caída en la selectividad a CO2 al aumentar la temperatura de reacción, lo que puede estar relacionado con la presencia de Nb2O5 segregado en el soporte. 5. Referencias. [1] E.C. Njagi, H.C. Genuino, C.K. Kingóndu, C-H. Chen, D. Horvath, S.L. Suib, International J. Hydrogen Energy, 36 (2011) 6768-6779. [2] A. Martínez-Arias, D. Gamarra, M. Fernández-García, A. Hornés, P. Bera, Zs. Koppány, Z. Schay, Catal. Today, 143 (2009) 211-217. [3] H. Zou, S. Chen, W. Lin, J. Natural Gas Chemistry, 17 (2008) 208-211. [4] G. Sedmark, S. Hocevr, J. Levec, J. Catal., 213 (2003) 135-150. [5] A. Martínez-Arias, M. Fernández-García, O. Gálvez, J.M. Coronado, J.A. Anderson, J.C. Conesa, J. Soria, G. Munuera, J. Catal., 195 (2000) 207–216. [6] A. Martínez-Arias, M. Fernández-García, J. Soria, J. Conesa, J. Catal., 182 (1999) 367-377. [7] J. Wang, S. Lin, T. Huang, Appl. Catal. A: Gen., 232 (2002) 107-102. [8] S. Kacimi, J. Barbier Jr., R. Taha, D. Duprez, Catal. Lett., 22 (1993) 343-350. [9] Lj. Kundakovic, M. Flytzani-Stephanopoulos, Appl. Catal. A: Gen., 171 (1998) 13-29. [10] J. Xiaoyuan, L. Guanglie, Z. Renxian, M. Jianxin, C. Yu, Z. Xiaoming, Appl. Surf. Sci., 173 (2001) 208-220. [11] M. Luo, Y. Zhong, X. Yuan, X. Zheng, Appl. Catal. A: Gen., 162 (1997) 121-131. [12] P. Ratnasamy, D. Srinivas, C. Satyanarayana, P. Manikandan, R. Senthil Kumaran, M. Sachin, V. Shetti, J. Catal., 221 (2004) 455-465. [13] N. Bion, F. Epron, M. Moreno, F. Mariño, D. Duprez, Top. Catal. 51, (2008) 76-88. [14] Z. Liu, R. Zhou, X. Zheng, J. Molec. Catal. A, 267 (2007) 137-142. [15] A. Martínez-Arias, A.B. Hungría, M. Fernández-García, J.C. Conesa, G. Munuera, J. Phys. Chem. B, 108 (2004) 17983-17991. [16] P. Bera, A. Hornés, A.L. Cámara, A. Martínez-Arias, Catal. Today, 155 (2010) 184191. [17] Y-Z. Chen, B-J. Liaw, H-C. Chen, International J. Hydrogen Energy, 31 (2006) 427435. [18] Z. Wu, H. Zhu, Z. Qin, H. Wang, J. Wang, Appl. Catal. B: Env., 98 (2010) 204-212. [19] E. Moretti, M. Lenarda, L. Storaro, A. Talon, T. Montanari, G. Busca, E. RodríguezCastellón, A. Jiménez-López, M. Turco, G. Bagnasco, R. Frattini, Appl. Catal. A: Gen., 335 (2008) 46-55. [20] K. Sirichaiprasert, S. Pongstabodee, A. Luengnaruemitchai, J. Chi. Int. Chem. Eng., 39 (2008) 597-607. 174 Capítulo 7 [21] I. Dobrosz-Gómez, I. Kocemba, J.M. Rynkowski, Appl. Catal. B: Env., 83 (2008) 240-255. [22] M. Thammachart, V. Meeyoo, T. Risksomboon, S. Osuwan, Catal. Today, 68 (2001) 53-61. [23] J. Silvestre-Albero, F. Coloma, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Appl. Catal. A: Gen., 304 (2006) 159-167. [24] H.S. Roh, H.S. Potdar, K.W. Jum, S.Y. Han, J.W. Kim, Catal. Lett., 93 (2004) 203-207. [25] M. Paulis, M. Martín, D.B. Soria, A. Díaz, J.A. Odriozola, M. Montes, Appl. Catal. A: Gen., 180 (1999) 411-420. [26] S.-H. Chai, H.-P. Wang, Y. Liang, B.-Q. Xu, J. Catal., 250 (2007) 342–349. [27] J. Li, G. Lu, K. Li, W. Wang, J. Li, G. Lu, K. Li, W. Wang, M. Casapu, A. Bernhard, D. Peitz, M. Mehring, M. Elsener, O. Kröcher, Appl. Catal. B: Env., 103 (2011) 79– 84. [28] I. Nowak, M. Ziolek, Chem. Rev., 99 (1999) 3603-3624. [29] F.A.C. Garcia, J.M.C. Silva, J.L. Macedo, J.A. Dias, S.C.L. Dias, G.N.R. Filho, Micropor. Mesopor. Mater., 113 (2008) 562-574. [30] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 58 (2005) 175-183. [31] A. Razeghi, A. Khodadadi, H. Ziaei-Azad, Y. Mortazavi, Chem. Eng. J., 164 (2010) 214-220. [32] C. Hu, Q. Zhu, Z. Jiang, Power Technol., 194 (2009) 109–114. [33] G. Águila, F. Gracia, P. Araya, Appl. Catal. A: Gen., 343 (2008) 16–24. [34] J. Guzman, S. Carrettin, J.C. Fierro-Gonzalez, Y. Hao, B.C. Gates, A. Corma, Angew. Chem. Int. Ed., 44 (2005) 4778-4781. [35] P. Fornasiero, G. Balducci, R. Di Monte, J. Kaspar, V. Sergo, G. Gubitosa, A. Ferrero, M. Graziani, J. Catal., 164 (1996) 173-183. [36] S. Ricote, G. Jacobs, M. Milling, Y. Ji, P.M. Patterson, B.H. Davis, Appl. Catal. A: Gen., 303 (2006) 35-47. [37] S. Xu, D. Sun, H. Liu, X. Wang, X. Yan, Catal. Commun., 12 (2011) 514-518. [38] A. Martinéz-Arias, D. Gamara, M. Fernández-García, A. Hornés, P. Bera, Zs. Koppány, Z. Schay, Catal. Today, 143 (2009) 211-217. [39] Z. Lendzion-Bielun, M.M. Bettahar, S. Monteverti, D. Moszynski, U. Narkiewicz, Catal. Lett., 134 (2010) 196-203. [40] H. Zou, S. Chen, Z. Liu, W. Lin, International J. Hydrogen Energy, 34 (2009) 93249333. 175 176 CAPÍTULO 8 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). Abstract. The effects of CO2 and H2O on the preferential CO oxidation in the presence of H2 (PROX) on M/0.7CeO2-0.3Nb2O5 (M = Pt, Au and Cu) catalysts have been investigated. It has been observed that each catalyst presents a different behaviour in the catalytic reaction depending on the gas composition. Furthermore, it was observed that, in the case of the simultaneous presence of both H2O and CO2, all the catalysts studied showed a decrease in the CO oxidation rate and in selectivity. 188 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). 1. Introducción. La mayor parte de los estudios sobre la reacción de oxidación preferencial de CO en presencia de H2 han sido realizados utilizando mezclas de gases compuestas por CO, O2, H2 y un componente inerte, He o N2 [1][2][3][4][5][6][7][8][9]. Sin embargo, este modelo no simula completamente las condiciones reales de un sistema de reformado, ya que además de los gases mencionados, hay una cierta cantidad de CO2 y H2O presente en la mezcla de alimentación. Por ejemplo, en el reformado de metanol [10], la concentración aproximada de la corriente de gases generada es de 25% de CO2 y 10-15% de H2O. Por lo tanto, es esencial investigar la influencia de estos gases en la reacción PROX. En catalizadores de platino, por ejemplo, debido a la elevada entalpía de adsorción de CO, la superficie metálica se cubre fácilmente con una capa de CO, que apenas queda afectada por la presencia de CO2 y de H2O en la corriente gaseosa. Así, el único efecto de estos gases se deriva de su adsorción en el soporte [3][11]. Caso contrario sucede con los catalizadores de Au, debido a que el CO se une solo débilmente a la superficie de este metal y, por lo tanto, el cubrimiento superficial por CO se ve alterado en gran medida por la presencia de H2O y de CO2, que también pueden adsorberse sobre la superficie del metal [12][13]. En este capítulo se estudiará la influencia de la presencia de CO2 y H2O, presentes en la corriente gaseosa de alimentación, sobre el comportamiento catalítico de catalizadores de platino, oro y cobre soportados sobre óxidos de cerio modificado con niobio (denominados Pt/0,7CeO2-0,3Nb2O5, Au/0,7CeO2-0,3Nb2O5 y Cu/0,7CeO2-0,3Nb2O5). 2. Experimental. 2.1. Preparación y caracterización de los catalizadores. En este estudio se han utilizado los catalizadores preparados y caracterizados en los Capítulos 5, 6 y 7 (Pt/0,7CeO2-0,3Nb2O5, Au/0,7CeO2-0,3Nb2O5 y Cu/0,7CeO2-0,3Nb2O5, respectivamente). 2.2. Ensayos catalíticos. El comportamiento catalítico de las muestras en la reacción de oxidación de CO se evaluó en experimentos de reacción a temperatura programada 178 Capítulo 8 (313–473 K) y a presión atmosférica, utilizando una mezcla de gases compuesta por 20% H2, 2% CO, 2% O2, 5% CO2, 5% H2O y balanceada con He. El procedimiento experimental se describió con detalle en el Capítulo 2. Antes de la determinación del comportamiento catalítico, los catalizadores se redujeron in situ a 473 K (en el caso del catalizador de Au) y a 523 K (en el caso del catalizador de Pt) durante 1 h en flujo de H2 (50 ml·min-1). El catalizador de cobre no fue reducido. Los productos de reacción obtenidos fueron analizados por cromatografía de gases. Los cálculos de conversión de CO y O2 y de selectividad hacia CO2 han sido descritos en el Capítulo 2. 3. Resultados y discusión. 3.1. Comportamiento catalítico. Para facilitar la comparación del comportamiento catalítico de los diferentes catalizadores, la composición de la corriente de reacción se modificó de tres formas diferentes: (i) adicionando sólo CO2, (ii) adicionado sólo H2O, y (iii) adicionando ambos compuestos, CO2 y H2O, simultáneamente. Con el fin de comparar el efecto en los tres catalizadores, se han representado de forma separada, los perfiles de conversión de CO y de selectividad a CO2, en cada una de las condiciones de alimentación. Estos perfiles se presentan en la Figura 8.1, Figura 8.2 y Figura 8.3, en función de la temperatura de reacción, para los catalizadores Pt/0,7CeO2-0,3Nb2O5, Au/0,7CeO2-0,3Nb2O5 y Cu/0,7CeO2-0,3Nb2O5 respectivamente, con distinta composición en la corriente de alimentación: (i) sin la adición de CO2 y H2O (modelo ideal), (ii) con CO2, (iii) con H2O, (iv) con CO2 y H2O. 179 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). 100 (a) Conversión de CO, % 80 60 40 Modelo ideal CO2 20 H2O CO2 y H2O 0 300 320 340 360 380 400 420 440 460 Temperatura, K 100 (b) Modelo ideal CO2 H2O Selectividad a CO2, % 80 CO2 y H2O 60 40 20 0 300 320 340 360 380 400 420 440 460 Temperatura, K Figura 8.1. Variación de la conversión de CO (a) y selectividad a CO2 (b) en función de la temperatura para el catalizador Pt/0,7CeO2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). 180 Capítulo 8 100 (a) Conversion de CO, % 80 60 40 Modelo ideal CO2 20 H2O 0 300 CO2 y H2O 320 340 360 380 400 420 440 460 Temperatura, K 100 Modelo ideal CO2 (b) H2O 80 Selectividad a CO2, % CO2 y H2O 60 40 20 0 300 320 340 360 380 400 420 440 460 Temperatura, K Figura 8.2. Variación de la conversión de CO (a) y selectividad (b) en función de la temperatura para el catalizador Au/0,7CeO2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). 181 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). 100 (a) Conversión de CO, % 80 60 40 Modelo ideal CO2 20 H2O 0 300 CO2 y H2O 320 340 360 380 400 420 440 460 Temperatura, K 100 (b) Selectividad a CO2, % 80 60 40 Modelo ideal CO2 20 H2O 0 300 CO2 y H2O 320 340 360 380 400 420 440 460 Temperatura, K Figura 8.3. Variación de la conversión de CO (a) y selectividad (b) en función de la temperatura para el catalizador Cu/0,7CeO2-0,3Nb2O5 estudiado bajo diferentes condiciones de reacción: corriente de alimentación sin CO2 y H2O (modelo ideal – negro), con CO2 (rojo), con H2O (azul) y con H2O y CO2 (verde). 182 Capítulo 8 3.1.1. Efecto de la adición de CO2 en la actividad catalítica. Los resultados de conversión de CO en función de la temperatura se muestran en la Figura 8.1. En ella se observa la influencia de la composición de la corriente de gas de alimentación sobre la actividad catalítica de la muestra Pt/0,7CeO2-0,3Nb2O5. Como se puede apreciar, la adición de CO2 genera una ligera mejoría en la actividad catalítica a bajas temperaturas, aunque también una mayor disminución a temperaturas más elevadas. Paralelamente, se puede apreciar una ligera disminución de la selectividad. Este mismo comportamiento ha sido observado por Ayastuy y col. [1] para catalizadores de Pt soportados en CeZrO. Según estos autores, la presencia de CO2 parece afectar el mecanismo de reacción probablemente a través de la modificación de la distribución de los productos adsorbidos sobre el platino. Además, a temperaturas bajas el efecto de envenenamiento de CO se ve claramente reducido, lo que justifica el ligero aumento en la actividad catalítica. No obstante, también se ha encontrado en la literatura que la presencia de CO 2 en el flujo inhibe la oxidación de CO en catalizadores Pt/CeO 2, debido a la formación de carbonatos superficiales sobre el óxido de cerio que desactivan sus propiedades redox [2]. Como se puede observar en la Figura 8.1, la presencia de CO2 ejerce un mayor efecto (y beneficial) sobre la oxidación de hidrógeno, de tal forma que la selectividad hacia el CO2 disminuye. Para los catalizadores Au/0,7CeO2-0,3Nb2O5 y Cu/0,7CeO2-0,3Nb2O5, cuyo comportamiento se presenta en la Figura 8.2 y Figura 8.3, respectivamente, se observa una disminución de la conversión de CO y de la selectividad con la adición de CO2. Este efecto negativo puede deberse a la adsorción competitiva de CO (e H2) y CO2 en la superficie del catalizador. En la literatura se han encontrado resultados similares para diferentes catalizadores de oro y cobre [3][4][5][6][7][8][9]. Zou y col. [6] han estudiado la conversión de CO sobre catalizadores CuZrCeO utilizando DRIFTs, y han observado que el CO2 presente en la corriente de reacción bloquea los sitios de adsorción de CO e H2, de tal forma que la capacidad de conversión de CO disminuye. Monyanon y col. [7] estudiaron catalizadores de oro y oro-platino soportados sobre óxido de cerio, y encontraron que la disminución de la actividad catalítica está relacionada con la formación de grupos carbonato sobre la superficie del catalizador. Además, también puede producirse la reacción inversa de desplazamiento del gas de agua. Mariño y col. [10] también han propuesto que la disminución en la conversión de CO y en la selectividad tras la adición de CO2 puede estar relacionada con la adsorción competitiva de CO 2 en sitios activos de cobre y/o a la inhibición de la movilidad del oxígeno por la 183 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). formación de carbonatos superficiales en el soporte de óxido de cerio. Gamarra y col. [12] también observaron, utilizando operando-DRIFTs, que la desactivación de los catalizadores de CuO-CeO2 causada por la presencia de CO2 en el gas de alimentación está relacionada con la formación de carbonatos superficiales y, como consecuencia de ello, la disminución de la interfase redox del catalizador. 3.1.2. Efecto de la adición de H2O sobre la actividad catalítica. La adición de agua en la corriente de alimentación afecta de forma diferente a cada uno de los tres catalizadores estudiados. En el caso del catalizador Pt/0,7CeO2-0,3Nb2O5, Figura 8.1, se puede observar que la presencia de agua afecta muy poco a la actividad catalítica, produciendo apenas una pequeña mejora en la misma. Esto puede indicar que, de alguna forma, la presencia de grupos -OH en la superficie del soporte favorece la actividad catalítica. Estos resultados están de acuerdo con los obtenidos en el estudio de la reacción por DRIFTs (Capítulo 5), que ponían de manifiesto la influencia de la presencia de grupos hidroxilos superficiales en la reacción de oxidación de CO. Parinyasawan y col. [14] encontraron la misma tendencia en relación al aumento de la actividad catalítica en catalizadores de PdPt/CeO2. Sin embargo, Ayastuy y col. [1] evaluaron la actividad catalítica de Pt/CeZrO2 y observaron que la presencia de agua hace disminuir la actividad catalítica a bajas temperaturas, aunque a temperaturas más elevadas casi no afecta la actividad. Además, observaron que sólo se obtenía un efecto positivo en la reacción para una composición determinada del óxido mixto (50:50). El catalizador Au/0,7CeO2-0,3Nb2O5 se comporta de manera muy similar al catalizador de platino a temperaturas elevadas. Sin embargo, a bajas temperaturas se aprecia una caída en la actividad catalítica, acompañada de una mejora en la selectividad, Figura 8.2. Este resultado está de acuerdo con los presentados por Avgouropoulos y col. [4]. Se han realizado diferentes estudios sobre el efecto del agua en la oxidación de CO sobre catalizadores de oro. Por ejemplo, Daté y col. [13] han estudiado catalizadores de oro soportados en diferentes materiales, y han observado que la presencia de humedad afecta a la actividad catalítica, con una fuerte dependencia de la concentración de agua y del soporte. Además se ha propuesto que el agua interviene en la reacción a través de la activación del oxígeno y favoreciendo la descomposición de carbonatos. Estos carbonatos, formados durante la reacción, pueden recubrir los sitios activos en la interfase metal-soporte y desactivar el catalizador. Haruta y col. [15] han observado un aumento en la conversión de CO con la introducción de agua en catalizadores Au/Fe 2O3. Boccuzzi y col. [16] 184 Capítulo 8 también han notado una mejora en el comportamiento catalítico de catalizadores Au/TiO2 a bajas temperaturas, mientras que Bollinger y col. [17] han reportado que la presencia de agua perjudica la actividad catalítica para el mismo catalizador. Grisel y col. [18], estudiando catalizadores de Au/Al 2O3 y Au/MOx/Al2O3 (M = Mg y Mn) han observado un efecto negativo para la oxidación de CO con la presencia de agua en el sistema para catalizadores de Au/MnOx/Al2O3, y han justificado que este efecto está relacionado con el envenenamiento de las vacantes de oxígeno del MnOx. Según estos autores, todos los catalizadores estudiados presentan el mismo efecto en cuanto a disminución de la conversión de CO, una vez que el agua bloquea los sitios de adsorción de monóxido de carbono en el oro. Sin embargo, se ha observado una mejora en la actividad catalítica para catalizadores que contienen óxido de magnesio. Este efecto puede estar relacionado con una segunda reacción donde grupos -OH del MgO proporcionan el oxígeno necesario para la oxidación de CO. Para el catalizador de Cu/0,7CeO2-0,3Nb2O5, Figura 8.3, se observa una importante disminución de la actividad catalítica con la presencia de agua en el sistema. Esta desactivación puede estar relacionada con un bloqueo de los sitios activos superficiales por moléculas de agua, lo que limita el acceso de las moléculas reactivas a la superficie del catalizador [7][12][19]. Parket y col. [8] han propuesto que la presencia de agua bloquea los sitios activos de los catalizadores de CuO–CeO2/Al2O3 a bajas temperaturas. 3.1.3. Efecto de la adición de CO2 y H2O en la actividad catalítica. En el caso de la adición simultánea de CO2 y H2O a la corriente de alimentación, se puede apreciar el efecto negativo de estos dos compuestos en la actividad catalítica, independiente del catalizador utilizado. Esta observación se debe probablemente a su adsorción competitiva sobre los sitios activos. Es interesante destacar que la disminución de la actividad catalítica que presentan los catalizadores de Pt y Au es similar a la que se produce cuando se añade solamente CO2. Es decir, que el agua no afecta negativamente la actividad catalítica en presencia de CO2. Sin embargo, en el caso del catalizador de Cu, como ha sido mencionado anteriormente, la adición simultánea de CO2 y H2O sí afecta negativamente a la reacción, siendo este efecto mucho más pronunciado que en el caso de la adición de los compuestos por separado. Este comportamiento ha sido observado también por otros autores [4][7][8][14][20][21][22]. 185 Influencia del CO2 y del H2O en la oxidación preferencial de CO sobre catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). Ayastuy y col. [2] estudiaron catalizadores de Pt/CeO2 y observaron que la actividad se ve muy afectada por la presencia tanto de CO2 como de H2O en el sistema, y este efecto depende de la temperatura utilizada. A bajas temperaturas la actividad catalítica disminuye; sin embargo, a temperaturas más elevadas este efecto es insignificante. Njagi y col. [23] han observado una disminución de la actividad catalítica en catalizadores de óxido de cobre y manganeso a temperaturas inferiores a 323 K por la adsorción de estos gases en los sitios activos. Sin embargo, a temperaturas más elevadas, superiores a 348 K, este efecto se torna menos pronunciado debido a que la temperatura favorece la desorción de CO2 y de H2O. Monyanon y col. [7] también encontraron un efecto negativo de la presencia de CO2 y H2O en la actividad, principalmente a bajas temperaturas. Este hecho está fuertemente relacionado con la presencia de carbonatos y de vapor de agua que compiten con el CO por los sitios activos. Wu y col. [21] han atribuido la disminución de la conversión de CO en catalizadores de óxido de cobre a la adsorción competitiva entre CO y CO2 en la superficie del catalizador y al bloqueo superficial por las moléculas de agua adsorbida en los sitios activos. Finalmente, Gamarra y col. [12] han propuesto que el efecto negativo del CO2 se debe a la formación de carbonatos, y el del agua al bloqueo de sitios activos por moléculas de agua adsorbidas. 4. Conclusión. En este capítulo se estudió la influencia de la presencia de CO2 y/o H2O en la corriente de alimentación del proceso PROX en catalizadores M/0,7CeO2-0,3Nb2O5 (M= Pt, Au y Cu). Los resultados obtenidos han demostrado que la actividad catalítica se ve afectada por la presencia de cada uno de estos compuestos. De manera general, en condiciones más reales de reacción (en presencia de CO2 y de H2O) se puede observar que la conversión de CO se ve afectada negativamente. El efecto de la desactivación debido a la presencia de agua y de CO2 en la corriente de alimentación está principalmente relacionado con un bloqueo de los sitios activos superficiales por estas dos moléculas, lo que limita el acceso de las moléculas reactivas a los sitios activos para la reacción. 5. Referencias. [1] J.L. Ayastuy, M.P. González-Marcos, A. Gil-Rodríguez, J.R. González-Velasco, M.A. Gutiérrez-Ortiz, Catal. Today, 116 (2006) 391-399. [2] J.L. Ayastuy, A. Gil-Rodríguez, M.P. González-Marcos, M.A. Gutiérrez-Ortiz, International J. Hydrogen Energy, 31 (2006) 2231 – 2242. 186 Capítulo 8 [3] M.M. Schubert, A. Venugopal, M.J. Kahlich, V. Plzak, R.J. Behm, J.Catal., 222 (2004) 32-40. [4] G. Avgouropoulos, M. Manzoli, F. Boccuzzi, T. Tabakova, J. Papavasiliou, T. Ioannides, V. Idakiev, J. Catal., 256 (2008) 237-247. [5] E. Moretti, M. Lenarda, L. Storaro, A. Talon, T. Montanari, G. Busca, E. RodríguezCastellón, A. Jiménez-López, M. Turco, G. Bagnasco, R. Frattini, Appl. Catal. A: Gen., 335 (2008) 46-55. [6] H. Zou, S. Chen, Z. Liu, W. Lin, International J. Hydrogen Energy, 34 (2009) 93249333. [7] S. Monyanon, S. Pongstabodee, A. Luengnaruemitchai, J. Power Sources, 163 (2006) 547-554. [8] J.W. Park, J.H. Jeong, W.L. Yoon, Y.W. Rhee, J. Power Sources, 132 (2004) 18-28. [9] O.H. Laguna, E.M. Ngassaa, S. Oraá, A. Álvarez, M.I. Domínguez, F. RomeroSarria, G. Arzamendi, L.M. Gandía, M.A. Centeno, J.A. Odriozola, Catal. Today, 180 (2012) 105-110. [10] F. Mariño, C. Descorme, D. Duprez, Appl. Catal. B: Env., 58 (2005) 175-183. [11] M.M. Schubert, M.J. Kahlich, H.A. Gasteiger, R.J. Behm, J. Power Sources, 84 (1999) 175–182. [12] D. Gamarra, A. Martínez-Arias, J. Catal., 263 (2009) 189–195. [13] M. Daté, M. Okumura, S. Tsubota, M. Haruta, Angew. Chem. Int. Ed., 43 (2004) 2129-2132. [14] A. Parinyasawan, S. Pongstabodee, A. Luengnaruemitchai, International J. Hydrogen Energy, 31(2006) 1942-1949. [15] M. Haruta, A. Ueda, S. Tsubota, R.M. Torres Sanchez, Catal. Today, 29 (1996) 443447. [16] F. Boccuzzi, A. Chiorino, J. Phys. Chem. B, 104 (2000) 5414-5416. [17] M.A. Bollinger, M.A. Vannice, Appl. Catal. B: Env., 8 (1996) 417-443. [18] R.J.H. Grisel, B.E. Nieuwenhuys, J. Catal., 199 (2001) 48-59. [19] M. Daté, M. Haruta, J. Catal., 201 (2001) 221-224. [20] Y-Z Chen, B.-J Liaw, H-C. Chen, International J. Hydrogen Energy, 31 (2006) 427435. [21] Z. Wu, H. Zhu, H. Wang, L. Huang, J. Wang, Appl. Catal. B: Env., 98 (2010) 204212. [22] G. Avgouropoulos, T. Ioannides, H.K. Matralis, J. Batista, S. Hocevar, Catal. Lett., 73 (2001) 33-39. [23] E.C. Njagi, H.C. Genuino, C.K. Kingondu, C. Chen, D. Horvath, S.L. Suib, International J. Hydrogen Energy, 36 (2011) 6768-6779. 187 188 CAPÍTULO 9 Conclusiones generales. 192 Conclusiones generales. En este trabajo de investigación se ha analizado el efecto que ejerce la fase activa, la naturaleza del precursor metálico, la naturaleza del soporte, la influencia de la proporción de diferentes dopantes, y la influencia de la composición de los gases de alimentación, en el proceso de oxidación preferencial de CO en presencia de hidrógeno (PROX). Como resultado de este estudio se han obtenido las siguientes conclusiones generales: La primera variable estudiada ha sido la influencia de diferentes precursores de platino, con presencia o ausencia de cloro, en catalizadores Pt/CeO2 para la reacción PROX. Con los resultados obtenidos ha sido posible concluir que el catalizador libre de cloro presenta mejores resultados en cuanto a la oxidación de CO a bajas temperaturas. Además, se propone un posible mecanismo de reacción. A temperaturas superiores a 373 K la oxidación de CO ocurre con el mismo mecanismo en ambos catalizadores, es decir, la reacción tiene lugar en la interfase metal-soporte, entre CO adsorbido sobre el metal y oxígeno proporcionado por el soporte, según el mecanismo del Mars-Krevelen. Sin embargo, a temperaturas inferiores a 373 K se propone un mecanismo de reacción diferente para el catalizador libre de cloro, el cual parece estar relacionado con la participación de grupos -OH superficiales en el soporte. En una segunda etapa se ha estudiado una serie de catalizadores de platino soportado sobre óxido de cerio dopado con itrio. Se observa que, la presencia de Y (III) facilita la reducción del Ce (IV) y consecuentemente, la movilidad y el suministro de oxígeno en el soporte. Adicionalmente, se ha apreciado la presencia de grupos carbonato más estables en la superficie de estos catalizadores. Este hecho se traduce en una baja actividad catalítica, principalmente para elevadas proporciones de itrio. Además, los resultados obtenidos por DRX y Raman indican la posibilidad de formación de un óxido mixto. En una tercera etapa se ha realizado el estudio de la influencia de la adición de niobio en el óxido de cerio como soporte de catalizadores de platino. Para esto se ha preparado una serie de catalizadores con diferentes proporciones cerio/niobio. Se ha observado que la adición de niobio favorece la reducción del óxido de cerio. Además, los resultados de PROX indicaron que los catalizadores que utilizan estos materiales mixtos como soporte son más activos y selectivos que los soportados en óxido de cerio puro. Este hecho puede estar relacionado con la débil adsorción del CO en 190 Capítulo 9 el soporte, hecho que está de acuerdo con los resultados obtenidos por DTP. En una cuarta etapa se ha preparado catalizadores de oro soportados sobre CeO2, 0,7CeO2-0,3Nb2O5 y 0,7CeO2-0,3Y2O3. Los datos de RTP concluyeron que la adición del oro favorece la reducibilidad de los soportes, aunque este efecto es menos acentuado en el catalizador dopado con itrio. Los resultados de actividad catalítica indican que la conversión de CO depende fuertemente de la concentración de oxígeno en el gas de alimentación, de forma que, elevadas concentraciones de oxígeno favorecen la conversión de CO. Sin embargo, este incremento va asociado, desafortunadamente, a un descenso en la selectividad, es decir, corrientes ricas en oxígeno también favorecen la oxidación de hidrógeno a agua. Además, el catalizador Au/0,7CeO2-0,3Nb2O5 presenta mejores resultados para la conversión de CO que el catalizador Au/0,7CeO2-0,3Y2O3. Este hecho está relacionado con el tamaño de partícula de oro en los diferentes catalizadores. También se han estudiado catalizadores de cobre soportado sobre una serie de óxidos de cerio dopados con niobio. Se observa, en primer lugar, que la actividad catalítica es independiente del contenido en cobre de los catalizadores, hecho que motivó el uso de una baja carga de cobre (4% en peso). Finalmente, se observa que el comportamiento catalítico es independiente de la presencia de niobio en el soporte. Finalmente, se ha estudiado la influencia de la presencia de CO2 y/o H2O en la corriente de alimentación, usando catalizadores M/0,7CeO2-0,3Nb2O5 (M = Pt, Au y Cu). Los resultados obtenidos demuestran que la actividad catalítica se ve afectada por la presencia de estos compuestos, de tal forma que disminuye la conversión de CO. El efecto de desactivación debido a la presencia de agua y de CO2 en la alimentación está relacionado principalmente con un bloqueo superficial inducido por estos, lo que limita el acceso de las moléculas reactivas a la superficie del catalizador y, por ende, a los sitios activos. 191 192 CURRICULUM VITAE Curriculum Vitae Erika de Oliveira Jardim nació el 23 de Octubre de 1981 en Belo Horizonte – Minas Gerais, Brasil. Se graduó en Química en 2005 en la Universidade Federal de Minas Gerais, Brasil. En 2007 obtuvo el Título de Máster en Química Inorgánica, Modificação química de rejeitos de poliestireno para produção de materiais com aplicação tecnológica, en la misma universidad. Ha realizado su tesis doctoral en el programa de Ciencias de Materiales en la Universidad de Alicante, España. También realizó estancias en diferentes países como Uruguay, Portugal y Escocia donde desarrolló diferentes temas en el área ambiental. Lista de publicaciones. Artículos. O.S.G.P. Soares, E.O. Jardim, A. Reyes-Carmona, J. Ruiz-Martínez, J. SilvestreAlbero, E. Rodríguez-Castellon, J.J.M. Órfão, A. Sepúlveda-Escribano, M.F.R. Pereira, Effect of support and pre-treatment conditions on Pt–Sn catalysts: Application to nitrate reduction in water. Journal of Colloid and Interface Science, 369 (2012) 294-301. E.O. Jardim, S. Rico-Francés, M. Gonçalves, A. Sepúlveda-Escribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Study of Pt nanotubes carbon catalysts to CO oxidation process (PROX) in H2 presence. Applied Catalysis B: Environmental, 113-114 (2011) 72-78. M. Gonçalves, L. Sánchez-García, E.O. Jardim, J. Silvestre-Albero, F. Rodríguez-Reinoso, Ammonia removal using activated carbons: Effect of the surface chemistry in dry and moist conditions. Environmental Science & Technology, 45 (2011) 10605-10610. 194 J. Vernimmen, M. Guidotti, J. Silvestre-Albero, E.O. Jardim, M. Myrjam, O. Lebedev, G.V. Tendeloo, R. Psaro, F. Rodríguez-Reinoso, V. Meynen, P. Cool, Immersion calorimetry as a tool to evaluate the catalytic performance of titanosilicate materials in the epoxidation of cyclohexene. Langmuir, 27 (2011) 3618-3625. C.V. Grossa, E.O. Jardim, M.J. Silva, M.H. Araujo, R.M. Lago, A Catalyst with acid and superabsorvent properties for the esterification of fatty acids. Fuel, 89 (2010) 257-259. A. Silvestre-Albero, E.O. Jardim, E. Bruijn, V. Meynen, P. Cool, A. SepúlvedaEscribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Is there any microporosity in ordered mesoporous silicas? Langmuir, 25 (2009) 939-943. M.G. Rosmaninho, E.O. Jardim, F.C.C. Moura, G.L. Ferreira, V. Thom, M.I. Yoshida, M.H. Araujo, R.M. Lago, Hidrólise parcial da superfície do PET: Transformando um rejeito em um material de troca catiônica para aplicação ambiental. Química Nova, 32 (2009) 1673-1676. M.G. Rosmaninho, E.O. Jardim, F.C.C. Moura, G.L. Ferreira, V. Thom, M.I. Yoshida, M.H. Araujo, R.M. Lago, Surface hydrolysis of post-consumer PET to produce absorbents for cationic contaminants. Journal of Applied Polymer Science, 102(6) (2006) 5284-5291. Patente depositada. E.O. Jardim, S. Botrel, M.H. Araujo, R.M. Lago, Processo de produção de uma resina superabsorvente a partir de poliestireno, (2007) CTIT, Universidade Federal de Minas Gerais. Participación en congresos. E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Effect of Nb doping in the catalytic behaviour of Pt/CeO 2 195 catalysts in the selective CO oxidation reaction (PROX).V Jornadas Científicas del Instituto Universitario de Materiales (2012) Alicante - España. E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Efecto de la química superficial de nanotubos de carbono sobre el comportamiento de catalizadores de Pt en la reacción PROX. XI Reunión Grupo Español del Carbón (2011) Badajoz - España. J. Vernimmen, M. Guidotti, J. Silvestre-Albero, E.O. Jardim, V. Meynen, R. Psaro, F. Rodríguez-Reinoso, P. Cool, Immersion calorimetry as a powerful tool to evaluate titanosilicate catalysts in the epoxidation of cyclohexene. 4th International Symposium Advanced Micro- and Mesoporous Materials (2011) Riviera - Bulgaria. J. Vernimmen, M. Guidotti, J. Silvestre-Albero, E.O. Jardim, V. Meynen, R. Psaro, F. Rodríguez-Reinoso, P. Cool, Immersion calorimetry as a powerful tool to evaluate titanosilicate catalysts in the epoxidation of cyclohexene. 5th International FEZA Conference (2011) Valencia - España. E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Catalizadores de CuO soportados sobre CeO2 dopado para la reacción de oxidación selectiva de CO. Sociedad Española de Catálisis SECAT (2011) Zaragoza - España. E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Effect of Nb doping in the catalytic behaviour of Pt/CeO2 catalysts in the selective CO oxidation reaction (PROX). Europacat (2011) Glasgow - Escocia. R. Buitrago-Sierra, E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Effect of Nb doping in the catalytic behaviour of Pt/CeO2 catalysts in the WGS reaction. Europacat (2011) Glasgow - Escocia. 196 E.O. Jardim, S. Rico-Francés, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Estudio de la oxidación selectiva de CO en catalizadores de Pt y Au soportados sobre CeO2. V Jornadas Científicas de Instituto Universitario de Materiales (2011) Alicante - España. J. Vernimmen, M. Guidotti, J. Silvestre-Albero, E.O. Jardim, V. Meynen, R. Psaro, F. Rodríguez-Reinoso, P. Cool, Synthesis of Ti-containing combined micro- and mesopourous materials for the catalystic epoxidation of ciclohexene. 2nd International Conference of Nanostructured Multifunctional Materials – NMM (2010) Iasi - Romania. J. Vernimmen, M. Guidotti, J. Silvestre-Albero, E.O. Jardim, V. Meynen, R. Psaro, F. Rodríguez-Reinoso, P. Cool, Immersion calorimetry as a powerful tool to evaluate titanosilicate catalysts in the epoxidation of cyclohexene. 1st International Workshop of the European Nanoporous Materials Institute of Excellence – ENMIX (2010) Antwerp - Bélgica. J. Silvestre-Albero, E.O. Jardim, A. Sepúlveda-Escribano, G. Rupprechter, Catalizadores Pd/Al2O3 en la reacción de hidrogenación selectiva de 1,3butadieno: Efecto de la presencia de Sn. Congreso Iberoamericano de Catálisis – XXII CICAT (2010) Viña del Mar - Chile. E.O. Jardim, J.A. Anderson, J. Silvestre-Albero, A. Sepúlveda-Escribano, F. Rodríguez-Reinoso, Estudio de la influencia del precursor de platino en catalizadores de Pt/CeO2 para la reacción de oxidación de CO en presencia de H2. Congreso Iberoamericano de Catalisis – XXII CICAT (2010) Viña del Mar Chile. E.O. Jardim, A. Silvestre-Albero, E. Bruijn, V. Meynen, P. Cool, A. SepúlvedaEscribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Presence or absence of microporosity in ordered mesoporous silicas. 16th International Zeolite Conference joint with the 7th International Mesostructured Materials Symposium – IZC-IMMS (2010) Sorrento - Italia. 197 O.S.G.P. Soares, E.O. Jardim, J. Ruiz-Martínez, A. Sepúlveda-Escribano, J. Silvestre-Albero, J.J.M. Orfão, M.F.R. Pereira, Pt-Sn catalyst for nitrate reduction in water: effect of the support. Carbons for Energy Storage and Environmental Protection – CESEP (2009) Torremolinos - España. E.O. Jardim, M. Gonçalves, A. Sepúlveda-Escribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Estudio de catalizadores de Pt soportados en nanotubos de carbón para el proceso PROX. Nuevas Fronteras de la Catálisis – SECAT (2009) Ciudad Real - España. E.O. Jardim, A. Silvestre-Albero, E. Bruijn, V. Meynen, P. Cool; A. SepúlvedaEscribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Is there any microporosity in ordered mesoporous silicas? 1st International Workshop Nanoporous Materials in Energy and Environment – NAPEN (2008) Creta Grecia. E.O. Jardim, R.A.V. Rios, A. Sepúlveda-Escribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, D.P. Heinrich, S. Rezai, J. Weitkamp, Study of the hydrophobicity in actived carbons. 1st International Workshop Nanoporous Materials in Energy and Environment – NAPEN (2008) Creta - Grecia. E.O. Jardim, A. Silvestre-Albero, E. Bruijn, V. Meynen, P. Cool, A. SepúlvedaEscribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, Estudio de la presencia o ausencia de microporosidad en materiales ordenados de silicio. XXXIII Reunión Ibérica de Adsorción (2008) Móstoles - España. E.O. Jardim, R.A.V. Rios, A. Sepúlveda-Escribano, J. Silvestre-Albero, F. Rodríguez-Reinoso, D.P. Heinrich, S. Rezai, J. Weitkamp, Estudio del carácter hidrófobo de diferentes carbones activados. XXXIII Reunión Ibérica de Adsorción (2008) Móstoles - España. C.G. Vieira, A.L. Cardoso, L.C.A. Barbosa, M.J. Silva, R.M. Lago, E.O. Jardim, Aplicação do isopor reticulado como catalisador heterogêneo em reações de 198 esterificação do ácido oléico para produção de biodisel. Congreso - XXI The Ibero-American Symposium of Catalysis – SICAT (2008) Málaga - España. F. Magalhães, R. Lago, E.O. Jardim, N.T. Mogliazza, S.E.E. Botrel, J.D. Fabris, Compósitos carvão/óxidos de ferro produzidos a partir de Fe2O3 e alcatrão para a oxidação catalítica de contaminantes orgânicos com H 2O2. 14º Congresso Brasileiro de Catalises (2007) Porto de Galinhas - Brasil. E.O. Jardim, R.C. Lois, M.G. Rosmaninho, M.H. Araújo, R.M. Lago, Superabsorvente à base de poliestireno sulfonado reticulado: estudo do efeito do pH e salinidade na capacidade de absorção. 30ª Reunião Anual da Sociedade Brasileira de Química (2007) Águas de Lindóia – Brasil. E.O. Jardim, R.C. Lois, M.G. Rosmaninho, M.H Araújo, M.I. Yokhida, R.M. Lago, Uma nova proposta para o mecanismo de hidrólise do PET. Semana de Iniciação Científica (2005) Belo Horizonte – Brasil. E.O. Jardim, R.C. Lois, M.G. Rosmaninho, M.H. Araújo, M.I. Yokhida, R.M. Lago, Uma nova proposta para o mecanismo de hidrólise do PET. 28ª Reunião Anual da Sociedade Brasileira de Química (2005) Poços de Caldas – Brasil. J.A.D. Silva, E.O. Jardim, A.L.R.P. Júnior, E.N. dos Santos, M.H Araújo, R.C. Nunes, Síntese e caracterização de novos ligantes de bis-carbenos tridentados. 28ª Reunião Anual da Sociedade Brasileira de Química (2005) Poços de Caldas – Brasil. E.O. Jardim, E.G. Neves, M.G. Rosmaninho, M.H. Araújo, M.I. Yokhida, R.M. Lago, Adsorção de espécies catiônicas no poli(etileno tereftalato) – PET parcialmente hidrolisado. 17ª Encontro Regional da Sociedade Brasileira de Química (2004) Lavras – Brasil. 199 E.O. Jardim, C.L. Donnici, G.C. Azzellini, Síntese de precursores dendriméricos 2,2’-bipiridínicos substituídos. Semana de Iniciação Científica (2004) Belo Horizonte – Brasil. 200 Esta Memoria de Tesis Doctoral muestra el comportamiento de catalizadores de metales de transición soportados sobre óxidos parcialmente reducibles en la reacción de oxidación preferencial de CO en presencia de hidrógeno (PROX). Se ha analizado (i) la influencia del precursor metálico (utilizando dos precursores de platino: presencia o ausencia de cloro), (ii) el efecto de la fase activa (utilizando diferentes metales como el platino, oro y cobre), (iii) la naturaleza del soporte (óxido de cerio másico y óxido de cerio dopado con itrio ó niobio), (iv) el efecto de la porcentaje de dopante en el soporte y (v) el método de impregnación empleado en la preparación de los catalizadores sobre la actividad catalítica. Finalmente, se ha evaluado la influencia de la composición del gas de entrada, así como la presencia paralela de CO2 y H2O, simulando condiciones reales de gases de salida en procesos de reformado. Erika de Oliveira Jardim Laboratorio de Materiales Avanzados Departamento de Química Inorgánica Universidad de Alicante, Aptdo. 99 San Vicente del Raspeig, E-03080 Alicante, España E-mail: [email protected]