Fórmulas y PROPIEDADES COLIGATIVAS
Anuncio
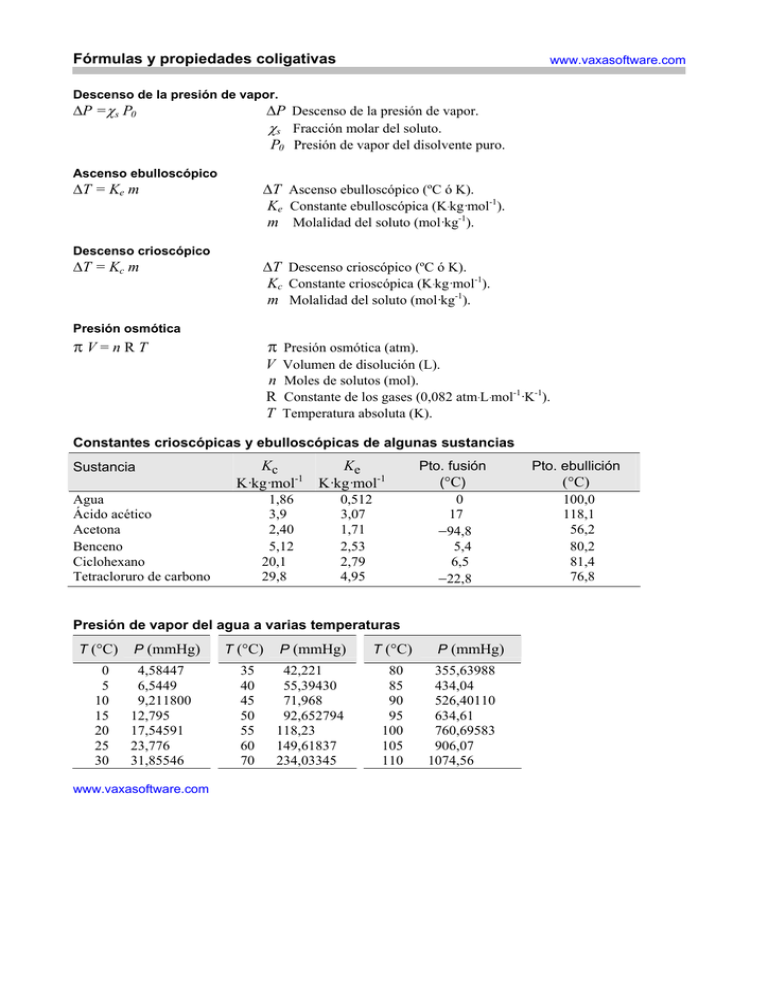
Fórmulas y propiedades coligativas www.vaxasoftware.com Descenso de la presión de vapor. ∆P =χs P0 ∆P Descenso de la presión de vapor. χs Fracción molar del soluto. P0 Presión de vapor del disolvente puro. Ascenso ebulloscópico ∆T = Ke m ∆T Ascenso ebulloscópico (ºC ó K). Ke Constante ebulloscópica (K·kg·mol-1). m Molalidad del soluto (mol·kg-1). Descenso crioscópico ∆T = Kc m ∆T Descenso crioscópico (ºC ó K). Kc Constante crioscópica (K·kg·mol-1). m Molalidad del soluto (mol·kg-1). Presión osmótica πV=nRT π V n R T Presión osmótica (atm). Volumen de disolución (L). Moles de solutos (mol). Constante de los gases (0,082 atm·L·mol-1·K-1). Temperatura absoluta (K). Constantes crioscópicas y ebulloscópicas de algunas sustancias Sustancia Kc Ke -1 K·kg·mol K·kg·mol-1 Agua Ácido acético Acetona Benceno Ciclohexano Tetracloruro de carbono 1,86 3,9 2,40 5,12 20,1 29,8 0,512 3,07 1,71 2,53 2,79 4,95 Pto. fusión (°C) 0 17 −94,8 5,4 6,5 −22,8 Presión de vapor del agua a varias temperaturas T (°C) 0 5 10 15 20 25 30 P (mmHg) 4,58447 6,5449 9,211800 12,795 17,54591 23,776 31,85546 www.vaxasoftware.com T (°C) P (mmHg) T (°C) 35 40 45 50 55 60 70 42,221 55,39430 71,968 92,652794 118,23 149,61837 234,03345 80 85 90 95 100 105 110 P (mmHg) 355,63988 434,04 526,40110 634,61 760,69583 906,07 1074,56 Pto. ebullición (°C) 100,0 118,1 56,2 80,2 81,4 76,8