EJERCICIOS REPASO UNIDAD 4 - Departamento de Física y Química
Anuncio
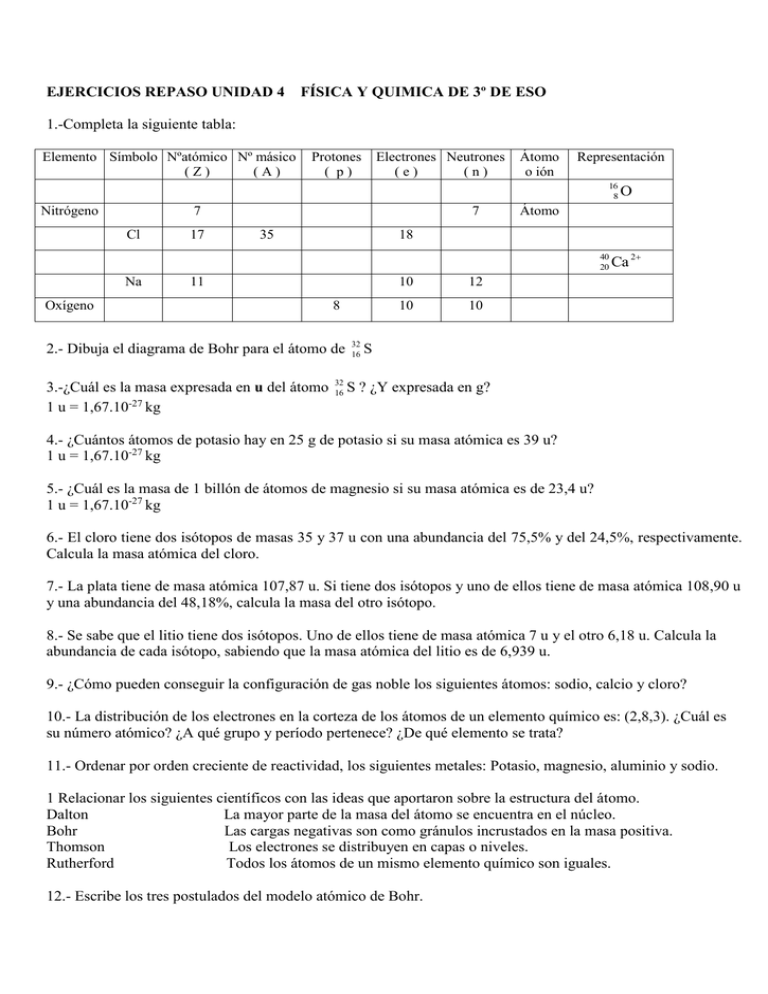
EJERCICIOS REPASO UNIDAD 4 FÍSICA Y QUIMICA DE 3º DE ESO 1.-Completa la siguiente tabla: Elemento Símbolo Nºatómico Nº másico (Z) (A) Protones ( p) Electrones Neutrones (e) (n) Átomo o ión Representación 16 8 Nitrógeno 7 Cl 17 7 35 Átomo 18 40 20 Na 11 Oxígeno 8 2.- Dibuja el diagrama de Bohr para el átomo de 3.-¿Cuál es la masa expresada en u del átomo 1 u = 1,67.10-27 kg O 32 16 32 16 10 12 10 10 Ca 2 S S ? ¿Y expresada en g? 4.- ¿Cuántos átomos de potasio hay en 25 g de potasio si su masa atómica es 39 u? 1 u = 1,67.10-27 kg 5.- ¿Cuál es la masa de 1 billón de átomos de magnesio si su masa atómica es de 23,4 u? 1 u = 1,67.10-27 kg 6.- El cloro tiene dos isótopos de masas 35 y 37 u con una abundancia del 75,5% y del 24,5%, respectivamente. Calcula la masa atómica del cloro. 7.- La plata tiene de masa atómica 107,87 u. Si tiene dos isótopos y uno de ellos tiene de masa atómica 108,90 u y una abundancia del 48,18%, calcula la masa del otro isótopo. 8.- Se sabe que el litio tiene dos isótopos. Uno de ellos tiene de masa atómica 7 u y el otro 6,18 u. Calcula la abundancia de cada isótopo, sabiendo que la masa atómica del litio es de 6,939 u. 9.- ¿Cómo pueden conseguir la configuración de gas noble los siguientes átomos: sodio, calcio y cloro? 10.- La distribución de los electrones en la corteza de los átomos de un elemento químico es: (2,8,3). ¿Cuál es su número atómico? ¿A qué grupo y período pertenece? ¿De qué elemento se trata? 11.- Ordenar por orden creciente de reactividad, los siguientes metales: Potasio, magnesio, aluminio y sodio. 1 Relacionar los siguientes científicos con las ideas que aportaron sobre la estructura del átomo. Dalton La mayor parte de la masa del átomo se encuentra en el núcleo. Bohr Las cargas negativas son como gránulos incrustados en la masa positiva. Thomson Los electrones se distribuyen en capas o niveles. Rutherford Todos los átomos de un mismo elemento químico son iguales. 12.- Escribe los tres postulados del modelo atómico de Bohr.











