En este género encontramos un ... visto con anterioridad: los esporulados. Básicamente tienen las características siguientes:
Anuncio

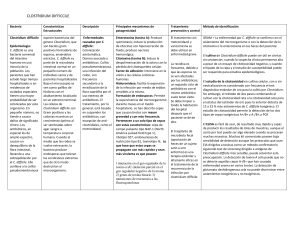
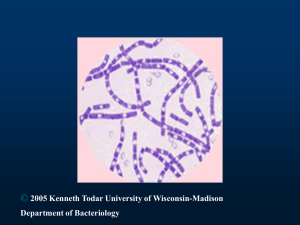
SEMANA 7 TEORÍA TEMAS 8 Y 9 A. BACILOS ESPORULADOS: Bacillus y Clostridium B. Corynebacterium y Mycoplasma GÉNERO: Clostridium. En este género encontramos un tipo morfolólogico de bacterias que no hemos visto con anterioridad: los esporulados. Básicamente tienen las características siguientes: Son muy resistentes al medio ambiente, debido a esporas que forman parte de su estructura. Al bacilo, que es mucho más vulnerable al ambiente y tiene la conformación típica de un Gram-negativo, se le llama forma vegetativa. La espora o esporas dentro del cuerpo bacteriano o fuera de él Las formas vegetativas pueden degradarse, no obstante las esporas pueden permanecer semanas o meses hasta que una corriente de aire, una mala cocción de alimentos, la inhalación de aerosolores o que sus toxinas hagan contacto con un hospedero sano, inicien los diversos cuadros clínicos. La posición de las esporas es importante en la diferenciación de especie: las hay TERMINALES, ubicadas completamente al final del bacilo, SUBTERMINALES, ubicadas antes de llegar al final del citoplasma de la bacteria, y en algunas especies raramente son visibles. Esto lo muestra la figura 1 y la figura 2 que se adjuntan a continuación. El género Clostridium está formado por un grupo heterogéneo de bacilos Grampositivos anaerobios esporulados. Está ampliamente distribuido en la naturaleza, principalmente en el suelo y en el tracto intestinal de muchas especies animales incluido el hombre, y puede causar infecciones de origen exógeno y de origen endógeno. En la actualidad se han descrito más de 150 especies, aunque sólo alrededor de 30 han sido asociadas con infección humana, siendo Clostridium perfringens la especie más frecuente. Muchas especies del género Clostridium tienen capacidad de producir potentes exotoxinas que son las responsables de ocasionar graves cuadros tóxicos. Clostridium perfringens puede elaborar una gran variedad de ellas (11 histotoxinas y 1 enterotoxina, la CPE) y, dependiendo de la producción de las cuatro toxinas principales, la especie se divide en cinco tipos (Tabla 1). 1 Figura 1. Bacterias esporuladas Gram-positivas. (Clostridium y Bacillus) Observe en el extremo inferior izquierdo un esporulado con espora Subterminal (i.e. C. botulinum, C. histolyticum, C. septicum). El resto son clostridios que han exoesporulado e incluso poseen flagelos peritricos. 2 Figura 2 Observe en la parte inferior, clostridios con esporas Terminales (i.e. C. difficile, C. tetani, C. cadaveris). Igualmente a la figura anterior, algunas poseen flagelos peritricos y otras no poseen ningún flagelo. Clostridium botulimun Por antonomasia, el botulismo es la enfermedad que usualmente se asocia con intoxicación alimentaria, y también es la más importante debido a su alta mortalidad. La toxina botulínica es una neurotoxina que provoca un cuadro de parálisis flácida, que lleva a la muerte por fallo respiratorio al afectar los músculos involucrados en la respiración, la cual provoca distensión de los sarcómeros que no se recuperan, lo que origina la parálisis flácida. Para imaginar la potencia de la toxina, basta la descripción de un brote en un restaurante italiano, relacionado con berenjenas enlatadas. Una de las pacientes intoxicadas fue una mesera que se comió un emparedado, para cuya preparación pinchó con un tenedor una rebanada de esa berenjena enlatada, pero decidió no ponerla en su emparedado y la devolvió a la lata, y con ese mismo tenedor terminó de colocar los ingredientes; la cantidad de toxina impregnada en el tenedor fue suficiente para que ella enfermera. La dosis letal es de 0.006 ng, suficiente para ser considerada como arma biológica. 3 ¿Por qué no hay registrados casos de botulismo en Costa Rica? 1. Posiblemente porque en él no es frecuente la preparación de enlatado. 2. Algunos han quedado sin diagnóstico etioiógico y se pueden haber catalogados como síndrome de muerte súbita o muerte en la cama. 3. En Costa Rica no tenemos las cuatro estaciones marcadas y el botulismo se asocia con alimentos envasados en las casas, que es donde se registran más casos. El reservorio de los clostridios es el suelo en muchas ocasiones, especialmente de C. botulinum. Ahora bien, ¿Cómo llega al envasado? 1. Clostridium botulinum es habitante normal del suelo, y llega a los alimentos, especialmente vegetales, por contaminación con tierra. 2. Sigue el proceso de escaldado que se hace a esos alimentos para eliminar las bacterias no esporuladas, o sea, la posible competencia. Este es un Punto Crítico de Control. 3. Una vez cerrado, el ambiente queda anaerobio, ideal para la bacteria. La incidencia será más alta en países donde se acostumbra almacenar alimentos en la casa, donde se dan inviernos drásticos. 4. TRATAMIENTO: Se basa en seroterapia (inmunidad artificial) semejante a la usada contra venenos de serpientes. El antídoto es la administración de Acs prefabricados anti-A, B, E los más importantes epitopos de la toxina botulínica. Cabe recordar que una vez que el paciente entra en muerte neurológica ninguna seroterapia le devuelve la vida. Clostridium perfringens 1. Sinónimo: Enteritis necrótica. 2. Signos y síntomas: Trastorno intestinal caracterizado por la aparición repentina de cólicos, seguidos de diarrea. La náusea es común. Por lo general no hay fiebre ni vómitos. 3. Bacteriología: C. perfringens es uno de los patógenos bacterianos más ampliamente distribuidos en el medio ambiente. Puede ser aislado de muestras de suelo y de agua y forma parte de la biota indígena intestinal de animales y humanos. Sin embargo, C. perfringens puede en ciertas ocasiones comportarse como un patógeno oportunista. En la actualidad, la toxinotipificación es el método más difundido de clasificación de C. perfringens. Este método tipifica a la bacteria en cinco tipos (A, B, C, D y E) según la producción de las toxinas alfa, beta, épsilon y iota (Tabla 1). 4. La toxina alfa (una fosfolipasa C, y una lecitinasa) juega un papel primordial en la patogenia de la gangrena gaseosa, la toxina beta de C. perfringens tipo C está implicada en la enteritis necrótica y la enterotoxina CPE de C. perfringens tipo A en las intoxicaciones alimentarias. Esto cuadros tóxicos, en general bien caracterizados, son principalmente infecciones exógenas. Pueden afectar a cualquier órgano o sistema, pero sobre todo a aquellos cercanos a las superficies mucosas, donde son parte abundante de 4 la biota comensal. Asimismo, se trata frecuentemente de infecciones mixtas en donde estos microorganismos se encuentran junto a otras bacterias anaerobias o facultativas. Su gravedad es, en general, la misma que la de otras infecciones polimicrobianas (sinergismo bacteriano), pero puede variar dependiendo de una serie de factores, provocando desde cuadros en donde su presencia es de dudosa significación a gravísimos cuadros de mionecrosis y de bacteriemias y septicemias con shock. Tabla 1. Clasificación de C. perfringens basada en la producción de toxinas: Celulitis crepitante Se trata de una infección que afecta, característicamente, a los tejidos subcutáneos o retroperitoneales; el músculo no está envuelto en una extensión significativa y permanece viable. Los hallazgos en el lugar de la infección incluyen crepitación a la palpación por la presencia de gas, a menudo más abundante que en la mionecrosis, dolor mínimo, edema, ligera decoloración de la piel y exudado oscuro, frecuentemente maloliente, que en la tinción de Gram suele mostrar células bacterianas típicas y abundantes neutrófilos. Generalmente, aparece después de un traumatismo, con un periodo de incubación de 3 días o más y con mínima toxicidad, aunque raramente puede evolucionar a un cuadro sistémico y fulminante, principalmente en inmunosupresos. Gangrena gaseosa Esta infección surge principalmente después de un traumatismo, bien como complicación de una herida penetrante y extensa, usualmente en una extremidad y con gran afectación de la masa muscular, o bien como complicación de una cirugía, principalmente de colon o tracto biliar, o después de un aborto séptico, parto u otra manipulación obstétrica. El traumatismo introduce al microorganismo, en su forma vegetativa o sus esporas, en los tejidos profundos y produce un ambiente anaerobio que favorece el crecimiento de éste y la producción de sus toxinas. La presencia de una enfermedad de base, como la diabetes, en el paciente es un factor favorecedor de la infección. La gangrena gaseosa se presenta con un curso rápidamente progresivo y devastador, caracterizado por una necrosis muscular y una grave toxicidad sistémica, con taquicardia, fiebre de bajo grado y una extrema ansiedad. El comienzo es brusco, con un fuerte dolor en el lugar del trauma que, al principio, puede presentarse sin otros síntomas locales. La enfermedad progresa rápidamente y, en minutos u horas, se puede observar alrededor de la herida una piel edematosa y con una palidez marmórea que puede ir cambiando a color bronce, seguido por la aparición de bulas hemorrágicas y enfisema subcutáneo. Puede producirse un espeso exudado marrón, serosanguinolento, con un característico olor dulzón distinto del olor 5 pútrido de otras infecciones anaeróbicas. Se suele observar gas por palpación, radiografía o escáner, aunque la crepitación puede ser un signo tardío. El diagnóstico temprano de la gangrena gaseosa es crítico, y se basa en los hallazgos clínicos, quirúrgicos y microbiológicos. Desde el punto de vista microbiológico, es muy importante el examen e informe urgente de la tinción de Gram de las muestras, en donde típicamente se observan numerosos bacilos Gram-positivos y escasos o ausentes leucocitos, por la acción de toxinas leucolíticas. Clostridium perfringens es el responsable del 80% de los casos de gangrena gaseosa postraumática. En agar sangre, producen un típico halo de doble hemólisis, una interna de hemólisis completa (ß-hemólisis) debida a la toxina theta y otra externa, más grande, de hemólisis incompleta (α-hemólisis) debida a la toxina alfa, en menos de 24 horas de incubación. Clostridium difficile. La toxina A de Clostridium difficile (TcdA) es generada por la bacteria junto con la toxina B y ambas constituyen los principales factores de virulencia producidos de dicha especie. Las toxinas actúan dañando la mucosa intestinal y causando los síntomas de la infección por Clostridium difficile, incluyendo la colitis pseudomembranosa. La TcdA es una de las más grandes toxinas bacterianas conocidas. Con un peso molecular de 308 kDa, es usualmente descrita como una potente enterotoxina, pero también tiene actividad citotóxica. La toxina actúa modificando proteínas del hospedero por la vía de la glicosilación, conduciendo a cambios en la actividad celular. El factor de riesgo para Clostridium difficile incluye un tratamiento con antibióticos que interfiera con las funciones beneficiosas de la biota indígena al hospedero y permita la colonización desmesurada de Clostridium difficile. Patogénesis de la diarrea asociada a Clostridium difficile (CDAD) La TcdA incluye diarrea, infiltración de neutrófilos, inflamación de la mucosa intestinal y necrosis de las células epiteliales. La TcdA daña las vellosidades intestinales y erosiona el borde en cepillo, causando erosión y salida de fluidos en el área dañada. Este daño causa la diarrea asociada. Patogénesis de la Colitis Pseudomembranosa (PMC) La TcdA puede inducir cambios que ocasionan una severa ulceración del colon. La toxina daña la mucosa colónica promoviendo la acumulación de fibrina y mucina, y las células muertas forman una capa de detritos en el colon a la cual la llamamos pseudomembrana. Esto va a causar una respuesta inflamatoria. El daño provocado por la TcdA causa: Aumento de la permeabilidad epitelial, producción de citoquinas, infiltrado de neutrófilos. Producción de especies reactivas al oxígeno (ROS). Degranulación de los mastocitos y daño directo a la mucosa. Al dañarse la mucosa, las uniones entre células se pierden y entran neutrófilos al intestino, que corresponde a un hecho específico de la PMC. Las toxinas A y B pueden inducir la llamada de más macrófagos, neutrófilos y degranulación de mastocitos, pero estos mediadores van a dañar más la mucosa y las bacterias van a entrar a circulación a causar un choque séptico y muerte. 6 GÉNERO: Bacillus. A. Bacillus cereus. Se ha asociado frecuentemente con arroz cocido que se ha guardado a temperatura ambiente, lo que podría relacionarse con contaminación con esporas del ambiente (posiblemente polvo) que germinan en ese alimente y producen la toxina. Pueden generarse dos tipos de cuadros clínicos, una leve diarrea, no son frecuente los vómitos, y el otro cuadro puede ser dolor de cabeza con náuseas, sin fiebre. B. Bacillus anthracis. 1. Sinónimos: Ántrax, pústula maligna, edema maligno, enfermedad de los cardadores de lana, enfermedad de los traperos. Afecta cabras, animales cubiertos de pelo o lana, trabajadores agrícolas, entre otros. 2. Enfermedad bacteriana aguda que por lo general ataca la piel, pero rara vez afecta el mediastino o las vías intestinales. En el carbunco cutáneo aparece primeramente prurito en la piel expuesta, seguido de una lesión que se vuelve papular, vesicular y en dos a seis días termina por ser una escara negra, lo rodea edema mínimo, moderado, a veces con pequeñas vesículas secundarias. Las infecciones no tratadas se diseminan a ganglios, luego a circulación y con ello aparecer septicemia o meningitis. Los síntomas iniciales por inhalación son mínimos e inespecíficos y en tres a cinco días aparecen los síntomas agudos de insuficiencia respiratoria, signos radiológicos de ensanchamiento mediastínico, fiebre y coque, y luego la muerte. El carbunco intestinal es raro y más difícil de identificar, excepto que tiende a manifestarse en brotes explosivos; el malestar abdominal es seguido de fiebre, septicemia y la muerte en el caso típico. 3. Tratamiento farmacológico: penicilina es el tratamiento preferido por 5 – 7 días. También son eficaces las tetraciclinas, la eritromicina y el cloranfenicol. 4. Ejemplos de lesiones cutáneas por ántrax: 7 GÉNERO: Corynebacterium. 1. La enfermedad se inicia con fiebre de 38ª a 39ºC, infección aguda en las amígdalas, faringe, laringe, la nariz y la mucosa respiratoria, la conjuntiva y las heridas abiertas de la mucosa bucal. Se producen los signos clásicos de la inflamación, se inflaman los ganglios y hay lesiones con una o varias placas membranosas grisáceas en el paladar blando que dejan una superficie con sangre al removerlas. 2. Es producida por Corynebacterium diphteriae o bacilo de Klebs-Loeffler. Se localiza en la nariz, la garganta y conjuntivas por el contacto directo con gotitas de saliva al hablar, toser, o estornudar. Generalmente ocurre en la infancia, de un niño a otro, o de una mascota que funcione como reservorio a otro hospedero sano. La letalidad es baja, entre un 5 a un 10%. 3. Diagnósticos diferenciales: faringitis bacteriana o viral, angina de Vincent, mononucleosis infecciosa, sífilis y candidiasis de la boca. GÉNERO: Mycoplasma. 1. Especie prototipo: Mycoplasma pneumoniae. (Causante de neumonía atípica primaria) 2. La principal característica como género es que son incapaces de formar una pared celular y por lo tanto sólo tienen membrana citoplasmática y se tiñen como Gram-negativas. Esta les confiere otras características: a) Pueden asumir diferentes formas, desde esferas a filamentos. b) Pueden atravesar filtros que retienen a las bacterias comunes. c) Se hinchan y explotan en medios que de repente se llenan de agua. d) Como la penicilina inhibe la pared celular, no se inhiben por altas concentraciones de penicilina, pero sí por otros antibióticos como eritromicina y tetraciclina. 3. Es una enfermedad febril de las vías respiratorias inferiores, con menor frecuencia hay faringitis, evoluciona a bronquitis hasta neumonía. El comienzo es gradual, con cefalalgia, malestar general, tos (a menudo paroxística) y por lo regular dolor subesternal (no 8 pleurítico). El esputo es escaso pero puede aumentar después. La infiltración pulmonar temprana en forma dispersa e irregular es más extensa en la radiografía de lo que sugieren los signos clínicos. La enfermedad varía desde una faringitis afebril hasta una enfermedad febril que afecta las vías respiratorias superiores o inferiores. 4. Laboratorio: En la tercera parte de los casos surge leucocitosis después de la primera semana; aumento de la VES; el título de crioaglutininas va acorde con la gravedad del caso, Inmunoensayo por Mycoplasma pneumoniae, cultivo en Agar Mycoplasma u otro específico. 9