Subido por
Carlos Andres Morales Flores
Diagramas de Equilibrio Hierro-Carbono: Ingeniería de Materiales
Anuncio

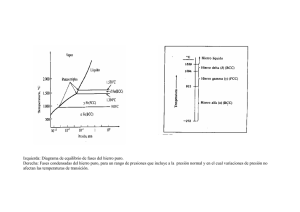
INGENIERIA DE MATERIALES Diagramas de Equilibrio Diagrama Hierro Carbono fases Aleación metálica: material que tiene propiedades metálicas que esta formado por varios elementos Ej. Acero al carbono ( Fe y C ) , Ac inox ( Fe, C , Cr , Ni) Fase porción físicamente homogénea: 1.La misma estructura o arreglo atómico 2.La misma composición aprox. 3.Una interfaz definida entre esta y las que la rodean. f ases a) Las tres formas del agua b) Agua y alcohol solubilidad ilimitada c) Agua y sal solubilidad limitada d) Aceite y agua prácticamente insolubles soluciones y solubilidad Solución química = soluto + solvente ( liquidas o sólidas ) Solubilidad es la cantidad de material o componente que se puede disolver sin formar una nueva fase. Solubilidad total > independiente de las cantidades Condiciones para solubilidad total reglas de Hume-Rothery 1. Atomos o iones ttamaño semejante ( radio atómico no mas 15% ) 2. Igual estructura cristalina 3. Los iones deben tener igual valencia 4. Las electronegatividades deben ser similares De no ocurrir 3 y 4 se forman compuestos Compuesto químico > composición fija soluciones y solubilidad Solubilidad limitada En determinados sistemas la solubilidad es limitada como ocurre por ejemplo en el caso de la salmuera Otro caso similar ocurre entre el Cu y el Zn en que la solubilidad aumenta con la temperatura solubilidad y soluciones sólidas a) El Cu y Ni líquidos son totalmente solubles entre sí b) Las aleaciones sólidas CuNi tienen solubilidad total y los átomos ocupan sitios aleatorios c) En las aleac. Cu-Zn con mas de 30% de Zn aparece una segunda fase debido a la solubilidad limitada del Zn en el Cu enfriamiento del hierro puro regla de la palanca A y B solubilidad total , x composición de la aleación w0 % de B en A , a temperatura T La recta LOS es una isoterma % de fase solida = % de fase liquida = w 0- wl ws - wl ws - wo ws - wl diagrama de fases binario con eutéctico Solubilidad total en estado liquido e insolubles en estado sólido Diagrama Pb-Sn Solubilidad sólida limitada y Punto eutéctico aceros transformación eutectoide α = Ferrita γ = Austenita perlita micro estructura Microestructura de un acero eutectoide enfriado lentamente. Perlita eutectoide , la fase oscura es cementita y la blanca ferrita Atacado con picral Aumento 650 x aceros transformación hipo eutectoide α = Ferrita γ = Austenita acero hipoeutectoide micro estructura Microestructura de un acero hipo eutectoide con 0,35% de C enfriado lentamente. El constituyente blanco es ferrita y el oscuro es perlita. Atacado con Nital Aumento 500 x aceros transformación hiper eutectoide α = Ferrita γ = Austenita acero hiper eutectoide micro estructura Microestructura de un acero hiper eutectoide con 1,2% de C enfriado lentamente. El constituyente blanco es cementita pro eutectoide que se formo en los limites de grano de la austenita y el resto es perlita laminar. Atacado con Picral Aumento 1000 x ddiagrama hierro grafito glosario Fase Solución y solubilidad Solución sólida Regla de la palanca Reglas de Hume Rothery Solidus – Liquidus - Solvus Eutéctico - Eutectodie Aleación hipo eutéctica Aleación hiper eutéctica Micro constituyente Acero Austenita Ferrita Cementita Perlita bibliografía recomendada Ciencia e Ingeniería de Materiales – Smith – Mc Graw Hills Ciencia e Ingeniería de los Materiales – Askeland – Thomson Ciencia e Ingeniería de los Materiales – Callister – Reverte