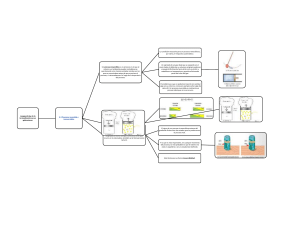
Sistema Sistema es la parte del universo observable o mundo físico que se somete a estudio. Son entidades macroscópicas con extensiones en el espacio y en el tiempo que están accesibles a los procesos normales de medición. Ejemplos típicos son un volumen de gas, un condensador, un líquido y su vapor, una disolución, un sólido cristalino. También es un sistema, objeto de estudio de la Termodinámica, un campo electromagnético. Medio ambiente Todo lo que está en el universo observable a excepción del sistema se denomina medio ambiente. Sistema Medio ambiente Superficie límite Lo que separa el sistema del medio ambiente se denomina superficie límite, envoltura o límite del sistema. De manera abstracta, diremos que los límites de un sistema son superficies matemáticas a las que dotamos de propiedades idealizadas, tales como rigidez e impermeabilidad. Los límites reales tienen propiedades aproximadas a las de los límites ideales termodinámicos. Tipos de sistemas en relacion a su limite Los sistemas en relación con el medio se clasifican en: a) abiertos, cuando tienen límites permeables al intercambio de materia con su medio ambiente; b) cerrados, cuando el intercambio puede ser sólo de energía, y c) aislados, cuando entre el sistema y el medio externo no existe interacción alguna. Variables termodinámicas Las variables termodinámicas, también denominadas “coordenadas”, son las magnitudes macroscópicas necesarias para la descripción del sistema. Para un sistema termodinámico consistente en un gas, un líquido o una mezcla de diferentes gases y líquidos, las variables termodinámicas son las masas de las distintas sustancias presentes, la presión, el volumen y la temperatura. Variables termodinámicas En un sistema en el cual se consideran superficies líquidas o películas, las variables correspondientes serían la tensión superficial, el área y la temperatura. El tratamiento termodinámico de un sistema magnético incluiría como variables la intensidad del campo magnético, la magnetización de la materia del sistema y la temperatura. En estos sistemas, además de la masa, se han dado solo tres variables, pudiendo haber más. La temperatura es la común a todos Estado de un sistema Se dice que el estado de un sistema está definido cuando se especifican todas las variables necesarias para describirlo. El estado de un sistema no da información sobre las transformaciones por medio de las cuales se llevó el sistema a ese estado. DEFINICIÓN GENERAL DE TRABAJO Es la transferencia de energía asociada con una fuerza que actúa a lo largo de una distancia. Si se tiene un cuerpo con cierta cantidad de masa (m) y se quiere desplazar desde una posición 1 hasta una posición 2, se aplica una fuerza F a lo largo de un desplazamiento, se dice entonces que se ha realizado una cierta cantidad de trabajo. DEFINICIÓN GENERAL DE TRABAJO dW = F * dx dW = F * dx Donde: F= es la fuerza aplicada en la misma dirección del desplazamiento. dx= indica la variación del desplazamiento dw= Cantidad de trabajo aplicado TRABAJO MECÁNICO DEFINICIÓN DE TRABAJO TERMODINÁMICO Se dice que un sistema efectúa trabajo cuando el único efecto externo al sistema pudiese ser el levantamiento de un peso. Es de suma importancia destacar que el trabajo se define como una interacción entre el sistema y sus alrededores. A un sistema no se le puede asignar un trabajo (no es algo que tenga un sistema) y por lo tanto no es una propiedad termodinámica. El trabajo también se define como una interacción de energía la cual no es causada por una diferencia de temperatura. CONVENCIÓN DE SIGNO La gran mayoría de los autores utilizan el siguiente convencionalismo: Trabajo realizado por un sistema se considera positivo (+). Trabajo realizado sobre el sistema se considera negativo (-). UNIDADES Como el trabajo se define como la fuerza que actúa a lo largo de un desplazamiento en la misma dirección de la fuerza. Sus unidades son de fuerza por desplazamiento. Las unidades mas comunes son: Sistema internacional: Joule = Newton x metro Sistema Inglés: Librafuerza x pie (también se usa con frecuencia la unidad “Btu”) UNIDADES Otras unidades: dina x cm. = 1 ergio Electrón voltio (ev): Trabajo requerido para mover un electrón a través de una diferencia de un voltio. 1 ev = 1,6 x 10-12 ergio = 1,18 x 10-19 lbfpie TRABAJO DE EXPANSIÓN Y COMPRESIÓN El Trabajo de frontera móvil para un proceso cuasi-equilibrio, es un proceso durante el cual el sistema permanece en equilibrio todo el tiempo. δW = Fext×dx TRABAJO DE EXPANSIÓN Y COMPRESIÓN Evaluando un gas encerrado en un cilindro émbolo sometido a un proceso de compresión. Fext : Fuerza externa que actúa en la interfaz comprimiendo el gas. dx: Desplazamiento causado por las comprensión Este desplazamiento se puede escribir en función de un volumen diferencial y el área del émbolo. TRABAJO DE EXPANSIÓN Y COMPRESIÓN TIPOS DE PROCESOS DE EXPANSIÓN Y COMPRESIÓN Para calcular el trabajo total requiere conocer la relación entre P y V durante el proceso. El área diferencial representa el trabajo realizado por el gas cuando el volumen varía una cantidad dv. El área completa representa el trabajo total realizado por el gas cuando este se expande de 1 a 2. PROCESO ISOMÉTRICO (gas Ideal) Proceso Isocórico o isométrico el volumen permanece constante y por lo tanto no se realiza trabajo. V1 = V2 PROCESO ISOBÁRICO Proceso en el cual la presión permanece constante. P1 = P2 PROCESO ISOTÉRMICO Para procesos isotérmicos, el trabajo de un sistema que cambia del volumen 1 al volumen viene dado por: 1 𝑊2 = 𝑃𝑑𝑉 = 𝑉2 𝑃𝑑𝑉 𝑉1 La variación de volumen respecto de la presión para gases ideales vienes dado por: 𝑃= 𝑛𝑅𝑇 𝑉 Reemplazamos en la integral 1 𝑊2 = 𝑉2 𝑉1 𝑛𝑅𝑇 𝑑𝑉 𝑉 V1 V2 PROCESO ISOTÉRMICO Resolviendo la integral 1 𝑊2 = 𝑉2 𝑉1 1 𝑊2 = 𝑛𝑅𝑇 1 𝑊2 𝑛𝑅𝑇 𝑑𝑉 𝑉 𝑉2 𝑉1 𝑑𝑉 𝑉 = 𝑛𝑅𝑇(ln 𝑉)𝑉2 𝑉1 ) 1 𝑊2 = 𝑛𝑅𝑇(ln 𝑉2 − ln 𝑉1 ) 𝑉2 ) 1 𝑊2 = 𝑛𝑅𝑇(ln 𝑉1 V1 V2 Expansión Reversible E Irreversible Suponemos al sistema como un cilindro que contiene un gas el cual mueve un objeto sobre la tapa Caso1. Proceso Irreversible Etapa 1 (expansión) Como vimos en la sección anterior para un proceso irreversible isotérmico (en una sola etapa) tenemos Wexp = - P (V2-V1) Suponiendo que P = Pop Etapa 2 (compresión) Para la compresión irreversible en una sola etapa, Wcomp = -P (V1-,V2) Suponiendo Pop=P Caso1. Proceso Irreversible El trabajo neto es la suma de estos dos procesos. Wciclo = - P2 (V2- V1) + P1(V1- V2) Wciclo = - (P2+ P1)(V2- V1) Esto da un trabajo negativo, es decir donde se destruye trabajo, el sistema ha regresado a su estado inicial pero, el entorno no. Se ha realizado trabajo en el entorno. Caso2. Proceso Reversible Etapa 1 expansión reversible isotérmico (en una infinidad de etapas) Para que un sistema sea completamente reversible se requiere de un tiempo infinito, por lo que los sistames reversibles son ideales Si suponemos Pop = P Wexp= - ∫P dV (de Vi a Vf) Caso2. Proceso Reversible Etapa 2 compresión reversible isotérmico. Wcomp=- ∫pdV (de Vf a Vi) Caso2. Proceso Reversible El trabajo total es: Wciclo = Wexp+ Wcomp = - ∫ViVfp dV - ∫VfVipdV Wciclo = - ∫ViVfp dV - ∫VfVip dV = 0 El sistema ha regresado a su estado inicial y el entorno también y no se ha realizado un trabajo neto. Y se dice que es un proceso reversible. Caso2. Proceso Reversible Etapa 1 expansión reversible isotérmico (en una infinidad de etapas) Para que un sistema sea completamente reversible se requiere de un tiempo infinito, por lo que los sistames reversibles son ideales Si suponemos Pop = P Wexp= - ∫P dV (de Vi a Vf) CONVENCIÓN DE SIGNO La gran mayoría de los autores utilizan el siguiente convencionalismo: Trabajo realizado por un sistema se considera positivo (+). Trabajo realizado sobre el sistema se considera negativo (-). CANTIDADES MÁXIMAS Y MÍNIMAS DE TRABAJO. Como dijimos anteriormente si el sistema realiza trabajo sobre los alrededores pierde energía debida al trabajo por lo que por convenio establecemos que w<0 Si el cambio de energía se debe solo al trabajo tenemos ΔU<0 U2−U1<0 U2<U1 CANTIDADES MÁXIMAS Y MÍNIMAS DE TRABAJO. Trabajo mínimo. Trabajo obtenido en un proceso isotérmico reversible donde el valor del cambio de energía interna es 0. Si ΔU=0 0=W+Q W=−Q Toda la energía que puede intercambiar el sistema en forma de calor se transforma en trabajo. Si además de isotérmico el proceso es reversible el trabajo obtenido será un mínimo posible. CANTIDADES MÁXIMAS Y MÍNIMAS DE TRABAJO. Trabajo Máximo. Para la compresión Pop debe ser ligeramente mayor que la presión del gas Pop = p + dp en cada etapa (proceso reversible). WM = - ∫ pdV W <WM −∑niPΔV<−∫V2V1PdV |W|>|WM| |−∑niPΔV|>|−∫V2V1PdV| Caso de la caída de agua. Nos damos cuenta que la intuición nos dice que el agua se desplaza desde una cota alta hasta una baja, pero espontáneamente no se puede devolver. Ahora, si nosotros colocásemos una rueda de agua en la cascada, lograríamos producir trabajo a partir del proceso Podemos ver como existen procesos que tienen una contrapartida que los devuelve a su estado original y otros que no lo tienen. Los primeros se denominan procesos reversibles y se definen como aquellos para los cuales se puede idear un proceso que devuelva al sistema y a sus alrededores a sus condiciones iniciales. Reversibilidad Tomemos como ejemplo la expansión al vacío de un gas: Reversibilidad Al romperse la membrana, el gas ocupará todo el volumen. Los alrededores no son alterados ya que no se ha hecho una expansión contra la atmósfera. El proceso es isotérmico sin transferencia de calor (suponiendo un comportamiento tipo gas ideal). Para volver al gas a su condición inicial se debe comprimir el sistema cilindro-pistón, y debido a que la compresión genera un aumento en la temperatura del gas, se debe retirar calor. Definición Termodinámica De Calor Es la energía que se transmite a través del límite de un sistema, en virtud de una diferencia de temperatura que existe con los alrededores. Cuando existe una diferencia de temperatura entre el sistema y su entorno, hay transferencia de energía como producto de los choques individuales de las moléculas del sistema con las de su entorno. Definición Termodinámica De Calor Si la frontera del sistema es rígida, la suma de estos trabajos microscópicos no pueden expresarse como una fuerza medida por un desplazamiento (trabajo). La suma de estos trabajos microscópico es esencialmente lo que denominamos calor. Calor es trabajo térmico a nivel microscópico. El calor no se almacena, la energía si. Tanto el calor como el trabajo son manifestaciones de energía en transito, por tal motivo solo la podemos observar a través de las fronteras de los sistemas.. Definición Termodinámica De Calor La variación de energía térmica Q que interviene en una variación de temperatura de un sistema de masa m es: Q = CΔT = mcΔT El calor específico varía ligeramente con la temperatura, aunque para la mayoría de las sustancias esta variación es despreciable. Calor latente Los cambios de fase en una sustancia son procesos que necesitan energía térmica, pero ocurren a temperatura constante. • Cuando la temperatura de un cuerpo aumenta por suministro de calor se origina un aumento de energía cinética por el movimiento de las moléculas. Cuando un material pasa de líquido a gaseoso las moléculas, que se mantenían en contacto, se alejan las unas de las otras. Esto requiere un trabajo contra las fuerzas de atracción, es decir, es necesario un suministro de energía para separar las moléculas, aunque no aumente su energía cinética (y por tanto, su temperatura) en el proceso. Calor latente Para sustancias puras los cambios de fase se dan a cualquier presión, pero a unas temperaturas determinadas. El agua pura cambia de sólido a líquido a 0ºC, y de líquido a gas a 100ºC. son los llamados puntos de fusión y ebullición. Para estas sustancias se requiere una cantidad de calor determinada para cambiar la fase de una cantidad dada de sustancia. El calor es proporcional a la masa de la sustancia: Q = mL Donde L es una constante característica de la sustancia y del cambio de fase en cuestión. Para agua a presión atmosférica Lf= 79,7 cal/g, y LV=540 cal/g. CONVENCIÓN DE SIGNO La mayoría de los autores utilizan el siguiente convencionalismo: Positivo (+), transmisión de calor a un sistema. Negativo (-), transmisión de calor desde un sistema (calor retirado del sistema). UNIDADES DE CALOR Kilocaloría, es la cantidad de calor transmitida para producir un cambio de temperatura de un Celsius (1 °C) a un kilogramo (1 kgm) de agua. BTU, Unidad Térmica Británica, la cantidad de energía requerida para incrementar la temperatura de una libramasa de agua (1 lbm) de agua un grado Fahrenheit (1°F). El calor total se denota con la letra Q; Ejemplo: 1Btu, 2 kcal UNIDADES DE CALOR El calor transferido por unidad de masa se denota con la letra q; Ejemplo: 1BTU/lbm, 1kcal/kgm El transferido por unidad de tiempo se denota con la letra, •Q También se utiliza cualquier otra unidad de energía como el Joule, ergios, Lbf*pie, etc MECANISMOS DE TRANSFERENCIA DE CALOR Conducción: es la transferencia de energía debida a las interacciones entre las partículas en el interior de un material. Q cond = -kt x A x dT/dx (Ley de Fourier) Convección: es la transferencia de energía entre la superficie de un sólido y un líquido o un gas debido al movimiento de un fluido. Qconv = h A (Ts – Tf) MECANISMOS DE TRANSFERENCIA DE CALOR Radiación: es la transferencia de energía mediante radiación electromagnética. La energía transferida por radiación puede emitirse desde una superficie o desde el interior de fluidos transparentes y sólidos. Comparación de Calor y trabajo Al igual que el calor, el trabajo es una interacción de energía entre un sistema y sus alrededores. La energía es capaz de cruzar la frontera de un sistema cerrado en forma de calor o de trabajo. En consecuencia, si la energía que cruza la frontera de un sistema cerrado no es calor, debe ser trabajo. Comparación de Calor y trabajo El trabajo es también una forma de energía como el calo r y, por lo tanto, tiene unidades de energía como kJ. El trabajo efectuado durante un proceso entre los estados 1 y 2 se denomina W12, o aún más simple W. Comparación de Calor y trabajo Una cantidad que se transfiere a o desde un sistema durante una interacción no es una propiedad puesto que la cantidad de dicha cualidad depende de algo más que un estado del sistema. El calor y la energía son mecanismos de transferencia de energía entre un sistema y sus alrededores y existen muchas similitudes entre ellas: Comparación de Calor y trabajo 1. Ambos se reconocen cuando cruzan las fronteras del sistema. Tanto a transferencia de calor como el trabajo son fenómenos de frontera. 2. Los sistemas poseen energía, pero no calor o trabajo. 3. Ambos se asocian con un proceso, no con un estado. A diferencia de las propiedades, ni el calor o el trabajo tienen significado en un estado. 4. Ambos son funciones de la trayectoria (sus magnitudes dependen de la trayectoria seguida durante un proceso, así como de los estados extremos).