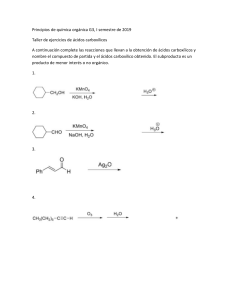
Taller de Química Orgánica: Ácidos, Ésteres, Aminas y Amidas
Anuncio
PARCIAL-TALLER NOMBRE: Mayling Janiris Castellanos Rozo. 1. Elabore un comparativo de las propiedades físicas y químicas de los ácidos carboxílicos, esteres, aminas y amidas. GRUPO FUNSIONAL Acidos Carboxilicos Esteres FORMULA GENERAL -CO2H R—COO—R' PROPIEDADES QUIMICAS PROPIEDADES FISICAS Son dependientes, cuyos cambios podrían originar los derivados de ácido. Son resistentes a la oxidación y a la reducción, pero el hidruro de litio y aluminio los reduce hasta los alcoholes. Según Bronsted, este grupo es ácido porque puede ceder un ion de hidrógeno. Los ácidos carboxílicos reaccionan rápidamente con soluciones acuosas de hidróxido de sodio y bicarbonato de sodio formando sales de sodio solubles. Para distinguir los ácidos carboxílicos insolubles en agua o solubles, se hacen pruebas de solubilidad en base acuosa. Los ácidos carboxílicos son moléculas con geometría trigonal plana. Presentan hidrógeno ácido en el grupo hidroxilo y se comportan como bases sobre el oxígeno carbonílico. Los puntos de fusión y ebullición son elevados ya que forman dímeros, debido a los enlaces por puentes de hidrógeno. En las reacciones de los ésteres, la cadena se rompe siempre en un enlace sencillo, ya sea entre el oxígeno y el alcohol o R, o entre el oxígeno y el grupo R-CO-, eliminando así el alcohol o uno de sus derivados. La saponificación de los ésteres, llamada así por su analogía con la formación de jabones, es la reacción inversa a la esterificación. Los ésteres se hidrogenan más fácilmente que los ácidos, empleándose generalmente el éster etílico tratado con Los ésteres pueden participar en los enlaces de hidrógeno como aceptadores, pero no como donadores. Esta capacidad de participar en los enlaces de hidrógeno les convierte en más hidrosolubles, pero las limitaciones de sus enlaces de hidrógeno los hace más hidrofóbicos. Esta falta de capacidad de actuar como donador de enlace de hidrógeno ocasiona que no puedan formar enlaces de hidrógeno entre Aminas Amidas RNH2 NHR o —NRR' una mezcla de sodio y alcohol moléculas de ésteres, lo que los hace más volátiles que un ácido o alcohol de similar peso molecular. Estas propiedades suelen ser muy similares a las del amoniaco, ya que al igual que éste las aminas son sustancias básicas; son aceptores de protones. Las aminas presentan reacciones de neutralización con los ácidos y forman sales de alquilamonio o sales de amina. . Las aminas son solubles en agua (aminas menores) y en solventes menos polares como éter, alcohol, benceno, etc. Las aminas tienen puntos de ebullición y de fusión más altos que los compuestos no polares de igual peso molecular, pero inferiores a los de alcoholes o ácidos carboxílicos. Casi todas las amidas son incoloras e inodoras. Los miembros inferiores de la serie son solubles en agua y en alcohol; la solubilidad en agua disminuye conforme aumenta la masa molar. El grupo amida es polar y, a diferencia de las aminas, las amidas son moléculas neutras. Todas las amidas, Presentan excelentes propiedades disolventes y son bases muy débiles, también éstas amidas excepto la primera de la serie, son sólidas a temperatura ambiente y sus puntos de ebullición son elevados, más altos que los de los ácidos correspondientes. 2. Realice un cuadro como el siguiente con todos los grupos funcionales vistos en clase en orden de prioridad descendente, indicar a que función química pertenecen, cual es la estructura química general para cada uno y la terminación característica para cada grupo (prefijos o sufijos, según sea el caso). -Grupos funcionales: alcanos, alquenos, alquinos, aromáticos, alcoholes, fenoles, éteres, aldehídos, cetonas, ácidos carboxílicos, esteres, aminas y amidas (este no es el orden, deben organizarlos). FUNCION QUIMICA OXIGENADA. La función quimica de los ácidos Carboxilicos básicamente vendría siendo la de oxidar el carbono primario que contiene tanto al carbonilo como al hidroxilo en sí mismo, estos se nombran anteponiendo la palabra ácidos y con el sufijo “oico”. OXIGENADA. Los ésteres al ser considerados un grupo funcional compuesto por un radical orgánico quien se encuentra unido al residuo de cualquier ácido oxigenado, orgánico o inorgánico. Los ésteres, en particular los acetatos de etilo y butilo, se utilizan como disolventes de nitrocelulosa y resinas en la industria de las lacas, así como materia prima para las GRUPO FUNCIONAL ESTRUCTURA QUIMICA TERMINACION EN NOMENCLATURA (IUPAC) PREFIJO SUFIJO Acidos Carboxilicos R–(C=O)–OH -oico Carboxi- Esteres R—COO—R' -ato Oxicarbonil- condensaciones de ésteres. NITROGENADA. Las amidas no sustituidas de los ácidos carboxílicos alifáticos se utilizan ampliamente como productos intermedios, estabilizantes, agentes de desmolde para plásticos, películas, surfactantes y fundentes. También las amidas se utilizan mucho en la síntesis de polímeros, como por ejemplo el nailon, que son poliamidas encadenadas y también poliuretanos. También se utilizan como herbicidas, repelentes de insectos y medicinas. OXIGENADA. Los aldehídos y las cetonas son funciones en segundo grado de oxidación. Se consideran derivados de un hidrocarburo por Amidas NHR o —NRR' -amida Aldehidos R–CHO -al Carbonoil- Formil- sustitución de dos átomos de hidrógeno en un mismo carbono por uno de oxígeno, dando lugar a un grupo oxo (=O). A veces los aldehídos aromáticos sirven como agentes saborizantes. OXIGENADA. Una cetona es un compuesto orgánico que tiene un grupo funcional carbonilo unido a dos átomos de carbono, a diferencia de un aldehído, en el que el grupo carbonilo se une a al menos un átomo de hidrógeno. Las cetonas y cetoácidos son combustibles alternativos para el cuerpo que se fabrican cuando hay escasez de suministro de glucosa. Se fabrican en el hígado de la descomposición de las grasas. Las cetonas se forman cuando no hay suficiente azúcar o glucosa para Cetonas R-CO-R´ -ona Oxo- alimentar las necesidades de combustible del cuerpo. OXIGENADA. La función alcohol se caracteriza por la presencia del hidroxilo OH, en sustitución de un hidrógeno en un átomo de carbono. Los alcoholes se utilizan como productos químicos intermedios y disolventes en las industrias de textiles, colorantes, productos químicos, detergentes, perfumes, alimentos, bebidas, cosméticos, pinturas y barnices. Algunos compuestos se utilizan también en la desnaturalización del alcohol, en productos de limpieza, aceites y tintas de secado rápido, anticongelantes, agentes espumígenos y en la flotación de minerales. Alcoholes ROH -ol Hidroxi- OXIGENADA. Las propiedades químicas mencionadas, hacen del Fenol un buen antioxidante, que actúa como un agente de captura de radicales. El Fenol sufre múltiples reacciones de substitución electrofílica, tales como Halogenación y sulfonación. También reacciona con compuestos carbonílico, tanto en medio ácido como básico. NITROGENADAS. Las aminas son compuestos orgánicos multifuncionales que derivan del amoníaco. Al igual que el amoníaco, las aminas son bases débiles y pueden neutralizar componentes ácidos y mantener el equilibrio del pH en una amplia variedad de productos y aplicaciones. Fenoles C6H6O -ol Aminas RNH2 -amina Hidroxi- Amino- OXIGENADA. El éter dietílico es un líquido incoloro de olor dulce. Se usa ampliamente como solvente y en la fabricación de otras substancias químicas. También se ha usado como anestésico. HIDROCARBUROS. En la actualidad, los principales usos de los compuestos aromáticos como productos puros son: la síntesis química de plásticos, caucho sintético, pinturas, pigmentos, explosivos, pesticidas, detergentes, perfumes y fármacos. HIDROCARBUROS. Los alquenos son hidrocarburos que contienen enlaces dobles carbonocarbono. Se emplea frecuentemente la palabra olefina como sinónimo. Los alquenos abundan en la naturaleza. El eteno, es un Eteres R-O-R´ -éter Aromaticos C6H6 -Orto -Meta -Para Alquenos CnH2n / H2C=CH2 -eno Alcoxi- compuesto que controla el crecimiento de las plantas, la germinación de las semillas y la maduración de los frutos. HIDROCARBUROS. Los alquinos son utilizados principalmente como combustibles, el alquino de mayor importancia comercial es el acetileno o etino. Que les permite cortar los metales y soldarlos. HIRDOCARBUROS. Los alcanos a partir del hexadecano en adelante constituyen los componentes más importantes del aceite combustible y aceite lubricante. La función de los últimos es la de actuar como agentes anticorrosivos, puesto que su naturaleza hidrofóbica implica que el agua no puede llegar a la superficie del metal. Alquinos CnH2n-2 / HC≡CH -ino CnH2n+2 / H3C–CH3 Alcanos -ano 3. Nombre los siguientes compuestos: A. Acido - 4 –metilpentanoico. B. Acido - 3 – oxociclohexanocarboxilico. C. Acido – 3 – eno – 5 – inohexanoico D. Acido - 2 - nitro benzoico E. Acido – 2 – fenilpropanoico F. 3 – oxo – pent - 4 – enoato de metilo G. Ácido butano dioico H. 6 – oxociclo hept – 3 – eno carboxilato de metilo I. Metanoato de Isopropilo J. 4 - bromo - 3 – hidroxibutanoato de metilo K. Acido - 2 – amino propanoico L. Metil [5 – (metil amino) pentil] amino M. Metano tricarboxamida N. 2 - carbamoil propanoato de metilo O. N - etil – N – metil benzamida P. N - etil propanamida Q. Ciclopentano carboxamida R. Acido – 4 – carbamoil bencenocarboxilico. 4. Dibuje la estructura de los siguientes compuestos a. Ácido ciclohexanodicarboxílico j. Ácido 3-carbamoílciclohexanocarboxílico b. Acido 2-hexen-4-inoico c. Ácido heptano dioico k. Ciclohexa-1,3-dieno-1,2-diamina l. trifenilamina d. Benzoato de t-butilo m. N,N-dimetil-4-ciclohexenamina e. Ácido 3-ciclohexenocarboxílico n. N,N-dimetil-3-hexanamina f. Ácido 2-hidroxi-3-oxohexanoico o. N,N-Dibencilpropanamida g. 3-Oxobutanoato de etilo p. N-Vinilformamida h. 3-Butenoato de propilo q. Butanodiamida i. 3-Metilciclohexanocarboxilato de etilo r. N-Etil-N-metilciclobutanocarboxamida.