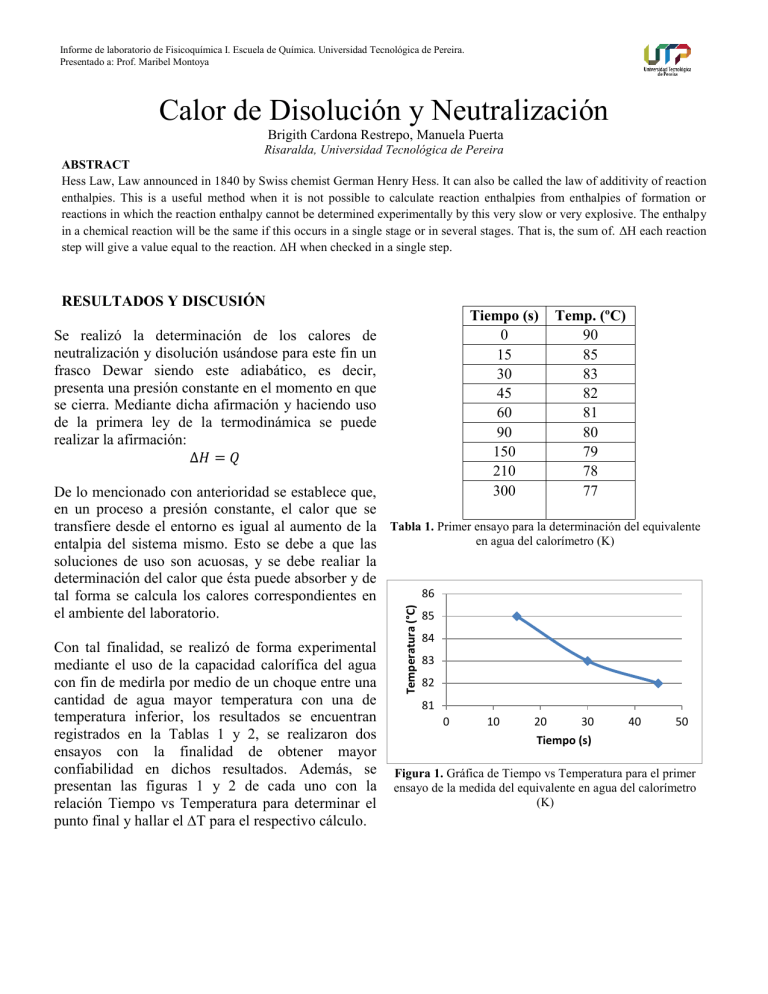
Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. Presentado a: Prof. Maribel Montoya Calor de Disolución y Neutralización Brigith Cardona Restrepo, Manuela Puerta Risaralda, Universidad Tecnológica de Pereira ABSTRACT Hess Law, Law announced in 1840 by Swiss chemist German Henry Hess. It can also be called the law of additivity of reaction enthalpies. This is a useful method when it is not possible to calculate reaction enthalpies from enthalpies of formation or reactions in which the reaction enthalpy cannot be determined experimentally by this very slow or very explosive. The enthalpy in a chemical reaction will be the same if this occurs in a single stage or in several stages. That is, the sum of. ΔH each reaction step will give a value equal to the reaction. ΔH when checked in a single step. RESULTADOS Y DISCUSIÓN Tiempo (s) 0 15 30 45 60 90 150 210 300 Se realizó la determinación de los calores de neutralización y disolución usándose para este fin un frasco Dewar siendo este adiabático, es decir, presenta una presión constante en el momento en que se cierra. Mediante dicha afirmación y haciendo uso de la primera ley de la termodinámica se puede realizar la afirmación: ∆𝐻 = 𝑄 Temp. (ºC) 90 85 83 82 81 80 79 78 77 Con tal finalidad, se realizó de forma experimental mediante el uso de la capacidad calorífica del agua con fin de medirla por medio de un choque entre una cantidad de agua mayor temperatura con una de temperatura inferior, los resultados se encuentran registrados en la Tablas 1 y 2, se realizaron dos ensayos con la finalidad de obtener mayor confiabilidad en dichos resultados. Además, se presentan las figuras 1 y 2 de cada uno con la relación Tiempo vs Temperatura para determinar el punto final y hallar el ∆T para el respectivo cálculo. Temperatura (°C) De lo mencionado con anterioridad se establece que, en un proceso a presión constante, el calor que se transfiere desde el entorno es igual al aumento de la Tabla 1. Primer ensayo para la determinación del equivalente en agua del calorímetro (K) entalpia del sistema mismo. Esto se debe a que las soluciones de uso son acuosas, y se debe realiar la determinación del calor que ésta puede absorber y de 86 tal forma se calcula los calores correspondientes en el ambiente del laboratorio. 85 84 83 82 81 0 10 20 30 40 50 Tiempo (s) Figura 1. Gráfica de Tiempo vs Temperatura para el primer ensayo de la medida del equivalente en agua del calorímetro (K) Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. 2 Tiempo (s) 0 15 30 45 60 75 90 105 120 135 150 −𝑚𝐻2 𝑂 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝑇𝑜𝐻2 𝑂 ) = 𝐾(𝑇𝑓 − 𝑇𝑜𝑓𝑟𝑎𝑠𝑐𝑜 ) Temp. (ºC) 90 82 81 80,4 80 79 78,8 78 77,5 77,1 77 1𝑐𝑎𝑙 −200𝑔 º𝐶 𝑔 (77 º𝐶 − 90 º𝐶) 𝐾= (77 º𝐶 − 20 º𝐶) 𝐾 = 45,6140 Temperatura (°C) Tabla 2. Segundo ensayo para la determinación del equivalente en agua del calorímetro (K) 83 82 81 80 79 78 77 76 0 50 100 150 𝑐𝑎𝑙 º𝐶 Se llegó a que la Temperatura final fueron 77ºC y la inicial del frasco Dewar de 20ºC obteniendo así K=45,6140 cal/ºC. Posteriormente, se procedió a la determinación del calor de disolución haciendo uso de un volumen de agua conocida el cual se encuentra en agitación constante y se hace adición de una determinada masa de NaOH sólido conocido, el comportamiento de la temperatura con el tiempo se encuentra registrado en la tabla 3 y se realiza la gráfic para una mejor visualización del punto final de disolución (figura 3). 200 Tiempo (s) Figura 2. Gráfica de Tiempo vs Temperatura para el segundo ensayo de la medida del equivalente en agua del calorímetro (K) Se puede observar que ambos gráficos presentan un comportamiento similar, y la variación entre ambos resultados no es significativa, ya que tanto el punto inicial como el final tienen el mismo valor, por esta razón se puede realizar un promedio y así tener más cercanía a un valor real. Luego de la determinación de las temperaturas, la masa usada en cada experimento (aprox. 200g) y con la capacidad calorífica del agua se pueden reemplazar en la ecuación y de esta manera obtener el K, así: 𝛥𝐻 = −𝑚𝐻2 𝑂 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝑇𝑜) −𝐾(𝑇𝑓 − 𝑇𝑜) Tiempo (s) 0 15 30 45 60 75 90 105 120 135 150 165 Temp. (ºC) 23 24 25 25 26 26 26,1 27 27 27 27 27 Tabla 3. Incremento en la temperatura con respecto en la disolución de una masa de NaOH en agua Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. respectivos cambios de unidades obteniéndose que −10,6286 𝑘𝑐𝑎𝑙 el calor de disolución es de 28 Temperatura (°c) 3 27 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝑂𝐻 26 25 24 23 22 0 50 100 150 200 Tiempo (s) Se procede a la determinación del porcentaje de error. |10,6286 − 18,6402| %𝐸 = ×100 10,6286 %𝐸 75,38% Figura 3. Gráfica del incremento en la temperatura con respecto en la disolución de una masa de NaOH en agua Se observó un porcentaje de error alto y se puede atribuir a errores mediante la experimentación, ya Mediante la observación de la gráfica resulta difícil que no se cuenta con un ambiente químico hacer la determinación del punto final de la adecuado y se está sujeto a errores del manejo de disolución puesto que se presentan diferentes reactivos, presión y exactitud de la persona que temperaturas que llegan a ser constantes por cierto lleva a cabo el procedimiento. tiempo, sin embargo en el primer aumento de temperatura se observa un crecimiento mucho más Además, se realizó la misma determinación con un significativo que los siguientes, finalmente se mayor valor en masa de NaOH, teniéndose el valor observa una temperatura casi constante a los 27°c y experimental de 3,9917g, la vaiación respecto al por ende, se tomará esta como base para la reliación tiempo se registra en la tabla 4, además su de los cálculos pertinentes para obtener el calor de respectiva gráfica se observa en la figura 4. disolución, además de considera el Cp muy cercano Tiempo (s) Temp. (ºC) al del agua y el K calculado anteriormente. De 0 23 forma tal que: 15 24 𝛥𝐻 = −𝑚𝐻2 𝑂+𝑁𝑎𝑂𝐻 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝑇𝑜) − 𝐾(𝑇𝑓 − 𝑇𝑜) 30 25 45 26 Puesto que es un sistema adiabático: 60 26 75 27 𝑄𝑠𝑙𝑛 = −( 𝑚𝐻2 𝑂+𝑁𝑎𝑂𝐻 𝐶𝑝𝐻2 𝑂 + 𝐾)(𝑇𝑓 − 𝑇𝑜) 90 27 105 27 Se obtiene finalmente reemplazando valores: 120 27 𝑄𝑠𝑙𝑛 = −(202,1265 𝑔 × 1 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 ) (27 º𝐶 − 23 º𝐶) 𝑄𝑠𝑙𝑛 = −990,962 𝑐𝑎𝑙 Se tiene en cuenta la masa de NaOH usado en disolución pues es una propiedad extensiva: −990,962 𝑐𝑎𝑙 40 𝑔 𝑑𝑒 𝑁𝑎𝑂𝐻 −18,6402 𝐾𝑐𝑎𝑙 𝑥 = 2,1265𝑔 𝑑𝑒 𝑁𝑎𝑂𝐻 1 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝑂𝐻 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝑂𝐻 Según la teoría, el Calor de disolución para el NaOH es de -44.5 kJ/mol, se realizan los Tabla 4. Incremento en la temperatura con respecto en la disolución de una masa de NaOH en agua (4g) Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. 4 resultados obtenidos se observan en la tabla 5, 6, 7, 8 y 9, respectivo para cada ensayo realizado. Temperatura (°C) 28 27 26 25 24 23 • Ensayo 1. Volumen de agua 100 mL- volumen de H2SO4 5 mL. • Ensayo 2. Volumen de agua 150 m- volumen de H2SO4 5 mL. • Ensayo 3. Volumen de agua 200 mL- volumen de H2SO4 5 mL • Ensayo 4. Volumen de agua 250 mL- volumen de H2SO4 5 mL • Ensayo 5. Volumen de agua 300 mL- volumen de H2SO4 5 mL 22 0 50 100 150 Tiempo (s) Figura 4. Gráfica del incremento en la temperatura con respecto en la disolución de una masa de NaOH en agua 𝛥𝐻 = −𝑚𝐻2 𝑂+𝑁𝑎𝑂𝐻 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝑇𝑜) − 𝐾(𝑇𝑓 − 𝑇𝑜) Puesto que es un sistema adiabático: 𝑄𝑠𝑙𝑛 = −( 𝑚𝐻2 𝑂+𝑁𝑎𝑂𝐻 𝐶𝑝𝐻2 𝑂 + 𝐾)(𝑇𝑓 − 𝑇𝑜) Se obtiene finalmente reemplazando valores: 𝑄𝑠𝑙𝑛 = −(203,9917 𝑔 × 1 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 ) (27 º𝐶 − 23 º𝐶) 𝑄𝑠𝑙𝑛 = −998,4228 𝑐𝑎𝑙 Tiempo (s) 0 15 30 45 60 75 90 Tabla 5. Soluto líquido (ensayo 1). 𝑄𝑠𝑙𝑛 = −(105 𝑔 × 1 −998,4228 𝑐𝑎𝑙 40 𝑔 𝑑𝑒 𝑁𝑎𝑂𝐻 −10,005 𝐾𝑐𝑎𝑙 𝑥 = 3,9917𝑔 𝑑𝑒 𝑁𝑎𝑂𝐻 1 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝑂𝐻 𝑚𝑜𝑙 𝑑𝑒 𝑁𝑎𝑂𝐻 |10,6286 − 10,005| %𝐸 = ×100 10,6286 %𝐸 = 5,87% Por otra parte, se pudo observar que con una mayor cantidad de NaOH se obtiene un porcentaje de error pequeño esto puede ser a que es más apreciable la interacción a mayor cantidad de soluto. Temp. (ºC) 31 31 32,3 32,3 32,3 32,3 32,3 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 ) (32,3 º𝐶 − 31 º𝐶) 𝑄𝑠𝑙𝑛 = −195,8 𝑐𝑎𝑙 Tiempo (s) 0 15 30 45 60 75 90 Temp. (ºC) 30,5 30,5 30,5 30,5 30,5 30,5 30,5 Tabla 6. Soluto líquido (ensayo 2). Posteriormente se realizó el procedimiento con un 𝑄𝑠𝑙𝑛 = −(155 𝑔 × 1 𝑐𝑎𝑙 + 45,6140 𝑐𝑎𝑙 ) (30,5 º𝐶 − 30,5 º𝐶) º𝐶𝑔 º𝐶 soluto líquido siendo este ácido sulfúrico concentrado, realizándose ensayos diferentes con 𝑄𝑠𝑙𝑛 = 0 𝑐𝑎𝑙 una variabilidad en la cantidad de agua, los Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. Tiempo (s) 0 15 30 45 60 75 90 Temp. (ºC) 30,8 29 28,7 28,7 28,7 28,7 28,7 5 Para el cálculo de N1 es necesario la siguiente ecuación 𝑚𝑜𝑙 𝑎𝑔𝑢𝑎 𝑛1 = 𝑚𝑜𝑙 𝑠𝑜𝑙𝑢𝑡𝑜 Se hace los cálculos pertinentes para pasar de mililitros a moles tanto para el agua como para el ácido sulfúrico, con densidades de 1 g/ml y 1,84 g/ml. Se obtuvo la gráfica presente en la figura 5. 200 Tabla 7. Soluto líquido, (ensayo 3). 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 150 ) (28,7 º𝐶 − 30,8º𝐶) n1 𝑄𝑠𝑙𝑛 = −(205 𝑔 × 1 100 𝑄𝑠𝑙𝑛 = 526,3 𝑐𝑎𝑙 50 0 Tiempo (s) 0 15 30 45 60 75 90 Temp. (ºC) 32 29 28 28 28 28 28 Tabla 8. Soluto líquido, (ensayo 4). 𝑄𝑠𝑙𝑛 = −(255 𝑔 × 1 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 ) (28 º𝐶 − 32 º𝐶) 𝑄𝑠𝑙𝑛 = 1202,5 𝑐𝑎𝑙 Tiempo (s) 0 15 30 45 60 75 90 Temp. (ºC) 25 27 27 27 27 27 27 Tabla 9. Soluto líquido (ensayo 5). 𝑄𝑠𝑙𝑛 = −(305 𝑔 × 1 𝑐𝑎𝑙 º𝐶𝑔 + 45,6140 𝑐𝑎𝑙 º𝐶 𝑄𝑠𝑙𝑛 = −701,23 𝑐𝑎𝑙 ) (27 º𝐶 − 25º𝐶) -1000 -500 0 500 1000 1500 Q Figura 4. Relación de moles respecto a Q. Finalmente, se realizó la determinación del calor de neutralización donde reaccionaron el HCl (200mL) y NaOH (150mL), se tomaron las temperaturas de ambas soluciones antes de poner en contacto, al adicionar ambas en el frasco Dewar se tomaron temperaturas cada 15s (Tabla 10) y se observó su comportamiento por medio de una gráfica (Figura 5). Tiempo (s) Temp. (ºC) 0 27,8 15 27,8 30 28 45 28 60 28 Tabla 4. Incremento en la temperatura con respecto al tiempo en la reacción de neutralización entre el NaOH y el HCl. Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. Temperatura (°C) 6 CONCLUSIONES 28,05 28 27,95 27,9 27,85 27,8 27,75 0 10 20 30 40 • El frasco Dewar es un sistema ideal para realizar ciertas mediciones de temperaturas pues permite asumir valores de presión constantes al ser un sistema adiabático, como se observó en el análisis de la práctica existen ciertas desviaciones en cuanto a sensibilidades y valores que no seguían una tendencia ideal. • En cuanto a los calores de disolución y neutralización, al ser tan pequeños pueden ser difíciles de observar, sin embargo, se pueden observar como suceden y las utilidades que tiene estos dentro de las industrias químicas. • Una determinación de entalpia de una reacción química debe ser la misma o aproximadamente igual si esta se produce en una etapa o en dos etapas. La energía generada por la combustión del carbón es bastante grande, lo cual, sumado a su bajo costo y relativa abundancia, nos demostró las virtudes por las cuales es ampliamente usado en la obtención de energía. 50 Tiempo (s) Figura 5. Incremento en la temperatura con respecto al tiempo en la reacción de neutralización entre el NaOH y el HCl. En la figura 5 se presenta una pequeña cresta antes de la estabilización de la temperatura, esto indica que la homogenización de la solución o la respuesta del termómetro no es instantánea [1] sin embargo luego de unos instantes se puede observar la estabilización de la temperatura la cual se toma como punto final de neutralización y se aplica a la ecuación: 𝑇𝑎+𝑇𝑏 )+ 2 𝛥𝐻 = 𝑚𝑎𝑐𝑖+𝑏𝑎𝑠𝑒 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝐾(𝑇𝑓 − 𝑇𝑜) • Considerando nuevamente un proceso adiabático: 𝑄𝑑 = 𝑚𝑎𝑐𝑖+𝑏𝑎𝑠𝑒 𝐶𝑝𝐻2 𝑂 (𝑇𝑓 − 𝑇𝑎+𝑇𝑏 )+ 2 𝐾(𝑇𝑓 − 𝑇𝑜) Reemplazando los datos correspondientes: 𝑄𝑑 = 350 𝑔 𝑥 1 𝑐𝑎𝑙 º𝐶 𝑥 𝑔 (28 º𝐶 − 48 º𝐶 2 )+ 45,6140 𝑐𝑎𝑙 º𝐶 (28 º𝐶 − 23 º𝐶) 𝑄𝑑 = 1628,07 𝑐𝑎𝑙 Este valor corresponde al calor de neutralización desprendido por mol neutralizado, para poder expresarlo como calor de neutralización (Qn) se tiene en cuenta: 150 𝑚𝐿 𝑁𝑎𝑂𝐻 1 𝑚𝑜𝑙 𝑁𝑎 𝑂𝐻 1 𝑚𝑜𝑙 𝑑𝑒 𝐻2 𝑂 × 1000 𝑚𝐿 1 𝑚𝑜𝑙 𝑁𝑎𝑂𝐻 = 0,15 𝑚𝑜𝑙𝑒𝑠𝐻2 𝑂 𝑄𝑛 = −1628,07 𝑐𝑎𝑙 −10,85 𝐾𝑐𝑎𝑙 = 0,15 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 𝐻2 𝑂 𝑚𝑜𝑙 𝑑𝑒 𝐻2 𝑂 REFERENCIAS [1]. ALBA, J. E. D., VALENCIA, M. A., & Hoover, A. (2008). Fisicoquímica Aplicada. Fundamentación Experimental. Pereira. Universidad Tecnológica de Pereira. Fisicoquimica, (2016). Calor de Neutralización. [online] Geocities.ws. Available at: http://www.geocities.ws/todolostrabajossallo/fic o2 [Accessed 2 Nov. 2016]. Termoquímica-Ley de Hess [En línea]. <http://www.quimicayalgomas.com/quimicageneral/termoquimica-ytermodinamica/termoquimica-ley-de-hess/> [Citado en 26 de abril de 2015]. Informe de laboratorio de Fisicoquímica I. Escuela de Química. Universidad Tecnológica de Pereira. 7









