Herramientas diagnósticas, de prevención y manejo de la sífilis
Anuncio

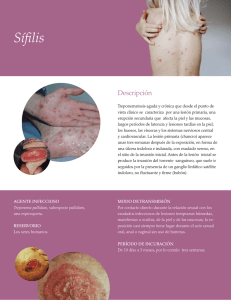
Herramientas diagnósticas, H e r r a m i e n t a s d i a g n ó s t i c a s , de prevención y manejo de d e p r e v e n c i ó n y m a n e j o d e la sífilis materna y congénita: l a s í f i l i s m a t e r n a y c o n g é n i t a : panorama general p a n o r a m a g e n e r a l Luis Fernando Mejía Rivera, MD Pediatra e infectólogo Centro Médico Imbanaco de Cali Corporación IPS Saludcoop Universidad Libre de Cali Perspectiva general de la enfermedad La sífilis es una infección de transmisión sexual (ITS), curable con tratamiento antimicrobiano adecuado, considerada como un problema grave de salud pública en países en desarrollo y reemergente en países desarrollados al afectar a más de 12 millones de personas en el mundo. Se estima que más de 2 millones de mujeres embarazadas se infectan con sífilis cada año en el planeta, y un número significativo de casos (692.100 a 1,53 millones) no reciben tratamiento. Los Centros para el Control y Prevención de Enfermedades (CDC, por su sigla en inglés) calculan que 55.400 personas en los Estados Unidos contraen nuevas infecciones de sífilis al año. En 2011, hubo 45.042 nuevos casos de sífilis reportados, en comparación con unos 48.298 nuevos diagnósticos de infección por el VIH y 321.849 casos de gonorrea. De los nuevos casos de sífilis, 13.970 fueron de sífilis primaria y secundaria, las fases más tempranas y más infecciosas de esta enfermedad. En 2011, el 72% de sífilis primaria y secundaria se presentó en hombres que tienen relaciones sexuales con hombres. También, hubo 360 informes de niños con sífilis congénita en este año1. Cuando ocurre en la mujer embarazada, fácilmente se transmite al feto, ocasionando, hasta en un 81% de los casos, complicaciones que incluyen muerte fetal o neonatal temprana, prematurez, bajo peso o infección congénita2,3. La Organización Mundial de la Salud (OMS) estima alrededor de 420.000 abortos y mortinatos al año a nivel mundial. Su transmisión vertical es prevenible si la madre es diagnosticada y tratada oportunamente. Si todas las gestantes fueran tamizadas para sífilis, y las positivas CCAP Volumen 13 Número 1 19 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general fuesen tratadas con al menos una dosis de penicilina, más del 97% de los neonatos evitarían la infección13. Es por esto por lo que los casos de sífilis congénita en nuestro país son inaceptablemente elevados, y reflejan serios problemas en la atención prenatal de la gestante. La transmisión al feto se estima entre el 60 y 90% cuando la madre se encuentra en fase de sífilis activa no tratada, el 10-40% durante sífilis latente y el 2% de riesgo luego de dos años de enfermedad14,17. En las últimas décadas, el incremento de la infección en la población general de países no desarrollados ha permanecido estable o registra incrementos significativos, particularmente en ciertos grupos poblacionales más vulnerables. Los grupos de mayor riesgo son: fármaco-dependientes, poblaciones con acceso limitado a la consulta médica, grupos con iniciación sexual muy temprana, bajo nivel educativo, ciudades con prostitución creciente en edades jóvenes y bajo nivel socioeconómico, y pacientes VIH positivos. En estos últimos, la enfermedad presenta mayor virulencia y dificultad para ser tratada, y se la considera además un facilitador de la transmisión y adquisición del VIH, en razón del paralelismo epidemiológico de ambas afecciones –Joint United Nations Programme on HIV/AIDS. Consultation on STD interventions for preventing HIV: what is the evidence? Geneva; 2000 (Unaids/03.04e)–. En Colombia, la sífilis congénita y gestacional es de notificación obligatoria, y las cifras reportadas por el Sistema de Vigilancia en Salud Pública (Sivigila) son unas de las más altas en Latinoamérica y el Caribe. La prevalencia de sífilis gestacional en el país es del 1,6% (siete veces mayor a la prevalencia de VIH en mujeres embarazadas, 0,22%). En 2011, Colombia reportó 2,9 casos de sífilis congénita/1.000 nacidos vivos (Sivigila. Vigilancia rutinaria. 2012. Disponible en: http://ww.ins.gov.co/lineas-deaccion/subdirección-vigilancia/sivigila/paginas/vigilancia-rutinaria.aspx), un valor que es casi seis veces mayor a la meta estipulada por 20 Precop SCP la Organización Panamericana de Salud (OPS) en su Plan de Eliminación de Sífilis Congénita (objetivo = alcanzar cifras menores a 0,5 casos de sífilis congénita/1.000 nacidos vivos, incluidos los mortinatos). Para llegar a esta meta, se requiere que más del 95% de las gestantes infectadas sean detectadas y tratadas, logrando reducir la prevalencia de sífilis durante la gestación a menos del 1,0%. El litoral pacífico colombiano aporta al país un número significativo de casos cada año, siendo el puerto de Buenaventura, en el Valle del Cauca, una de las zonas más afectadas, con un reporte en el año de 2010 de 141 casos de sífilis congénita, de los cuales nueve terminaron en desenlace fatal11. La OMS, en sitios con limitaciones para el acceso a los métodos diagnósticos, recomienda el manejo sindromático de enfermedades con úlceras genitales (genital ulcer disease, GUD) para cobertura de tratamiento para sífilis y chancroide, documentándose una relativa significativa caída en la prevalencia de sífilis primaria entre pacientes con GUD en países donde el manejo sindromático fue implementado4. Sin embargo, la mayoría de los individuos infectados con sífilis no tienen síntomas clínicos. Los recién nacidos de madres infectadas están en riesgo de adquirir la infección in utero, resultando en seria morbimortalidad perinatal. La sífilis congénita puede ser prevenida si la infección en la madre es detectada y tratada al momento del segundo trimestre. Los análisis de screening para prevención de la sífilis congénita se han convertido en el foco principal de los programas de control de esta enfermedad. Las tasas de sífilis primaria y secundaria aumentaron significativamente en la pasada década, generando renovación en su atención, diagnóstico y tratamiento. Los hombres que tienen sexo con otros hombres se han visto particularmente afectados, como también la coinfección con el virus de inmunodeficiencia humana (VIH); no obstante, los incrementos de estas tasas también se notan en mujeres, así Luis Fernando Mejía Rivera como en todas las categorías etarias e identidades étnicas. Simultáneamente, la presencia de sífilis congénita también se ha elevado, requiriendo atención especial y acentuando de nuevo la necesidad del cuidado temprano y continuado prenatal, y la búsqueda de sífilis en todas las mujeres embarazadas5. Entre los factores que contribuyen a la persistencia de la sífilis congénita como problema de salud pública, cabe destacar las barreras de acceso a los servicios del control prenatal o su acceso tardío, falla en la capacitación al personal, dificultad en la administración y seguimiento del tratamiento a la gestante y su pareja, y el estigma y la discriminación relacionados con las ITS. Existen subregistros acerca de la evolución de los títulos serológicos de las pruebas no treponémicas que permiten la determinación de la efectividad del tratamiento o la estimación de sus fallas durante la gestación6. Definiciones y características de la enfermedad La sífilis es una infección sistémica que compromete múltiples órganos, con predominio del tejido cerebral y el sistema fagocítico-mononuclear (SFM), particularmente en el feto infectado, y que ocurre en diferentes estados en el tiempo en ausencia de tratamiento adecuado. Hace parte del grupo de infecciones de transmisión sexual (ITS) y es causada por una bacteria móvil, alargada, de pequeño tamaño, Gram negativa, de la familia Espiroqueta (filo Spirochaetes, clase Spirochaetes, orden Spirochaetales), emparentada con bacterias del género Borrelia y la familia Leptospiraceae, el Treponema pallidum, descubierta en 1905 (Schaudinn y Hoffmann), que no es cultivable in vitro y la cual tiene particular importancia clínica durante el embarazo por el alto riesgo de infección transplacentaria del feto. El ser humano es el único reservorio u hospedero natural de esta bacteria y su transmisión ocurre exclusivamente por vías sexual, transplacentaria (aumentando a medida que transcurre el embarazo y disminuyendo con la progresión de la sífilis materna) y perinatal, por presencia de lesiones primarias de chancro sifilítico en el canal de parto o en los pezones durante la lactancia, si bien la bacteria no se transmite a través de la leche materna. La transmisión también puede ocurrir en cualquier etapa del embarazo, pero el riesgo mayor de infección fetal se presenta durante la etapa tardía de este. La sífilis se transmite generalmente al feto cuando la embarazada tiene una enfermedad activa (RPR 1:8 o mayor) con una evolución de menos de cinco años, sin tratamiento adecuado. La infección congénita se asocia con resultados adversos severos en el producto, incluyendo17: • • • • • • • • • Abortos espontáneos (29,2%). Muerte perinatal (13,3%). Hidrops fetal no inmune. Parto pretérmino (25%). Bajo peso al nacer y retardo del crecimiento intrauterino. Anormalidades congénitas. Sífilis congénita activa en el neonato (22%). Secuelas a largo término en los que sobreviven, tales como sordera y alteraciones neurológicas. Puede llevar a muerte intrauterina en el 30%, a muerte neonatal en el 10% y a trastorno neonatal en el 40%. El hablar de sífilis temprana siempre se refiere a las fases primaria (‘chancro’ sifilítico en el sitio de inoculación), secundaria (diseminación con presencia de lesiones dérmicas generalizadas y mucosas) y temprana latente de la infección (duración de la infección < 1 año). Estos son los estados de la sífilis que ocurren típicamente en los primeros años después de adquirir la infección y están clásicamente asociados con transmisión sexual. La sífilis latente se define como una infección asintomática, con serología positiva y examen físico negativo. Una persona puede reinfectarse en múltiples ocasiones durante su vida sexual activa y cada uno de los episodios infecciosos puede tener una historia natural similar, si bien la susceptibilidad a la reinfección por sífilis se reduce inmediatamente CCAP Volumen 13 Número 1 21 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general después de un episodio de esta infección que ha sido tratado adecuadamente; cualquier inmunidad adquirida es de corto plazo. La sífilis gestacional (SG) es aquella que se diagnostica durante la gestación, el aborto reciente o el puerperio inmediato, y se puede encontrar en cualquiera de las fases de la enfermedad (úlceras genitales o lesiones compatibles con sífilis secundaria) o con pruebas treponémicas (incluidas pruebas treponémicas rápidas) o no treponémicas positivas o reactivas, en quien no ha recibido tratamiento adecuado para sífilis durante la presente gestación o fue reinfectada o no recibió tratamiento adecuado (definición de la OPS en 2007). Se hace confirmación de caso de sífilis gestacional en toda mujer embarazada, puérpera o con aborto reciente con prueba no treponémica reactiva mayor o igual 1:8 diluciones o en menor dilución con prueba treponémica positiva. Cuando la madre es infectada en las primeras semanas de gestación, se produce un daño fetal severo y un pequeño porcentaje termina en aborto espontáneo; si se infecta después de la semana 16 de gestación, esta evoluciona hacia el aborto en el 25%, mortinato en el 25% o infección congénita en cerca del 50% de los casos y solo un pequeño porcentaje de los niños nacerá sano; la infección de las madres al final de la gestación se traduce en una amplia transmisión a los fetos, el 60% de los cuales nacerán aparentemente sanos. La sífilis congénita (SC) ocurre cuando la madre con sífilis transmite la infección al producto durante la gestación, ya sea por vía hematógena transplacentaria o durante el parto por el contacto del neonato con lesiones en los genitales maternos. Las lesiones clínicas se forman a partir de la semana 16 de gestación cuando el sistema inmunológico se ha desarrollado, aunque el treponema puede pasar a la circulación fetal desde la novena semana. Al menos 2/3 de los neonatos de mujeres con sífilis no tratadas resultan infectados. Se estima que, de todas las gestantes con sífilis no tratada, solo el 20% llegará al término de la gestación y el neonato será 22 Precop SCP normal7. En el caso del recién nacido, debido a que la infección se realiza por vía hematógena transplacentaria, la enfermedad no presenta el período primario, comenzando en el secundario. De los niños con sífilis congénita temprana, entre el 60 y 78% son asintomáticos al nacer y 2/3 tendrán síntomas entre las 3 y 8 semanas. Un caso probable de sífilis congénita se refiere a todo aborto, recién nacido vivo o muerto de mujer con evidencia clínica o con pruebas no treponémicas o treponémicas positivas o reactivas durante la gestación, parto o puerperio no tratada o tratada inadecuadamente con uno o más de los siguientes factores: • Haber tenido otra ITS durante la gestación. • No haber tenido seguimiento serológico después del tratamiento o que haya sido inapropiado. • No haber tratado a los contactos. • Haber presentado respuesta serológica deficiente que certifique la respuesta terapéutica. • Recién nacido con uno de los siguientes requisitos: – Resultado serológico (VDRL/RPR) reactivo hasta el título 1:4. – Criterios clínicos, de laboratorio y radiológicos de sífilis en el recién nacido. – Títulos de VDRL cuatro veces mayores en el niño que en la madre o lo que equivale a un cambio en dos o más diluciones de los títulos maternos. – IgM específica reactiva. Caso confirmado A: – Caso probable a quien en el seguimiento se detectó aumento en dos o más diluciones de título inicial menor que 1:8. Recién nacido con una de las siguientes condiciones: • Prueba sifilítica reactiva en LCR. • Identificación del T. pallidum por microscopia de campo oscuro, fluorescencia directa u otra tinción especial que permita su identificación en lesiones del neonato, la placenta, el cordón umbilical o el material de autopsia. – Recién nacido con las siguientes condiciones: pruebas treponémicas y no treponémicas reactivas; evidencia clínica de sífilis: presencia de Luis Fernando Mejía Rivera hepatoesplenomegalia (71%), fiebre (42%), falla del crecimiento (33%), lesiones cutáneo-mucosas (68%) (pénfigo sifilítico consistente en erupción descamativa y bulosa; erupción macular rosadocobrizo con descamación fina que no toma el tronco anterior; pápulas y placas infiltrativas de color rojizo en región peribocal, miembros, palmas, plantas, perianales y perigenitales; paroniquia; alopecia; condiloma lata), linfadenopatías (14%), osteocondritis y periostitis dolorosas (78%), epifisitis (generalmente del radio, fémur, húmero y fíbula), bandas radiolúcidas en huesos, rinitis mucopurulenta (14%), pseudoparálisis, anormalidades del sistema nervioso central (neurosífilis = 23%) (leptomeningitis e hidrocefalia, accidente cerebrovascular, enfermedad meningovascular crónica, hipopituitarismo), anormalidades oftalmológicas (corioretinitis, glaucoma, uveítis), ictericia o anemia, hemolisis autoinmune, neumonitis (17%), pseudoparálisis (15%), ascitis (9%)8,18. • Hollier, en el caso de sífilis fetal intrauterina confirmada en una pequeña muestra de 24 fetos, encontró hepatomegalia en el 66%, asociada a ascitis en el 12% de ellos. Las transaminasas hepáticas estaban elevadas en el 88% de los estudios de cordocentesis intrauterina, anemia en el 26%, trombocitopenia en el 35%. Concluyen que las transaminasas se elevan en la infección temprana y las alteraciones hematológicas son manifestaciones tardías de la enfermedad. Esta hipótesis necesita ser confirmada con estudios que incluyan un número mayor de casos18. • Caso confirmado B: recién nacido con signos y síntomas compatibles con sífilis congénita a quien no se le pudo realizar seguimiento ni pruebas de laboratorio. • Caso compatible: recién nacido asintomático clasificado como caso probable a quien no se le pudo realizar seguimiento ni pruebas de laboratorio. Gust analizó 14.627 casos de sífilis congénita reportados en los Estados Unidos entre 19921998. De ellos, 182 nacieron vivos y murieron posteriormente (1,2%). La mortalidad se produjo en el 91,8% de los casos antes de los 28 días y en todos antes de los tres meses de vida. El 89% de los que fallecieron tenían menos de 37 semanas de gestación y el 87% pesaba menos de 2.500 g al nacer. En el 87,4% de los casos, las madres no fueron tratadas o el tratamiento fue inadecuado. En los restantes casos, el tratamiento se realizó en forma adecuada pero los títulos no descendieron cuatro veces al nacimiento20. Herramientas diagnósticas Existe un amplio rango de herramientas diagnósticas disponibles (tabla 1), teniendo en cuenta que la respuesta inmune está mediada tanto por inmunidad de tipo celular como humoral por inmunoglobulinas IgG, IgM e IgA. Identificación de ‘Treponema pallidum’ La identificación directa de T. pallidum no es usada rutinariamente porque la mayoría de las personas con sífilis son asintomáticas. La identificación de treponemas es posible solamente en personas con presencia de lesiones de sífilis primaria y secundaria (figura 1). No es posible cultivar T. pallidum en el laboratorio; la técnica consiste en microscopia de campo oscuro en extendidos de material húmedo extraído de las lesiones. Los treponemas tienen características morfológicas y motilidad particulares. La microscopia en campo oscuro tiene una sensibilidad entre el 74-86% y una especificidad cercana al 97%, pero la confiabilidad de los resultados depende de la experiencia del técnico que lleva a cabo el análisis. El test en microscopia para detección de anticuerpos por fluorescencia directa (direct fluorescent antibody-T. pallidum testing, DFA-TP) utiliza anticuerpos conjugados con fluoresceína para exponer al microorganismo en secciones de tejido o lesiones, no requiere de organismos móviles y es una prueba más sensible y específica que la técnica de microscopia en campo oscuro, pero es técnicamente más demandante y costosa9. Las técnicas de amplificación de bases de ácidos nucleicos, así como las de reacción en CCAP Volumen 13 Número 1 23 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general cadena de polimerasa (PCR), las cuales pueden detectar cantidades tan pequeñas como 10 treponemas en muestras de lesiones, tejido placentario y otros tejidos o líquidos corporales, han mejorado enormemente la sensibilidad de los métodos de detección directa. Existen múltiples ensayos disponibles de PCR, los cuales detectan simultáneamente T. pallidum, virus herpes simple tipo 2 y Haemophilus ducreyi, y han sido usados para determinar el diagnóstico etiológico en pacientes con GUD, al igual que para validar los algoritmos en el manejo sindromático9. limitaciones, por sus requerimientos técnicos y por exposición de dichos infantes a antimicrobianos antes de la obtención de las muestras, que tornan negativas dichas pruebas. En general, la mayor parte de los recién nacidos con infección por T. pallidum a nivel del sistema nervioso central pueden ser identificados por medio del examen físico, pruebas de laboratorio convencionales y estudios radiográficos. Sin embargo, la identificación de todos estos infantes requiere el empleo de pruebas adicionales, incluyendo igM-immunoblotting en suero y PCR12. La sensibilidad para PCR-T. pallidum (polymerase chain reaction-Treponema pallidum), en estudios seleccionados para revisión sistemática, resulta más alta en el análisis de muestras de úlceras primarias genitales o anales (78,4%; 95% CI: 68,2-86,0) y en sangre de recién nacidos con sífilis congénita (83%; 55,0-95,2), en tanto que las especificidades para todos los estudios revisados está alrededor del ~95%, excepto para la medición en sangre. Los valores reunidos mostraron que PCR-T. pallidum es más eficiente para confirmar que para excluir la etiología de sífilis, principalmente en lesiones de la piel, siendo un instrumento útil para el diagnóstico en úlceras, especialmente cuando la serología es aún negativa y en ajustes médicos en zonas con alto predominio de sífilis10. Pruebas serológicas para ‘screening’ y detección de casos Los métodos de detección directa para confirmación de sífilis congénita también son de utilidad en programas de vigilancia de la enfermedad. En un recién nacido sintomático o producto de una madre infectada que no ha sido tratada adecuadamente, el diagnóstico de sífilis congénita puede ser confirmado utilizando técnicas de microscopia o moleculares para la identificación de T. pallidum en lesiones, úlceras, secreciones nasofaríngeas, líquido cefalorraquídeo, sangre de cordón umbilical, tejido placentario u otros tejidos corporales. Si bien las espiroquetas pueden ser visualizadas en valoraciones del líquido cefalorraquídeo en recién nacidos infectados, estas tienen 24 Precop SCP Las pruebas serológicas continúan siendo los métodos de elección para el diagnóstico de sífilis. La infección por T. pallidum produce diferentes patrones de respuesta serológica (figura 1). En el Reino Unido, se hacen pruebas prenatales universales para sífilis, demostrando oportunidad de tipo costo-efectivo, incluso con prevalencias reportadas de 0,06 por 1.000 nacidos vivos (año 2000). Los anticuerpos contra antígenos fosfolípidos en la superficie del treponema producen reacciones cruzadas con antígenos tipo cardiolipina en mamíferos. Pruebas serológicas de floculación (grado de precipitación) para detectar estos anticuerpos fosfolípidos han sido desarrolladas como pruebas screening no específicas, tales como la prueba rapid plasma reagin (RPR) y la venereal diseases research laboratory (VDRL). Estas pruebas son simples, rápidas, económicas y han mostrado excelente sensibilidad, especialmente en fases tempranas de la infección. Las mayores desventajas son que estas no pueden ser utilizadas en sangre completa; requieren una centrífuga o microscopios para su procesamiento; y pueden producir resultados falsos positivos. En mujeres embarazadas, un 28% de resultados RPR positivos pueden ser falsos positivos biológicos. Pueden ocurrir Luis Fernando Mejía Rivera resultados falso negativos cuando estos anticuerpos se encuentran en exceso (conocido como el fenómeno de prozona). Pueden presentarse reacciones cruzadas con otras infecciones treponémicas, incluyendo pian (Treponema pertenue) o pinta (Treponema carateum). Todas las pruebas no treponémicas pueden presentar fenómenos de prozona –RPR falsos negativos– como ausencia de reacción inmune cuando las muestras son fuertemente reactivas debido a exceso de anticuerpos, por lo que es conveniente titularlas siempre. Esto es especialmente cierto cuando la prueba se realiza con muestra no diluida y con un procedimiento incorrecto (como dispersar el antígeno sobre la muestra no extendida en el círculo de reacción). La temperatura de los reactivos es igualmente importante en relación con la sensibilidad. También puede obtenerse un resultado negativo en las fases muy tempranas del período primario, incluso cuando la visualización de las treponemas es positiva; otro problema que podemos encontrar es el fenómeno de prozona, que consiste en un resultado negativo o positivo débil que se observa hasta en un 2% de los infectados, especialmente en la fase de sífilis primaria tardía o la infección secundaria. Para solventar esas situaciones, hay que efectuar diluciones séricas mayores cuando existe sospecha fundada, como ocurre en las mujeres embarazadas, usuarios de drogas por vía parenteral o pacientes con otras enfermedades de transmisión sexual. Si hay sospecha clínica de infección secundaria, se deben prescribir al laboratorio pruebas con muestras que deberán diluir el suero por lo menos a la dilución de 1:16 para descartar el fenómeno de prozona. En pruebas screening, no treponémicas –ARP, VDRL, RPR–, se logra positividad luego de un mes de enfermedad, en tanto que la prueba treponémica FTA-ABS eleva sus niveles más tempranamente. Las pruebas no treponémicas pueden ser del tipo cualitativas o cuantitativas. Los títulos para las pruebas RPR y VDRL aumentan en pacientes con infección aguda, reinfección o reactivaciones de infecciones pasadas que no fueron adecuadamente tratados. Alrededor del 72-84% de los pacientes con sífilis primaria o secundaria muestran descensos hasta cuatro veces en los títulos de RPR o VDRL seis meses después de haber completado un tratamiento apropiado. Las tasas de serorreversión dependen de los títulos pretratamiento y del estado de la enfermedad. Individuos con su primer episodio de infección tienen mayor probabilidad de serorrevertir que aquellos en quienes la infección repite. Las pruebas no treponémicas son, por lo tanto, útiles no solamente en la identificación de infección activa, sino también en la monitorización de la efectividad a los tratamientos (figura 1). Las pruebas treponémicas, como la pruebas de haemagglutination para T. pallidum (TPHA), el test de aglutinación de partículas T. pallidum (TPPA) y la prueba de absorción de anticuerpos treponémicos por fluorescencia (FTA-ABS), son utilizadas para confirmar tests screening positivos. La prueba de microhemaglutinación (MHA-TP), la cual también puede ser usada para confirmar tests positivos, no está disponible fácilmente a nivel comercial. Los tests treponémicos son más costosos, requieren equipamiento y experiencia técnica, y, por lo tanto, están disponibles en laboratorios de referencia. La prueba Western Blot (immunoblotting) ha sido propuesta como una alternativa a la FTA-ABS como confirmatoria, es más sensible que la FTA-ABS pero menos sensible que la TPPA. Las tasas de falsos positivos son ligeramente menores en las pruebas treponémicas respecto a las no treponémicas. Las pruebas treponémicas no se usan generalmente para screening, porque no muestran ser tan sensibles como las no treponémicas en las primeras 2-3 semanas de un estado primario de sífilis. Los anticuerpos treponémicos usualmente persisten a lo largo de la vida, produciendo que estas pruebas tengan menor utilidad como confirmatorias en zonas donde la prevalencia de la infección es alta; tampoco son útiles para la monitorización en la efectividad de un tratamiento. Las pruebas treponémicas se informan positivas o negativas, no se negativizan con el tratamiento y no se relacionan con la actividad de la enfermedad. CCAP Volumen 13 Número 1 25 26 Precop SCP US$0,40 Requiere organismos vivos. La especificidad se compromete por la presencia de detritus o formas treponémicas endógenas Costo promedio estimado Comentarios No requiere organismos vivos No distingue entre las subespecies pallidum y pertenue La mayoría de reactivos RPR requieren refrigeración US$0,50 Mínima complejidad Rotador Laboratorio local Fácil 93-98% Fácil 94-98% 84-98% Test rápido Los reactivos requieren refrigeración US$0,50 Mínima complejidad Microscopio de luz US$3,00 Permite altos rendimientos como screening, pero no distingue entre infección activa y tratada en el pasado La mayoría de los tests son estables a temperatura ambiente por más de seis meses. Los tests no distinguen entre infección activa e infección pasada tratada Moderada complejidad Test confirmatorio. No distingue entre infección activa y tratada en el pasado US$3,00 Especializado Incubador Laboratorio referencia Laboratorio intermedio, laboratorio referencia Incubador Complejo 98-100% 85-100% TPHA-TPPA Moderado 97-100% 82-100% EIA US$0,55-3,00 Mínima complejidad Ninguno particular Laboratorio local Laboratorio local Fácil 98% 78-100% VDRL RPR 86-100% Test treponémicos Test no treponémicos Test confirmatorio. No distingue entre infección activa y tratada en el pasado US$3,00 Especializado Microscopio de fluorescencia Laboratorio referencia Complejo 94-100% 70-100% FTA-ABS Fuente: adaptada de Peeling RW, Ye H. Bulletin World Health Organization 2004;82(6). DFA-TP: direct fluorescent antibody-Treponema pallidum testing; PCR: polymerase chain reaction; RPR: rapid plasma regain test; VDRL: venereal diseases rearch laboratory test; EIA: enzyme immunoassay; TPHA-TPPA: T. pallidum haemagglutination assay-T. pallidum particle agglutination test; FTA-ABS: fluorescent treponemal antibody absorption test. Especializado Entrenamiento necesario US$14,00 Especializado Moderada complejidad Microscopio de luz con condensador de campo oscuro Equipo requerido US$3,00 Equipo especializado Microscopio de fluorescencia Laboratorio local Dónde usar Facilidad de uso Laboratorio referencia 99% Laboratorio intermedio, laboratorio referencia 89-100% 85-97% Especificidad 91% Complejo 73-100% 74-86% Sensibilidad Detección de DNA (PCR) Moderado Detección de antígeno (DFA-TP) Microscopia campo oscuro Criterio Fácil Screening Para pacientes que presentan una úlcera o lesión Tabla 1. Comparación entre los tests de sífilis Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general Luis Fernando Mejía Rivera Figura 1. Patrones comunes de reactividad serológica en pacientes con sífilis FTA-Abs % de pacientes con pruebas positivas 100 TPHA 80 60 No tratados IgMa 40 VDRL / RPR 20 Tratados 2 4 6 8 10 12 2 10 Semanas Momento de infección 20 Años Tiempo Posinfección Lesión primaria Primaria Lesión secundaria Secundaria Latente (asintomática) Terciaria IgM por ELISA o FTA-Abs 195 o Inmmunoblot WHO 04.69 a Fuente: adaptada de Peeling RW, Ye H. Bulletin World Health Organization 2004;82(6). La prueba VDRL, que mide anticuerpos contra antígenos de la membrana celular modificada del Treponema, puede informar resultados falsos positivos debido a enfermedades autoinmunes, exantemas virales, vacunaciones y drogas intravenosas, en cuyos casos los títulos son 1:4 o menores. La RPR (reaginas rápidas en plasma) es un ensayo más económico, más fácil de realizar y de leer. Los títulos suelen ser una dilución mayor que los de la VDRL. Los títulos de RPR de 1:8 o mayores son considerados signos de actividad de la enfermedad o contagio reciente. Pruebas serológicas para sífilis congénita Muchos recién nacidos se muestran asintomáticos al momento de nacer. El serodiagnóstico de sífilis congénita en menores de 15 meses de edad puede confundirse por la transferencia pasiva de inmunoglobulina G (IgG) de la placenta al feto y este no se recomienda en menores nacidos de madres seropositivas (tabla 2). Recién nacidos de madres con sífilis no tratada deben ser tratados a pesar de sus resultados en las pruebas. Recién nacidos de madres con pruebas treponémicas y no treponémicas reactivas CCAP Volumen 13 Número 1 27 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general deben ser evaluados con el mismo test cuantitativo no treponémico que se utilizó en su madre, preferiblemente tomado en el mismo momento. Títulos de RPR en el recién nacido que son cuatro veces más altos que los de su madre sugieren marcadamente la presencia de sífilis congénita, y el menor debe ser tratado apropiadamente. Sin embargo, estudios de sueros pareados de madres y menores infectados pueden mostrar que menos del 30% de los niños tienen títulos mayores que los de sus madres. La sífilis congénita puede no ser excluida en recién nacidos que no tienen incrementos de los títulos cuatro veces mayores en la prueba RPR, ya que los tratados tempranamente en el curso de la enfermedad pueden no desarrollar niveles suficientemente altos de anticuerpos para su detección. Anticuerpos del tipo inmunoglobulina M (IgM) pueden ser detectados en más del 80% de los niños sintomáticos, pero datos en su sensibilidad son limitados. El factor reumatoide en sueros fetales puede causar resultados falsos positivos, especialmente con la prueba FTAABS IgM. Utilizando técnicas immunoblot para determinar la respuesta IgM, producen mayores sensibilidades que la 19S (IgM) FTA-ABS o enzimo-inmunoensayos (EIAs), pero sus resultados deben ser interpretados con precaución, porque la respuesta IgM toma tiempo para desarrollarse en recién nacidos y puede estar disminuida con tratamientos tempranos, un resultado IgM negativo puede no ser utilizado para excluir la infección congénita. Serodiagnóstico de sífilis en mujeres embarazadas Pruebas de screening prenatal utilizando tests no treponémicos son factibles y económicas en la mayoría de países en desarrollo. En mujeres gestantes, las pruebas no treponémicas son propensas a dar resultados falsos positivos tanto que los resultados deben ser confirmados con pruebas treponémicas. Resultados falsos positivos se asocian usualmente con títulos bajos. De allí que, en zonas con alta prevalencia donde 28 Precop SCP hay limitaciones para acceder a tests confirmatorios, una mujer con títulos no treponémicos >/=8 debe ser tratada. No obstante, dada la morbilidad importante y la mortalidad potencial asociadas con la infección congénita y la falta de pruebas RPR cuantitativas en muchos escenarios, todas las mujeres embarazadas con resultados positivos en una prueba treponémica o no treponémica deben ser tratadas inmediatamente. El riesgo asociado con la sífilis no tratada en embarazadas por mucho sobrepasa el riesgo de ‘sobretratamientos’ de madres con resultados falsos positivos. Diferentes guías en los Estados Unidos y Europa recomiendan screening prenatal durante el primero y el tercer trimestre y al momento del parto12,13. Por una variedad de razones, el screening prenatal generalmente ocurre mucho menos en países en desarrollo. En madres que han sido tratadas, un poco menos del cuádruple en los títulos no treponémicos sugieren que el tratamiento ha fallado o la madre ha sido reinfectada. Lamentablemente, para la mayor parte de las mujeres que son diagnosticadas durante el screening prenatal, hay tiempo a menudo insuficiente para la confirmación del éxito en el tratamiento, representado en una disminución del cuádruple en sus títulos antes del parto. Serodiagnóstico de sífilis en madres VIH-infectadas La interpretación de los resultados en las pruebas serológicas es complicada en pacientes que están también infectadas por el virus de la inmunodeficiencia humana (VIH). No existen suficientes datos para determinar si las pruebas serológicas para sífilis en mujeres embarazadas o neonatos funcionan adecuadamente si la mujer está infectada tanto con sífilis como con VIH. Las alteraciones en la funcionalidad de los linfocitos B en pacientes VIH pueden resultar en resultados biológicos RPR falsos positivos o en niveles IgM séricos elevados, especialmente en sujetos usuarios de drogas inyectables. Pruebas serológicas falsamente negativas han sido también reportadas. Microscopia de campo oscuro; DFA-TP; EIA-IgM; RPR o VDRL cuantitativa RPR o VDRL cuantitativa Ninguna RPR o VDRL cuantitativas; EIA-IgM; pruebas rápidas treponémicas RPR o VDRL; pruebas rápidas treponémicas Ninguna Microscopia de campo oscuro; DFA-TP; EIA-IgM; RPR o VDRL cuantitativa; pruebas rápidas treponémicas RPR o VDRL; pruebas rápidas treponémicas Laboratorios regionales Laboratorios de baja complejidad RPR o VDRL cuantitativa Microscopia de campo oscuro; EIA-IgM; RPR o VDRL cuantitativa RPR o VDRL; EIA; TPHA-TPPA o FTA-ABS Pruebas moleculares; RPR o VDRL; TPHA-TPPA o FTA-ABS Laboratorios de referencia RPR o VDRL; pruebas rápidas treponémicas Microscopia de campo oscuro; DFA-TP; RPR o VDRL; pruebas rápidas treponémicas; EIA-IgM RPR o VDRL; pruebas rápidas treponémicas Microscopia en campo oscuro; DFA-TP; RPR o VDRL; pruebas rápidas treponémicas; EIA-IgM Sitios centinelas RPR o VDRL cuantitativas Pruebas moleculares; EIAIgM; RPR o VDRL cuantitativa RPR o VDRL; EIA; TPHATPPA o FTA-ABS Pruebas moleculares; RPR o VDRL; TPHA-TPPA o FTAABS Laboratorios de referencia Fuente: adaptada de Peeling RW, Ye H. Bulletin World Health Organization 2004;82(6). El serodiagnóstico de un recién nacido de una madre infectada que es reactiva para las pruebas treponémicas no se recomienda por la transferencia pasiva de anticuerpos IgG a través de la placenta; la sospecha de sífilis congénita puede ser confirmada por títulos de RPR en el recién nacido >/= veces mayores que los títulos maternos. Sin embargo, un resultado negativo no excluye la presencia de sífilis en el menor. EIA-IgM no es una prueba recomendada en recién nacidos asintomáticos debido a su baja sensibilidad. La falta de test de sensibilidad y especificidad para el diagnóstico de la sífilis congénita significa que todos los recién nacidos de madres con sífilis deberían ser tratados a pesar de los resultados en las pruebas. ** * DFA-TP: direct fluorescent antibody-Treponema pallidum testing; PCR: polymerase chain reaction; RPR: rapid plasma regain test; VDRL: venereal diseases research laboratory test; EIA: enzyme immunoassay; TPHA-TPPA: T. pallidum haemagglutination assay-T. pallidum particle agglutination test; FTA-ABS: fluorescent treponemal antibody absorption test. Asintomática** Sintomática Sífilis congénita* Asintomática Sintomática Sífilis materna Test para vigilancia Test para el diagnóstico o screening Tabla 2. Herramientas para la prevención y el control de la sífilis materna y congénita en diferentes escenarios Luis Fernando Mejía Rivera CCAP Volumen 13 Número 1 29 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general Las pruebas no treponémicas son útiles para detectar la infección por sífilis (pasada o presente), evaluar la efectividad del tratamiento y, en pacientes con historia de tratamiento previo para la sífilis, sirven para determinar la posibilidad de reinfección. El resultado cuantitativo de las pruebas no treponémicas (ej., títulos) usualmente aumentará en la infección temprana, llegará a su pico en la etapa secundaria y disminuirá poco a poco con el tiempo, incluso en la ausencia de tratamiento. La RPR y VDRL son pruebas clínicamente equivalentes; sin embargo, el título de un paciente se debe evaluar en el tiempo utilizando siempre el mismo tipo de prueba, si es posible analizada por el mismo laboratorio, a fin de evitar variaciones cuantitativas entre ellas; por ejemplo, en algunos casos, los títulos de la RPR pueden resultar un poco más elevados que los VDRL para una misma muestra. Una visión hacia el futuro La iniciativa para el diagnóstico de enfermedades de transmisión sexual (SDI, por su sigla en inglés) de la Unicef/UNDP/World Bank/ WHO-Programa Especial para la Investigación y la Educación en Enfermedades Tropicales, recientemente ha iniciado un programa para el desarrollo, evaluación y aplicación de pruebas que incluyen criterios enmarcados en el acrónimo Assured (en inglés): affordable (económico), sensitive (sensible), specific (específico), user-friendly (uso amigable), es decir, puede ser realizado en pocos pasos simples y con mínimo entrenamiento, rapid and robust (rápido y sólido), equipment-free (libre de equipos) y deliverable to developing countries (aplicable en países en desarrollo). Las enfermedades de transmisión sexual se enfocan en pruebas orientadas por la iniciativa Assured que son más apropiadas para detección de sífilis, clamidia genital e infecciones por gonococo en escenarios de cuidado médico primario en países en desarrollo. Pruebas prometedoras están siendo seleccionadas para 30 Precop SCP futuras evaluaciones, utilizando, por ejemplo, sangre completa. El desarrollo de pruebas rápidas que puedan distinguir entre infección activa o tratada, y que idealmente empleen especímenes tomados de métodos no invasivos, como saliva u orina, se convierten en una prioridad urgente. Manejo de la sífilis congénita Existen diversas variables que influyen en la decisión del tratamiento neonatal: documentación de sífilis en la madre, tratamiento materno adecuado, evidencia clínica, paraclínica o radiológica de sífilis neonatal, y comparación de los títulos serológicos de la madre y el recién nacido, idealmente usando una misma prueba no treponémica. El CDC de Atlanta, en el año 2006, propone cuatro escenarios para la evaluación y manejo del recién nacido con sífilis congénita. Las mujeres embarazadas que resultan seropositivas para la sífilis deben ser consideradas infectadas a menos que tengan un historia de tratamiento adecuado bien documentado y las pruebas serológicas secuenciales hayan disminuido apropiadamente después de la terapia. Ningún recién nacido debe ser dado de alta del hospital antes de que se hayan revisado los resultados de la serología realizada durante el parto en la madre y el neonato. La penicilina es el único esquema recomendado por la CDC para el tratamiento de la sífilis durante el embarazo, así como para la prevención de la sífilis en el recién nacido. Las mujeres tratadas para la sífilis durante el embarazo deben ser cuidadosamente monitoreadas usando los títulos serológicos (ej., mensualmente en mujeres con riesgo alto de reinfección o en áreas geográficas con alta prevalencia de sífilis); además, se debe prestar atención especial al manejo de las parejas sexuales de una mujer tratada para sífilis durante el embarazo para prevenir la reinfección. Luis Fernando Mejía Rivera Los estudios clínicos sugieren que la primera dosis de penicilina trata al feto en el 95% de los casos y las subsiguientes dosis a la madre17. Manejo de los resultados positivos de las pruebas no treponémicas durante el embarazo La eficacia del tratamiento depende de la edad gestacional en la cual se realiza. Las guías actuales del CDC y de la OMS para tratamiento materno recomiendan una única dosis de penicilina benzatínica para el tratamiento de la sífilis temprana y, en el caso de enfermedad con más de un año de duración o si se desconoce su evolución, tres dosis en forma semanal. Se considera respuesta apropiada al tratamiento el descenso de cuatro veces los títulos luego de tres meses en sífilis primaria o secundaria y seis meses en el caso de latente temprana17. Para asegurar el diagnóstico y manejo óptimos de los niños nacidos de madres con serología reactiva para la sífilis durante el embarazo, se sugiere lo siguiente (el esquema de decisiones describe la evaluación y manejo basado en las pautas de la CDC-2002): • Examen físico completo de la madre y el hijo. • Debe considerarse qué tan adecuado y oportuno fue cualquier tratamiento recibido por la madre (antes del embarazo, durante el embarazo, > 4 semanas antes del parto, o en las 4 semanas finales del embarazo). Tabla 3. Estado de infección en el neonato Cambios serológicos esperados* Recién nacido no infectado Para el tercer mes: disminución en el título no treponémico. Pruebas serológicas reactivas debido a la transferencia pasiva de anticuerpos maternos. Para el sexto mes: pruebas no treponémicas revierten a no reactivas. Recién nacido infectado pero tratado adecuadamente Para el sexto mes: pruebas no treponémicas revierten a no reactivas. Después de 15-18 meses: pruebas no treponémicas no reactivas. Para el tercer mes: disminución en el título treponémico. Infección congénita persistente Se necesita reevaluar y posiblemente repetir el tratamiento con 10 días de penicilina parenteral. * Después de 15-18 meses: prueba serológica treponémica permanece reactiva. Después de 6-12 meses: no hay disminución (o hay un aumento) en el título no treponémico; o A los 18 meses: las pruebas no treponémicas permanecen reactivas. La respuesta serológica después del tratamiento puede ser más lenta en los niños tratados después del período neonatal. • Evaluación de laboratorio con microscopia de campo oscuro o pruebas de anticuerpos fluorescentes en cualquier lesión de piel o fluido anormal, tal como secreción nasal. • Debe considerarse el tipo de tratamiento materno (penicilina benzatínica vs. tratamiento sin penicilina). • Debe considerarse la respuesta serológica materna al tratamiento (se debe descartar la falla terapéutica en la madre). • Deberá realizarse la prueba no treponémica cuantitativa (RPR o VDRL) en ambos, la madre y el neonato, durante el parto. CCAP Volumen 13 Número 1 31 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general Seguimiento después del tratamiento Todos los recién nacidos serorreactivos o los recién nacidos de madres serorreactivas al momento del parto deben ser objeto de un examen de seguimiento y pruebas serológicas no treponémicas cada 2-3 meses, hasta que los títulos de estas disminuyan a dos diluciones (cuatro veces) o se reviertan a no reactivos. El examen del LCR deberá repetirse cada seis meses en aquellos recién nacidos que presentaron un LCR anormal inicialmente hasta que los resultados del LCR se normalicen. Una VDRL reactiva en el LCR o resultados anormales en el LCR que no pueden atribuirse a otra causa requieren retratamiento, debido a la posibilidad de neurosífilis. En los niños no infectados nacidos de madres infectadas (o nacidos de madres con historia de sífilis previamente tratada), la RPR debe revertirse a no reactiva a los seis meses. En los niños infectados, la RPR puede tomar hasta los 12 meses de vida para revertirse a no reactiva; el FTA generalmente permanece reactivo después del tratamiento (aun después de los 15 meses de edad). Recién nacidos y neurosífilis Es difícil llevar a cabo el diagnóstico de compromiso del SNC y la indicación de realización de punción lumbar es discutida en los recién nacidos asintomáticos. La incidencia de neurosífilis en recién nacidos sintomáticos varía entre el 22 y 66%17. Se observan casos de VDRL en LCR y análisis citoquímicos falsamente negativos. También, se reportan casos de VDRL en LCR falsamente positivos. En 92 recién nacidos con diagnóstico presuntivo de sífilis, se practicaron 74 punciones lumbares con un caso de neurosífilis. La madre tenía títulos de 1:16; en el cordón los títulos fueron 1:1; en sangre periférica, 1:32, y el recién 32 Precop SCP nacido era sintomático. Con estos hallazgos, los autores proponen reconsiderar la realización de PL en recién nacidos asintomáticos. Beeram no encontró diferencia en celularidad y proteínas en el estudio citoquímico de una población con diagnóstico presuntivo de sífilis y de un grupo control evaluado por riesgo de infección inespecífica. Solo 2 de 329 pacientes asintomáticos (0,6%) tuvieron VDLR positivo, los cuales tenían indicación de tratamiento por la historia materna de sífilis no tratada o tratamiento inadecuado19. Los recién nacidos con neurosífilis son generalmente sintomáticos. En los casos que no presentaron síntomas, la valoración paraclínica estuvo alterada. Las embarazadas en estos casos tuvieron títulos de RPR o VDRL iguales o mayores a 1:8, el tratamiento se efectuó en el último mes o no se utilizó penicilina. Conclusiones El principio primordial de la prevención y eliminación de la sífilis congénita es la detección y el tratamiento de la infección gestacional para prevenir la transmisión de la madre al hijo, y, en tal sentido, es necesario diseñar un enfoque nacional unificado enfocando la atención al tamizaje, diagnóstico y tratamiento adecuado de la mujer embarazada, y no esperar al diagnóstico y tratamiento de recién nacidos infectados. Entre muchos factores que intervienen en la persistencia de la sífilis gestacional y la sífilis congénita en nuestro medio, se encuentran identificados el acceso tardío al control prenatal, el desconocimiento de la población sobre el impacto de la enfermedad en el feto y el neonato, la pobre vigilancia del cumplimiento de los esquemas de tratamiento y de los contactos sexuales, y la falta de seguimiento clínico institucional con actividades de retroalimentación interinstitucional entre las diferentes entidades de salud nacional. CCAP Volumen 13 Número 1 Escenario 2 Madre no tratada, tratada inadecuadamente o sin registro de tratamiento o madre tratada con eritromicina (macrólidos) u otro diferente a penicilina o madre tratada en las últimas 4 semanas del parto. Reportar: al Sivigila como caso de sífilis congénita. Escenario 4 Madre cuyo tratamiento fue adecuado antes del embarazo y los títulos maternos permanecieron bajos y estables antes y durante el embarazo y al parto (VDRL </=1:2; RPR </=1:4). Madre sin evidencia de reinfección o recaída. Seguimiento: Clínico y serológico = 3, 6, 12 meses. Si la prueba no treponémica inicial es reactiva, el seguimiento se hace hasta que sea no reactiva o disminuya 4 veces. Con compromisos de SNC: realizar análisis en LCR: cada 6 meses hasta que se torne negativo. Tratamiento: Penicilina benzatínica 50.000 UI/kg/dosis IM (DU). No requiere exámenes fuera del VDRL. Escenario 3 Madre tratada durante el embarazo con tratamiento adecuado según el estado y antes de las últimas 4 semanas del embarazo y madre sin evidencia de reinfección o recaída. Fuente: basada en Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines 2006. Si se pierde más de un día de tratamiento, deberá reiniciarse completo. Tratamiento: (recomendado para nuestro medio) Penicilina G cristalina 100.000 150.000 UI/kg/día, administrado 50.000 UI/kg/dosis IV cada 12 horas los primeros 7 días de vida y luego 50.000 UI/kg/ dosis IV cada 8 horas hasta completar 10 días. Exámenes VDRL en LCR, conteo de leucocitos y proteínas. Hemoleucograma y recuento plaquetario. Radiografía de huesos largos. De acuerdo a la clínica = radiografía de tórax, pruebas de función hepática, ecografía de cráneo, evaluación oftalmológica y potenciales auditivos. Escenario 1 Exámen físico anormal consistente con sífilis congénita: títulos séricos no treponémicos >4 veces los maternos (2 diluciones) o microscopia de campo oscuro o flulorescencia de AC positivos en líquidos corporales o secreciones. Reportar al Sivigila como caso de sífilis congénita. Una prueba no treponémica positiva (RPR o VDRL) con una prueba treponémica no reactiva representan una reacción biológica falsamente positiva sin riesgo de infección para el feto. Neonato con exámen físico normal + títulos no treponémicos iguales o </=4 veces los maternos (incluso no reactivos). Recién nacido de madre con prueba no treponémica reactiva (VDRL o RPR) Figura 2. Escenarios de tratamiento para sífilis congénita Luis Fernando Mejía Rivera 33 Herramientas diagnósticas, de prevención y manejo de la sífilis materna y congénita: panorama general La combinación de los datos clínicos de cada recién nacido junto con los de la madre permiten situar un escenario terapéutico correspondiente y, en consecuencia, optimizar el tratamiento antimicrobiano para cada caso, llevando a disminuir estancias hospitalarias, costos para el sistema de salud y para sus usuarios, con una adecuada curación de la enfermedad; adicionalmente, se deben fortalecer las actividades de notificación obligatoria de los casos de sífilis congénita y sífilis gestacional, para lograr un conocimiento amplio de los factores demográficos asociados y de las dificultades que se presenten en el diagnóstico, tratamiento y seguimiento, y en la implementación de políticas de salud pública encaminadas a la eliminación de la enfermedad de la sífilis congénita. El tratamiento de la sífilis congénita con penicilina es efectivo, de fácil realización y bajo costo. Referencias 1. Dobson SR, Kaplan S, Weisman L. Update, congenital syphilis. CDC and AAP; 2012. 2. Schmid GP, Stoner BP, Hawkes S, Broutet N. The need and plan for global elimination of congenital syphilis. Sex Transm Dis 2007;34(7 Suppl):S5-10. 3. Kamb ML, Newman LM, Riley PL, Mark J, Hawkes SJ, Malik T, et al. A road map for the global elimination of congenital syphilis. Obstet Gynecol Int 2010:1-6. 4. World Health Organization. HIV/AIDS and STD surveillance: epidemiological fact sheets by country. Geneva: WHO; 1998. 5. Mattei PL, Beachkofsky TM, Gilson RT, Wisco OJ. Syphilis: a reemerging infection. Am Fam Physician 2012;86(5):433-40. 6. Vanegas-Castillo N, et al. Tratamiento de la sífilis gestacional y prevención de la sífilis congénita en un hospital público en Bogotá, 2010 - investigación original. Revista Facultad de Medicina, Universidad Nacional de Colombia 2011;59(3): 167-89. 7. Berman SM. Maternal syphilis: pathophysiology and treatment. Bull World Health Organ 2004;82(6):433-8. 8. Walker GJ, Walker DG. Congenital syphilis: a continuin but neglected problem. Semin Fetal Neonatal Med 2007;12(3): 198-206. 9. Peeling R, Ye H. Bulletin World Health Organization 2004; 82(6). 10. Gayet-Ageron A, Lautenschlager S, Ninet B, Perneger TV, Combescure C. Sensitivity, specificity and likelihood ratios of PCR in the diagnosis of syphilis: a systematic review and metaanalysis. Sex Transm Infect 2013;89(3):251-6. 11. Micheloww IC, Wendel GD Jr, Norgard MV, Zeray F, Leos NK, Alsaadi R, et al. Central nervous system infection in congenital syphilis. N Engl J Med 2002;346(23):1792-8. 34 Precop SCP 12. United States Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines 2002. MMWR Morbility and Mortality Weekly Report 2002;51(RR6):18-30. 13. Goh BT, van Voorst Vadeer PC; European Branch of the International Union against Sexually Transmitted Infection and the European Office of the World Health Organization. European guideline for the management of syphilis. Int J STD AIDS 2001;12 Suppl 3:14-26. 14. Rubiano LC. Informe epidemiológico semana 52 de 2011. Prioridad Salud Sexual y Reproductiva. Cali: Secretaría de Salud Departamental del Valle del Cauca; 2012. 15. Blencowe H, Cousens S, Kamb M, Berman S, Lawn JE. Lives Saved Tool supplement detection and treatment of syphilis in pregnancy to reduce syphilis related stillbirths and neonatal mortality. BMC Public Health 2011;11 Suppl 3:S9. 16. NeoReviews 2010;11(12). 17. Morales M, Estevan M. Actualización en sífilis congénita temprana. Archivos Pediátricos Uruguayos 2011;83(1):35-9. 18. Hollier LM, Harstad TW, Sanchez PJ, Twickler DM, Wendel GD Jr. Fetal syphilis: clinical and laboratory characteristics. Obstet Gynecol 2001;97(6):947-53. 19. Beeram MR, Chopde N, Dawood Y, Siriboe S, Abdin M. Lumbar puncture in the evaluation of possible asymptomatic congenital syphilis in neonates. J Pediatr 1996;128(1):125-9. 20. Gust DA, Levine WC, St Louis ME, Braxton J, Berman SM. Mortality associated with congenital syphilis in the United States, 1992-1998. Pediatrics 2002;109(5):E79-9. Disponible en: http://www.aapublications.org.cgi/content/abstract /109/5/c79