Unidad 3, 3 - Departamento de Química Orgánica
Anuncio

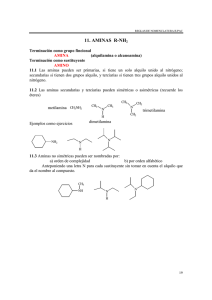
Unidad III 3.3.Enlaces simples carbonooxigeno , 3.4.carbono -azufre, 3.5. carbono- nitrógeno Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. Propiedades de los éteres • Oxigeno hibridación sp3 • Enlace polar C-O Puntos de ebullición Propiedades físicas • Éteres no pueden formar puentes de hidrógeno con otras moléculas de éter, por lo que tienen un punto de ebullición más bajo que los alcoholes. • Moléculas de éter forman puentes de hidrógeno con moléculas de agua y alcohol. Ellos son aceptores de enlaces de hidrógeno. Propiedades físicas • Efecto solvatación • Formación de Complejos. Reactivo de Grinard enlaces borano H _ + O B H H BH3 THF electrones no enlazantes del éter estabilizan el borano (BH3). Éteres corona • Éteres corona puede acomplejar cationes metálico en el centro del anillo. • El tamaño del anillo de éter determinará qué catión puede solvatar mejor. • Los éteres corona a menudo permite acomplejar sales inorgánicas polares en disolventes orgánicos no polares. Autooxidación • Productos de autooxidación son explosivos. • Nunca destilar a sequedad. Unidad 3.5 ENLACE SIMPLE CARBONONITROGENO Clasificación • Primaria (1º ): Tiene un grupo alquilo unido al nitrógeno (RNH2). • Secundaria (2º ): Tiene dos grupos alquilo unidos al nitrógeno (R2NH). • Terciaria (3º ): Tiene tres grupos alquilo unidos al nitrógeno (R3N). • Cuaternaria (4º ): tiene cuatro grupos alquilo unidos al nitrógeno y el nitrógeno tiene una carga positiva (R4N +). Sales cuaternarias de amonio • El átomo de nitrógeno tiene cuatro grupos alquilo unidos. • El nitrógeno está cargado positivamente. Nombres comunes • Los nombres comunes de las aminas se forman a partir de los nombres de los grupos alquilo unidos al nitrógeno, seguido por el sufijo -amina Amina como sustituyente • En una molécula con un grupo funcional de prioridad más alta, la amina se nombra como sustituyente. Nomenclatura IUPAC • Nombre en base a la cadena de carbono más larga. • El -o del alcano se sustituye con la terminación amina. Aminas Aromáticas • En aminas aromáticas, el grupo amino está unido a un anillo de benceno. • El compuesto original se llama anilina Aminas heterocíclicas Estructura de Amina • Nitrógeno con hibridación sp3 y un par de electrones libres. Puntos de ebullición • N-H es menos polar que O-H. • Enlaces de hidrógeno más débiles, por lo que las aminas tendrán un punto de ebullición más bajo que el alcohol correspondiente. • Las aminas terciarias no pueden formar puentes de hidrógeno, por lo que tienen puntos de ebullición inferiores a las aminas primarias y secundarias Puntos de ebullición Basicidad • Solo el par de electrones sobre el nitrógeno puede aceptar un protón de un ácido. • Las soluciones acuosas son básicas pKb amoniaco = 4,74. • Alquil aminas son bases más fuertes que el amoniaco. • Aumentar el número de grupos alquilo disminuye el poder de solvatación de iones, por lo que aminas 2º y 3º son similares a las 1º en basicidad. Sales de amonio • Sólidos iónicos con altos puntos de fusión. • Soluble en agua. • Sin olor a pescado. Purificación de aminas Reactividades relativas La protonación de una amina no forma un compuesto con un buen grupo saliente Por lo que las aminas no pueden sufrir reacciones de sustitución ni de y eliminación Comúnmente las aminas son bases orgánicas Los sustituyentes convierten al N una base mas fuerte que el amoniaco Efecto resonante • Bases mas débiles Las aminas como nucleófilos. Nucleófilos y bases La reacción de eliminación de Hofmann Una sal cuaternaria de amonio puede someterse a una reacción de eliminación con una base fuerte tal como ion hidróxido. La reacción de Hofmann es una SN2 MECANISMO Regioselectividad en la reacción de eliminación de Hofmann • El producto menos sustituido es el producto principal de la reacción (Hofmann producto). La base retira el H de el enlace b-carbono unido al más hidrógenos ¿Debido a que el grupo saliente es pobre? El estado de transición es un carbanión. Recordemos que los fluoruros de alquilo tienen estados de transición como carbanión, debido a que el grupo saliente es pobre. Debe ser un hidróxido cuaternario Solución acuosa de óxido de plata convierte un haluro de amonio cuaternario a un hidróxido de amonio cuaternario. La alquilación de aminas por halogenuros de alquilo • Procede por el mecanismo SN2. • Haluros de alquilo secundarios van a dar productos de eliminación. • Un problema importante son las múltiples alquilaciones, se obtienen mezclas complejas. Alquilación exhaustiva • Alquilación exhaustiva forma la sal de cuaternatia de amonio. • Condiciones básicas suaves (NaHCO3) se utilizan para desprotonar los intermedios y neutralizar el ácido formado. Alquilación con exceso de amonio • La reacción con exceso de NH3 para formar la amina primaria con da buenos rendimientos. • Se elimina el exceso de amoníaco por evaporasión después de la reacción Exhaustiva metilación de aminas • El yoduro de metilo se utiliza generalmente como agente de metilación. • El grupo saliente es la amina neutral. Conversión a la sal de hidróxido • La sal de yoduro se convierte en la sal de hidróxido por tratamiento con óxido de plata y agua. • El hidróxido servirá como la base en la etapa de eliminación. Oxidación de aminas • Aminas son fáciles de oxidar, incluso en el aire. Los agentes oxidantes comunes: H2O2, MCPBA. • aminas2º oxidan a hidroxilamina (-noH). • aminas 3º oxidan a óxido de amina (R3N + -O-). Preparación de óxidos de amina • Las aminas terciarias se oxidan a óxidos de amina, a menudo en buenos rendimientos. • H2O2 o peroxiácido pueden ser utilizados para esta oxidación. • El N-óxido puede sufrir eliminación para formar alquenos en una reacción análoga a la eliminación de Hofmann. Reordenamiento de Cope • mecanismo E2. • El óxido de amina actúa como su propia base a través de un estado de transición cíclico, por lo que no se necesita una base fuerte Síntesis de Gabriel • El ion ftalimida es un nucleófilo fuerte, desplaza el haluro o tosilato de iones de haluro de alquilo (SN2). • El calentamiento de la ftalimida N-alquilo con hidrazina separa la amina primaria y la hidrazida muy estable de ftalimida. Información básica de los Tioles Características, rescataban mercurio de allí el nombre de mercapatanos