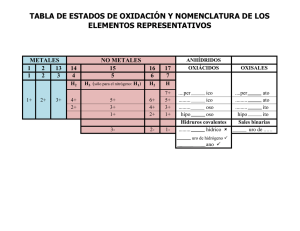
Estimación de la incertidumbre de medida en medicina de
Anuncio

Co ng re so Na cio n al de lL ab or ato rio F. Javier Gella Cl BioSystems, S.A Universidad Autónoma Barcelona íni co 20 15 EXCELENCIA DEL LABORATORIO CLÍNICO C on gr es oN ac ion al de lL ab or ato rio Cl ín ico 20 15 ISO C 15189, 5.5.1.4. on g re El laboratorio debe determinar la incertidumbre. so Cuantitativos Na ciocon paso intermedio cuantitativo. Cualitativos na Revisar periódicamente l d la estimación de la incertidumbre. el La Considerar la incertidumbre bopara interpretar los ra valores medidos. tor Proporcionar la incertidumbre a losiousuarios que la Cl soliciten. íni co 20 15 ENFOQUE CLÁSICO: TEORÍA ERRORES C on gr es oN EXACTITUD ac ionerror de medida al de lL ab or atoaleatorio error sistemático error rio Cl VERACIDAD PRECISIÓN íni c o2 01 5 NUEVO ENFOQUE: INCERTIDUMBRE C on gr es Errores de medida oN ac ion Errores sistemáticos Errores aleatorios al de l La Estimables No estimables bo ra tor Corrección io Cl íni Incertidumbre co Resultado ± 2 01 5 EXACTITUD: Incertidumbre + trazabilidad C on gr es oN ac ion al Trazabilidad: atributo de un valor de lL ab or2 mmol/L resultado: 103 ato rio Cl Incertidumbre: valor asociado ín ico 20 15 INCERTIDUMBRE DE MEDIDA C on g Formarede expresar la “calidad” de un resultado de medida. so Na cio al resultado de una medición, Parámetro, asociado que caracteriza lana dispersión de los valores que l d ser atribuidos al mesurando podrían razonablemente el La Parámetro: s b medida No confundir con error de o ra Tiene diversos componentes to rio Define un intervalo de posibles resultados Cl y que contiene el valor verdadero íni co 20 15 GUIAS GENERALES C on gr es Guide toothe Expression of Uncertainty in Na (GUM): 1993, BIPM-IFCC-ISOMeasurement cio IUPAC na Guidelines for evaluating and expressing the ld el measurement results. NIST, uncertainty of NIST La 1993 bo Quantifying uncertainty in analytical ra tor measurement. Eurachem, 1995 i Expression of the uncertainty of omeasurement in Cl calibration. EAL, 1997 íni co 20 15 GUIAS LABORATORIO CLINICO C on gr Uncertainty of measurement in quantitative medical e testing. sAo laboratory implementation guide. AACB, Na 2004. cio Recomendaciones n para la estimación de la al incertidumbre de medida de en el laboratorio clínico. SEQC, 2009. lL ab Expression of measurement uncertainty in laboratory or ato EP29-A, 2012. medicine; Approved guideline. CLSI, rio Medical laboratories. Practical guide for Cl the estimation of measurement uncertainty. ISO, íni Technical specification N414 (draft), 2015.co 20 15 PRINCIPIOS GENERALES C on g Se rasume que cualquier error sistemático es es o Ncorregido o ignorado. eliminado, ac efectos aleatorios sobre el resultado Se evalúan los i de una medida.on al de en el que se encuentra el Se establece un intervalo l L magnitud medida con un valor verdadero de la ab determinado nivel de confianza. or ato una estimación La complejidad y el coste de obtener rio de la incertidumbre deben ser proporcionales con los requisitos de exactitud aplicables aC la utilización lín clínica de los resultados. ico 20 15 ESTIMACIÓN DE LA INCERTIDUMBRE (GUM) C on gr es INICIO Especificar el mensurando Paso 1 oN ac Identificar las fuentes de incertidumbre Paso 2 ion Paso 3 Simplificar por agrupamiento de las fuentes a ld Cuantificar los componentes Cuantificar el los componentes agrupados de la Llosacomponentes restantes Cuantificar incertidumbre bo Transformar los componentes ra en desviación estándar tor io estándar Paso 4 Calcular incertidumbre combinada Calcular la Cl incertidumbre Revisar y si es necesario reevaluar í combinada los componentes mayores ni c FIN Calcular la incertidumbre expandida o 20 15 ESTIMACIÓN DE COMPONENTES C on gr esAlgunos componentes pueden estimarse y ser Tipo A) o N mediante el valor de una s de caracterizados ac medidas repetidas. Ej.: ion la imprecisión interdiaria al d el resultados de distribución Tipo B) Otros originan La desconocida y es necesario atribuir presunta bo distribución y valor de s. ra tor io Cl íni co 20 15 TIPO C B: DISTRIBUCIONES on gr enormal so Na -a rectangular cio n +a s = a/3 al de -a lL +a ab or s = a/3 triangular -a +a s = a/6 ato Ejemplos de fuentes de incertidumbre: rio Pureza ≥ 98% (rectangular) Enrase en una probeta/matraz (triangular) Valor asignado a un calibrador (normal) Cl ín ico 20 15 ISO C 15189:2013, 5.5.1.4 on g re 1. Los componentes pertinentes de la NOTA so incertidumbre son aquellos asociados con el proceso de mediciónNa real, comenzando con la presentación de c o procedimiento de medición y la muestra ial n obtención del valor medido. terminando con la a l de lL ab or ato No incluir incertidumbres pre/postanalíticas rio Cl íni co 20 15 ABAJO-ARRIBA Y ARRIBA-ABAJO C on gr BOTTOM-UP (GUM) es o ESTIMACIÓN NaU MEDIDA cio COMBINACIÓN n al TOP-DOWN (en desarrollo, validación) CUANTIFICACIÓN DE CADA UNA DE LAS FUENTES u1 u2 u3 u4 u5 u6 DATOS DE LA VALIDACIÓN/CONTROL DEL PROCEDIMIENTO DE MEDIDA de u7 IDENTIFICACIÓN DE TODAS LAS FUENTES CONOCIMIENTO DEL PROCEDIMIENTO DE MEDIDA (en verificación) lL ab or SIMPLIFICACIÓN POR AGRUPAMIENTO DE FUENTES u1 u2 ato rio u3 IMPRECISIÓN u4 u5 SESGO Cl ín COMBINACIÓN ico 20 ESTIMACIÓN U MEDIDA 15 EJEMPLO: MODELO BOTTOM-UP C on gr es oN ac ion Diagrama de Ishikawa = causa-efecto = espina de pez Espectrómetro del instrumento Longitud de onda Procesamiento de los datos Medidas en el instrumento Redondeo Temperatura Anchura de banda Paso de luz Exactitud de las absorbancias Linealidad de las absorbancias al Volumen de muestra y reactivo de lL Tiempos de incubación y lectura Valores aberrantes ab or Interferentes Línea base Extracción de la muestra Lotes de reactivos Temperatura de conservación pH Exposición a la luz Centrifugación… Calibración (factor) Caducidad o estabilidad ato rio Blanco de reactivo Blanco de muestra Sesgo (veracidad) etc… Tratamiento de las muestras Reactivos CONCENTRACIÓN CATALÍTICA de GGT Factores de corrección Cl ín Imprecisión ico 20 15 EJEMPLO GGT: BOTTOM-UP C on gr es de incertidumbre (uncertainty budget) Presupuesto oN ac ion al de lL ab or ato rio Cl íni c Fuentes de incertidumbre Imprecisión Lotes de reactivos Exactitud de las absorbancias 1,00 1,00 Contribución u (%) 0,9310 0,5388 Var (u²) (%) 0,8668 0,2903 1,00 0,4666 0,2177 3,43 0,3965 0,1572 1,00 0,3430 0,1176 1,00 0,1424 0,0203 0,92 0,1225 0,0150 3,12 0,0936 0,0088 Unidad Tipo Origen us cs (%) % % A A Experimental Experimental 0,9310 0,5388 Abs A Certificado 0,4666 Longitud de onda nm B pH Linealidad de las absorbancias Volúmenes de muestra y de reactivo Temperatura % B % A % B ˚C B INCERTIDUMBRE COMBINADA (%) INCERTIDUMBRE EXPANDIDA (%), K = 2. Certificado del 0,1155 patrón Certificado 0,3430 Verificación 0,1424 Especificaciones 0,1336 técnicas Calibración 0,0300 o 2 1,70 3,39 01 5 ISO C 15189:2013, 5.5.1.4 on gr es o NLas incertidumbres de medida se pueden NOTA 2. ac calcular utilizando los valores de la magnitud ion obtenidos por medición de los materiales de control al de la magnitud en condiciones de precisión intermedia de que incluyen tantos cambios de rutina como sean lL abla ejecución normalizada razonablemente posibles en or por ejemplo, cambios de un procedimiento de medida, a tor en los lotes del reactivo y del calibrador, operadores io diferentes, mantenimiento programado del Cl instrumento de medida. íni co 20 15 ABAJO-ARRIBA Y ARRIBA-ABAJO C on gr BOTTOM-UP (GUM) es o ESTIMACIÓN NaU MEDIDA cio COMBINACIÓN n al TOP-DOWN (en desarrollo, validación) CUANTIFICACIÓN DE CADA UNA DE LAS FUENTES u1 u2 u3 u4 u5 u6 DATOS DE LA VALIDACIÓN/CONTROL DEL PROCEDIMIENTO DE MEDIDA de u7 IDENTIFICACIÓN DE TODAS LAS FUENTES CONOCIMIENTO DEL PROCEDIMIENTO DE MEDIDA (en verificación) lL ab or SIMPLIFICACIÓN POR AGRUPAMIENTO DE FUENTES u1 u2 ato rio u3 IMPRECISIÓN u4 u5 SESGO Cl ín COMBINACIÓN ico 20 ESTIMACIÓN U MEDIDA 15 EJEMPLO: MODELO TOP-DOWN C on gr es oN ac ion Espectrómetro del instrumento Longitud de onda Procesamiento de los datos Medidas en el instrumento Redondeo Temperatura Anchura de banda Paso de luz Exactitud de las absorbancias Linealidad de las absorbancias Línea base Volumen de muestra y reactivo al de Tiempos de incubación y lectura lL Valores aberrantes ab or Interferentes Extracción de la muestra Lotes de reactivos Temperatura de conservación Blanco de reactivo ato rio Caducidad o estabilidad Sesgo (veracidad) etc… Tratamiento de las muestras CONCENTRACIÓN CATALÍTICA de GGT Blanco de muestra Exposición a la luz Centrifugación… Calibración Reactivos Factores de corrección Cl ín Imprecisión ico 20 15 FUENTES INCERT.- MODELO TOP-DOWN C on g re interdiaria Imprecisión so Na al calibrador incertidumbre de medida Valor asignado cio Corrección de sesgos na ld Definición del mensurando: el no puede ser cuantificada, pero puede ser reducida La o eliminada mediante la detallada especificación del b mensurando. or a tor particular. No se Interferencias: afectan a muestra oC incluyen en la estimación de la iincertidumbre para muestras típicas de pacientes. Limitación del lín ico procedimiento de medida. 20 15 DEFINICIÓN DEL MENSURANDO C a) b) c) d) e) on g re a medir: proteína, colesterol, Hb, nº Analito so leucocitos. Na Sistema: suero, cio orina, sangre venosa, LCR. na y unidad: concentración de Tipo de magnitud l de concentración catalítica sustancia (mmol/L), lL (nKat/L). ab Procedimiento de medida: solo en o algunos ra casos forma parte de la definición: conc. catalítica, inmunoensayos. tor io forma parte de Material de referencia: solo en algunos casos Cl la definición: UI. íni co 20 15 IMPRECISIÓN C on gr es La mayor parte de los componentes de la o incertidumbre Na de medida de la fase analítica se encuentran contenidos en la estimación de la cio imprecisión interdiaria (CV) que se obtiene empleando n al materiales de control. de Utilizar suficiente nº del Ldatos (por ej. de 6 meses) para recoger las diferentesab fuentes de incertidumbre. or a Incluir varias calibraciones topara recoger la rio de calibración. incertidumbre generada por el proceso Cl Valor del mensurando cercano a losínivalores de co decisión clínica. Habitualmente 2 valores. 20 15 Imprecisión a largo plazo C on 14 12 EMP 10 8 L ím ite d e c o n tr o l ( 1 3 s = 5 ,7 % ) 6 e rro r (% ) grCV = 1,9 %, CV esinicial largo plazo = 2,5 % oN ac ion cambio al corrección de lL ab or ato rio Cl íni co 20 15 4 2 0 -2 -4 -6 -8 -1 0 -1 2 -1 4 0 10 20 sem anas 30 40 VALOR ASIGNADO AL CALIBRADOR C on gr e so Es necesario conocer la incertidumbre y la Nametrológica de los valores asignados a trazabilidad los materialescde ioncalibración que se utilizan. a Si son materiales lcomerciales, el fabricante debe de proporcionar estos datos l L y el factor de cobertura empleado para expresar laaincertidumbre. bo ra valor asignado al La incertidumbre estándar del tor calibrador no debería variar mucho ientre o C lotes. lín Puede ser la principal fuente de incertidumbre ¡¡ ico 20 15 CORRECCIÓN DE SESGOS C on gr se identifican en la validación del Sesgos: e so de medida. Eliminar, corregir o ignorar. procedimiento Na Cuando se corrige cio mediante un factor, la corrección tiene una incertidumbre na asociada (ufc). l d la veracidad, pero aumentan la Las correcciones mejoran el incertidumbre La Los errores sistemáticos bo ocasionados en el uso rutinario del procedimiento rade medida por las t or calibraciones, se diferencias entre las distintas io comportan de forma aleatoria a largo Cl plazo, con lo ínrecoge que este componente de incertidumbre se en el i co CV. 20 15 INCERTIDUMBRE COMBINADA C on gr es mediante las ecuaciones de propagación Se calcula oN del error aleatorio: ac ion alu = s + s + ... de lL a u = CV +bCV or + ... ato r io más complejas: Las ecuaciones pueden ser bastante Cl varias magnitudes de entrada, coeficientes de íni sensibilidad, correlación entre fuentes, … co 20 15 c c 2 p 2 p 2 q 2 q CALCULO DE LA INCERTIDUMBRE C on gr es o N u = CV2 + u 2 + u 2 c cal fc ac ion relativos (%) avalores ld e l Lpara un nivel de confianza Se recomienda expresarla ab del 95% (incertidumbre expandida, Uc). Para ello, se o multiplica el valor de uc por K = r2. ato rio C2l 2 2 Uc = 2 x CVid + ucal + ufc ín ico 20 15 EJEMPLO 1 C on gr es : Hormona del crecimiento en suero Mensurando o sanguíneo,Nµg/L. ac ion Datos: al CVid: 7,3 % de l L la incertidumbre del Calibrador: Se desconoce ab valor asignado. o ra referencias de Error sistemático: No existen t or veracidad asequibles al laboratorio. io Cl Cálculos: íni co Uc = 2 x 7,32 = 15 % 20 15 EJEMPLO 2 C on gr es : Albúmina en orina, mg/L. Mensurando oN Datos: a CVid: 5,7 % c(18 ion mg/L), 3,6 % (57 mg/L) Calibrador: U del valor 1,8 % (k = 2). a u = 1,8/2 = 0,9 % l d el una comparación con un proced. Error sistemático: En L ab lineal, se encontró ES de referencia por regresión or95 %: 0,872 a 0,935). significativo: b = 0,902 (i.c a tor . Se incorporó un fc = 1,11 (1/0,902) u = 100 x (0,935 – 0,872)/4 = 1,6 % io C Cálculos: lín i co 2 2 2 Uc = 2 x 5,7 + 0,9 + 1,6 = 12 % 20 15 cal fc EXPRESIÓN DE LA INCERTIDUMBRE C on gr es Se recomienda expresarla para un nivel de confianza oN del 95% (incertidumbre expandida, k = 2). ac ion de medida: Para un procedimiento al uno o varios niveles de U relativa (%) para de concentración lL abcifras significativas, p.e. Debe expresarse con dos or 4,2%, 16%. ato Para el resultado de la medición: Urio absoluta, p.e. Cl 12,3 ± 1,4 mmol/L íni Mismo nº decimales que resultado. co 20 15 UTILIDAD C on gr es o Nque la exactitud es adecuada para la Asegurar finalidad prevista. ac ionde exactitud U < Requisito al de fuentes de variabilidad. Identificar las principales lL abla significación de un Interpretación objetiva de or cambio entre dos valores consecutivos. ato rio Interpretación objetiva de la significación de un Clde decisión resultado en comparación con un valor íni clínica. co 20 15 REQUISITOS DE EXACTITUD C on g re denominaciones. ¿Quieren decir lo mismo? Distintas so Requisitos Na(requirements) de exactitud ciocalidad analítica Requisitos de namínimas de la calidad analítica Especificaciones ld Objetivos (goals) de ecalidad analítica lL Objetivos para las prestaciones analíticas ab or ato rio Cl íni co 20 15 REQUISITOS Y OBJETIVOS C on gr es Un requisito (no requerimiento) es una necesidad o o N establecida, generalmente implícita u expectativa ac 9000:2005). Es una exigencia. obligatoria (ISO ion Una especificación al es un documento que de establece requisitos. l La Para la autorización-certificación-acreditación bo del laboratorio. ra El diccionario define objetivo (= to meta) como un fin r io una acción o un intento al que se dirige o encamina Cl u operación. íni Para la mejora contínua de la calidad. co 20 15 REQUISITOS/OBJETIVOS EXACTITUD C on Requisitos para: g re Solo sexactitud (incertidumbre, error total) oN Posible también: ac ion Imprecisión al (sesgo) Error sistemático de Establecimiento: No hayl L normas. Si legislación en ab algunos paises. or a tor modelos: Conferencia Milán (2014). Diferentes io 1) Efecto sobre resultados clínicos C l íni 2) Variabilidad biológica co 3) Estado tecnología (CLIA, BAK, Consenso España) 20 15 VARIABILIDAD BIOLÓGICA C on g re de exactitud analítica se relaciona con la El grado so biológica. variabilidad Na mensurandosc con gran variabilidad biológica precisan ion de medida (y viceversa). menor exactitud al de Criterio objetivo. lL abde calidad de los Permite establecer “niveles” or deseable, óptimo. procedimientos de medida: mínimo, ato rio Cl íni co 20 15 VARIABILIDAD BIOLÓGICA: Inconvenientes C on gr es o N biológica tiene inconvenientes para La variabilidad el establecimiento ac de requisitos de exactitud ion el individuo. Varía mucho según al Algunos datos de escasa de fiabilidad. Gran diversidad entrel los La datos publicados. En algunos casos resultan brequisitos or ato excesivamente laxos y otros excesivamente rio estrictos. Cl íni co 20 15 ERROR TOTAL: Ejemplos C on g re actual tecnología EAT: Estado so Na VB (des) cio na Calcio 2,4 ld Glucosa el 6,9 La Hierro b31o r Sodio 0,9 Alanina aminotransferasa 32 Albúmina 3,9 EAT CLIA EAT Ale EAT Esp 10 11 10 10 16 10 20 14 21 6,1 5,0 C23l ín 20 at3,2 or io 20 10 23 ico14 20 15 REQUISITOS/OBJETIVOS: ¿Para qué? C on g En el rdesarrollo de un nuevo sistema de medida e so Na En validación/verificación procedimiento de medida cio En el control interno na l d de aceptación de los En EQAS como criterio el resultados de un laboratorio: La Usar el criterio definido bo por los organizadores. ra tor io Cl íni co 20 15 REQUISITOS DE EXACTITUD C on gr es oN no legales legales lab no cert/acred a ISO lab cert/acred ISO cio REQUISITOS na ALERTA NO CONFORMIDAD l INCUMPLIMIENTO SANCIONES de lL ab or cont. calidad ato verificación/validación (verificaciones) rio Cl nuevos proced nuevos proced íni resultados medida asequibles medida lab co muestras 20 15 REQUISITO DE EXACTITUD C on gr Error e máximo so permitido (EMP): Forma de expresar la exactitud Narequerida c ion médica de un resultado, es Para la interpretación al es sistemático o aleatorio o irrelevante si el error de mezcla lL ab no contienen errores Asegurar que los resultados o ra Errores inferiores iguales o superiores al máximo. tor inmediatas. son tolerables y no exigen acciones io Cl Valor relativo porcentual íni co 20 15 CONSIDERACIONES SOBRE EL EMP C on gr No eseel soerror habitual (en la mayoría de los resultados Nes muy inferior) ac ion tendrán un error de medida Muy pocos resultados superior al máximoalpermitido de lL No escoger valores innecesariamente estrictos: ab orencontrar un Más difícil (o inviable) será procedimiento de medida conatlas or prestaciones io necesarias C Los procedimientos de control serán lmás íni complejos (o inviables) co 20 15 ALBÚMINA SUERO C on gr : 5, regla: 1 , pFR: 0,3 % es oN ac ion al de lL ab or ato rio CV: 2 %, 3s 14 12 E M P = 1 0 % ( C L IA ) 10 8 13s = 6 % e rro r (% ) 6 4 2 0 -2 -4 -6 -8 -1 0 -1 2 -1 4 0 10 20 sem anas 30 Cl ín ico 40 20 15 ALBÚMINA SUERO C on gr : 2, regla: 1 , pFR: 4,5 % es oN ac ion al de lL ab or ato rio CV: 2 %, 2s 14 12 10 8 12s = 4 % e rro r (% ) 6 4 2 0 -2 -4 -6 E M P = 3 ,9 % (V B d e s ) -8 -1 0 -1 2 -1 4 0 10 20 sem anas 30 Cl ín ico 40 20 15 CONSECUENCIAS (ISO) C on gr es oN aconforme cio na ld resultados el control entregar result pacientes concesión La tratar corregir bo repetir r at no conforme or io Cl acción correctiva íni co 20 15 ACCIONES C on gr es oN ac seleccionar un procedimiento ion de medida al d el validar el procedimiento de medida La bo seleccionar las reglas de control interno r establecer el requisito de exactitud (error de medida máximo permitido) seleccionar el procedimiento de control externo utilizar el procedimiento de medida y el control interno y externo ato rio acción correctiva Cl ín ico 20 15 no conformidades REQUISITOS Y OBJETIVOS C on gr es EMP: requisito de exactitud laboratorios certificados o oN acreditados. ac Cualquier evidencia ion de error > EMP: "no conformidad". a l d de la tecnología". Basado en el "estado el La de calidad analítica: Especificaciones u objetivos bo del procedimiento de indicación del "nivel de calidad" r ato medida. rio Su incumplimiento ocasional no genera Cl una "no conformidad". íni co En base a la variabilidad biológica. 20 15 Co ng re so Na cio n al de lL ab or ato rio Cl ín ico 20 15