Descargar Archivo
Anuncio

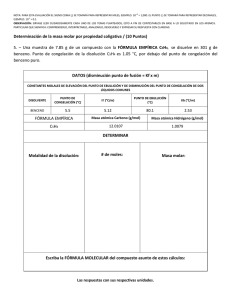
Prof. Coordinadora Eliana Guerrero F. GUIA PROPIEDADES COLIGATIVAS 2016 Nombre: _____________________________ Curso: 2°________ Fecha: _____________ Aprendizajes Esperados: Describir investigaciones científicas clásicas o contemporáneas relacionadas con las propiedades coligativas. Explicar las relaciones entre la temperatura y la concentración de las soluciones, y algunos de sus usos tecnológicos. Explicar las relaciones existentes entre la presión y la concentración de las soluciones, y algunos de sus usos tecnológicos. FÓRMULAS Descenso de la presión de vapor. PA = P°A x XA PB = P°B x XB Pdisolución = PA + PB ΔP =Xs x P0 ΔP = Descenso de la presión de vapor. Xs = Fracción molar del soluto. P0 = Presión de vapor del disolvente puro. Ascenso ebulloscópico ΔTe = P. eb disolución – P. eb solvente puro = Ke x m ΔTe = Ascenso ebulloscópico (ºC ó K). Ke = Constante ebulloscópica (K·kg·mol-1). M = Molalidad del soluto (mol·kg-1). Descenso crioscópico ΔTc = P.c. solvente puro – P.c. solución = Kc x m ΔTc = Descenso crioscópico (ºC ó K). Kc = Constante crioscópica (K·kg·mol-1). m = Molalidad del soluto (mol·kg-1). Presión osmótica π = nRT V ó π = MRT π = Presión osmótica (atm). V = Volumen de disolución (L). n = Mol de soluto (mol). R = Constante de los gases (0,082 atm·L·mol T = Temperatura absoluta (K). M = molaridad(mol/L) 1 1. La siguiente figura, muestra dos líquidos A y B que se encuentran en recipientes abiertos, pero a su vez éstos se encuentran en un sistema cerrado como lo indica la situación 1. Al cabo de un tiempo el sistema presenta la situación 2. Con respecto a la presión, es correcto concluir que: 1) ___________________________________________________________________________ 2. Van’t Hoff, estaba fuera de los círculos más representativos en la Química del XIX, pues daba clase en una escuela veterinaria de Utrech, en Holanda. Sin embargo, llegó a ser el primer premio Nóbel de Química. Aunque Dalton en 1804, hizo las primeras gráficas de variación de presión vapor con la temperatura, se le atribuye a Van’t Hoff su divulgación. Si te dan las curvas de 3 conocidos disolventes: agua, benceno y etanol. Con respecto a cada solvente es correcto concluir que: 1) ________________________________________________________________________ 2) ________________________________________________________________________ 3) ________________________________________________________________________ 3. Si te dicen que las presiones de vapor de 3 disolventes A, B y C, a 50 ºC, son 0,5; 1 y 1,5 atm, respectivamente, en condiciones normales, ¿cuál es el estado físico de cada solvente? Solvente A: ___________________________________________________________________ Solvente B: ___________________________________________________________________ Solvente C: ___________________________________________________________________ 2 4. Von Babo en 1847, encontró que al agregar una sal al agua, tenía lugar un descenso relativo en la presión de vapor de la disolución, respecto a la del disolvente puro, que siempre se mantenía constante a cualquier temperatura, sin embargo no fue capaz de encontrar una relación para dicha constante. Wüllner en 1856, determinó que dicha constante era una expresión de la concentración que hoy se refiere a la a) molaridad b) molalidad c) fracción molar d) normalidad 5. Se tienen cuatro soluciones de glucosa en agua acuerdo a la siguiente tabla: Solución W X soluto 0,019 Q 0,024 P 0,021 H 0,06 a) ¿Cuál solución presenta mayor y menor presión de vapor? b) ¿Cuál es la fracción molar para el solvente de la solución Q? 6. Calcula los puntos de ebullición y congelación de una solución que contiene 2,0 g de azúcar (C2H22O11) disueltos en 100 g de agua. Ke del agua es 0,512 °C. R: 100,0296 °C y -0,10788 °C 7. Calcula el punto de congelación y de ebullición de una disolución 0,30 m de naftaleno en benceno (datos: Kc benceno = 5,12 °C/mol; Pc benceno = 5,50 °C; Ke benceno = 2,53 °C/mol; Pe benceno = 80, 10 °C). R: 3,97 °C y 80,86 °C 8. Calcula la presión de vapor a 20 °C de una disolución que contiene 50 g de metanol en 250 g de etanol. Las presiones de vapor del metanol y el etanol 20 °C son 95 mm Hg y 45 mm Hg respectivamente. R: 56,15 mm Hg 9. La presión de vapor del agua pura a 25 °C es 23,76 mm Hg. Calcula el descenso de la presión de vapor del agua en una disolución de 34,2 g de azúcar en 450 g de agua. R: 23,66 mm Hg 10. Calcula el punto de ebullición del almíbar formado por 50 g de azúcar en 100 g de agua. Ke agua se de 0,512 °C. R: 100,74 °C 11. Calcula el punto de congelación del almíbar mencionado en el ejercicio 5. R: -2,7156 °C 12. En un experimento se desea obtener la masa molecular de un producto sintético. Para ello se prepara una disolución de 2,0 g de este compuesto en 50,0 g de benceno. Tras una operación simple, se obtiene el punto de congelación de la disolución igual a 4,5 °C. ¿Cuál es la masa molecular del producto sintético? Kc benceno =5,10 °C R: 226 g/mol 13. Un investigador sintetiza suero para inmunizar animales de experimentación frente a una enfermedad. El suero contiene una proteína X de concentración 0,010 M a 20 °C. Calcula la presión osmótica de la solución. R: 0,24 atm. 14. Un grupo de alumnos de química desea obtener la masa molecular de la hemoglobina presente en la sangre. Para ello preparan una solución con 3,2 g de hemoglobina en suficiente agua hasta alcanzar 250 mL. enseguida miden la presión osmótica de la solución obteniendo un valor de 3,6 mm Hg a 25 °C. Calcula la masa molecular de la hemoglobina. R: 66,554 g/mol 15. Un radiador de un automóvil tiene una capacidad de 7 L de agua. ¿Qué masa de anticongelante etilenglicol (C2H4 (OH)2) debiera agregarse al agua para qué esta se mantenga líquida hasta los 5 °C? R: 1167 g 16. ¿cuál es la presión osmótica en una disolución acuosa de un hidrato de carbono 0,3 M a 25 °C R: 7,33 atm. 17. Determine el valor de la Kc del agua sabiendo que al disolver 0,146 g de CCl3CHO en 13,0 g de agua se obtuvo un punto de congelación de - 0,14 °C R: 1,86 °C 3