Tema 2
Anuncio

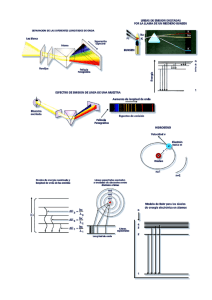
Química Orgánica General Dra. Maribel Plascencia Jatomea Departamento de Investigación y Posgrado en Alimentos, DIPA Laboratorio de Microbiología y Micotoxinas 3er piso, Edificio 5P “Dr. Manuel Sánchez Lucero” E-mail: [email protected] Capítulo 2: Hibridación y enlaces Distribución electrónica Enlaces Hibridación Naturaleza de los enlaces químicos Si se conoce la naturaleza de los enlaces en una molécula, se pueden hacer muchas predicciones acerca de sus propiedades físicas y químicas. La forma en que una sustancia se comporta esta directamente relacionada con los átomos que contiene y con la forma en que dichos átomos están conectados. Para comprender las propiedades y reacciones de los compuestos orgánicos se debe empezar por comprender su estructura. En 1924, el físico francés Louis de Broglie sugirió que los electrones, además de ser partículas, también tenían propiedades de ondas. Dos años después, Erwin Schrodinger expresó la energía de un electrón en un átomo de hidrógeno en términos de una ecuación de onda con una serie de soluciones llamadas funciones de onda, que se simbolizaban por la letra griega (psi). La posición exacta de un e- no puede localizarse sin certeza, aunque la probabilidad de encontrar un e- en un determinado punto viene dada por el cuadrado de la función de onda (2) en ese punto. A partir de la ecuación de Schrodinger es posible determinar la probabilidad de encontrar un e- en un determinado punto en el espacio. Orbital atómico Es una región del espacio donde existe una alta probabilidad (superior al 90%) de encontrar un electrón. Esto supone considerar al electrón como una nube difusa de carga alrededor del núcleo, con mayor densidad en las zonas donde la probabilidad de que se encuentre dicho electrón es mayor. Los orbitales se describen especificando su tamaño, forma y orientación en el espacio. Repasar Orbital atómico s de forma esférica y simétrica alrededor del núcleo. La forma se obtiene al hacer girar la sección transversal alrededor de su diámetro. Orbital atómico p de forma ovoide; sus ejes son perpendiculares entre si, por lo que se localizan en los ejes x, y y z de las coordenadas cartesianas, con un orbital por eje, y se denominan orbitales px, py y pz, respectivamente. Cada ovoide doble constituye un solo orbital p. La ecuación de Schrodinger describe también otros orbitales posibles, tales como los orbitales atómicos d, f, g y h. Repasar Orbitales s. El tamaño del orbital s aumenta al aumentar el número cuántico principal (n). Generalmente se representan los límites de los orbitales atómicos de Schrödinger de manera que el orbital englobe al 90% de la distribución de densidad electrónica. En el caso de los orbitales s la representación es una esfera, de mayor radio cuánto mayor sea n. Repasar Orbitales p La forma de los orbitales p es de dos lóbulos situados en lados opuestos al núcleo y con un nodo en él. Hay tres tipos de orbitales p ( ; ml= -1,0,1) que difieren en su orientación. No hay una correlación simple entre los tres números cuánticos magnéticos y las tres orientaciones: las direcciones x, y y z. Los orbitales p del nivel n se denominan npx, npy, npz Los orbitales p al igual que los s aumentan de tamaño al aumentar el número cuántico principal. Repasar Orbitales d En el tercer subnivel tenemos 5 orbitales atómicos (para n>3 l =2; ml=-2,-1,0,1,2) con diferentes orientaciones sen el espacio. Aunque el orbital 3dz2 difiere en su forma de los otros cuatro, los cinco orbitales d tienen todos la misma energía. Otros orbitales de mayor energía Repasar Para n>4 hay 7 orbitales f ( =3 y ml=-3,-2,-1,0,1,2,3) . Los orbitales f son importantes para comprender el comportamiento de los elementos con número atómico mayor a 57. Para valores de >4 se tienen los orbitales g y subsiguientes (a partir de f sigue el orden alfabético de las consonantes). En química general nos bastará con los orbitales s, p y d para comprender las propiedades de los elementos. Uno de los orbitales f Hay 6 orbitales f más Además de estar cargados negativamente, los eposeen la propiedad del espín. El número cuántico de espín de un e- puede tener un valor de +½ o –½. De acuerdo con el principio de exclusión de Pauli, dos e- pueden ocupar un mismo orbital sólo cuando tienen espines opuestos, también llamados “apareados”. Cuando se llenan los orbitales 2p, los e- van ocupando distintos orbitales uno a uno antes de que haya un orbital ocupado con dos eEste es un principio general para los orbitales de la misma energía que se conoce como la regla de Hund. Una vez llenos los orbitales 2s y 2p, el siguiente nivel es el 3s, seguido de los orbitales 3px, 3py y 3pz. Los e- de estos orbitales se encuentran más lejos del núcleo que los de los orbitales 2s y 2p y tienen mayor energía. Número de electrones en el orbital indicado Elemento Hidrógeno Número atómico 1 1s 2s 2px 2py 2pz 3s 1 Helio 2 2 Litio 3 2 1 Berilio 4 2 2 Boro 5 2 2 1 Carbono 6 2 2 1 1 Nitrógeno 7 2 2 1 1 1 Oxígeno 8 2 2 2 1 1 Flúor 9 2 2 2 2 1 Neón 10 2 2 2 2 2 Sodio 11 2 2 2 2 2 1 Magnesio 12 2 2 2 2 2 2 Configuración electrónica Explica cómo los electrones se distribuyen entre los diversos orbitales en un átomo Número de electrones en el orbital o subnivel 1s1 Número cuántico n Momento angular del número cuántico l Diagrama de un orbital ●- H + 1s1 Tarea 1. Ejercicios de configuración electrónica Fecha de entrega: martes 04 de febrero de 2014 1. Escriba a) la configuración electrónica de: Radio b) 74W c) 94Pu d) 52Te2- e) 78Pt2+ Tarea 1. Continuación… Fecha de entrega: martes 04 de febrero de 2014 2. Escriba la configuración electrónica de: Sr, Cr, I, Cl. Clasifique y explique a qué grupo, período y bloque de la tabla periódica pertenece cada uno. 3. ¿Cuál de estas especies tiene más electrones desapareados: a) 16S+ b) 16S c)16S- 4. Defina electronegatividad y compare valores para los elementos: Cr-, As-, Br. Justifique su respuesta. 5. Dados los siguientes pares de especies químicas: a) Fe3+ y Mn2+ b) Ca y Mg, c) S y Cl, d) Cl- y Br-, e) Cl y Cl- Explique en cada par, qué entidad química tiene mayor tamaño atómico y/o tamaño iónico. 6. Considere los átomos de 31Ga y 17Cl a) Justifique la ubicación de c/u de dichos átomos en la tabla periódica b) Los valores de los radios atómicos son 99 y 125; explique cuál corresponde al Ga y cuál al Cl. Enlace químico Definición: es la unión entre átomos de un compuesto, es decir, cuando 2 átomos se aproximan lo suficiente es posible que los e- de sus capas más externas interaccionen, produciéndose una combinación que da como resultado que los átomos se unan. Formación de la molécula de flúor Formación del Enlace Un enlace resulta de un traslape de orbitales atómicos en átomos vecinos •• H + •• • • Cl •• H • • Cl •• Traslape de H (1s) y Cl (2p) Cada átomo tiene su electrón desapareado Tipos de Enlaces Enlace Iónico Iones con cargas opuestas son atraídos mediante fuerzas electrostáticas Enlace Covalente Covalente Polar Covalente No Polar Enlace Metálico La gran mayoría de los compuestos orgánicos están unidos a través de enlaces coovalentes El tipo de enlace puede calcularse encontrando la diferencia de electronegatividad de 2 átomos enlazados Electronegatividad: mide la atracción de un átomo hacia los electrones de un enlace. ELECTRONEGATIVIDAD • Rangos de 0.7 a 4.0, • Valores grandes: tendencia a ganar electrones. H 2.1 Li 1.0 Na 0.9 Be 1.5 Mg 1.2 K 0.8 Rb 0.8 Ca 1.0 Cs 0.7 Fr 0.7 Ba 0.9 Ra 0.9 Cl 3.0 Br 2.8 He Ne Ar Kr - I 2.5 At 2.2 Xe Rn - F 4.0 Ti 1.5 Cr 1.6 Fe 1.8 Sr 1.0 Menor electronegatividad Ni 1.8 Zn 1.8 As 2.0 Mayor electronegatividad Diferencia de Electronegatividad Si la dif. de Electronegatividad es: 1.7 a 4.0: Iónico 0.4 a 1.7: Covalente Polar 0.0 a 0.3: Covalente No Polar Ejemplo: NaCl Na = 0.9, Cl = 3.0 Diferencia: 2.1 Es un enlace iónico Grupo funcional Conjunto de átomos unidos en una forma determinada y con propiedades características. Estructura Nombre de la de la clase clase R-H Alcano CH3CH3 Etano RCH=CHR Alqueno CH2 ━ CH2 Etileno RC ≣ CR Alquino HC ≣ CH Acetileno RX Halogenuro de alquilo CH3CH2Cl Cloruro de etilo RCOOH Ácido carboxílico CH3COOH Ácido acético RCHO Aldehído CH3CHO Acetaldehído RCOR Cetona CH3COCH3 Acetona ROH Alcohol CH3CH2OH Alcohol etílico ROR Éter CH3CH2OCH2CH3 Éter etílico RNH2 Ejemplo Nombre del ejemplo Amina CH3CH2NH2 Etilamina RCOOR’ Éster CH3COOCH2CH3 Acetato de etilo RCONH2 Amida CH3CONH2 Acetamida RCOX Halogenuro de ácido CH3COCl Cloruro de acetilo Para mayor claridad: En las fórmulas estructurales, los electrones (e-) de la capa de valencia (la exterior) se representan con puntos. El número de e- en la capa de valencia del átomo es igual al número de la familia (columna), tal como aparece en la tabla periódica de los elementos. CONFIGURACIONES ELECTRÓNICAS Y ELECTRONES DE VALENCIA Para formar compuestos covalentes estables es necesario que se combine un número apropiado de átomos de elementos diferentes o del mismo elemento, de tal manera que haya dos e- alrededor del H y ocho e- alrededor del C, O, N o F. Comúnmente habrá también ocho ealrededor del S, Cl, Br y I. Existen compuestos en los que hay más de ocho e- en la capa de valencia (Ejemplos: SF6, ClF3, BrF3 y ICl3), aunque la mayoría de los compuestos orgánicos tiene ocho e- en la capa de valencia de los átomos participantes. Disposición de los átomos de carbono en: Diamante Grafito Enlace covalente En 1816, G.N. Lewis sugirió el modelo de enlace químico covalente o de pares de electrones compartidos. Propuso que la compartición de dos electrones por dos átomos de hidrógeno permitía a cada uno tener la configuración electrónica estable de capa llena análoga al helio (He2). Dos átomos de hidrógeno, cada uno con un solo electrón Molécula de hidrógeno: enlace covalente formado por un par de electrones compartidos Las fórmulas estructurales en dónde los electrones se representan por puntos, se denominan estructuras de Lewis. En el flúor, el enlace covalente proporciona a cada átomo de flúor ocho electrones en su capa de valencia y una configuración electrónica estable, equivalente a la del gas noble neón: De acuerdo al modelo de Lewis, los elementos de la segunda fila de la tabla periódica, Li, Be, B, C, N, O, F, Ne, están limitados hasta un total de ocho electrones (compartidos y no compartidos). El hidrógeno está limitado a dos. Regla del octeto Al formar un compuesto, los elementos ganarán, perderán o compartirán electrones para dar la configuración electrónica estable, caracterizada por ocho electrones de valencia. La mayoría de los elementos obedece a ésta regla. Aproximación de Lewis para compuestos orgánicos como el metano y el tetrafluoruro de carbono: Metano: CH4 Tetrafluoruro de carbono: CF4 Si la estructura es un ión, se agregan o eliminan electrones para darle la carga apropiada. Ejemplos: ClO3- CO32- Excepciones a la regla del octeto Los átomos de los elementos que se encuentran después del segundo periodo de la tabla periódica, pueden acomodar más de ocho e- en su capa externa. Ejemplos: PCl5 y SF6 Algunas moléculas o iones sumamente reactivos tienen átomos con menos de ocho e- en su capa externa. Ejemplo: BF3 (trifluoruro de boro) Definición de enlace covalente: Es aquel que se forma cuando dos átomos comparten un par de electrones y se representa mediante un par de puntos o, simplemente mediante un guión. Ejemplos: Cloruro de hidrógeno Agua El átomo de azufre aporta ambos electrones para su unión con dos de los átomos de oxígeno. En el ácido sulfúrico y en la mayoría de los ácidos que tienen oxígeno, el hidrógeno se encuentra unido a un átomo de oxígeno y no al átomo central, es decir, el azufre en el caso del ácido sulfúrico. Es necesario tener dobles enlaces para que cada uno de los tres átomos complete su capa de valencia. Formación de enlaces covalentes y orbitales moleculares Los orbitales atómicos pueden tener uno o dos electrones. A su vez, dos átomos en que cada uno tenga un orbital con un e-, pueden combinar sus orbitales atómicos formando un orbital molecular. Formación del enlace covalente: se forma cuando dos átomos, A y B, se acercan lo suficiente y en la dirección adecuada para que el e- no apareado del átomo A sea atraído fuertemente por los núcleos de ambos átomos. Al mismo tiempo, el e- no apareado del átomo B es atraído fuertemente por los núcleos de los átomos A y B. Entonces, el orbital atómico de uno de los átomos se superpone al del otro átomo, produciéndose un enlace covalente. En un enlace covalente, cada átomo contribuye con un electrón para formar el orbital molecular. Orbital molecular: región en el espacio que rodea ambos núcleos y en la cual hay la mayor probabilidad de encontrar un par de e- de unión. Generalmente se representa como una nube de carga negativa que envuelve los dos núcleos; la nube representa dos e-. Formación de un orbital molecular de la molécula de H2 a) Orbitales atómicos de dos átomos de hidrógeno. b) Superposición de dos orbitales atómicos. c) Orbital molecular de la molécula de hidrógeno. Cada uno de los dos e- de este orbital molecular puede encontrarse en un momento dado, en cualquier parte del mismo. Ambos e- son atraídos por los dos núcleos mediante una fuerza electrostática. Polaridad de los enlaces y moléculas. En los enlaces covalentes, los e- no se comparten necesariamente en la misma medida por los átomos que se conectan. Si uno de los átomos atrae a los e- hacia sí con mayor fuerza que el otro, entonces la distribución de los e- esta polarizada y se denomina enlace covalente polar. Moléculas polares: Son aquellas que tienen un extremo positivo y otro negativo. Para que una molécula sea polar, debe tener uno o más enlaces polares y éstos deben estar distribuidos de tal manera que su resultante dé centros positivos y negativos separados, en la molécula. Orientación de moléculas polares: (a) sin campo eléctrico; (b) con campo eléctrico. El HF tiene un enlace covalente polar. El F atrae a los e- con mayor fuerza que el H. El centro de la carga (-) en la molécula está más cerca del F, mientras que el centro de la carga (+) está más cerca del H. Esta polarización de la densidad electrónica en el enlace H-F se presenta de varias formas: El CO2 tiene dos enlaces polares C-O, pero la molécula no es polar. Esto se debe a que la molécula de CO2 es lineal y el centro de las dos cargas negativas coincide con el centro de la carga positiva (el átomo de carbono). La molécula de H2O tiene dos enlaces polares O-H; además, el ángulo de enlace del O en la molécula es de 105° y el centro de la carga positiva se encuentra entre los átomos de H. El centro de la carga (+) y (-) no coinciden, por lo que la molécula es polar. Ejemplo de enlace covalente polar: HCl. El átomo de Cl, con su mayor electronegatividad, atrae a los e- enlazantes más cerca de él. Esto hace que el átomo de H esté algo deficiente de e- y le de una carga positiva parcial (+). El átomo de Cl se hace parcialmente rico en e- y por lo tanto tiene una carga negativa parcial (-). La dirección de la polaridad de un enlace polar algunas veces se representa como En el HCl esto se expresa de la siguiente forma: Electronegatividad: tendencia de un átomo para atraer hacia él los e- en un enlace covalente. Un elemento electronegativo atrae los e-, mientras que un átomo electropositivo los cede. La electronegatividad aumenta a lo largo de un periodo en la tabla periódica (en la 2da fila, el elemento más electro(-) es el F y el más electro(+) es el Li. La electronegatividad disminuye al bajar en el grupo, por lo que el F es más electro(-) que el Cl. Cuando los centros de las cargas (+) y (-) están separados uno de otro, constituyen un dipolo. La polaridad de una molécula se expresa, generalmente, mediante el momento dipolar, , que es función del producto de las cargas por la distancia entre éstas. La unidad es el Debye, D. = carga x distancia Las moléculas que no tienen momento dipolar se llaman moléculas No Polares. Polaridad de los enlaces Un enlace covalente será polar si une átomos que difieren en su tendencia a atraer electrones, es decir, que difieren en electronegatividad. Cuanto mayor sea la diferencia en electronegatividad, más polar será el enlace. De los elementos que encontraremos en química orgánica, la electronegatividad más elevada la presenta el F > O > N > Cl > Br > C. El H no difiere mucho del C, no se sabe con certeza si es más electronegativo o menos. Las polaridades de los enlaces están íntimamente ligadas tanto a las propiedades físicas como a las químicas. La polaridad de los enlaces puede conducir a polaridades de moléculas, afectando considerablemente a los puntos de fusión y ebullición, y a la solubilidad. La polaridad también determina el tipo de reacción que puede suceder en ese enlace, e incluso afecta a la reactividad de los enlaces cercanos. Hibridación Formación de las moléculas de metano (CH4), etileno (CH2=CH2) y acetileno (CH3≡CH3) Hibridación del carbono sp3, sp2, sp. Si se considera que los enlaces covalentes entre los elementos de menor peso atómico se forman por la superposición de orbitales s y p, se puede suponer que las propiedades de estos enlaces no serán las mismas que las de los orbitales que las formaron. Se puede establecer una buena correlación con las propiedades reales si la formación de los orbitales moleculares se describe en términos de orbitales atómicos híbridos. Orbitales atómicos híbridos Resultan de la combinación de las propiedades de los orbitales s, p, d y f. La mayoría de las moléculas orgánicas se pueden describir satisfactoriamente usando solo tres de estos orbitales híbridos, el sp3, sp2 y sp. Orbital híbrido sp3: combinación apropiada de las descripciones matemáticas de un orbital s y tres orbitales p. Orbital sp2: híbrido de un orbital s y dos orbitales p. Orbital sp: híbrido de un orbital s y un orbital p. Los orbitales atómicos del mismo átomo se combinan para formar orbitales híbridos. ¿Por qué? Porque los orbitales híbridos son más direccionales, además de que tienen interacciones de enlaces más efectivas. Los elementos de la segunda fila hibridizan usando sus orbitales s y p ( sp, sp2, sp3). Formación de orbitales híbridos sp3 metano (CH4) El C tiene un e- no apareado en cada uno de los dos orbitales p, por lo que se espera que forme el compuesto CH2. (Lo forma, pero el CH2 es una molécula altamente reactiva cuyas propiedades se centran en torno a la necesidad de procurarle al carbono dos enlaces adicionales). Los e- de valencia de un átomo de C (que se usan en el enlace) son los de nivel externo, es decir, los e- 2s y 2p. Para disponer de cuatro e- no apareados, se promueve uno de los e- 2s a un orbital p vacío: Forma de los orbitales de valencia del carbono: Existe un electrón en cada uno de los orbitales. Disposición de los cuatro átomos de hidrógeno del metano: En la formación de los orbitales híbridos sp3 intervienen un orbital s y tres orbitales p. H H C H H La configuración electrónica del átomo de carbono en el momento de combinarse sería: 1s2 2(sp3)4 Los 4 orbitales sp3 deben orientarse en ángulos de 109.5° uno respecto del otro. Presencia de enlaces sigma. La disposición espacial de los orbitales sp3 es aquella que les permite separarse al máximo. Se dirigen hacia los vértices de un tetraedro regular. El ángulo entre dos orbitales cualesquiera es el tetraédrico, de 109.5º Orbitales híbridos sp3. (a) Corte transversal y forma aproximada de un orbital aislado, dirigido a lo largo de un eje. (b) Representación de esfera, con omisión del pequeño lóbulo posterior. (c) Cuatro orbitales, con ejes dirigidos hacia los vértices de un tetraedro. Condiciones para que exista hibridación: Los orbitales que se hibridan deben de tener energías muy próximas. La energía liberada en la formación de enlaces con los orbitales hibridados debe ser superior a la energía que se liberaría en la formación de los mismos enlaces con los orbitales sin hibridar, y la diferencia debe ser mayor que la energía consumida en la hibridación. Al cumplirse estas condiciones se favorece la formación de orbitales híbridos, pues las estructuras resultantes son más estables. Formación de orbitales híbridos sp2 Etileno (CH2=CH2) En la formación de dobles enlaces, el C adopta la hibridación trigonal, sp2. Como indica su denominación, en la hibridación sp2 intervienen un orbital s (el 2s) y dos orbitales p (los 2px y 2py). Los orbitales híbridos se disponen en un plano formando ángulos de 120°, siendo el conjunto perpendicular al orbital 2pz que queda sin hibridar. hibridación H H C = C H H La configuración electrónica del carbono en el momento de combinarse sería: 1s2 2(sp2) 2pz1 Este tipo de hibridación se da en los casos de formación de doble enlace carbono-carbono, por ejemplo, en la molécula de etileno. . Formación de orbitales híbridos sp Acetileno (CH≡CH) Hibridación diagonal sp. Como indica su nombre, en ella intervienen un orbital s (el 2s) y otro p (el 2py). Los orbitales híbridos se disponen alineados formando ángulos de 180°, y dirigidos según el eje OY. Los orbitales 2px y 2pz que no intervienen en la hibridación conservan su forma y posición. El enlace triple es aún más reactivo que el doble enlace debido a la presencia de los dos enlaces . hibridación H-C ≡ C-H Configuración electrónica del carbono en el momento de combinarse: 1s2 2(sp)2 2px1 2pz1 Este tipo de hibridación se da en los casos de formación de triple enlace: carbono-carbono, por ejemplo, en la molécula de acetileno. En el triple enlace C-C, uno de los enlaces es un enlace (2sp-2sp) y los otros dos son enlaces (2px-2px y 2pz-2pz). Debido a la hibridación sp, el acetileno es una molécula lineal con ángulos de enlace H-C-C de 180º. Preguntas generadoras: ¿Por qué es necesario hacer una clasificación de compuestos? ¿Qué entiende por grupo funcional? ¿En que parte de la molécula se llevan a cabo las reacciones?