Tema_3 - Informer Salamanca
Anuncio

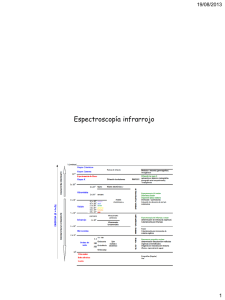
TEMA 3. ESPECTROFOTOMETRÍA DE ABSORCIÓN EN EL INFRARROJO. 3.1. REGIONES DEL ESPECTRO INFRARROJO Y CARACTERÍSTICAS GENERALES. Subdivisiones habituales del espectro infrarrojo. Región. Infrarrojo próximo (NIR). Longitud de onda (𝝀) en µm 0.714 a 2.50 (710 a 2500 nm) Infrarrojo medio o 2.50 a 25 fundamental (MIR). (2500 a 25000 nm) (2.5 a 25)10-4cm Infrarrojo lejano (FIR). 25.0 a 100 (2.5·10-4 a 0.1cm) Numero de onda (𝝂̅) en cm-1. 14000 a 4000 4000 a 400 400 a 100 (transf.Fourier) Tránsitos energéticos (aplicación). Vibraciones de tensión de los H (análisis cuantitativo) 260·10-21J 80·10-21J Esp. vibracionales Vibraciones en general (análisis cualitativo y cuantitativo de grupos funcionales) 80·10-21J 8·1021J Esp. Vibracionales Vibraciones de esqueleto (moléculas grandes) 8·10-21J 2·10-21 Esp. Vibracionales 𝑬 = 𝒉 · 𝝂 = 𝒉 · 𝒄⁄𝝀 = 𝒉 · 𝒄 · 𝝂̅ Regiones del espectro Un aumento del número de onda significa un aumento en la energía. 21 Algunas generalidades de la espectroscopia IR. Al analizar un espectro IR con el objeto de obtener información estructural resultan útiles las siguientes indicaciones: 1. Analizar el espectro en orden decreciente de número de ondas buscando inicialmente la presencia de grupos funcionales. 2. La significación de una banda depende tanto de la región espectral donde se encuentra como de la intensidad. Así una banda, aún débil, en la región más cercana a 200cm-1 es una fuerte indicación de la presencia de triples enlaces en la molécula. Por otra parte la presencia de una banda aun de intensidad media o fuerte en la región 1300-1000 cm-1 puede carecer de utilidad en la determinación estructural. 3. La ausencia de bandas de una región puede ser un criterio de utilidad equivalente a la presencia de las mismas. 4. Deben tenerse en cuenta siempre las condiciones de registro de un espectro IR. Así, para los espectros registrados en solución deben eliminarse del análisis las zonas de fuerte absorción del disolvente. Lo mismo es válido por los espectros registrados en suspensiones, donde deben excluirse las bandas asociadas con el agente dispersor. La región infrarroja (IR) del espectro electromagnético abarca una radiación con valores de numero de onda (𝜈̅ ) que varían aproximadamente de1400 a 33 cm-1, o de longitudes de onda (𝜆) entre 0.75 y 300 µm. No obstante la mayoría de las medidas que se emplean en el IR se han limitado a la región que va de 4000 a 670 cm-1 (25 a 15 µm), IR medio o fundamental. La espectroscopia IR se usa a menudo para la identificación de compuestos orgánicos, ya que sus espectros son generalmente complejos y proporcionan numerosos máximos y mínimos, que pueden emplearse con fines de comparación. El espectro de absorción IR de un compuesto orgánico representa una de sus propiedades físicas casi única. Con la excepción de los isómeros ópticos, no hay dos compuestos que presenten curvas de absorción idénticas. Además de su aplicación en el análisis cualitativo, la espectroscopia IR se emplea también en análisis cuantitativo (de menor importancia que aquel). 3.2. Aspectos teóricos de la Absorción Infrarroja. En un espectro de IR a diferencia del ultravioleta y visible (UV-vis), se observa gran variedad de máximos y mínimos. Los datos IR, suelen representarse gráficamente con % de transmitancia (%𝑇) en lugar de la absorbancia (A), como es la corriente. Además, muchos investigadores optan por usar la unidad de cm recíprocos (cm-1) para la abscisa, en lugar de la longitud de onda (cm, µm y nm). 22 Esta preferencia se sustenta en que considerando la ecuación: 𝐸 = ℎ · 𝑐 · 𝜈̅ = ℎ · 𝜈 Se aprecia proporcionalidad directa entre el número de onda (𝜈̅ ) y la energía, así como la frecuencia de la radiación (𝜈). Además la frecuencia de radiación puede relacionarse con las diferentes frecuencias de vibración molecular. 3.2.1. REQUISITOS EN ESPECTROSCOPIA DE IR. Muchas transiciones electromagnéticas requieren de las regiones UV-vis, la absorción de radiación IR está limitada en gran parte a especies moleculares para las cuales existen pequeñas diferencias de energía entre distintos estudios vibratorios y rotatorios. Δ= energía de transición vibracional Por otro lado, para absorber radiación IR, una molécula debe experimentar un cambio neto en el momento dipolar, debido a su movimiento vibratorio o rotatorio. Δ𝜇 ≠ 0 (𝜇 = 𝑞 · 𝑟; Momento dipolar) 𝜇 = ∑ 𝑞 · 𝑟 Ejemplo: cuando fluctúa la distancia entre los centros de la molécula, caso de la vibración se establece un campo eléctrico oscilante que puede actuar recíprocamente, con el campo de vibración. Si la frecuencia (𝜈), de la radiación es igual a la frecuencia (𝜈̅ ) de la vibración natural de la molécula, se produce una transferencia neta de energía que implica un cambio en la amplitud de vibración ⇒ absorción de radiación. 23 Condición necesaria para que pueda darse absorción en el infrarrojo. Solo cuando una molécula sufre, al vibrar, un cambio en su momento dipolar es cuando el campo eléctrico oscilante de la radiación puede interaccionar con la molécula y provocar un tránsito energético. La molécula debe experimentar un cambio en el momento dipolar como consecuencia de su movimiento de vibración. El concepto de momento dipolar surge porque la distribución de carga alrededor de una molécula no es simétrica (por ejemplo el HCl) y se define por: Las moléculas homonucleares como el O2, N2, Cl2… no cambian su momento dipolar (µ), al vibrar y no absorben en el infrarrojo. Transiciones vibratorias-rotatorias. Los niveles de energía vibratorios están cuantizados y las distintas energías corresponden a la región del IR de 13000 a 670 cm-1 (0.710 a 15 µm) (IR próximo y medio). El interés de los espectros de IR, es sobre todo en soluciones y sólidos en los que los efectos rotatorios son mínimos. Los tipos de vibraciones moleculares corresponden a la categoría básica de extensión y flexión. Una vibración por extensión, supone un cambio continuo en la distancia interatómica (simetría y asimetría). Moléculas lineales. Las vibraciones por flexión, supone un cambio en el ángulo de dos enlaces y son de cuatro tipos: a) b) c) d) Tijeras. Oscilación. Sacudida. Torsión. En una molécula que contiene más de dos átomos (poli-atómico) puede haber interacción o acoplamiento de vibraciones. El resultado del acoplamiento supone un cambio en las características de las vibraciones. (Trans.tipo extensión y flexión). En el tratamiento de estas vibraciones se pueden contemplar dos moléculas, el modelo de oscilador armónico según la mecánica clásica y el oscilador armónico según la mecánica cuántica. 24 FIGURAS MOLECULA LINEAL DEL CO2 VAPOR (a) ⊝= 𝐶+ =⊝ (b) (c) ⃖ = 𝐶 =⊝ ⊝ ⊝= 𝐶⃖+ =⊝ Figura 3.2. Vibraciones de tensión del dióxido de carbono (a) forma normal (el dentro del átomo de carbono es el centro de gravedad de cargas positivas y negativas). (b) tensión sintética (iniciativa en infrarrojo) r permanece en el cero durante la tensión. (c) tensión asimétrica (activa a infrarrojo). Modos de vibración de moléculas triatómicas no lineales (por ejemplo H2O vapor o el H2O en CCl4). Modos normales: Flexión en el plano (de tijereteo en el plano). Tensión simétrica (extensión simétrica). Tensión asimétrica (extensión asimétrica). Estas tres son la descomposición de: 25 Modos de moléculas triatómicas lineales (por ejemplo CO2 gas). Flexión en el plano (De tijeretazo en el plano). Flexión en el plano (De tijeretazo en el plano). Tensión simétrica. Tensión asimétrica (O anti simétrica). 3.2.2. Modelo teórico según la mecánica clásica. En este modelo se suponen dos masas conectadas por un resorte. Una perturbación en una de estas produce una vibración llamada movimiento armónico simple. a) Considérese una masa unida a otra inmóvil, el desplazamiento (por extensión) de una distancia, x, se justifica por la ley de Hooke. 𝑭 = −𝒌 · 𝒙 (F: fuerza resultante y k: constante de fuerza, depende del resorte). b) La energía potencial, puede tomarse cero, cuando la masa esta en reposo o en equilibrio. Pero al comprimir o extender el resorte, la energía potencial es distinta de 0. 𝑑𝐸 = −𝐹 · 𝑑𝑥; sustituyendo 𝑑𝐸𝑝 = 𝑘 · 𝑥 𝑑𝑥 Integrando entre los límites de 0 y x. 𝐸 𝑦 ∫ 𝑑𝐸 = 𝑘 ∫ 𝑥𝑑𝑥 0 0 𝐸 = 1⁄2 · 𝑘 · 𝑥 2 La energía potencial es cero en el equilibrio y presenta valor máximo, cuando el resorte está extendido (+x) o comprimido (-x) a su máxima amplitud. 26 c) Por otro lado la frecuencia vibratoria (𝜈clásica) puede abstenerse, por 𝐹 = 𝑚 · 𝑎 (masa · aceleración). Ley de Newton. 2 𝑎 = 𝑑 𝑥⁄𝑑𝑡 2 (Segunda derivada de la distancia respecto del tiempo) que sustituyendo: 2 𝑚 · [𝑑 𝑥⁄𝑑𝑡 2 ] = −𝑘 · 𝑥 ⇒ 𝑢𝑛𝑎 𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛 𝑒𝑠 𝑞𝑢𝑒 𝑥 = 𝐴 · 𝑠𝑒𝑛 (√ 𝑘 · 𝑡) 𝑚 𝑚 El periodo “𝜏” se da por un valor de t, cuando 𝑡 = 2𝜋√ 𝑘 , luego como la frecuencia es el reciproco de su periodo (𝜏 = 1⁄𝜈 ) 𝜈𝑐𝑙á𝑠𝑖𝑐𝑎 = 1 1 𝑘 √ = 𝜏 2𝜋 𝑚 Para el caso de un sistema formado por dos masas m1 y m2 conectadas por un resorte (m=masa reducida, molécula di-atómica) 𝑚 ·𝑚 𝜇 = 𝑚 1+𝑚2 , entonces la frecuencia vibratoria clásica se puede representar 1 2 𝜈𝑐𝑙á𝑠𝑖𝑐𝑎 = 1 𝑘 1 𝑘(𝑚1 + 𝑚2 ) √ = √ 2𝜋 𝜇 2𝜋 𝑚1 · 𝑚2 Para el caso de vibraciones moleculares, se lleva a cabo un tratamiento similar. 3.2.3. Modelo teórico según la mecánica cuántica. 27 La naturaleza “cuatizada” de las energías vibratorias no puede contemplarse con las ecuaciones anteriores, pero si podemos utilizar el término de oscilador armónico simple, para la obtención de ecuaciones según la mecánica cuántica. La energía potencial (Ep), según la mecánica cuántica se presenta por la ecuación de Schödinger: 𝐸 = (𝜈 + 1⁄2) ℎ 𝑘 1 1 𝑘 √ ≡ ℎ · (𝜈 + ) √ 2𝜋 𝜇 2 2𝜋 𝜇 Donde 𝜈 es el número cuántico vibratorio que solo puede tomar valores positivos incluido el cero (0, 1, 2, 3…); además la energía de un oscilador está cuantizada: E0, E1, E2… por ello la E está relacionada con la descrita en el modelo clásico según: 𝐸 = (𝜈 + 1⁄2)ℎ𝜈𝑐𝑙á𝑠𝑖𝑐𝑎 En el caso de producirse “transiciones” en los niveles de energía, la Eradiación debe de ser igual a la ΔE entre los estados cuantizados. 𝐸𝑟𝑎𝑑𝑖𝑎𝑐𝑖ó𝑛 = ℎ · 𝜈𝑟𝑎𝑑𝑖𝑎𝑐𝑖ó𝑛 = Δ𝐸 = ℎ · 𝜈𝑐𝑙á𝑠𝑖𝑐𝑎 = ℎ 𝑘 √ 2𝜋 𝜇 Regla de selección: La E de transición de niveles debe ser idéntica. Además por la mecánica cuántica, las únicas transiciones son aquellas en las que el número cuántico vibratorio cambia por unidad. ΔV=±1(+1→absorción, -1→emisión) Si deseamos poner la radiación en número de onda,𝜈̅ : 𝑘(𝑚1 +𝑚2 ) 𝜈̅ = 𝜈⁄𝑐 = 𝑐 · 2𝜋 √ 1 1 𝜈̅ = 𝑚1 ·𝑚2 1 𝑘(𝑚1 + 𝑚2 ) √ 2𝜋𝑐 𝑚1 · 𝑚2 28 Ejemplo: Debido a una regla de selección (ΔV=+1) solo se absorbe la luz cuando: 𝐸0 ⟶ 𝐸1 𝐸1 − 𝐸0 = 𝛥𝐸 𝐸1 ⟶ 𝐸2 𝐸2 − 𝐸1 = 𝛥𝐸 𝐸2 ⟶ 𝐸3 𝐸3 − 𝐸2 = 𝛥𝐸 ℎ 𝑘 Iguales 𝛥𝐸 = 2𝜋 √𝜇 Por lo tanto el espectro infrarrojo de esta molécula solo debería tener un pico a la frecuencia correspondiente de esa energía: 𝛥𝐸 = ℎ · 𝜈𝑟𝑎𝑑𝑖𝑎𝑐𝑖ó𝑛 Para vibraciones de frecuencia mayor (debidas a valores de k más grandes o masas más pequeñas). 𝐸 = (𝜈 + 1/2) ℎ 𝑘 √ 2𝜋 𝜇 Habrá un espacio mayor entre los niveles y el pico aparecerá a frecuencias mayores. 3.3 instrumentación en espectroscopia infrarroja. Los espectrofotómetros infrarrojos tienen los mismos componentes básicos que los empleados en las regiones del UV-vis. No obstante se aprecian algunas diferencias. Espectrofotometro infrarrojo de haz simple. 29 3.3.1. Componentes de los espectrofotómetros infrarrojos. a) FUENTES (DEGRADACIÓN): La fuente IR común es un sólido incandescente, calentado eléctricamente a T: 1200 y 2200K La intensidad radiante máxima se produce a 𝜆: 1.7 a 2 µm (5000 a 6000 cm-1). A un lado y otro de estos valores de 𝜆, la intensidad desciende continuamente. Se usan tres tipos de fuentes: Emisor de Nerst de incandescencia: formado por oxidos de tierras raras (Zr, Th, Cs) en un cilindro de 1 a 2 mm de diámetro y 20 mm de longitud. Fuente Globan: compuesto de una barra de carburo de Si (SiC), 5 mm de diámetro y 50 mm de longitud. Alta resistencia. Fuente de filamento (alambre) incandescente: compuesto de una espiral de alambre de ni-cromo. W, dentro de un cilindro de cerámica. Alta duración, pero menor intensidad. Otros: Arco de mercurio (adecuada en IR lejano, 𝜆 >50µm). Lámpara de filamento de wolframio (adecuada en la zona del IR más cercano, de 4000 a 128000 cm-1 o de 2.5 a 0.78 µm). Fuente láser de CO2 (útil en la franja de 900 a 1100 cm-1 → IR medio, o de 11 a 9 µm, también es útil en la determinación de especies como, NH3, butadieno, benceno, etanol, NO2, tricloroetileno…) b) MONOCROMADORES: Consiste en un sistema variable de ranuras o rendijas de entrada y salida, con varios espejos. No se emplean lentes (problemas de aberraciones comáticas). Ranuras estrechas: menores anchos de banda, mejor definición, ausencia de radiación dispersa. Prismas: en la construcción de prismas se emplea: Cuarzo y LiF (IR próximo) NaCl cristalino (material más común, IR fundamental) KBr y CsBr (IR lejano) Red de difr++4 c) DETECTORES: Se hace difícil la detección en el IR, debido a la baja intensidad de las fuentes y a la poca energía del fotón IR. La señal eléctrica de un detector IR es pequeña, se requieren amplificadores de señal. El sistema detector limita la sensibilidad del aparato. 30 Detectores térmicos, dependen del efecto de calentamiento de la radiación. Tenemos tres tipos: Termopares: se basan en el efecto Peltier, se produce un potencial entre dos uniones de metales (Δ𝜀 = Δ𝜀(𝑇)). Un buen receptor responde a un cambio de temperatura de 10-6 ºC. Bolómetros: es un tipo de termómetro de resistencia construido con laminas de metales Ni y Pt. Presentan un cambio de resistencia relativamente grande con la temperatura. Un caso particular es el de Ge, ideal para radiación de 5 a 400 cm-1 (2000 a 5 µm) Detectores neumáticos (células) de Golay: formado por un termómetro de gas sensible. El gas encerrado es calentado por la radiación que llega , el aumento de presión se convierte en una señal eléctrica. También se usan detectores fotoconductores, de una delgada película de cristales semiconductores como SPb (el más común, sensible en la región de 0.8 a 0.3 µm (12500 a 500 cm-1), SePb y Ge. Este tipo de materiales provoca excitación de electrones no conductores hasta un estado excitado. 3.3.2. Manejo de muestras y tipos de cubetas. Los espectros moleculares UV-vis se obtienen, en su mayoría de los casos con disoluciones diluidas del analito. Para conseguir que la A se encuentre dentro del intervalo óptimo, se ajusta la concentración y el espesor de cubeta. Esto no es posible en el IR, debido a que no 31 existen buenos disolventes que sean transparentes en toda la región de interés. La manipulación de la muestra se hace difícil y requiere tiempo. a) Muestras gaseosas: Se introduce un líquido de bajo punto de ebullición o un gas en la cubeta en la que se ha hecho vacio. Existen diferentes tipos de cubetas y longitudes de paso que van desde unos pocos cm hasta 10 o más metros. b) Muestras en disolución liquida (se suele emplear en IR). Ventajas Reproductividad de los resultados. Poder elegir la concentración de la muestra y la longitud de la cubeta. Inconvenientes Es muy difícil encontrar un disolvente que no absorba fuertemente la región del infrarrojo. Puede darse reacción química entre los disolventes y la muestra. Disolventes. Rara vez se utilizan agua y alcoholes, no solo porque absorben intensamente, sino también porque atacan a los haluros de metales alcalinos que son utilizados en las ventanas de las cubetas. El disulfuro de carbono es un disolvente común para la región entre 1300 a 625 cm-1. Por su parte, el CCl4 es un disolvente común para la región 4000 a 1300 cm-1. No hay disolventes polares que sean transparentes en grandes regiones del infrarrojo. Algunos pueden usarse en regiones limitadas como el cloroformo (Cl3CH), dioxano y dimetil fornamida. Cubetas. Debido a que los disolventes absorben el infrarrojo las cubetas sueles ser estrechas, (0.1-1 mm). Se requieren concentraciones en torno al 0.1 a 10% Las cubetas suelen ser desmontables con espaciadores de teflón para variar la longitud, el paso óptico. log 1 =𝐴 =𝜀·ℓ·𝑐 𝑇 c) Muestras de líquidos puros. Cuando se dispone de disolvente apropiado se suele hacer el espectro del líquido puro. 32 Se comprime al líquido puro entre dos palancas de sal de roca de 0.01 mm de espesor. Se forma una película muy delgada con un paso óptico corto que da espectros satisfactorios con fines cualitativos. d) Muestras de sólidos. Los sólidos pueden ser suspendidos en un medio transparente adecuado: 1) Tomando de 2 a 5 mg de muestra finalmente triturada (tamaño de partículas < 2 µm, para que no se pierda radiación por dispersión) se suspenden en 2 gotas de aceite Nujol. Esta mezcla de 2 fases se examina luego como una película entre dos placas de sal. 2) Tomando 1 mg de muestra finalmente triturada se mezcla con 100 mg de polvo de KBr desecado (con mortero). Esta mezcla se comprime en un troquel a la vez que se hace vacío (para eliminar el aire y vapor de agua). La pastilla transparente resultante se instala en el portacubeta para hacer el espectro. 3.4. APLICACIONES DE LA ESPECTROSCOPIA DE IR. 3.4.1. ANÁLISIS CUALITATIVO. La base del análisis cualitativo, por IR está en que dos sustancias que absorben en el IR, nunca lo hacen con la misma intensidad en las mismas frecuencias. Un espectro IR de una sustancia es una “huella” tan única como la huella dactilar de una persona. a) Las frecuencias de grupos funcionales son casi invariables, lo que hace posible establecer si un grupo está presente o ausente en una molécula. b) Existen tablas con frecuencias de grupo y atlas que recogen esa información (gráficos de correlación). Los análisis por IR son rápidos, requieren un pequeña cantidad de muestra y no la destruyen. 3.4.2. ANÁLISIS CUANTITATIVO. a) Presenta dificultades. Proximidad entre picos de poca energía de las radiaciones IR, absorbancia de los disolventes…etc b) Desviación de la ley de Beer: 33 c) Calibrado del aparato. Ajuste del 100% T Ajuste del 0% T d) Determinación de la transmitancia de la muestra. 1. Método puntual. Se miden alternativamente espectros de la muestra y del disolvente frente al haz de referencia no obstruido: 𝑇 𝐼 𝑇𝑑𝑖𝑠𝑜𝑙𝑣𝑒𝑛𝑡𝑒 = 𝑑𝑖𝑠𝑜𝑙𝑣𝑒𝑛𝑡𝑒⁄𝐼 𝑇𝑚𝑢𝑒𝑠𝑡𝑟𝑎 = 𝑚𝑢𝑒𝑠𝑡𝑟𝑎⁄𝐼 ℎ𝑎𝑧 ℎ𝑎𝑧 Donde T es la transmitancia y la I es la intensidad Si Ihaz permanece constante se puede calcular la verdadera transmitancia de la muestra. 𝐼 𝐼 𝑇 = 𝑚𝑢𝑒𝑠𝑡𝑟𝑎⁄𝐼 = 𝑚𝑢𝑒𝑠𝑡𝑟𝑎⁄𝐼 ℎ𝑎𝑧 𝑑𝑖𝑠𝑜𝑙𝑣𝑒𝑛𝑡𝑒 2. Método de línea base. Se usa la misma cubeta para todas las determinaciones. Las medidas se realizan sobre el propio espectro en puntos definidos. T0→ Transmitancia del disolvente. TS→ Transmitancia de la muestra. GRAFICA 𝑇 𝑇 𝑇 = 𝑆⁄𝑇 → 𝑐𝑜𝑚𝑜 𝐴 = − log 𝑇 = log 0⁄𝑇 0 𝑆 EJEMPLO DE ANALISIS DE GASES POR IR DE ACUERDO CON LA OSHA 34 35