REPASO 1ª PRUEBA RECUPERACIÓN FISICA Y QUIMICA 3º ESO
Anuncio

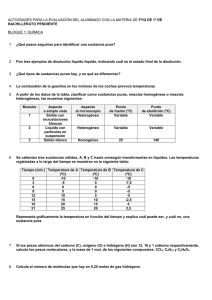
REPASO 1ª PRUEBA RECUPERACIÓN FISICA Y QUIMICA 3º ESO A entregar el día del examen. Se tendrá en cuenta el trabajo y el esfuerzo realizado para superar la asignatura. 1.- Enumera y explica las etapas del método científico. 2.- Notación científica y redondeo. Escribe las siguientes cantidades en notación científica y redondea con dos decimales. a) 657 b) 0.00058 c) 12580000000 d) 0.0021 e) 321 f) 12 g) 0.00000012 h) 78000000000 i) 9757000000 j) 0.00023 3.- Estados de agregación. Cambios de estado. Punto de fusión y punto de ebullición. Completa el siguiente diagrama de cambios de estado: SÓLIDO LÍQUIDO GASEOSO 4.- Magnitudes fundamentales y derivadas. Unidades del sistema internacional. Múltiplos y submúltiplos. Expresa en unidades del Sistema Internacional las siguientes medidas: 0,2 km 0, 039 mm 3500 g 4 cm 2h 25’ 312 cl 75 cm3 20 km/s 0,0108 km 35 g/ m3 5,009 hm 87 km/h 0,215 Tg 300 mA/min 20,903 dg 5.- Tablas y gráficas. Al estudiar el movimiento de un objeto, se han obtenido los siguientes resultados: Posición (cm) Tiempo (s) a) b) 4 0 16,5 4 24 8 29 10 54 20 Representa la gráfica de la posición en función del tiempo. Halla la expresión matemática que relaciona la posición y el tiempo. c) d) Señala, en la gráfica, el tiempo que corresponde a la posición 40 cm. Halla por extrapolación, la posición que correspondería a 22 s. 6.- Materia. Propiedades generales y características. Densidad. a) Se disuelven 15 g de cloruro de sodio en 60 g de agua. Calcula el tanto por ciento en masa de soluto en la disolución obtenida. b) Si la densidad de la disolución del cloruro de sodio del apartado anterior es 1,17 g/mL, ¿qué volumen tendremos de disolución? 7.- La presión y factores que influyen en la presión. Las leyes de los gases. 8.- Mezclas y sustancias puras. Mezclas heterogéneas y mezclas homogéneas. Elementos y compuestos. 9.- Métodos de separación de mezclas heterogéneas y homogéneas. Explica cómo separarías las siguientes mezclas y disoluciones: a) vinagre y aceite (líquidos inmiscibles) b) alcohol y agua c) hierro y azufre d) sal, agua y polvo de yodo insoluble en agua 10.- Disoluciones. Tipos: diluida, saturada, concentrada y sobresaturada. 11.- Solubilidad. La solubilidad del sulfato de aluminio a 25ºC es 5g de sulfato/100g de agua y a 86ºC es de 90g/100g de agua. a) ¿Qué cantidad de agua necesito para disolver 250 g de sulfato a 86ºC? b) ¿Cuánto sólido aparecería si bajo la temperatura a 25ºC? REPASO 2ª PRUEBA RECUPERACIÓN FISICA Y QUIMICA 3º ESO A entregar el día del examen. Se tendrá en cuenta el trabajo y el esfuerzo realizado para superar la asignatura. 1. Enuncia los tres postulados de la teoría atómica de Dalton 2.- Explica cómo es el átomo en la actualidad 3.- Completa la siguiente tabla: Especie Número atómico Si 14 As Número másico Número protones Número neutrones Bi+3 33 126 51 Catión/anión/ neutro 14 75 Sb-3 Número electrones 80 122 4.- Si el número atómico del Se es 34 distribuye sus electrones en las capas K, L, M y N. 5.- Explica que es un isótopo y pon un ejemplo. 6.- Explica brevemente como se forma el enlace iónico, covalente y metálico y cuáles son las propiedades de las sustancias que forman. 7.- Explica cómo se distribuyen los elementos en la tabla periódica. Indica el número de periodos y el número de grupos (indica el nombre de los grupos que conoces). 8.- Calcula la masa molecular y la composición centesimal de las siguientes sustancias: H2SO4, NaCl, Na2CO3 y K3PO4. 9.- Calcula el número de moles que hay en 10 g de cada una de las sustancias del ejercicio anterior. 10.- Ajusta las reacciones siguientes: a) Ag2SO4 + NaCl Na2SO4 + AgCl b) Cr2O3 + Al Al2O3 + Cr c) CuFeS2 + O2 SO2 + CuO + FeO d) H2SO4 + C H20 + SO2 + CO2 11.- En el laboratorio hemos pesado 20 g de CaCO3. Calcula: a) el número de moles de CaCO3 b) el número de moléculas de CaCO3 c) el número de moles de oxígeno d) los gramos de calcio Nota: Utiliza los datos de la tabla periódica para los ejercicios que necesites. Compuesto Cl2 O7 Nomenclatura sistemática Nomenclatura de Stock Nomenclatura tradicional Óxido de plomo (IV) Trihidruro de hierro Amoniaco HCl Hidróxido de mercurio (I) Trióxido de azufre Óxido estánnico HNO3 Óxido de níquel (III) Acido hipoyodoso Óxido de sodio Co(OH)3 Fosfina Hidruro áurico Tetraoxosulfato (VI) de hidrógeno