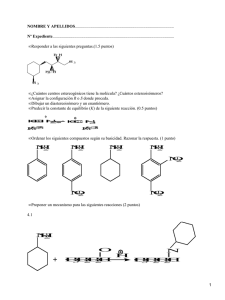
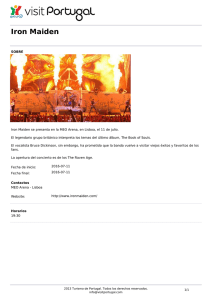
protema 3
Anuncio

PROBLEMAS SOBRE CARBANIONES 1. Ordenar cada serie de compuestos en orden de acidez decreciente: O (a) CH3 CH2 NO 2, (CH 3) 2CHCPh, CH 3CH2 CN, CH2 (CN) 2 (b) [(CH3 )2 CH]2NH, (CH3)2 CHOH, (CH3 )2 CH2 , (CH3 )2 CHPh (c) O O O O O O OCH 3 OCH 3 O O CH 3 O (d) O O 2.-. Dibujar las estructuras de cada uno de los enolatos posibles para cada cetona. Indicar cuál crees que estará más favorecida en una desprotonación controlada cinéticamente. ¿Cuál será el enolato más estable en cada caso? O (a) (c) (b) O O (d) O 3.- Proponer estructuras para los productos que se generen las siguientes reacciones: Et3N, DMF, (a) O TMSCl H O 1. KH, THF (b) 2. BrCH2COOCH3 CO2Me O H (c) 1. LiN(TMS)2, THF, -78oC t Bu O H 2. TMSCl O O 1. LDA, THF, HMPA, -78oC (d) 2. CH3CHICOOMe O H 1. LDA, THF, -78oC (e) O 2. TMSCl H CO2Me H (f) 1. LDA, THF, -78oC O 2. HMPA; MeI, THF H 1. LDA, THF, -78oC (g) 2. MeI O 1. Li, NH3 (l) (h) 2. MeI O 1. Li, NH3 (l) (i) H 2. MeI, THF O H OTBS 1. KN(TMS)2, THF, -78oC (j) 2. MeI H CHO 1. LICA, THF, HMPA (k) COOMe 2. ICH2CH(OMe)2 (l) CO2Et OH 1. LDA (2eq), THF, HMPA, -78oC O 2. MeI O (m) CN 1. LDA, THF, -78oC 2. I(CH2)3OR CN 1. LDA, THF,HMPA (n) 2.Br H 1. KOH, DMF CN (o) 2. Br(CH2)2OH O O 1. LDA (1 eq) (p) Ph 2. MeI (1 eq) O (q) OTMS O 1. LDA (2 eq) Ph 2. MeI (1 eq) CO2Et 1. NaOEt/EtOH CO2Et 2. (r) Cl Cl 4.- Proponer estructuras para los compuestos de las siguientes reacciones: de condensación aldólica. (a) (b) NaOH/H2O CH3CH2CH2CHO CH3COCH2CH2CHO NaOH/H2O O H (c) NaOH/H2O + O O NaOH/H2O O HCl (d) PhCHO + (e) PhCHO + OMe aq KOH/MeOH (f) O O O O (g) aq KOH/MeOH O (h) TsOH, benzè reflux (-H2O) O HO O (i) HCl 1N H O THF, calor O OTBDPS H aq KOH/EtOH (j) MeO CHO O OMe OBn NO2 H 5% aq HCl (k) O EtOH, calor O O O 10% aq KOH/MeOH (l) O (m) 120 oC O aq HCl O acetona O O (n) 1. LICA, CH3CHO, -80oC 2. Ac2O/py 3. DBU, Tol, reflujo CO2Et (o) BnO O O NaOMe/MeOH 5.- La reacción de la dicetona A con NaOD en D2O proporciona una mezcla de las cetonas conjugadas B y C. Proponer un mecanismo que explique razonablemente la formación de los dos compuestos. O O O D NaOD-D2O O D D + D D CD3 D A D D D D 94% B D 6% C 6.- Proponer estructuras para los compuestos de anulación de Robinson que se obtienen en las siguientes secuencias sintéticas: O O Cl (a) benceno, calor O CN TsOH O (b) O NaOMe/MeOH (c) CO2Me THPO O Tolueno (-H2O) pirrolidina O benceno/MeOH benceno O (d) Et3N O + O MeO TMSO (e) MeOH 1. MeLi, DME PhCOOH Et3N NaOMe, MeOH SiMe3 2. O 7.- El compuesto B a partir de A mediante una secuencia de reacciones que son una alternativa al método de Robinson y que se describe a continuación: O OH THPO 1. Ac2O, NaOAc 2. MeLi, éter 3. KOH, H2O, MeOH O THPO O A B Explicar la transformación de A en B. ¿Qué compuestos de partida serian necesarios para obtener B mediante el proceso de anulación de Robinson? 8.- Dar las estructuras de los compuestos formados en las siguientes reacciones de Wittig: O (a) Ph3P C(CH3)2 CO2Me H LiH, THF AcO O (b) N H Ph3P(CH2)3COOH Br BOC NaH, DMSO O (EtO)2PCHCOOMe Na CHO (c) DME CHO CHO (d) Ph3P COOEt tol, 80oC O O (e) Ph3P CHCH3 CHO THF, 0 oC CHO CO2H Ph3P CH TBDPSO (f) 7 BnO (g) THF, HMPA OBn CHO Ph3P C(CH3)2 N O THF Bn OHC Ph3PCH2CH2CH3 Br OtBu (h) MeOOC n-BuLi, THF (i) OBn O Ph3PCH2CH3 Br PhLi, THF HO 9.- Proponer un mecanismo que explique las siguientes conversiones: a) O O O Ph3P COOEt + CHO COOEt NaH O b) O P(MeO)2 COOMe O OH OH NaOMe MeOH O O O COOMe O c) 1. LDA, THF 2. H3C O PPh3 I O OEt 3. HCl, H2O 10.- Proponer las estructuras de los productos resultantes de las siguientes reacciones: CHO CH3OCH2SiMe3 (a) H BuLi OBn OTES Ph3P CHCOCH3 (b) O H CHO (c) n-BuLi +S S MeO SiMe3 O (d) TBSO Me3SiCH2COOEt OTBS LDA 11.- Proponer procedimientos para la preparación de los compuestos siguientes a partir de los que se indica en cada caso, o de sustancias fácilmente disponibles. 1.- Acetilciclopentano, del acetoacetato de etilo 2.- Ácido octanoico, del malonato de etilo 3.- 2-Etoxicarbonilcilohexanona, de la ciclohexanona 4.-.2-Metil-3-oxopentanoato de etilo, del ácido propiónico 5.- 4.-Ciclohexil-3-oxobutanoato de etilo 6.- Dipentilcetona, del acetoacetato de etilo 7.- 2,5-Dimetilciclopentanona, de la ciclopentanona 8.- 2-Etilhexanoato de etilo 9.- 2,2-Dietil-1,3-Ciclohexanodiona 10.- 2,6-Heptanodiona O O 11.- 12. Sugerir reactivos y condiciones de reacción adecuadas para efectuar las siguientes conversiones: (a) 2-metilciclohexanona en 2-benzil-6-metilciclohexanona (b) O O en H3C CN CN en (c) N CH2Ph N CH2Ph O OSiMe3 en (d) O O (e) en Br H3C O (f) O en Br 13. Predecir el producto mayoritario en cada una de las siguientes reacciones: Ph (a) CO 2Et CO 2Et (b) (c) Ph Ph 1. 1 equiv. LiNH2 / NH3 2. MeI exc. CO2 Et 1. 2 equiv. LiNH2 / NH3 CO2 H 2. MeI exc. CO2 H 1. 2 equiv. LiNH2 / NH 3 CO2 Et 2. MeI exc. 14 Sugerir compuestos de partida sencillos y condiciones de reacción adecuadas para obtener los siguientes compuestos mediante un procedimiento que incluya la alquilación de un carbono nucleofílico: (a) CN PhCH2CH2CHPh O (b) O OCH3 (c) ácido 2,3-difenilpropanoico 15. Sugerir compuestos de partida sencillos y condiciones de reacción adecuadas para obtener los siguientes compuestos mediante un procedimiento que incluya una reacción de Michael: (a) 4,4-dimetil-5-nitropentan-2-ona (b) (c) ácido 2-fenil-3-oxociclohexanoacético O 2,3-difenilglutarato de dietilo (d) O 16. La reacción de cetonas sencillas como la 2-butanona o fenilacetona con cetonas ,-insaturadas da ciclohexenonas si la reacción se hace calentando con metanol y metóxido sódico. Explicar cómo se forman estas ciclohexenonas y que estructuras son posibles 17. Determinar como podrían prepararse las siguientes moléculas a partir de los materiales de partida que se indican: O MeO P MeO (a) O MeO P MeO O O 18. Las acetofenonas sustituidas reaccionan con fenilpropiolato de etilo en condiciones de reacción de Michael para dar pironas. Formular un mecanismo para la reacción: Ph R R + O PhC CCO 2Et Ph O O 19. Sugerir un mecanismo para la siguiente reacción: H + N MeO 2C MeO2 C CO2 Me CH 3CN H N CO 2Me CH 3 CH 3 20. Indicar las condiciones de reacción o una serie de reacciones que permitan efectuar las siguientes conversiones sintéticas: O O CHOH (a) Ph (b) Ph O Ph CN Ph O (c) CO2Et O O O CH2OH O O (d) EtO OEt O O O CH3 (e) MeO MeO O C CH2 H O MeO MeO H (f) MeO MeO CH3 CH3 (g) O CHOCH3 21. Sugerir un mecanismo para las siguientes transformaciones: O O CO2Me (a) CH3 NaH, benzeno CO2Me O O OHC OH CH2P(OCH3)2 (b) H t-BuOK O t-BuOH O CH3 O CH3 O (c) CH3 O O CH3 NaOH, MeOH CH3 O (d) NaOEt O O CO2Et CH3 O EtO2C O O O 22. Se ha sugerido que el ácido tetraacético (o un equivalente biológico) es un intermedio en la biosíntesis de compuestos fenólicos naturales. Se ha descrito su síntesis y rápida conversión en ácido orselínico. Sugerir un mecanismo para la formación de ácido orselínico en las condiciones indicadas: 23. Se ha desarrollado un método sintético general de ciclación que utiliza haluros de viniltrifenilfosfonio, del que se muestran dos ejemplos. Comentar el mecanismo y sugerir dos tipos adicionales de anillos que podrían sintetizarse con esta estrategia: O CO2Et CO2Et CHO ONa CO2Et NaH H3C + H2C C PPh3 H CO2Et acetonitrilo + H2C C PPh3 H O 24. Los compuestos A y B son intermedios claves en una síntesis total del colesterol. Explicar su formación mediante las reacciones mostradas: 25. La elastasa es una sustancia implicada en la artritis, diferentes tipos de inflamaciones, enfisema pulmonar y pancreatitis. La elastasa puede inhibir un compuesto llamado elastina. Se ha descrito una síntesis de la elastina en la que el compuesto E es un intermedio clave. Sugerir una síntesis del compuesto E a partir de hexanoato de metilo y hexanal: 26. El reactivo A se ha utilizado en la síntesis de moléculas complejas a partir de precursores sencillos. Por ejemplo, el enolato de la 3-pentanona, tratado inicialmente con A, y después con benzaldehido da B, en forma de dos diastereómeros en proporción 2:1. Explicar los mecanismos por los cuáles transcurre esta síntesis: