CINÉTICA QUÍMICA
Fundamentos de
Espectrofotometría
Laboratorio de Equilibiro y Cinética
Sem 2010-1
Introducción 2ª parte del curso
• Cinética Química: Estudio de la velocidad
(rapidéz) de las reaciones
¿cómo se puede medir la velocidad de una reación?
• Cinética Química: Estudio de los factores que
afectan la velocidad de las reaciones
¿Cómo se puede modificar la velocidad de una reacción?
¿cómo se puede medir la velocidad de
una reación?
Cambio de color
Cambio en la presión del O2
Cambio en la conductividad
RP
Velocidad =
P =t
R
t
CAMBIO EN LA
CONCENTRACIóN
respecto al tiempo
Espectroscopía
Es el método de análisis óptico más
usado en el área de investigación
Estudio de la interacción de la
RADIACIÓN con la MATERIA
como una función de la longitud
de onda ( ).
Radiación
Energía=h
=hc/
h, cte. Planck
C, vel luz
, frecuencia
longitud de onda
Espectroscopía de Absorción
hv
Absorbancia UV-Vis
Una
TRANSICIÓN
desde un nivel bajo a un
nivel alto de energía
acompañado
de
una
transferencia de energía
se llama absorción.
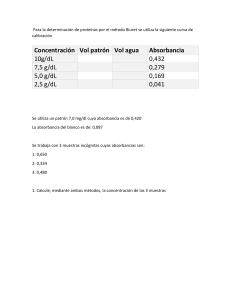
Se hacen determinaciones
- Cualitativas
-Cuantitativas
Espectrometría
Es la técnica espectroscópica utilizada
para determinar la concentración de una
sustancia.
Es la CUANTIFICACIÓN de la
cantidad de energía radiante
absorbida por las moléculas de una
muestra en función de las longitudes
de onda específicas.
Espectrofotómetro
Instrumentación típica de un
espectrofotómetro
Fotodetector, que mide
cuantitativamente la
radiación que pasa por la
muestra
Monocromador que separa la
banda de longitud de onda
deseada
Transmitancia y Absorbancia
I0
I
Transmitancia = I/I0 (valores entre 0 - 1)
Absorbancia = -log (I/I0)
100
I
80
Absorbancia
Transmitancia %
I en el detector
0
60
40
20
0
0
0.2 0.4 0.6 0.8
I
1
2.5
2
1.5
1
0.5
0
0
0.2 0.4 0.6 0.8
I
1
Absorbancia aceptable entre 0.1 – 1.0
Valores altos y bajos de absorbancia son poco confiables
Ley de Lambert-Beer
Establece que hay una relación lineal entre la
absorción de luz a través de una sustancia y la
concentración de la sustancia.
A = ε· l · c
Donde:
A = absorbancia
= Coeficiente de extinción molar (M-1 cm-1)
l = longitud de la celda (cm).
…concentración es
absorbancia
1.2
Curva
Patrón
Absorbancia
1
0.8
0.6
ε· l
0.4
0.2
0
0
20
40
60
80
100
[concentración]
120
Determinación de la concentración de yodo
en una solución acuosa
KI
I+
I2
+
K
I3-
+
2 x 10-4 M
Muy poco soluble en agua
Soluble en agua
Absorbancia
Longitud de onda
Seleccionar una longitud de onda y
hacer curva patrón
1.2
Curva
Patrón
Absorbancia
1
0.8
0.6
ε· l
0.4
0.2
0
0
20
40
60
80
100
[concentración]
120
 0
0