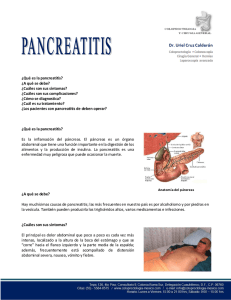
Insuficiencia pancreática exocrina
Anuncio

Páncreas Función de la nutrición en la patogenia y manejo de las alteraciones del páncreas exocrino Kenneth W. SIMPSON BVM&S, PhD, MRCVS, Dipl ACVIM, Dipl ECVIM-CA En 1984, Kenneth Simpson se licenció en Medicina y Cirugía Veterinarias (BVM&S) en la Universidad de Edimburgo. Después de obtener un doctorado (PhD) en la Universidad de Leicester en 1988, gracias a su trabajo dedicado a la función pancreática e intestinal canina, continuó su formación clínica en la Universidad de Pensilvania y en la Universidad de Ohio. Actualmente es profesor asociado en el departamento de Medicina de la Universidad de Cornell, en donde continúa sus investigaciones clínicas sobre medicina interna y gastroenterología. E l páncreas exocrino desempeña una función primordial en la digestión y absorción de los nutrientes. Los acini pancreáticos sintetizan y secretan enzimas como la lipasa, la tripsina y la amilasa, que hidrolizan los lípidos, las proteínas y los carbohidratos, respectivamente. Las células del conducto pancreático secretan bicarbonato que mantiene el nivel óptimo de pH para los procesos de digestión y de absorción, así como el factor intrínseco que permite la absorción de la cobalamina (vitamina B12). Además, el páncreas exocrino también produce, péptidos bacteriostáticos y defensinas, que regulan la flora del tracto gastrointestinal superior, y participan en el mantenimiento de la mucosa intestinal y de la homeostasia de la glucosa. Las disfunciones del páncreas exocrino se caracterizan, principalmente, por la pérdida de masa funcional del páncreas (insuficiencia pancreática exocrina), o inflamación (pancreatitis), con la consecuente aparición de diarrea y pérdida de peso, o dolor abdominal y vómitos respectivamente. Este capítulo explica la importancia de la nutrición en la patogenia y en el manejo de las enfermedad pancreática exocrina del perro. 162 1 - Insuficiencia pancreática exocrina 1 - Insuficiencia pancreática exocrina Diagnóstico > Visión global El diagnóstico de la insuficiencia pancreática exocrina (IPE) se realiza basándose en un historial y signos clínicos compatibles (Tabla 1), y tras descartar las causas infecciosas, parasitarias, metabólicas y anatómicas de la diarrea del intestino delgado y de la pérdida de peso. El diagnóstico se confirma al comprobar que la concentración sérica de tripsinógeno circulante (trypsine-like inmunorreactivity o TLI) es inferior a la normal (Westermarck y Wiberg, 2003). Heces grises o amarillas 99% Aumento del volumen fecal 95% Defecación > 3 veces/día 90% Pérdida de peso o caquexia 90% Frecuentes flatulencias 88% Diarrea varias veces por semana 77% Coprofagía 61% Polidipsia 51% Vómitos 38% Trastornos cutáneos Páncreas TABLA 1 - SÍNTOMAS MÁS FRECUENTES QUE SE HAN OBSERVADO EN 109 PASTORES ALEMANES CON IPE* EN COMPARACIÓN CON 186 PASTORES ALEMANES SANOS 14% (sin diferencias con respecto al grupo testigo) (Fuente: Raiha y Westermack, 1989) * IPE: Insuficiencia pancreática exocrina > Signos clínicos Los perros que padecen IPE suelen acudir a la consulta por una diarrea crónica (heces voluminosas, con aspecto blando y coloración entre amarillenta y grisácea) (Figura 1) y por pérdida de peso (entre moderada y extrema), acompañadas de un apetito voraz. También son frecuentes la pica y la coprofagia. Muchos perros presentan un deterioro del estado del pelaje (pérdida de pelo, eczema, sequedad, escamas) y, en ocasiones, se observa polidipsia y una clara disminución de la masa muscular. © M. Weber Puede aparecer poliuria y polidipsia cuando la insuficiencia pancreática exocrina es causada por pancreatitis crónica complicada por diabetes mellitus. También puede asociarse a la IPE un síndrome abdominal agudo debido a una torsión mesentérica. > Pruebas complementarias • Pruebas clinicopatológicas Los análisis hematológicos y bioquímicos habituales están poco alterados en los perros que padecen IPE. En algunos perros se observa un aumento moderado de la alanina aminotransferasa (ALT) y una disminución del colesterol. La hipoproteinemia no es característica de la IPE y su presencia sugiere que una enfermedad primaria del intestino delgado más que la IPE, es la causa de la diarrea y de la pérdida de peso. Figura 1 - Las heces de los perros con insuficiencia pancreática a menudo son voluminosas, blandas, decoloradas y muy olorosas. La hiperglucemia y la glucosuria en perros con signos de IPE sugieren la existencia de una diabetes mellitus secundaria a una pancreatitis crónica o a una hipoplasia pancreática. 163 1 - Insuficiencia pancreática exocrina Las concentraciones séricas de cobalamina (vitamina B12) y de vitaminas A y E pueden encontrarse muy disminuidas en perros con IPE. Por el contrario, la concentración sérica de folatos suele estar incrementada. En perros con insuficiencia pancreática inducida experimentalmente, las concentraciones séricas de zinc y de cobre están disminuidas, mientras que el hierro sérico y la saturación de la transferrina aumentan. • Diagnóstico específico El diagnóstico específico de IPE se realiza mediante la confirmación de una concentración inferior a la normal de inmunorreactividad tripsinoide ( TLI) en una muestra de suero tomada en ayunas (Williams y Batt, 1988). Se considera que la TLI sérica procede únicamente del páncreas y constituye un indicador de la masa pancreática y de la inflamación (Simpson et al., 1991). Páncreas En los perros con IPE causada por atrofia o inflamación crónica, la cantidad de TLI que pasa del páncreas a la circulación general es menor y, al hacer la prueba, se detecta una concentración inferior a la normal (Figura 2). FIGURA 2 - INTERPRETACIÓN DE LOS VALORES DEL TEST DE INMUNORREACTIVIDAD TRIPSINOIDE (TLI) EN PERROS EN AYUNAS IPE ¿IPE parcial? Rango de valores normales Concentración sérica (µg /l) 2,5 5,0 35,0 Los perros sanos, generalmente, tienen una concentración de TLI en ayunas (desde la víspera por la tarde) superior a 5 µg/l (rango normal: 5-35 µg/l) mientras que, los perros con IPE debida a una disminución de masa pancreática, tienen un nivel en ayunas inferior a 2,5 µg/l. Para las concentraciones comprendidas entre 2,5 y 5 µg/l, se puede considerar que el perro está bien o que padece una IPE parcial y debe repetirse la prueba después de asegurarse de que el ayuno se realiza correctamente. ERRORES DIAGNÓSTICOS La IPE debe distinguirse de las enfermedades intestinales primarias. La asociación de diarrea, pérdida de peso, apetito voraz y valores de laboratorio relativamente normales en un perro mayor y de una raza predispuesta (p. ej., Pastor Alemán) (Figuras 3 y 4) sugiere firmemente una IPE. La existencia de una diarrea del intestino grueso, vómitos frecuentes, mucosas pálidas o ictéricas, edema o ascitis debe hacer que se consideren otros diagnósticos más probables. La hipoproteinemia no es característica de una IPE simple y hace pensar más en una enteropatía perdedora de proteínas. No hay que fiarse sólo del resultado de la prueba TLI sin otros signos que apoyen la existencia de IPE. 164 Es posible que los perros que presenten concentraciones de TLI intermedias persistentemente tengan una IPE parcial que podría evolucionar hacia una IPE completa (Wiberg et al., 1999a; Wiberg y Westermarck, 2002). La TLI es una prueba sencilla y fiable que permite confirmar el diagnóstico de IPE. Sin embargo, si el resultado de la prueba de la TLI no concuerda con los signos clínicos, es conveniente repetirla después de ayunar durante una noche, para excluir la posibilidad de que hubiera un error en la preparación de la muestra o en la técnica de manipulación. Esta prueba no detectará condiciones que originen una destrucción intraluminal de las enzimas pancreáticas, como los estados de hiperacidez debido a un gastrinoma o a un mastocitoma. Pero en estos casos existen otros signos como hematemesis o esofagitis que se distinguen de una IPE primaria. > Diagnóstico diferencial El diagnóstico diferencial de IPE debe incluir todas las posibles causas de diarrea del intestino delgado y de pérdida de peso (Tabla 2). 1 - Insuficiencia pancreática exocrina Infecciosa Giardia, Histoplasmosis, bacterias patógenas (Salmonella, Campylobacter), Ficomicosis, Micobacterias Metabólica Hipoadrenocorticismo, Patología hepática, Patología renal Dietética Intolerancia o alergia alimentaria Insuficiencia pancreática exocrina Primaria o secundaria Patología del intestino delgado Estructural Obstrucción parcial: intususcepción, cuerpo extraño, neoplasia, linfangiectasia y malformaciones congénitas Inflamatoria Enteritis eosinofílica, linfoplasmocitaria, granulomatosa Neoplásica Linfosarcoma, adenocarcinoma, leiomioma, fibrosarcoma Sobrecrecimiento bacteriano Secundaria, idiopática Funcional Trastornos de la motilidad, idiopática Páncreas TABLA 2 - DIAGNÓSTICO DIFERENCIAL DE DIARREA CRÓNICA DE INTESTINO DELGADO Porcentaje de casos FIGURA 3 - FRECUENCIA DE DISTRIBUCIÓN POR EDADES EN EL MOMENTO DEL DIAGNÓSTICO DE INSUFICIENCIA PANCREÁTICA EXOCRINA EN 199 PASTORES ALEMANES Y 102 PERROS DE OTRAS RAZAS (Se han expresado los resultados como porcentaje de casos dentro de cada grupo) (Fuente: Hall et al., 1991) Pastores Alemanes Otras razas Edad (años) FIGURA 4 - FRECUENCIA DE DISTRIBUCIÓN DE RAZAS EN 301 CASOS DE INSUFICIENCIA PANCREÁTICA CANINA (Se han expresado los resultados como número de perros por raza) (Fuente: Hall et al., 1991) Pastor Alemán Mestizos Cavalier King Charles Collies Terriers Spaniels Otros En el Pastor Alemán y en el Collie de pelo largo, la atrofia pancreática viene precedida de una infiltración linfocitaria (Westermarck et al., 1993a; Wilberg et al., 1999b). 165 1 - Insuficiencia pancreática exocrina Epidemiología > Factores de riesgo FIGURA 5 - IMÁGENES DE IPE DEBIDA A UNA ATROFIA DE LOS ACINI PANCREÁTICOS Y A PANCREATITIS CRÓNICA La atrofia de los acini pancreáticos (AAP) representa, probablemente, la causa más frecuente de IPE en el perro (Figura 3). Se puede sospechar la existencia de una atrofia acinar pancreática en los perros con IPE y menores de 5 años de edad. En los perros más mayores, la IPE se debe con mayor frecuencia a la evolución de una pancreatitis degenerativa (Hall et al., 1991). Los perros que padecen pancreatitis crónica recurrente tienen un alto riesgo de desarrollar una IPE. > Predisposición racial Páncreas Se ha diagnosticado IPE en gran variedad de razas (Figura 4). 5A - Pancreatitis crónica. La fibrosis y la atrofia son evidentes en esta sección del páncreas de un perro con IPE secundaria a una pancreatitis (x 10; tinción HE). Se ha descrito una predisposición familiar a la atrofia de los acini pancreáticos en el Pastor Alemán, el Collie y el Setter Inglés (Westermarck, 1980; Boari et al., 1994; Moeller et al., 2002; Wiberg, 2004). Puesto que cuando la enfermedad evoluciona hacia su estado final, es imposible determinar la causa de la atrofia, se han realizado estudios prospectivos sobre la AAP canina. Estos estudios longitudinales han demostrado que en el Pastor Alemán y en el Collie de pelo largo con IPE subclínica confirmada por la prueba TLI, la atrofia pancreática viene precedida de una marcada infiltración linfocitaria (Westermarck et al., 1993a; Wiberg et al., 1999b). Esto sugiere fuertemente una base autoinmunitaria para la AAP. No hay evidencias de una carencia de factores tróficos (p. ej., colecistoquinina o CKK) o de que los anticuerpos antipancreáticos participen en el origen de la AAP. Una raza como el Schnauzer Miniatura parece estar sobrerrepresentada en los casos de pancreatitis recurrente y podría tener una predisposición a la IPE. Mecanismos fisiopatológicos de la IPE 5B - La inflamación linfocitaria precede al desarrollo de una IPE en los perros con atrofia hereditaria de los acini pancreáticos (x 40; tinción HE). 5C - Las células de los islotes, teñidas por la insulina (de color marrón) y rodeadas por mucho tejido exocrino atrofiado, son relativamente normales en los perros con IPE. (La tolerancia a la glucosa es anormal pero responde a un suplemento de enzimas; véase el texto correspondiente) (x 20; inmunotinción para la insulina). La mayoría de las veces, la IPE canina es la consecuencia de una disminución importante de la masa pancreática causada por una atrofia de los acini pancreáticos o por una pancreatitis crónica (Figura 5). La hipoplasia pancreática concomitante con IPE y diabetes mellitus ha sido observada muy pocas veces. La IPE también puede ser secundaria a: – una mayor destrucción o una disminución de la actividad de las enzimas pancreáticas en pacientes con hipersecreción ácida, – una disminución de la síntesis y secreción enzimáticas debido a una malnutrición grave. Es necesario que se produzca una pérdida importante de masa pancreática exocrina (aproximadamente, el 90%), ya sea por atrofia o por inflamación crónica, para que se manifiesten los signos clínicos de IPE (Simpson et al., 1992). Los principales signos de IPE son la diarrea, la pérdida de peso y un apetito voraz atribuidos directamente a una disminución de las concentraciones intraduodenales de enzimas pancreáticas, bicarbonato y otros factores, lo cual provoca una malasimilación de las grasas, carbohidratos y proteínas (Figura 6). También se han documentado casos de malabsorción de las vitaminas liposolubles y cobalamina, así como modificaciones cuantitativas y cualitativas de la flora bacteriana del intestino delgado, en perros con IPE (Williams et al., 1987; Westermarck et al., 1993b; Adamama-Moraitou et al., 2002). Se observa una concentración sérica de cobalamina inferior a la normal en, aproximadamente, el 75% de los perros que padecen IPE, lo que puede ser la consecuencia de un déficit de factor intrínseco, alteraciones en la unión entre el factor intrínseco y la cobalamina ( pH intestinal, ausencia de proteasas) o de consumo de cobalamina por bacterias (Figura 7) (Batt et al., 1989; Simpson et al., 1989a; Simpson et al., 1993). Otras anomalías encontradas en perros con IPE incluyen alteraciones en: – la homeostasis de la glucosa (intolerancia subclínica a la glucosa) (Rogers et al., 1983), 166 1 - Insuficiencia pancreática exocrina – los péptidos reguladores pancreáticos y gastrointestinales (p. ej., polipéptido intestinal vasoactivo, polipéptido inhibidor gástrico, somatostatina, polipéptido pancreático) (Hellmann et al., 1991), – la regulación del crecimiento de la mucosa del intestino delgado, la síntesis y la degradación de enzimas (Batt et al., 1979; Sorensen et al., 1988; Simpson et al., 1989b). FIGURA 6 - FISIOPATOLOGÍA DE LA INSUFICIENCIA PANCREÁTICA EXOCRINA potencial osmótico nutrientes mal digeridos Bacterias sales biliares àcidos grasos hidroxilados HCO3 ¿Factor intrínseco? ¿Péptidos bacteriostáticos? pH volumen fecal esteatorrea creatorrea amilorrea secreción de agua en el colon actividad enzimática del páncreas precipitación de las sales biliares absorción de la vitamina B12 absorción de folatos Páncreas Enzimas lesiones de la mucosa Resumen de las modificaciones intraluminales y extraluminales que tienen lugar cuando se produce una insuficiencia pancreática exocrina. FIGURA 7 - ABSORCIÓN DE LA COBALAMINA EN EL PERRO Después de ingerir el alimento, la cobalamina se libera al estómago. A continuación se une de manera no específica a una proteína de enlace de origen salival y gástrico llamada haptocorrina. El factor intrínseco (FI), una proteína que favorece la absorción de la cobalamina en el íleon, se produce en el estómago y en el páncreas del perro. A pH ácido, la cobalamina tiene mayor afinidad por la haptocorrina que por el FI y, por lo tanto, es en el estómago donde la mayor parte de la cobalamina se une a la haptocorrina. Al entrar en el duodeno, la haptocorrina es degradada por las proteasas pancreáticas y la cobalamina es transferida al FI, un proceso que se ve facilitado por la elevada afinidad del FI por la cobalamina a pH neutro. El complejo “cobalamina-FI” circula por el intestino hasta que se une a unos receptores específicos (antes se llamaban receptores de la cobalamina-FI, pero recientemente se han denominado cubilina) situados en las microvellosidades de la membrana apical en el borde de cepillo de los enterocitos del íleon. La cobalamina sufre entonces una transcitosis hacia la circulación portal y se une a una proteína llamada transcobalamina 2 (TCII), que es la mediadora para la absorción de la cobalamina. Una parte de la cobalamina asimilada por los hepatocitos es rápidamente (en una hora en el caso del perro) re-excretada en la bilis unida a la haptocorrina. Hígado Estómago Páncreas Vesícula biliar Diafragma Intestino delgado Circulación portal La cobalamina de origen hepatobiliar es transferida junto con la cobalamina de origen alimentario hacia el FI y es absorbida a través de receptores específicos, estableciéndose así una recirculación enterohepática de la vitamina. En el perro, las concentraciones bajas de cobalamina sérica están asociadas a una insuficiencia pancreática exocrina, a trastornos intestinales graves, a anomalías de los receptores FI-Cbl, así como a enfermedades asociadas a una proliferación bacteriana intestinal, como la estasis intestinal. Cobalamina Haptocorrina Factor intrínseco (FI) Cubilina Transcobalamina 2 (TCII) 167 1 - Insuficiencia pancreática exocrina Páncreas FIGURA 8 - ESTUDIO DE UN CASO DE IPE – HEMBRA BÓXER ESTERILIZADA DE 7 AÑOS Anamnesis y examen clínico - Perdida de peso (desde hace 6 meses), diarrea crónica (más de 6 defecaciones diarias desde hace 3 meses), apetito voraz. - Muy delgada (índice corporal de 1/5), nódulos cutáneos de 3x2 mm en el lado izquierdo del cuello y en el flanco derecho. - Tratada previamente con una fluoroquinolona (enrofloxacina), prednisona (10 días) y metronidazol sin ningún signo de mejoría. Análisis iniciales Hematocrito 39% Proteínas totales 7,5 g/dl BUN 30-40 mg/dl Glucosa Discusión Análisis de orina 86 mg/dl Densidad 1,041 pH 6,5 ++ (sin importancia dada la densidad urinaria) proteínas Análisis fecales Giardia: prueba ELISA, ZnSO4 negativo Muchos organismos del tipo Clostridium perfringens en la placa TLI Cobalamina Folato 5,58 µg/L (5-25) 184 pg/mL (175-550) 27 ng/mL (4-13) Ecografía: hiperecogenicidad difusa del hígado; resultado dudoso Radiografías torácicas: normales Hemograma Hematocrito % 44 (42-57) Aspiraciones de los nódulos cutáneos: sangre VCM (fl) 74 (63-74) Leucocitos (miles/µl) 8,1 (6,2-14,4) Pruebas de coagulación: normales (TP - TPTA) Neutrófilos (miles/µl) 6,6 (3,4-9,7) Linfocitos (miles/µl) 1,4 (1,3-4,7) Plaquetas (miles/µl) 475 (179-483) La diarrea crónica, la pérdida de peso y la polifagia sugieren una maldigestión y/o una malabsorción. El aumento de las enzimas hepáticas hace pensar en una hepatopatía primaria o secundaria en respuesta a los corticoides exógenos o a una patología gastrointestinal. El nivel bajo de colesterol indica una patología del intestino delgado, una IPE o una patología hepática, y en ausencia de otros elementos que muestren un problema de síntesis hepática (proteínas y BUN normales), sólo quedan las hipótesis de patología gastrointestinal o de IPE. Una prueba de la TLI normal descarta provisionalmente la sospecha de la IPE y sugiere que el alto nivel de folatos y el nivel bajo normal de cobalamina se deben a una alteración intestinal. Debido a la importancia del adelgazamiento y en ausencia de un diagnóstico definitivo, se realiza una laparotomía exploratoria para obtener biopsias a nivel gastrointestinal, hepático, y de los nódulos mesentéricos. Durante la cirugía, se encontraron una bola de trapo de 10 cm en el estómago y otra de 6 cm en el yeyuno. Se consideraron accidentales puesto que no causaban obstrucción y, con toda seguridad, eran secundarias a la polifagia. Se observó un engrosamiento de la pared gástrica y una atrofia importante del páncreas. Diagnóstico tras la laparotomía exploratoria Perfil bioquímico Albúmina (g/dl) 3,9 (3,1-4,1) Globulina (g/dl) 3,0 (1,9-3,6) ALP (U.I./l) 1130 (12-122) ALT (U.I./l) 357 (25-106) GGT (U.I./l) 33 (0-10) Colesterol (mg/dl) 106 (124-335) Insuficiencia pancreática exocrina, gastritis posiblemente vinculada a la presencia de Helicobacter, linfadenopatía reactiva secundaria a una patología gastrointestinal. En el transcurso de los dos meses siguientes, la perra pasa de 20 a 25 kg, las heces son normales y su estado general mejora. Discusión Los antecedentes de una importante pérdida de peso, diarrea y polifagia asociados a una proteinemia normal y a un nivel bajo de colesterol son típicos de una IPE. El incremento de las enzimas hepáticas, en especial el de la ALP, es superior al que cabría esperar en una IPE, pero esto podría deberse al tratamiento anterior con corticosteroides así como a la presencia de cuerpos extraños en el intestino. Las concentraciones de cobalamina y folatos refuerzan la sospecha de una IPE o de un síndrome de estasis intestinal. Histopatología Páncreas: atrofia con inflamación linfoplasmocitaria, fibrosis aún residual del tejido acinar Hígado: Hepatopatía vacuolar, multifocal, en racimo Estómago: Infiltración linfoplasmocitaria moderada; nódulos linfáticos con fuerte infiltración linfoplasmocitaria; ++++ organismos de tipo Helicobacter Duodeno/yeyuno/íleon: muestras en placas de Peyer Nódulos linfáticos mesentéricos: hiperplasia 168 No se observó ninguna obstrucción en la ecografía o al realizar la laparotomía, así que las variaciones en las concentraciones de cobalamina y folatos, probablemente, son consecuencia de la IPE. Sin embargo, el resultado de 5,28 en la prueba de la TLI es un argumento fuertemente en contra de una IPE. Normalmente, los perros con IPE dan un resultado inferior a 2,5. En este caso, la histología confirma una atrofia secundaria a una infiltración linfocitaria. Puede que al ser pequeña la cantidad de tejido pancreático inflamado, fuera suficiente para mantener la TLI en un rango normal, mientras que la secreción exocrina se encontraba drásticamente reducida. Desafortunadamente, el propietario no quiso realizar otras pruebas de TLI para a afinar la interpretación de este resultado. 1 - Insuficiencia pancreática exocrina Hay pocos estudios disponibles sobre la situación de los oligoelementos en una IPE. Un estudio realizado en el Pastor Alemán con IPE indica que las concentraciones séricas de cobre y zinc son normales. Sin embargo, se ha demostrado recientemente que, tras efectuar una ligadura del conducto pancreático, dichas concentraciones disminuyen mientras que la concentración de hierro y el coeficiente de saturación de la transferrina aumentan (Adamama-Moraitou et al., 2001). No está claro el significado clínico de las alteraciones relativas a los oligoelementos. La malasimilación grave de los nutrientes durante la IPE puede dar lugar a una malnutrición proteica y calórica (Figura 8) que compromete aún más la función pancreática residual, la absorción intestinal y la homeostasis metabólica. Páncreas Las alteraciones dermatológicas se presentan de manera muy variable en el Pastor Alemán con IPE y su presencia puede estar relacionada con la malnutrición proteica y calórica, con déficits de oligoelementos y minerales y con reacciones de intolerancia alimentaria. Tratamiento > Suplemento enzimático La insuficiente secreción enzimática por parte del páncreas exocrino obliga a suministrar una preparación de enzimas exógenas en las comidas. Solo deben utilizarse preparados enzimáticos en polvo con recubrimiento gastrorresistente de manera que resistan la acidez gástrica. La otra posibilidad es proporcionar páncreas fresco. Hay que tener en cuenta que los suplementos utilizados estén mantenidos en buenas condiciones y que no estén caducados. La dosis recomendada para un perro es 0,25-0,4 g/kg peso corporal/comida o 2 cucharaditas/20 kg de peso/comida (Westermarck et al., 1987; Wiberg et al., 1998). Los suplementos de enzimas deben mezclarse con la comida. La preincubación no afecta significativamente al resultado (Pidgeon y Strombeck, 1982). Si se observa que cesa la diarrea y que aumenta el peso en las dos semanas siguientes al comienzo del tratamiento, hay que probar a disminuir el suplemento enzimático hasta alcanzar la dosis efectiva más baja. Si el tratamiento falla, se puede intentar cambiar de lote o de presentación o aumentar las cantidades enzimáticas. Si no se obtiene ninguna respuesta con 0,4 g/kg de extracto pancreático en polvo o con 3 g/kg peso corporal/harina de páncreas entero, el suplemento enzimático no es sin duda el motivo del fracaso del tratamiento. > Micronutrientes La malabsorción lipídica conlleva una disminución de la absorción de vitaminas liposolubles.Se han descrito en Pastores Alemanes con IPE, concentraciones bajas de vitaminas A y E .Se puede administrar vitamina E por vía oral (400-500 UI una vez al día durante un mes). Quizá sería conveniente examinar el estado de la vitamina K en los perros que presentan una IPE con signos de coagulopatía confirmados en el laboratorio. La carencia de cobalamina puede provocar múltiples efectos en el organismo (Figura 9). La suplementación oral de enzimas pancreáticas no compensa dicho déficit, por lo que se recomienda una administración parenteral complementaria. En el perro, la administración parenteral de una sola dosis mensual de cianocobalamina (250-500 µg SC una vez al mes) es suficiente para prevenir la recidiva de los trastornos metabólicos durante un mes. La malabsorción de la cobalamina no desaparece después de la suplementación enzimática, por lo que se recomienda su tratamiento complementario de por vida. Alimentación para los perros con IPE El papel esencial del páncreas exocrino en la digestión y asimilación de los nutrientes implica que la IPE es una enfermedad especialmente sensible a una intervención dietética. En teoría, la alimentación más conveniente para la mayoría de perros con IPE debiera ser altamente digestible, baja en lípidos (los lípidos son considerados como los nutrientes más difíciles de asimilar porque la actividad de En la mayoría de los perros, es posible una disminución del 50% de la dosis inicial del suplemento enzimático (Simpson et al., 1994). Esta adaptación de la posología es importante ya que el coste de las enzimas pancreáticas constituye un obstáculo al tratamiento para la mayoría de los propietarios que finalmente prefieren solicitar la eutanasia del animal. 169 1 - Insuficiencia pancreática exocrina FIGURA 9 - FUNCIÓN DE LA VITAMINA B12 EN EL ORGANISMO Lucha contra el envejecimiento Páncreas Lucha contra la anemia Síntesis de proteínas La vitamina B12, desempeña un papel fundamental en la síntesis de proteínas y en la producción de glóbulos rojos e interviene como coenzima en numerosas reacciones bioquímicas esenciales. la lipasa limita su digestión) y baja en fibras (las fibras no son digestibles, disminuyen la densidad energética y obstaculizan la acción de las enzimas pancreáticas). Sin embargo, un estudio realizado en 116 perros con IPE no ha demostrado una disminución significativa de la mortalidad en los perros que habían recibido un alimento dietético especial (30% de mortalidad, n=73) con respecto a los que habían recibido un alimento estándar (35% de mortalidad; n=43) (Hall et al., 1991). > Ventajas potenciales de un contenido elevado en materias grasas Totalmente al contrario de las recomendaciones clásicas sobre una dieta baja en grasas cuando hay una IPE, en un ensayo se demostró que, en los perros con IPE experimental, la digestibilidad de las proteínas, lípidos e hidratos de carbono era mejor con las dietas que tenían un 43% de calorías lipídicas que con los que contenían sólo entre un 18 y un 27% (Suzuki et al., 1999). La mejor conservación de las enzimas pancreáticas exógenas, en concreto de la lipasa, podría explicar este hecho. Cuando se induce una IPE experimental, el contenido de lípidos en las heces depende más de la digestibilidad de los lípidos que de la cantidad de lípidos ingerida (Pidgeon, 1982; Pidgeon y Strombeck, 1982). En un caso clínico, tres Pastores Alemanes con IPE y alergia alimentaria recibieron un alimento formulado a base de hidrolizado de soja y de arroz, conteniendo un 19% de grasas en materia seca (es decir, un 40,8% de las calorías lipídicas). Este alimento demostró una buena tolerancia digestiva, mejoró la calidad de las heces y del pelaje y permitió una ganancia de peso de entre 2 y 10 kg con respecto al alimento anterior, además de permitir la recuperación de una condición corporal óptima tras un periodo de 2 meses (Biourge y Fontaine, 2004). Dichas observaciones sugieren que las dietas ricas en materias grasas y altamente digestibles no están contraindicadas en el tratamiento de la IPE. Tradicionalmente, se consideraba que un suplemento dietético con triglicéridos de cadena media (2-4 ml/comida) era un buen método de proporcionar energía a los perros que presentaban una malnutrición grave y que consumían alimentos altamente digestibles pero con bajo contenido en lípidos. Puesto que no existen datos que sostengan estas afirmaciones, se 170 • Suplementación enzimática inadecuada Esta es, sin duda, la principal causa de fracaso del tratamiento. Algunos perros desarrollan tal aversión hacia el suplemento enzimático, que a veces hay que utilizar páncreas fresco si los intentos por conseguir que ingiera el polvo resultan inútiles. Como efecto secundario ocasional de la suplementación enzimática, se ha descrito una estomatitis que desaparece si se reduce el aporte un 50% (Rutz et al., 2002). Por otra parte, en la mayoría de los perros con IPE, se debe considerar la posibilidad de disminuir la dosis de enzimas una vez que remiten los síntomas. Finalmente, en otro ensayo, un alimento bajo en lípidos (13% de calorías lipídicas) junto con el aporte de un suplemento enzimático (2,5 g/300 g de alimento) consiguió una ganancia media de peso, en los perros, del 24% en un periodo de cuatro meses, unida, además a una buena respuesta clínica en 17 de los 20 perros (Simpson et al., 1994). Sin embargo, la función de la alimentación no está clara, ya que la condición corporal de 11 de los 20 perros se mantuvo con éxito después del periodo de ensayo utilizando distintos tipos de alimentos. • Sobrecrecimiento bacteriano Una IPE puede afectar a la cantidad y composición de la flora del intestino delgado y comprometer la respuesta del huésped hacia una flora normal o anormal. Estas alteraciones desaparecen, normalmente, tras el tratamiento enzimático. Sin embargo, en algunos casos, es necesario administrar antibióticos para eliminar la diarrea. En estos perros, el fracaso del tratamiento podría indicar que la IPE está asociada a una disminución de la síntesis de enzimas por parte de la mucosa intestinal. Cuando la medida de las concentraciones séricas de cobalamina y folatos no permite identificar con precisión la presencia de una flora anormal, se puede proponer un tratamiento con oxitetraciclina (20 mg/kg VO 3x/día durante 28 días) o con tilosina (10 mg/kg VO 3x/día). • Patología del intestino delgado Los resultados de las pruebas hematológicas y bioquímicas de rutina son casi siempre normales en caso de IPE no complicada: por ese motivo, hay que buscar posibles anomalías como, por ejemplo, una hipoproteinemia que pueda sugerir una enteropatía perdedora de proteínas. • Modificaciones dietéticas Sólo cuando se hayan comprobado las causas frecuentes de fracaso terapéutico (suplementación enzimática inadecuada, proliferación bacteriana o intolerancia, además de patologías concomitantes del intestino delgado), hay que plantearse las modificaciones nutricionales. El tratamiento alimentario de las enfermedades de intestino delgado se basa normalmente en la utilización de un alimento altamente digestible que contenga arroz como fuente de almidón y restringido en grasas. Si se sospecha de una sensibilidad alimentaria, debe utilizarse una dieta hipoalergénica a base de proteína hidrolizada. Los hidrolizados se obtienen de la proteolisis enzimática de las proteínas originales, la cual da lugar a péptidos con un tamaño suficientemente pequeño como para que ya no puedan ser reconocidos por el sistema inmune ni desencadenen una reacción inmunitaria (Guilford, 1996). Además, estos péptidos son altamente digestibles, por lo que se disminuye su tiempo de permanencia en la luz intestinal. Los hidrolizados de soja son muy utilizados para prevenir la alergia alimentaria en los bebés y en los terneros (Lallès et al., 1995; Terracciano et al., 2002). Si los síntomas gastrointestinales desaparecen tras la prueba alimentaria (en general, en una o dos semanas) es necesario realizar el test de provocación para confirmar el diagnóstico de intolerancia alimentaria. Es necesaria la adición de antígenos específicos como los de vaca, soja o pollo a la dieta que indujo la remisión para apoyar la hipótesis de hipersensibilidad. 171 Páncreas > Fracaso del tratamiento La mejora observada en los perros (n=14) alimentados con una dieta seca “con contenido moderado en lípidos, altamente digestible y baja en fibras” durante cuatro semanas, frente a los perros que recibían su alimento de mantenimiento habitual, se limitaba a una tendencia a la reducción de borborigmos, de flatulencias y del volumen fecal, en 8 de los 14 perros (Westermarck et al., 1990). Otro estudio realizado en 21 perros con IPE no consiguió demostrar que una dieta baja en fibras y en grasas (13% de calorías lipídicas) tuviera un beneficio significativo con respecto al alimento de mantenimiento estándar o a la dieta casera (Westermarck et al., 1995). 1 - Insuficiencia pancreática exocrina puede evitar dicho suplemento proporcionando un alimento rico en materia grasa, con mayor densidad energética, que favorezca la rápida recuperación de la condición corporal óptima. La importancia de los cambios nutricionales para el tratamiento de la IPE no está todavía clara. Puesto que el gasto asociado a las dietas específicas constituye, a menudo, un motivo de eutanasia, se puede orientar la prescripción inicial hacia un alimento de mantenimiento de buena calidad, altamente digestible, al que le hayan añadido un suplemento enzimático adecuado. Si la respuesta al tratamiento resulta insuficiente, se puede considerar la posibilidad de realizar otra prescripción dietética (véase el apartado “Fracaso del tratamiento”). Si la respuesta al tratamiento sigue siendo débil, debe probarse un tratamiento contra la acidez para proteger las enzimas pancreáticas y modificaciones empíricas de la alimentación, al tiempo que se revisa cuidadosamente el diagnóstico de IPE y se tienen en cuenta otros problemas subyacentes. Deben someterse a un examen del intestino delgado aquellos perros en que esté confirmada la IPE, pero que respondan débilmente a un suplemento enzimático apropiado y a un tratamiento antibiótico. Conclusión/pronóstico En la mayoría de los perros que padecen IPE, un alimento de mantenimiento de alta cantidad suplementado con enzimas pancreáticas en polvo puede solucionar la mayor parte de los trastornos asociados a esta patología, aunque el coste relativamente alto del suplemento enzimático y de los alimentos específicos tal vez afecte significativamente al resultado y precipite la eutanasia. Cuando además hay asociada una pancreatitis o diabetes, el pronóstico es más reservado. FIGURA 10 - PASTOR ALEMÁN QUE PADECE INSUFICIENCIA PANCREÁTICA EXOCRINA (A) Antes del tratamiento © Reproducción amablemente autorizada por J. Fontaine © Reproducción amablemente autorizada por J. Fontaine 1 - Insuficiencia pancreática exocrina Páncreas Es interesante constatar que la utilización de un alimento a base de hidrolizado de soja y con un contenido en lípidos relativamente alto, ha resultado eficaz para conseguir un aumento de peso, disminuir la diarrea y mejorar el aspecto del pelo de tres perros con IPE que no habían respondido a los tratamientos dietéticos anteriores asociados a extractos pancreáticos (Biourge y Fontaine, 2004)(Figura 10). (B) Después del tratamiento Antes (A) y después (B) de un tratamiento dietético con un alimento a base de hidrolizado de soja y de arroz. 172 P R El coste de las enzimas pancreáticas es demasiado alto para el propietario del perro. ¿Hay soluciones alternativas? Para reducir el coste del tratamiento enzimático, es posible suministrar al perro páncreas fresco de vaca o de cerdo, que puede congelarse en raciones individuales. No obstante, la administración de un extracto pancreático en polvo generalmente resulta más práctica, y la dosis puede disminuirse con el tiempo, lo cual reduce el coste del tratamiento. ¿Hay que pre-incubar el alimento con las enzimas pancreáticas? No. Es suficiente con espolvorear las enzimas sobre el alimento y mezclarlo bien. No es necesaria una pre-incubación. ¿El perro va a tener que tomar suplementos de enzimas pancreáticas durante toda su vida? Normalmente, así es. No obstante, la cantidad de enzimas a menudo se puede disminuir a menos de la mitad con el transcurso del tiempo. Incluso puede suceder que algunos perros se mantengan sin tomar ninguna enzima. ¿Un perro que padece insuficiencia pancreática puede utilizarse para la reproducción? La atrofia acinar del páncreas es hereditaria en ciertas razas como el Pastor Alemán y Collie de pelo largo. Por ello no se recomienda la utilización para la cría de perros que padecen IPE o que proceden de líneas que presentan ésta enfermedad. 173 Páncreas Preguntas frecuentes Preguntas frecuentes sobre la insuficiencia pancreática exocrina Bibliografía Bibliografía Adamama-Moraitou K, Rallis T, Papasteriadis A et al - Iron, zinc, and copper concentration in serum, various organs, and hair of dogs with experimentally induced exocrine pancreatic insufficiency. Dig Dis Sci 2001; 46(7): 1444-57. Páncreas Adamama-Moraitou KK, Rallis TS, Prassinos NN et al - Serum vitamin A concentration in dogs with experimentally induced exocrine pancreatic insufficiency. Int J Vitam Nutr Res 2002; 72(3): 177-82. Batt RM, Bush BM, Peters TJ - Biochemical changes in the jejunal mucosa of dogs with naturally occurring exocrine pancreatic insufficiency. Gut 1979; 20(8): 709-15. Batt RM, Horadagoda NU, McLean L et al Identification and characterization of a pancreatic intrinsic factor in the dog. Am J Physiol 1989; 256(3 Pt 1): G517-23. Biourge V, Fontaine J - Exocrine Pancreatic Insufficiency and Adverse Reaction to Food in Dogs: a Positive Response to a High-Fat, Soy Isolate Hydrolysate-Based diet. J of Nutrition 2004; 134: 2166S-2168S. Boari A, Williams DA, Famigli-Bergamini P Observations on exocrine pancreatic insufficiency in a family of English setter dogs. J Small Anim Pract 1994; 35: 247-251. Guilford WG - Adverse reactions to food and Nutritional management of gastrointestinal diseases. In: Strombeck’s small animal gastroenterology 1996; Guilford WG, Center SA, Strombeck DR, Williams DA & Meyer DJ eds, 436-450 & 889-910. WB Saunders Company, Philadelphia, A. Hall EJ, Bond PM, Butt RM et al - A survey of the diagnosis and treatment of canine exocrine pancreatic insufficiency. J Small Anim Pract 1991; 32: 613-619. Hellmann J, Loppnow H - Hyperplasia of somatostatin and pancreatic polypeptide immunoreactive cells in dogs with idiopathic atrophy of the exocrine pancreas. Zentralbl Veterinarmed A 1991; 38(2): 80-9. Lallès, JP, Toullec R, Branco Pardal P et al. Hydrolyzed soy protein isolate sustains high nutritional performance in veal calves. J Dairy Sci 1995; 78: 194-204. Moeller EM, Steiner JM, Clark LA et al Inheritance of pancreatic acinar atrophy in German Shepherd Dogs. Am J Vet Res 2002; 63(10): 1429-34. 174 Pidgeon G - Effect of diet on exocrine pancreatic insufficiency in dogs. J Am Vet Med Assoc 1982; 181(3): 232-5. Pidgeon G, Strombeck DR - Evaluation of treatment for pancreatic exocrine insufficiency in dogs with ligated pancreatic ducts. Am J Vet Res 1982; 43(3): 461-4. Raiha M, Westermack E - The signs of pancreatic degenerative atrophy in dogs and the role of external factors in the etiology of the disease. Acta Vet Scand. 1989; 30(4): 447-52. Rogers WA, O’Dorisio TM, Johnson SE et al Postprandial release of gastric inhibitory polypeptide (GIP) and pancreatic polypeptide in dogs with pancreatic acinar atrophy. Correction of blunted GIP response by addition of pancreatic enzymes to a meal. Dig Dis Sci 1983; 28(4): 345-9. intestinal microvillar membrane proteins by polyacrylamide gel electrophoresis: a comparison between normal dogs and dogs with exocrine pancreatic insufficiency. Biochim Biophys Acta 1988; 955(3): 275-82. Suzuki A, Mizumoto A, Rerknimitr R et al - Effect of bacterial or porcine lipase with low- or high fat diets on nutrient absorption in pancreatic-insufficient dogs. Gastroenterology 1999; 116: 431-437. Terracciano L, Isoardi P, Arrigoni S et al - Use of hydrolysates in the treatment of cow’s milk allergy. Ann Allergy Asthma Immunol 2002; 89 (6 Suppl 1): 86-90. Westermarck E - The hereditary nature of canine pancreatic degenerative atrophy in the German shepherd dog. Acta Vet Scand 1980; 21(3): 389-94. Rutz GM, Steiner JM, Williams DA - Oral bleeding associated with pancreatic enzyme supplementation in three dogs with exocrine pancreatic insufficiency. J Am Vet Med Assoc 2002; 221(12): 1716-8. Westermarck E -Treatment of pancreatic degenerative atrophy with raw pancreas homogenate and various enzyme preparations. Zentralbl Veterinarmed A 1987; 34(10): 728-33. Simpson KW, Alpers DH, De Wille J et al - Cellular localization and hormonal regulation of pancreatic intrinsic factor secretion in dogs. Am J Physiol 1993; 265(1 Pt 1): G178-88. Westermarck E, Batt RM, Vaillant C et al Sequential study of pancreatic structure and function during development of pancreatic acinar atrophy in a German shepherd dog. Am J Vet Res 1993a; 54(7): 1088-94. Simpson KW, Johnstone JMS, Bell PRF et al Pancreatic function following partial pancreatectomy and anastomosis of the pancreatic duct to the stomach or duodenum in dogs. Res Vet Sci 1992; 52: 97-104. Westermarck E, Junttila JT, Wiberg ME - Role of low dietary fat in the treatment of dogs with exocrine pancreatic insufficiency. Am J Vet Res 1995; 56: 600-605. Simpson JW, Maskell IE, Quigg J et al - Long term management of canine exocrine pancreatic insufficiency. J Small Anim Pract 1994; 35: 133-138. Westermarck E, Myllys V, Aho M - Effect of treatment on the jejunal and colonic bacterial flora of dogs with exocrine pancreatic insufficiency. Pancreas 1993b; 8(5): 559-62. Simpson KW, Morton DB, Batt RM - Effect of exocrine pancreatic insufficiency on cobalamin absorption in dogs. Am J Vet Res 1989a; 50(8): 1233-6. Westermarck E, Wiberg M - Exocrine pancreatic insufficiency in dogs.Vet Clin North Am Small Anim Pract. 2003; 33(5):1165-79. Simpson KW, Morton DB, Sorensen SH et al Biochemical changes in the jejunal mucosa of dogs with exocrine pancreatic insufficiency following pancreatic duct ligation. Res Vet Sci 1989b; 47(3): 338-45. Simpson KW, Simpson JW, Lake S et al - Effect of pancreatectomy on plasma activities of amylase, isoamylase, lipase and trypsin-like immunoreactivity in dogs. Res Vet Sci 1991; 51: 78-82. Sorensen SH, Riley JE, Lobley RW et al Investigation of the physical properties of dog Westermarck E, Wiberg M, Junttila J - Role of feeding in the treatment of dogs with pancreatic degenerative atrophy. Acta Vet Scand 1990; 31(3): 325-31 Wiberg ME - Pancreatic acinar atrophy in German shepherd dogs and rough-coated collies. Etiopathogenesis, diagnosis and treatment. A review. Vet Q 2004; 26(2): 61-75. Wiberg ME, Lautala HM, Westermarck E Response to long-term enzyme replacement treatment in dogs with exocrine pancreatic insufficiency. J Am Vet Med Assoc 1998; 1; 213(1): 86-90. Bibliografía Wiberg ME, Saari SA, Westermarck E - Exocrine pancreatic atrophy in German Shepherd Dogs and Rough-coated Collies: an end result of lymphocytic pancreatitis. Vet Pathol 1999b; 36(6): 530-41. Wiberg ME, Westermarck E - Subclinical exocrine pancreatic insufficiency in dogs. J Am Vet Med Assoc 2002; 220(8): 1183-7. Williams DA, Batt RM, McLean L - Bacterial overgrowth in the duodenum of dogs with exocrine pancreatic insufficiency. J Am Vet Med Assoc 1987; 191: 201-206. 76. Williams DA, Batt RM - Sensitivity and specificity of radioimmunoassay of serum trypsin-like immunoreactivity for the diagnosis of canine exocrine pancreatic insufficiency. J Am Vet Med Assoc 1988; 192: 195-201. Páncreas Wiberg ME, Nurmi AK, Westermarck E - Serum trypsinlike immunoreactivity measurement for the diagnosis of subclinical exocrine pancreatic insufficiency. J Vet Intern Med 1999a; 13(5): 426-32. 175 2 - Pancreatitis aguda: diagnóstico Recordatorio diagnóstico El diagnóstico de la pancreatitis aguda se basa en una asociación coherente de signos clínicos, resultados clinicopatológicos y elementos de diagnóstico por imagen. Puede que sea necesaria una biopsia obtenida quirúrgicamente para confirmar el diagnóstico y para diferenciar una inflamación de una neoplasia. > Anamnesis La anamnesis puede desvelar episodios recientes de indiscreción, de ingestión de alimentos tóxicos (p. ej., chocolate o alimentos muy grasos) o de administración de medicamentos. Los signos clínicos más frecuentes son letargia, anorexia, posición encorvada, vómitos (con o sin sangre), diarrea (con o sin sangre), frecuencia respiratoria incrementada y abdomen voluminoso. Algunos perros pueden presentar ictericia precedida de vómitos. © KW Simpson Páncreas 2 - Pancreatitis aguda Perro con pancreatitis aguda. Se puede manifestar poliuria y polidipsia en perros con diabetes mellitus asociada a la pancreatitis. > Examen físico El cuadro clínico que acompaña la pancreatitis aguda es muy variable: abatimiento, deshidratación moderada con signos de dolor abdominal, síndrome abdominal agudo, estado de choque (taquicardia, tiempo de relleno capilar prolongado, sequedad de mucosas, hipotermia), petequias, ictericia y ascitis. En algunos perros es palpable una masa abdominal. > Pruebas complementarias – hallazgos clinicopatológicos • Hematología Los resultados son variables y van desde una ligera neutrofilia y un hematocrito ligeramente aumentado, pasando por una marcada leucocitosis con o sin desviación a la izquierda y una trombocitopenia, hasta una anemia y una neutropenia degenerativa con desviación a la izquierda. Cuando se detecta una trombocitopenia, se realizan pruebas de hemostasia (TP, TPTA, PDF o dímero D, fibrinógeno, antitrombina III) para determinar si el perro padece una coagulopatía intravascular diseminada (CID). • Pruebas de bioquímica sérica Entre las alteraciones de la bioquímica sérica que se puede encontrar, se incluyen: azoemia (prerrenal o renal), aumento de las concentraciones de las enzimas hepáticas (ALT, AST, ALP), hiperbilirrubinemia, lipemia, hiperglucemia, hipoproteinemia, hipocalcemia, acidosis metabólica y variaciones del sodio, del potasio y del cloruro séricos (generalmente, a la baja). • Análisis de orina Permite saber si la azoemia es de origen renal o prerrenal. En algunos perros con pancreatitis aguda se observa una proteinuria, que posiblemente es consecuencia de las lesiones glomerulares producidas por las enzimas pancreáticas y que, normalmente, es transitoria. La glucosuria o la cetonuria indican la presencia de una diabetes mellitus. • Enzimas pancreáticas específicas 176 Tradicionalmente en el perro se utilizaba el incremento de la actividad de la amilasa y de la lipasa séricas como indicadores de una inflamación pancreática. Sin embargo, dichas enzimas pueden encontrarse elevadas en patologías no pancreáticas y, por otro lado, perros con pancreatitis confirmada histológicamente pueden presentar una actividad normal de la lipasa (28-61% de los perros) y de la amilasa (31-47% de los perros) (Strombeck et al., 1981; Hess et al., 1998; Mansfield et al., 2003). Estas limitaciones han conducido al desarrollo de pruebas enzimáticas o de marcadores de origen pancreático como los niveles del tripsinógeno circulante (TLI trypsine-like inmunorreactivity), del péptido de la activación del tripsinógeno (PAT) y de la lipasa pancreática (test de inmunorreactividad de la lipasa pancreática o PLI). En algunos estudios se han observado concentraciones altas de TLI, PAT y PLI en perros con pancreatitis aguda experimental. Se han observado aumentos del PAT en el suero y la orina de los perros con pancreatitis grave, pero el PAT parece ser mejor indicador para el pronóstico que para el diagnóstico de una inflamación pancreática (Mansfield y Jones, 2000; Mansfield et al., 2003). La experiencia que se tiene con la PLI es todavía más limitada, aunque parece más prometedora que la TLI; el incremento de la PLI en el suero es más importante y duradero que el de la TLI. Aunque enfermedades como las nefropatías pueden hacer que la TLI, el PAT y la PLI aumenten. Páncreas Concentraciones normales, ligeramente disminuidas o aumentadas de TLI se han observado en perros con pancreatitis confirmada y el nivel de TLI no predice la gravedad de la enfermedad (Ruaux y Atwell, 1999). 2 - Pancreatitis aguda: diagnóstico No se ha evaluado por completo la utilidad de las pruebas TLI, PAT y PLI para el diagnóstico de la pancreatitis espontánea en el perro. • Radiografía Los hallazgos radiográficos en perros con pancreatitis son, generalmente, poco específicos: serosa mal definida, aumento de la opacidad en el cuadrante craneal derecho del abdomen, desplazamiento del duodeno ventralmente y/o hacia la derecha, dilatación del duodeno con disminución de su motilidad y desplazamiento caudal del colon transverso. En perros con pancreatitis crónica, ocasionalmente se puede encontrar un punteado que se corresponde con pequeñas calcificaciones, esto indica una saponificación de la grasa mesentérica alrededor del páncreas. Hallazgos ecográficos en un perro. Las radiografías torácicas permiten la detección de líquido pleural, un edema o una neumonía, que en el perro, pueden estar asociados a una pancreatitis. • Ecografía En otras alteraciones pueden darse signos ecográficos idénticos a los que se observa cuando hay una pancreatitis (Figura 11): en caso de tumor pancreático, edema del páncreas (asociado a una hipoproteinemia o a una hipertensión portal) y cuando las estructuras peripancreáticas se encuentran dilatadas (Lamb et al., 1995). La toma de muestras de las lesiones cavitarias, realizada por aspiración con aguja fina, puede resultar útil para diferenciar un absceso de un pseudoquiste. • Otros tipos de diagnóstico por imágenes © KW Simpson Un estudio realizado en perros que padecían una pancreatitis aguda mortal demostró que la ecografía puede ayudar a confirmar el diagnóstico de pancreatitis en 23 de cada 24 perros (Hess et al.,1998). Figura 11A - El páncreas aparece ligeramente aumentado con márgenes irregulares y ecogenicidad mixta. La grasa mesentérica de la zona craneal derecha del abdomen es hiperecogénica y dispersa el sonido. La tomografía de contraste es la técnica de elección de diagnóstico por imagen para las personas con pancreatitis y permite distinguir una necrosis pancreática de una pancreatitis moderada. En el perro sólo se ha utilizado para evaluaciones preliminares (Jaeger et al., 2003). • Paracentesis abdominal El análisis del líquido peritoneal puede ayudar a determinar las diferentes causas que provocan un síndrome abdominal agudo: pancreatitis, perforación gastrointestinal o rotura del conducto biliar. Puede realizarse una intervención quirúrgica en los pacientes que presenten una pancreatitis persistente o recurrente con el fin de confirmar el diagnóstico y de detectar una neoplasia o factores de complicación como una infección. La cirugía está indicada para drenar los abscesos pancreáticos y los pseudoquistes persistentes (Salisbury et al., 1988). La aparición de técnicas de laparoscopia puede ayudar a disminuir la morbilidad (Harmoinen et al., 2002). La cirugía también está indicada para colocar sondas de nutrición enteral (véase el apartado “Tratamiento nutricional”); debe considerarse la posibilidad de colocar una sonda de alimentación, antes de realizar una cirugía exploratoria, en aquellos perros que presenten indicios de pancreatitis. © KW Simpson • Cirugía Figura 11B - El duodeno, en su curvatura craneal, tiene un diámetro de 1,6 cm con un espesor de pared de 6,2 mm. Existe una cantidad moderada de gas en el duodeno que tiene un aspecto ondulado. Conclusión: sospecha de pancreatitis, peritonitis focal. 177 2 - Pancreatitis aguda: diagnóstico > Diagnóstico diferencial El diagnóstico diferencial de la pancreatitis aguda en el perro se centra, principalmente, en las causas de los vómitos y del dolor abdominal (Tabla 3). El conjunto de los antecedentes, el examen clínico, los análisis clinicopatológicos y las imágenes obtenidas se utiliza para diferenciar una pancreatitis de otras causas de vómito: metabólicas, infecciosas, polisistémicas, tóxicas, neurológicas e intraabdominales. TABLA 3 - DIAGNÓSTICO DIFERENCIAL DE LAS CAUSAS DE DOLOR ABDOMINAL Y VÓMITOS Páncreas Causas del dolor abdominal Gástrica Intestinal - Dilatación/vólvulo, ulceración - Obstrucción, intususcepción, rotura, torsión, enteritis Pancreática Hepática - Pancreatitis - Hepatitis aguda, rotura del conducto biliar, neoplasia hepática Esplénica Urogenital - Torsión, rotura, neoplasia - Nefritis, pielonefritis, rotura de la vejiga - Cálculos ureterales/uretrales, piometra, prostatitis Peritoneal - Peritonitis primaria o secundaria (química: bilis y orina; o séptica: rotura de una víscera hueca como la vejiga o el intestino, etc.) Causas de los vómitos • Intraabdominal Gástrica Intestinal • No gastrointestinal Metabólica/ Endocrina Medicamentosa Dolor pseudoabdominal - Discoespondilitis, prolapso de un disco vertebral - Gastritis, úlcera, neoplasia, obstrucción al flujo, cuerpo extraño - Motilidad / alteraciones funcionales - Enfermedad inflamatoria intestinal, neoplasia, cuerpo extraño, intususcepción, torsión, rotura, proliferación bacteriana - Alteraciones funcionales Tóxica Dietética Neurológica Infecciosa - Páncreas: pancreatitis, neoplasia pancreática - Hígado: colangiohepatitis, obstrucción biliar - Genitourinario: piometra, nefritis, nefrolitiasis, obstrucción urinaria, prostatitis - Peritonitis - Uremia, hipoadrenocorticismo cetoacidosis diabética - Encefalopatía hepática, hipercalcemia, septicemia - Digoxina, eritromicina, quimioterapia, apomorfina, xilacina - Estricnina, etilenglicol, plomo - Indigestión, intolerancia, alergia - Enfermedad vestibular, encefalitis, neoplasia, aumento de la presión intracraneal - Moquillo, parvovirus, hepatitis infecciosa canina, leptospirosis, salmonelosis Cuando el dolor abdominal constituye el signo principal de la consulta, hay que realizar rápidamente una radiografía, una ecografía y una paracentesis e iniciar un tratamiento de mantenimiento basado en los signos clínicos y los análisis clinicopatológicos efectuados inicialmente (Macintire,1988). Se puede observar una diarrea sanguinolenta en los perros que padecen pancreatitis aguda. Deben tenerse en cuenta la pancreatitis aguda y sus complicaciones (infección, pseudoquistes o formación de abscesos) en el diagnóstico diferencial de la ictericia y de la pirexia. > Errores frecuentes Es posible que se diagnostique erróneamente una pancreatitis cuando los signos clínicos o los análisis clínicopatológicos son los únicos criterios de diagnóstico utilizados. Una enteritis aguda, una obstrucción intestinal y diferentes causas de síndrome abdominal agudo pueden dar lugar a hallazgos clínicos y clinicopatológicos muy parecidos a los de una pancreatitis. 178 2 - Pancreatitis aguda: epidemiología Confiar demasiado en los marcadores séricos de las enfermedades pancreáticas puede llevar a un error de diagnóstico. Los aumentos de la amilasa y de la lipasa séricas se encuentran, habitualmente, en gran número de patologías y los valores normales no excluyen una pancreatitis. Las pruebas más específicas de la inflamación del páncreas como la TLI, el PAT y la PLI todavía no han sido completamente validados, por lo que su interpretación debe tomarse con cautela. Es necesario tener mucha experiencia en ecografía abdominal para ser capaz de detectar las variaciones de ecogenicidad y de tamaño del páncreas. Las imágenes obtenidas deben unirse a otros elementos de diagnóstico para confirmar o refutar una pancreatitis. La pancreatitis debe diferenciarse de una neoplasia o de otras causas de acumulación de líquido parenquimatoso como una hipertensión de la vena porta o una hipoproteinemia. Páncreas Epidemiología > Factores de riesgo El riesgo de pancreatitis es el más importante en los perros mayores o de mediana edad (más de 5 años) que tienen sobrepeso. No hay una clara predisposición de sexo. Un episodio de indiscreción alimentaria, el consumo de alimentos demasiado ricos en grasas y la administración de medicamentos (p. ej., azatioprina, fenobarbital y bromuro potásico) o de tóxicos (p. ej., organofosforados) en ocasiones preceden al desarrollo de los signos clínicos de pancreatitis en el perro (Simpson, 1993; Hess et al., 1999). Asimismo, las endocrinopatías como el hipotiroidismo, la diabetes mellitus y el hiperadrenocorticismo pueden representar factores de riesgo (Hess et al., 1999). De 221 perros con diabetes mellitus, el 13% presentaban signos histológicos de pancreatitis aguda. La hiperlipidemia representa también un factor de riesgo potencial (Hess et al., 2000). • Predisposiciones raciales El Schnauzer Miniatura, el Yorkshire, el Silky Terrier, y tal vez el Caniche Miniatura, tienen mayor riesgo de desarrollar una pancreatitis. Todavía no se comprende bien la etiología y la patogenia de la pancreatitis espontánea (Karne y Gorelick, 1999; Zyromski y Murr, 2003). Una gran variedad de factores están asociados o han sido señalados experimentalmente como causas de la pancreatitis aguda del perro. En la Figura 12 se resumen las causas potenciales de la pancreatitis que tienen relación con la nutrición. © Hermeline Mecanismos fisiopatológicos El Schnauzer Miniatura tiene un mayor riesgo de desarrollar una pancreatitis. FIGURA 12 - CAUSAS POTENCIALES DE PANCREATITIS RELACIONADAS CON LA NUTRICIÓN Clínicas Experimentales Indiscreción alimentaria Alimento muy rico en grasas o muy rico en grasas y bajo en proteínas Obesidad (a) Suplemento de etionina™ sin determinar: un análogo de la metionina (Simpson, 1993) Hiperlipidemia (b) Hiperestimulación por la CCK Administración i.v de ácidos grasos libres 12a 12b 179 2 - Pancreatitis aguda: mecanismos fisiopatológicos Páncreas Clínicamente, la inflamación del páncreas puede ser clasificada en lineas generales como aguda, aguda recurrente o crónica. Las pancreatitis agudas o agudas recurrentes se caracterizan por episodios inflamatorios repentinos y representan la forma más frecuente de pancreatitis en el perro. • Una pancreatitis aguda puede curarse o puede provocar una inflamación crónica (crónica o aguda recurrente) o una necrosis que pueden complicarse con una infección secundaria y con pseudoquistes o con la formación de abscesos (Figuras 13 y 14). • Una pancreatitis crónica se caracteriza por una débil degradación o una inflamación subclínica y puede constituir un factor de desarrollo de diabetes mellitus o de insuficiencia pancreática exocrina (IPE) en el perro. Figura 13 - Absceso pancreático El absceso pancreático es una complicación accidental de la pancreatitis aguda del perro. El tratamiento, generalmente, es quirúrgico. Sin tener en cuenta la causa inicial, una pancreatitis aparece generalmente cuando las enzimas digestivas son activadas prematuramente en el páncreas. Experimentalmente, la hiperestimulación pancreática con colecistoquinina (CCK), o con su análogo la ceruleína, la suplementación con metionina o la obstrucción del conducto pancreático conducen a la formación de grandes vacuolas en el interior de las células acinares. La formación de vacuolas parece ser la consecuencia de la falta de combinación entre la exocitosis del cimógeno y la circulación intracelular anormal de las enzimas digestivas y lisosómicas. Estas alteraciones intracelulares precipitarían la activación intracelular de las enzimas digestivas. Asimismo, una hiperestimulación pancreática podría explicar la pancreatitis espontánea del perro. La CCK normalmente es liberada por las células del duodeno como respuesta a la llegada de los lípidos y los aminoácidos a la zona intraluminal. La CCK regula y estimula la secreción pancreática y las contracciones de la vesícula biliar durante la digestión. Una alimentación muy rica en grasas podría estimular la liberación excesiva de colecistoquinina. La hiperestimulación podría también deberse a una hipercalcemia, a la presencia de organofosforados o a un nivel alto de glucocorticoides circulantes (que potenciarían la sensibilidad del páncreas a una hiperestimulación), aunque esto no ha sido demostrado. FIGURA 14 - PROPUESTA DEL MECANISMO DE EVOLUCIÓN DE LA PANCREATITIS EN EL PERRO (Fuente: Simpson y Lamb, 1995) Factores de riesgo Mecanismo desencadenante Liberación de enzimas y de mediadores inflamatorios Pancreatitis aguda Pancreatitis crónica Acumulación de líquido Efectos locales y sistémicos Pseudoquiste Bacterias Hipoperfusión Absceso Necrosis 180 Necrosis infectada FIGURA 15 - PANCREATITIS EDEMATOSA Y ACTIVACIÓN INTRAPANCREÁTICA DEL TRIPSINÓGENO PAT plasmática (nM/l) PAT en la orina (nM/l) B A C Horas Edema Ascitis Plasma Orina Zona hipoecogénica que corresponde a una acumulación de líquido. La pancreatitis edematosa se considera generalmente como la forma de pancreatitis más leve (A). Está relacionada con una activación autolimitante del tripsinógeno y con la liberación del péptido de la activación del tripsinógeno (PAT) en la circulación (B). En el cuadro clínico, la acumulación de líquido en el páncreas puede ser detectada por ecografía (C). La liberación de enzimas pancreáticas activas y de mediadores inflamatorios a partir del páncreas, como el factor de necrosis tumoral (FNT), la interleucina 1 (IL-1) y el factor de activación plaquetaria (FAP), aumenta la gravedad de la inflamación pancreática y afecta a la función de muchos órganos (respuesta inflamatoria sistémica), provocando alteraciones de los equilibrios hídrico, electrolítico y acidobásico (Denham y Norman, 1999; Ruaux et al., 1999; Brady y Otto, 2001; Mentula et al., 2004; Raraty et al., 2004). FIGURA 16 - NECROSIS PANCREÁTICA Y SUS CONSECUENCIAS A B Una pancreatitis grave se caracteriza por una trombosis y una necrosis pancreática (A) con liberación de enzimas y de mediadores inflamatorios, lo cual provoca una respuesta inflamatoria sistémica y una disfunción del órgano. Las consecuencias clínicas con respecto a la coagulación son la presencia de petequias (B) debidas a una trombocitopenia y la equimosis asociada a una coagulación intravascular diseminada. 181 Páncreas 2 - Pancreatitis aguda: mecanismos fisiopatológicos Una pancreatitis edematosa inducida por la hiperestimulación de la CCK en el perro se caracteriza por una activación rápida, aunque limitada en el tiempo, del tripsinógeno (Figura 15), lo cual sugiere que el páncreas posee un mecanismo de retrorregulación destinado a limitar la síntesis y la activación del tripsinógeno (véase el apartado “Tratamiento nutricional”) (Simpson et al., 1995). Este concepto de retrorregulación pancreática es importante para planificar una intervención nutricional en caso de pancreatitis aguda. 2 - Pancreatitis aguda: tratamiento nutricional Páncreas Lo que diferencia una pancreatitis moderada de una pancreatitis severa, potencialmente mortal, es el desarrollo de alteraciones multisistémicas. Esclarecer la respuesta inflamatoria sistémica es abrir la puerta a nuevos tratamientos de la pancreatitis aguda. Esto constituye actualmente uno de los ejes de investigación (Johnson et al., 2004; Oruc et al., 2004). Tratamiento nutricional > Identificar y prevenir o tratar los factores nutricionales asociados a la pancreatitis En el perro, la obesidad, la hiperlipidemia y los episodios de indiscreción pueden estar relacionados con una pancreatitis. Si dichos elementos están presentes, es conveniente buscar la causa subyacente para intentar prevenir futuros accesos de pancreatitis. > Aporte de nutrientes a los perros con pancreatitis Hacer recomendaciones nutricionales precisas cuando el perro padece una pancreatitis aguda es difícil debido a la ausencia de estudios fiables al respecto. Con frecuencia, las recomendaciones se basan en las observaciones empíricas. > El dilema entre alimentar y estimular al páncreas La secreción pancreática, en un perro que goza de buena salud, se produce como respuesta a la ingestión de nutrientes, fundamentalmente de lípidos y aminoácidos liberados en el duodeno (Figura 17). Si las cantidades ingeridas están restringidas o si la alimentación se realiza por vía intravenosa, la secreción pancreática disminuye (Stabile et al., 1984). Por lo tanto, es ampliamente aceptado que para permitir que el páncreas descanse, se debe suprimir la alimentación oral hasta la desaparición de los signos clínicos o cuando los síntomas persistan durante aproximadamente 72-96 horas tras el inicio de la alimentación parenteral. Este dogma prevalece todavía en medicina veterinaria y humana. FIGURA 17 - REGULACIÓN DE LA SECRECIÓN PANCREÁTICA (según Johnson, 1997) Células 1 Célula parietal Péptidos + aminoácidos Nervio vago Proteínas Lípidos Lípidos CCK Células S Secretina H+ Células del conducto pancreático H+ HCO-3 Enzima Células acinares CCK Las hormonas como la CCK y la secretina, el sistema parasimpático y los nervios del duodeno y del páncreas participan en la activación de la secreción pancreática como respuesta a la llegada de los alimentos. 182 Los pacientes con pancreatitis aguda alimentados por vía yeyunal (por ejemplo, mediante tubos orales transpilóricos), tienen menor morbilidad, sus estancias hospitalarias son más cortas y los gastos son menos elevados que aquellos alimentados totalmente por vía parenteral (Figura 17) (Kalfarentzos et al., 1997; McClave et al., 1997; Windsor et al., 1998; Powell et al., 2000; Pupelis et al., 2000; Paraskeva et al., 2001; Duerksen et al., 2002). Dado que hoy en día es posible situar sondas de yeyunostomía de forma no quirúrgica en el perro (por la nariz, el esófago o el estómago), el procedimiento quirúrgico no debería ser un factor limitante de esta técnica de alimentación. No obstante, sigue abierta la pregunta de si los perros que padecen una pancreatitis aguda necesitan realmente que se liberen los nutrientes en el yeyuno. El páncreas de los perros con pancreatitis aguda experimental (véase el apartado “Pancreatitis inducida por la CCK”) y el de las personas con pancreatitis aguda grave espontánea no son tan sensibles a la estimulación como un páncreas normal. Los perros que se recuperan de una pancreatitis natural muestran unas concentraciones de TLI circulante inferiores a las normales, lo cual sugiere que la síntesis de enzimas pancreáticas está autolimitada. Además, cuando hay una pancreatitis aguda en el hombre o en el perro, la nutrición enteral resulta interesante por la disminución de la respuesta inflamatoria sistémica y de la translocación bacteriana más que por la disminución de la estimulación pancreática. Desde este punto de vista, los tratamientos probióticos pueden resultar interesantes y están siendo sometidos a estudio en el hombre (Olah et al., 2002). La alimentación líquida por sonda nasoesofágica (41% de proteínas, 18% de lípidos, 3% de fibra bruta) tiene un efecto positivo sobre la permeabilidad intestinal y la morbilidad en los perros con parvovirosis. Esto apoya la idea de que la alimentación enteral en general, más que la yeyunal en particular, es la responsable de los efectos positivos de la nutrición enteral, aunque esto todavía tiene que ser valorado de manera crítica (Mohr et al., 2003). A pesar de la evidencia de los ensayos clínicos efectuados en el hombre y de los estudios experimentales realizados en el perro, la resistencia a alimentar a los perros con pancreatitis por vía enteral es algo que cabe esperar. Uno de los argumentos que se emplea con frecuencia para optar por la nutrición parenteral es que los vómitos son demasiado frecuentes para que se pueda utilizar la vía enteral. Sin embargo, estudios recientes demuestran que los perros con parvovirosis toleran bien la alimentación nasoesofágica a pesar de tener vómitos y diarreas graves. Los perros alimentados por vía enteral se recuperan más rápido, presentan mayor ganancia de peso y menor permeabilidad intestinal que los perros que se mantuvieron sólo por vía oral (Mohr et al., 2003). No se trata de suprimir totalmente la nutrición parenteral, pero su empleo debe limitarse a los perros que la necesiten realmente, por ejemplo, a aquellos a los que los vómitos constantes impiden un aporte energético suficiente. Cuando la nutrición parenteral esté indicada, se debe elegir entre la nutrición parenteral total o parcial. La elección de la nutrición parenteral parcial es un procedimiento más práctico y más manejable , y en muchos casos constituye un modo más seguro y más eficaz de responder a las necesidades nutricionales de los perros con pancreatitis o con enfermedades gastrointestinales (Chan et al., 2002). Curiosamente, los perros que reciben una combinación de nutrición enteral y parenteral parcial tienen una esperanza de vida superior a la de aquellos alimentados por vía parenteral total (Chan et al., 2002). 183 Páncreas 2 - Pancreatitis aguda: tratamiento nutricional No obstante, cada vez son más numerosos los argumentos existentes a favor de la nutrición enteral en el tratamiento de la pancreatitis aguda. En el hombre y en los animales, se ha demostrado que una alimentación por vía yeyunal (distal al lugar de estimulación pancreática) no exacerba la pancreatitis aguda (Vu et al., 1999; Qin et al., 2002, 2003). 2 - Estudio de un caso de pancreatitis Páncreas ESTUDIO DE UN CASO DE PANCREATITIS Historia clínica Numerosos vómitos (bilis), inapetencia, letargia desde hace 2 días. La perra tiene libre acceso al patio trasero y ha comido basura en otras ocasiones. Examen clínico Posición encorvada (A), abatimiento, sequedad de mucosas Tiempo de relleno capilar (TRC): 1,5 s Frecuencia cardiaca: 150 Temperatura: 38,9 °C Dolor abdominal A - Perra mestiza, de 8 años de edad, esterilizada El diagnóstico diferencial debe tener en cuenta los vómitos y el dolor abdominal (véase la Tabla 3). La sequedad de mucosas, el TRC incrementado y la frecuencia cardiaca son coherentes con una hipovolemia secundaria a los vómitos. El dolor abdominal es, sin duda, la causa de la frecuencia cardiaca elevada. El esquema diagnóstico inicial incluye un recuento sanguíneo, un análisis de orina, la medida de los parámetros bioquímicos básicos (proteinemia total, BUN, glucemia), un hemograma completo, así como la medida de la amilasa y de la lipasa. Serie de datos mínimos Hematocrito 53% Proteínas totales 7,9 (g/dl) BUN 30-40 (mg/dl) Glucemia 103 mg/dl Na 136 mmol/l K 4,5 mmol/l Lipemia evidente Análisis de orina densidad: 1.047 proteínas ++ pH: 6 La interpretación de los resultados indica una hemoconcentración con una ligera azoemia prerrenal. Se pone un catéter intravenoso y se realiza una perfusión de lactato de Ringer dos veces al día a una velocidad de mantenimiento. B - Radiografía abdominal C - Ecografía abdominal 1 - Zona hiperecogénica 2 - Saponificación de las materias grasas 3 - Zona hipoecogénica: acumulación de líquido Las radiografías (B) muestran una distensión gaseosa del duodeno y una ligera pérdida de la definición abdominal compatible con una peritonitis. Se realiza una ecografía: se aprecia un páncreas voluminoso, hipoecogénico (C) y una pequeña cantidad de líquido abdominal libre. 184 2 - Estudio de un caso de pancreatitis Perfil bioquímico Hematocrito (%) 52 (42-57) Albúminas (g/dl) 2,7 (3,1-4,1) VCM (fl) 72 (63-74) Globulinas (g/dl) 3,4 (1,9-3,6) Recuento leucocitario (miles/µl) 21,1 (6,2-14,4) ALP(U.I./l) 750 (12-122) Neutrófilos (miles/µl) 19 (3,4-9,7) ALT (U.I./l) 400 (25-106) Neutrófilos inmaduros (miles/µl) 1,1 (0-0,1) Colesterol (mg/dl) 400 (124-335) Linfocitos (miles/µl) 1,0 (1,3-4,7) Bilirrubina (mg/dl) 0,4 (0,1-0,2) Plaquetas (miles/µl) 290 (179-483) Amilasa (U/l) 2,400 (286-1124) Creatinina (mg/dl) 1,8 (0,5-1,3) Glucosa (mg/dl) 131 (60-120) Pruebas de coagulación Fibrinógeno incrementado Páncreas Análisis de sangre El suero es lipémico TTPA, TP y dímero D normales Interpretación Tratamiento Discusión No hay evidencias de causas metabólicas o endocrinas de vómito ni antecedentes de consumo de medicamentos o de tóxicos. El gas que llena el duodeno en las radiografías sugiere un íleo secundario a una patología intestinal, a una pancreatitis o a una peritonitis. La ecografía no muestra ninguna anomalía, excepto un páncreas voluminoso e hipoecogénico. Las pruebas de laboratorio indican que hay hemoconcentración (hematocrito aumentado y azoemia prerrenal), neutrofilia con desplazamiento hacia la izquierda, ligera hipoalbuminemia, elevación de las enzimas hepáticas, hipercolesterolemia, suero lipémico y aumento de fibrinógeno. El conjunto de todos estos elementos es compatible con el diagnóstico de pancreatitis aguda. Se establece, por lo tanto, un diagnóstico provisional de pancreatitis. La ausencia de trombocitopenia o de trastornos de la coagulación descarta una necrosis pancreática. Se inicia un tratamiento con electrolitos (cristaloides) dos veces al día y una perfusión de 10 ml/kg de almidón hidroxietilado. Se administra heparina para controlar la lipemia (100 u/kg SC). Se prescribe buprenorfina para el dolor abdominal (0,01 mg/kg SC cada 8 horas). Se inicia un tratamiento con ampicilina (20 mg/kg, vía IV, tres veces al día) debido a la desviación a la izquierda. El perro se mantiene estrictamente en ayunas durante 48 horas. Se controlan los signos vitales, el hematocrito y las proteínas, los electrolitos, el número de plaquetas y el peso corporal. Este perro presenta objetivamente los elementos asociados a una pancreatitis aguda. La respuesta relativamente rápida al tratamiento, así como la ausencia de trastornos de la coagulación, es compatible con una pancreatitis moderada, más que con una necrosante. El tratamiento alimentario de este caso sigue las normas convencionales. En vista de las recientes investigaciones experimentales efectuadas en el perro y en el hombre, se podría haber comenzado con una alimentación enteral mediante una sonda nasogástrica o nasoyeyunal; sin embargo, aún no está confirmado el interés de esta técnica en pacientes clínicos. Los vómitos y el dolor abdominal revierten al tercer día de tratamiento. El estado general del perro continúa mejorando; el tratamiento sintomático finaliza y el perro comienza un régimen alimentario con un contenido limitado en lípidos (debido a la hiperlipidemia). Si el perro hubiera presentado signos de una pancreatitis más grave o no hubiera respondido tan rápido al tratamiento, se hubiera iniciado una terapéutica más agresiva y un programa nutricional, como una transfusión de plasma o una colocación quirúrgica de una sonda yeyunal. 185 2 - Preguntas frecuentes > ¿Qué alimento hay que suministrar a los perros que se están recuperando de una pancreatitis? La vuelta a la alimentación de forma voluntaria por vía oral se realiza cuando se recupera el apetito y cuando cesan los vómitos y el dolor abdominal. Con frecuencia se considera necesario limitar la cantidad de grasas del alimento, puesto que estimulan la liberación de la CCK y la secreción pancreática. Sin embargo, los aminoácidos también son potentes estimuladores de la secreción de enzimas pancreáticas y su proporción no se limita. Páncreas Los alimentos ricos en lípidos (> 50 g/1.000 kcal) y bajos en proteínas (< 20 g/1.000 kcal) poseen un perfil de nutrientes idéntico al de los alimentos conocidos por inducir pancreatitis en el perro. Por lo tanto, hay que evitarlos. La obesidad es un factor de riesgo de pancreatitis que debe controlarse con un enfoque nutricional adecuado. Las dietas elementales provocan un grado de estimulación pancreática equivalente al originado por las dietas normales. La composición de una dieta casera debe variar en función de la naturaleza de la alteración pancreática observada. • Insuficiencia pancreática exocrina: Elegir ingredientes hiperdigestibles. El nivel óptimo de materias grasas varía según el caso: - si el índice corporal es muy bajo, hay que elegir una dieta adaptada a los estados caquécticos (véase capítulo 13) - en caso de intolerancia a las materias grasas, hay que orientarse hacia una dieta que contenga un nivel moderado de lípidos, adaptado a la hiperlipidemia (véase capítulo 7) En caso de ausencia de respuesta o de sospecha de alergia alimentaria, una dieta hipoalergénica representa la mejor alternativa (véase capitulo 2). • Pancreatitis aguda: hay que orientarse hacia una dieta que contenga un nivel moderado de lípidos, adaptado a la hiperlipidemia (véase capítulo 7). Preguntas frecuentes sobre la pancreatitis P R Mi perro acaba de recuperarse de una pancreatitis ¿ Hay algo que pueda hacer para evitar una recidiva? No es fácil responder a esta pregunta. Las recaídas generalmente son menos frecuentes cuando se limitan los factores de riesgo. Por ejemplo, evitando los excesos alimentarios así como ciertos medicamentos (como el fenobarbital y el bromuro potásico) de los que se sospecha que pueden desencadenar los episodios de pancreatitis. En caso de hiperlipidemia, una alimentación baja en grasas y el mantenimiento de un peso corporal óptimo pueden disminuir los riesgos de recaída. Hace una semana que se diagnosticó pancreatitis a mi perro. Ha dejado de vomitar pero ahora se ha puesto ictérico. ¿Qué está pasando? La aparición de una ictericia tras un episodio de pancreatitis aguda se asocia, generalmente, a una obstrucción del conducto biliar debido a la inflamación pancreática. El diagnóstico suele confirmarse con un análisis de sangre y una ecografía abdominal. Si el perro se mantiene alerta y su estado general es bueno, el tratamiento conservador consiste en vigilar los parámetros físicos y bioquímicos durante un par de semanas para ver si la hiperbilirrubinemia y la ictericia desaparecen o se agravan. Cuando una obstrucción biliar persiste durante más de dos o tres semanas, normalmente, se resuelve con cirugía. 186 Bibliografía Bibliografía Lamb CR, Simpson KW, Boswood A et al Ultrasonography of pancreatic neoplasia in the dog: a retrospective review of 16 cases. Vet Rec 1995; 137: 65-68. Chan DL, Freeman LM, Labato MA et al Retrospective evaluation of partial parenteral nutrition in dogs and cats. J Vet Intern Med 2002; 16(4): 440-5. Macintire DK - The acute abdomen - differential diagnosis and management. Seminars in Veterinary Medicine and Surgery Small Animal 1988; 3: 302- 310. Denham W, Norman J - The potential role of therapeutic cytokine manipulation in acute pancreatitis. Surg Clin North Am 1999; 79: 767-782. Mansfield CS, Jones BR - Plasma and urinary trypsinogen activation peptide in healthy dogs, dogs with pancreatitis and dogs with other systemic diseases. Aust Vet J 2000; 78(6): 416-22. Duerksen DR, Bector S, Parry D et al A comparison of the effect of elemental and immune enhanceing polymeric jejunal feeding on exocrine pancreatic function. J Parenter Enteral Nutr 2002; 26:205-8. Mansfield CS, Jones BR, Spillman T - Assessing the severity of canine pancreatitis. Res Vet Sci 2003; 74(2): 137-44. Harmoinen J, Saari S, Rinkinen M, et al The advent of laparascopic techniques may decrease morbidity (Evaluation of pancreatic forceps biopsy by laparoscopy in healthy beagles).Vet Ther 2002; 3(1): 31-6. Hess RS, Kass PH, Shofer FS, et al - Evaluation of risk factors for fatal acute pancreatitis in dogs. J Am Vet Med Assoc 1999; 214: 46-51. Hess RS, Saunders HM, Van Winkle TJ et al Clinical, clinicopathologic, radiographic, and ultrasonographic abnormalities in dogs with fatal acute pancreatitis: 70 cases (1986-1995). J Am Vet Med Assoc 1998; 213 (5): 665-670. Hess RS, Saunders HM, Van Winkle TJ et al Concurrent disorders in dogs with diabetes mellitus: 221 cases (1993-1998). Am Vet Med Assoc 2000; 15, 217(8):1166-73. Jaeger JQ, Mattoon JS, Bateman SW et al Combined use of ultrasonography and contrast enhanced computed tomography to evaluate acute necrotizing pancreatitis in two dogs. Vet Radiol Ultrasound 2003; 44(1): 72-9. Johnson LR - Gastrointestinal Physiology:Fifth edition, 1997; Mosby-Year Book Inc. St. Louis MO: 97. Johnson GB, Brunn GJ, Platt JL - Cutting edge: an endogenous pathway to systemic inflammatory response syndrome (SIRS)-like reactions through Tolllike receptor 4. J Immunol 2004; 172(1): 20- 4. Kalfarentzos F, Kehagias J, Mead N et al - Enteral nutrition is superior to parenteral nutrition in severe acute pancreatitis: results of a randomised prospective trial. Br J Surg 1997; 84:1665-9. Karne S, Gorelick FS - Etiopathogenesis of acute pancreatitis. Surg Clin North Am 1999; 79: 699- 710. McClave SA, Greene LM, Snider HL et al. Comparison of the safety of early enteral vs parenteral nutrition in mild acute pancreatitis. J Parenter Enteral Nutr 1997; 21:14-20. Mentula P, Kylanpaa ML, Kemppainen E et al Plasma anti-inflammatory cytokines and monocyte human leucocyte antigen-DR expression in patients with acute pancreatitis. Scand J Gastroenterol 2004; 39(2): 178-87. Mohr AJ, Leisewitz AL, Jacobson LS et al - Effect of early enteral nutrition on intestinal permeability, intestinal protein loss, and outcome in dogs with severe parvoviral enteritis. J Vet Intern Med 2003; 17(6): 791-8. Olah A, Belagyi T, Issekutz A et al -Randomized clinical trial of specific lactobacillus and fibre supplement to early enteral nutrition in patients with acute pancreatitis. Br J Surg 2002; 89:1103-07. Oruc N, Ozutemiz AO, Yukselen V et al Infliximab: a new therapeutic agent in acute pancreatitis? Pancreas 2004; 28(1): e1-8. Paraskeva C, Smailis D, Priovolos A et al. Early enteral nutrition reduces the need for surgery in severe acute pancreatitis. Pancreatology 2001; 1: 372. 88 Powell JJ, Murchison JT, Fearon KC - Randomized controlled trial of the effect of early enteral nutrition on markers of the inflammatory response in predicted severe acute pancreatitis. Br J Surg 2000; 87:1357- 81. Pupelis G, Austrums E, Jansone A et al Randomised trial of safety and efficacy of postoperative enteral feeding in patients with severe pancreatitis: preliminary report. Eur J Surg 2000; 166:383-7 Qin HL, Su ZD, Gao Q et al - Early intrajejunal nutrition: bacterial translocation and gut barrier function of severe acute pancreatitis in dogs. Hepatobiliary Pancreat Dis Int 2002; 1(1): 150-4. Qin HL, Su ZD, Hu LG et al - Parenteral versus early intrajejunal nutrition: effect on pancreatitic natural course, entero-hormones release and its efficacy on dogs with acute pancreatitis. World J Gastroenterol 2003; 9(10): 2270-3. Raraty MG, Connor S, Criddle DN - Acute pancreatitis and organ failure: pathophysiology, natural history, and management strategies. Curr Gastroenterol Rep 2004; 6(2): 99-103. Ruaux CG, Atwell RB - Levels of total alphamacroglobulin and trypsin-like immunoreactivity are poor indicators of clinical severity in spontaneous canine acute pancreatitis. Res Vet Sci 1999; 67(1): 83-7. Ruaux CG, Pennington HL, Worrall S et al Tumor necrosis factor-alpha at presentation in 60 cases of spontaneous canine acute pancreatitis. Vet Immunol Immunopathol 1999; 72: 369-376. Salisbury SK, Lantz GC, Nelson RW et al Pancreatic abscess in dogs : six cases (1978-1986). J Am Vet Med Assoc 1988; 193: 1104-8. Simpson KW - Current concepts of the pathogenesis and pathophysiology of acute pancreatitis in the dog and cat. Comp Cont Ed Prac Vet 1993; 15: 247- 253. Simpson KW, Beechey-Newman N, Lamb CR et al - Cholecystokinin-8 induces edematous pancreatitis in dogs which is associated with a short burst of trypsinogen activation. Dig Dis Sci 1995; 40: 2152- 2161. Simpson KW, Lamb CR - Acute pancreatitis in the dog. In Practice - Journal of Veterinary Postgraduate Clinical Study1995; 17: 328-337. Stabile BE, Borzatta M, Stubbs RS - Pancreatic secretory responses to intravenous hyperalimentation and intraduodenal elemental and full liquid diets. J Parenter Enteral Nutr 1984; 8(4): 377- 80. Strombeck DR, Farver T, Kaneko JJ - Serum amylase and lipase activities in the diagnosis of pancreatitis in dogs. Am J Vet Res. 1981; 42(11): 1966-70. Vu MK, van der Veek PP, Frolich M et al - Does jejunal feeding activate exocrine pancreatic secretion? Eur J Clin Invest 1999; 29:1053-9. Windsor AC, Kanwar S, Li AG et al. Compared with parenteral nutrition, enteral feeding attenuates the acute phase response and improves disease severity in acute pancreatitis. Gut 1998; 42: 431-5. Zyromski N, Murr MM - Evolving concepts in the pathophysiology of acute pancreatitis. Surgery 2003; 133(3): 235-7. 187 Páncreas Brady CA, Otto CM - Systemic inflammatory response syndrome, sepsis, and multiple organ dysfunction. Vet Clin North Am Small Anim Pract. 2001; 31(6): 1147-62. © Lenfant Páncreas Información nutricional de Royal Canin La insuficiencia pancreática exocrina afecta a todas las razas de perros pero el síndrome es particularmente frecuente en el Pastor Alemán y en el Collie, a la edad aproximada de 2 años. Puntos clave a recordar sobre la: Importancia de la nutrición en el tratamiento de los trastornos pancreáticos El síndrome de insuficiencia pancreática exocrina (IPE) es la consecuencia de la disminución de la digestión de los nutrientes en la luz intestinal, pero también de la alcalinización insuficiente del quimo, de la alteración de las enzimas del borde de la mucosa en cepillo y de la multiplicación bacteriana. Todo el conjunto implica una actividad anormal de las enzimas de la mucosa intestinal, así como una disminución del transporte de los carbohidratos, aminoácidos, ácidos grasos y vitaminas (especialmente, la vitamina B12) desde la luz intestinal hasta los enterocitos. 188 El tratamiento de la IPE consiste en añadir a los alimentos unos suplementos de enzimas pancreáticas y en alimentar a esos animales con una dieta altamente digestible. Las formas más eficaces de administración del suplemento enzimático son: - polvo pancreático 3 g/comida para un perro de 20-35 kg - páncreas fresco de cerdo o de vaca: 50-100 g/comida para un perro mediano. Se deben evitar los comprimidos porque a menudo se encuentran después, intactos en las heces. La preincubación del alimento con las enzimas no tiene ningún propósito. La mayoría de las veces, la dosis inicial puede reducirse al 50% tan pronto como el animal muestra una respuesta al tratamiento. Esta medida no es insignificante teniendo en cuenta el coste de los suplementos enzimáticos. Para la mayoría de los perros, este suplemento durará toda la vida. Se han descrito hemorragias bucales en los perros a los que reciben suplementos con enzimas pancreáticos. La reducción al 50% de la dosis, generalmente, elimina los signos clínicos. Información nutricional de Royal Canin 1 • El tratamiento nutricional de la insuficiencia pancreática Tradicionalmente, se recomendaba una dieta altamente digestible, baja en fibras y con un contenido moderado en grasas para el tratamiento dietético de la IPE. - La disminución de la proporción de fibras viene impuesto por la necesidad de conservar una dieta concentrada en energía (es difícil mantener el buen estado de los perros con insuficiencia pancreática). Por otra parte, el exceso de fibras puede inhibir la acción de las enzimas pancreáticas. - La recomendación de disminuir las grasas cuando hay una IPE pretende prevenir la diarrea estimulada por la presencia de ácidos grasos hidroxilados en la luz intestinal, los cuales favorecen la pérdida de agua. Estos ácidos grasos hidroxilados son producidos por la flora intestinal que prolifera como resultado de la llegada al intestino de materias grasas no digeridas. La malabsorción de las grasas es debida tanto a la deficiencia en lipasa pancreática como a la desconjugación de los ácidos biliares por la proliferación bacteriana. La importancia de las grasas Pronóstico La mayoría de los perros que padecen una insuficiencia pancreática, y que reciben un suplemento de enzimas y son alimentados dos veces al día, tienen una calidad de vida muy similar a la de los individuos sanos. Para los individuos que padecen una IPE asociada a una pancreatitis o a una diabetes, el pronóstico es más reservado. Si no se observa ninguna mejoría (aumento de peso, disminución de la diarrea y de la polifagia) en los 4-5 días siguientes al comienzo del tratamiento enzimático y dietético, es preciso iniciar un tratamiento antibiótico (metronidazol o tilosina) para controlar la proliferación bacteriana. Hipótesis: una dieta rica en grasas daría lugar a una mejor conservación de la lipasa del suplemento pancreático. Además, los perros con IPE toleran bien las dietas hiperdigestibles que contienen, aproximadamente, un 20% de materias grasas. Las dietas más ricas en grasas favorecen también el consumo energético de los animales con déficit de peso. Elección de una fuente de almidón altamente digestible Gracias a la gran digestibilidad de su almidón, el arroz es el cereal de elección en los perros con IPE, que además son mucho más susceptibles a las alergias e intolerancias alimentarias. Las primeras observaciones parecen indicar que una dieta basada en hidrolizados de proteínas podría tener un efecto muy favorable en los perros con IPE. El pequeño tamaño de los péptidos de estas dietas favorecería su digestión y su absorción. Conclusión Al contrario de lo que se suele pensar, los perros con IPE toleran un nivel importante de grasas en su dieta: estas permitirían una mejor conservación del suplemento enzimático se cuando pasa por el estómago. Las dietas basadas en proteínas hidrolizadas tendrían un efecto beneficioso no solamente sobre la función digestiva, sino también sobre la intolerancia alimentaria. Prevención de las deficiencias vitamínicas Las carencias de las vitaminas B12 y E son muy frecuentes en los perros que padecen IPE. También se han identificado carencias de las vitaminas A y K. Para corregirlas se necesita un suplemento por vía parenteral. © Lenfant Los estudios, sin embargo, contradicen dicha práctica. Una dieta rica en grasas (43% de las calorías) mejora la absorción de las grasas (y los signos clínicos) en los perros que padecen IPE en comparación con las dietas de mantenimiento estándares (27% de calorías lipídicas) o con las dietas bajas en grasas (16% de calorías). En el Pastor Alemán, un gen autosómico recesivo intervendría en la transmisión de la insuficiencia pancreática exocrina. Bibliografía Rutz GM, Steiner JM, Williams DA - Oral bleeding due to pancreatic extract in three dogs with exocrine pancreatic insufficiency. Proc 19th ACVIM 2001 ; 875 (abst#156). Westermarck E, Junttila JT, Wiberg ME Role of low dietary fat in the treatment of dogs with exocrine pancreatic insufficiency. Am J Vet Res 1995 ; 56: 600-605. Suzuki A, Mizumoto A, Rerknimitr R et al Effect of bacterial or porcine lipase with low- or high fat diets on nutrient absorption in pancreatic-insufficient dogs. Gastroenterology 1999 ; 116: 431-437. Wiberg ME, Lautala HM, Westermarck E Response to long term enzyme replacement treatment in dogs with exocrine pancreatic insufficiency. J Am Vet Med Assoc 1998 ; 213: 86-90. Wiberg M - Exocrine pancreatic insufficiency in dogs-An update. Proceeding of 12th ESVIM congress ; Munich, 2002: 103-105. Williams DA - The pancreas. In “Strombeck’s Small Animal Gastroenterology 3rd ed. Guilford, Center, Strombeck, Williams, Meyer eds, Saunders ; Philadelphia, 1996: 381-410. 189 Páncreas El enfoque tradicional Información nutricional de Royal Canin Páncreas 2 • Insuficiencia pancreática exocrina y reacciones de intolerancia alimentaria en el perro Interés de una dieta rica en grasas, formulada a partir de un hidrolizado de aislado de proteína de soja y de arroz Se trataba de cuatro animales machos, con edades comprendidas entre los 2,5 y los 9 años, que pesaban entre 31 y 40 kg y que padecían una IPE confirmada por la prueba TLI (TLI: de 0,88 a 5,08 mg/l). Los signos cutáneos característicos de las reacciones adversas a los alimentos son frecuentes en los perros con IPE, sobre todo en el Pastor Alemán. Por lo general, los perros con estos dos problemas responden mal a los suplementos enzimáticos y las dietas específicamente diseñadas para IPE. Todos los perros presentaban una diarrea recurrente, más o menos controlada con el consumo de un alimento hiperdigestible que incluía una fuente proteica nueva asociada a un suplemento enzimático. El siguiente estudio describe la respuesta positiva obtenida en 4 Pastores Alemanes con IPE y problemas cutáneos después de consumir un alimento seco con un 19% de materias grasas y que estaba formulado a base de hidrolizado de extracto proteico de soja y de arroz. Estos perros estaban delgados y presentaban problemas cutáneos de intensidad variable, compatibles con una reacción de intolerancia alimentaria. Los animales padecían una piodermitis y fueron tratados con cefalexina. No se les administraba ningún otro tratamiento, a parte del suplemento enzimático. Después de una semana de consumir, de manera exclusiva, el alimento descrito anteriormente, los cuatro perros presentaban heces normales y ninguno de ellos mostró signo de diarrea durante los tres meses siguientes. Durante dicho periodo, el índice corporal de los perros mejoró y ganaron entre 2 y 10 kg. En 3 de los 4 animales se controló por completo el prurito y los demás síntomas cutáneos. En este último, sólo persistía un prurito de intensidad media, así como algunas lesiones eritematosas y costras localizadas, asociadas a una hiperpigmentación. Los perros toleraron muy bien el alto nivel de materias grasas (40,8% de calorías de origen lipídico). Estos resultados sugieren que un alimento hiperdigestible y rico en grasas no está contraindicado en casos de IPE y que incluso podría ser beneficioso para la recuperación del estado corporal. ANÁLISIS DEL ALIMENTO Humedad 9% Proteínas 21% Materias grasas 19% Celulosa bruta 2,2% Fibras alimentarias totales 5,4% Cenizas 8% Energía metabolizable 4182 kcal/kg Lista de ingredientes: arroz, hidrolizado de extracto de soja, grasas animales, sales minerales, aceites vegetales (incluido el aceite de borraja), zeolita, fructooligosacáridos, aceite de pescado. Bibliografía Biourge VC, Fontaine J - Exocrine pancreatic insufficiency and adverse reaction to food in dogs: a positive response to a high-fat, soy isolate hydrolysate-based diet. J Nutr 2004 ; 134: 2166S–2168. 190 Información nutricional de Royal Canin Objetivo: EL HIDROLIZADO DEL EXTRACTO PROTEICO DE SOJA - los factores antinutricionales (p. ej., antitripsina) que inhiben la digestión de las proteínas y la correcta absorción de los nutrientes - los carbohidratos no digestibles, que pueden fermentar en el intestino grueso y producir flatulencias u otros problemas digestivos. El hidrolizado de soja se obtiene mediante la hidrólisis enzimática del extracto de soja. Comparado con las proteínas enteras del extracto de soja, el hidrolizado contiene polipéptidos de menor tamaño. Durante el proceso de purificación de las proteínas de soja, las sustancias indeseables son destruidas o eliminadas. Sus ventajas principales son: - una digestibilidad muy alta y una excelente tolerancia digestiva - menor posibilidad de provocar reacciones alérgicas. TÉCNICA DE OBTENCIÓN DEL HIDROLIZADO DEL EXTRACTO PROTEICO DE SOJA Granos de soja Torta de soja Descascarillado, aplastamiento Molienda Copos Extracción El extracto de soja es de las grasas una fuente de proteínas muy concentrada (85% de proteínas). La proteína de soja posee un perfil de aminoácidos muy bueno: su valor biológico es próximo al del huevo deshidratado y al de la caseína, con la condición de suplementar en metionina, un aminoácido esencial que es el factor limitante de los granos de soja. La digestibilidad del hidrolizado de soja supera el 96%, superior al de las mejores fuentes de proteínas de origen animal y comparable a las dos proteínas de referencia, la caseína y la proteína del huevo. El hidrolizado de soja se ha convertido en una proteína de referencia en la dietética humana y animal. La calidad de esta proteína es tal que se está empleando en sustitución de las proteínas de la leche en los bebés alérgicos, así como en los suplementos proteicos destinados a deportistas o a pacientes convalecientes. En medicina humana, las dietas a base de hidrolizado de soja son útiles para disminuir el riesgo de enteritis cuando se está siendo tratado con radioterapia o con quimioterapia. Copos desgrasados Extracto de soja Extracción con alcohol diluido + Precipitación protéica Hidrolizado de extracto de soja Hidrólisis enzimática COMPARACIÓN DE LA COMPOSICIÓN DE VARIOS PRODUCTOS OBTENIDOS DE LA SOJA Extracto hidrolizado 5 de soja Torta de soja 2,5 12 2 48 Granos 11,7 de soja 0 4,5 3 85 35,4 20 20 40 60 18 20 17 80 15,9 Humedad Proteínas Materias grasas Fibras totales Azúcares y cenizas 100 % 191 Páncreas Las proteínas de soja son conocidas como proteínas de excelente calidad pero la utilización de los granos de soja en la alimentación canina se encuentra limitado por: