1.- Calcule la entalpía de formación estandar del monóxido de
Anuncio

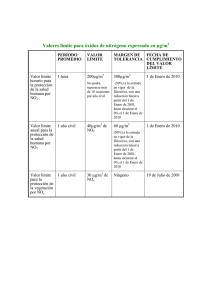
COMUNIDAD VALENCIANA / JUNIO 00. LOGSE / QUIMICA / TERMOQUIMICA / OPCION A / CUESTIÓN 1 1.- Calcule la entalpía de formación estandar del monóxido de nitrógeno a presión constante, expresándola en kJ/mol, a partir de las siguientes ecuaciones termoquímicas: N2 (g) + 2 O2 (g) " 2 NO2 (g) ∆H1 = 67,78 kJ 2 NO (g) + O2 (g) " 2 NO2 (g) ∆H2 = -112,92 kJ Solución: Formación de monóxido de nitrógeno: ½ N2 (g) + ½ O2 (g) • NO (g) Aplicando la ley de Hess, podemos combinar las reacciones y, por tanto las entalpías: ∆H0 f = ½ ∆H1 – ½ ∆H2 ∆H0 f = ½ (67,78) – ½ (-112,92) = 90,35 kJ/mol www.profes.net es un servicio gratuito de Ediciones SM