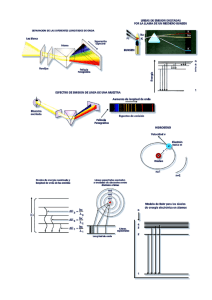
Utilidad de los números cuánticos
Anuncio

2do Medio > Química Números Cuánticos ¿Dónde se Ubica un Electrón? En la naturaleza, toda la materia tiene volumen y ocupa un espacio. Por ejemplo, es bastante sencillo mirar a tu alrededor y darte cuenta que tu cuaderno, lápiz de escribir, e incluso la mesa donde estás sentado corresponde a un elemento que tiene volumen y ocupa un espacio, por lo tanto es materia. Del mismo modo, el átomo, que es la unidad mínima que constituye la materia tiene un volumen y ocupa un espacio. Pero… ¿dónde se ubican y cómo se distribuyen las partículas subatómicas al interior del átomo? Ya has estudiado que dentro de un átomo, los protones y neutrones se ubican en una región central denominada núcleo. Mientras que los electrones se ubican en la periferia del átomo, en una región denominada corteza, la que está compuesta por varias “capas” o “zonas” de alta probabilidad donde es posible encontrar un electrón, como lo indica la imagen: Imagina que tu sala de clases es un átomo. En el centro puedes agrupar a los protones y neutrones representados por todas las mochilas de tus compañeros. Y alrededor, siguiendo una forma circular ordenan tres filas de 10 sillas. Supón que tú y nueve compañeros más son electrones: a) ¿Dónde se sentarían? ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… ………………………………………………………………………………………………… Números Cuánticos b) ¿Estarían todo el tiempo en la misma posición?, ¿Por qué? ……………………………………………………………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………… Esta misma situación ocurre en el átomo. Los electrones tienen naturaleza dual, son partículas pero además tienen una naturaleza eléctrica, por lo tanto su energía les impide estar quietos en una sola posición. ¿Es posible determinar la posición exacta de un electrón?, ¿por qué? ……………………………………………………………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………… Los números cuánticos son una propiedad de los electrones que describen la posición relativa en donde se ubican dentro de un átomo. El Modelo Mecano Cuántico, que es el modelo actual que describe la estructura atómica indica que es imposible conocer la posición exacta y velocidad a la que se desplaza un electrón pero que sí es posible conocer y determinar la zona probable en donde se encontrará. ¿Qué significan y cómo se pueden determinar los números cuánticos? ¡TE INVITAMOS A QUE LO DESCUBRAS CON ESTA GUÍA DE APRENDIZAJE! ¿Qué Aprenderé? El objetivo de esta guía de aprendizaje es que definas cada uno de los números cuánticos y operes con ellos para determinar los cuatro números cuánticos del electrón de un átomo. 2 Números Cuánticos Red Conceptual Los contenidos que trataremos en esta guía se estructuran de la siguiente forma: NÚMEROS CUÁNTICOS. Características generales. Aplicación de los números cuánticos. 1. Definición. 2. Valores que toman los números cuánticos. 1. Determinación de los números cuánticos de un electrón. 2. Ejercicios claves. El Actual Modelo Atómico Schrödinger describió el quinto modelo atómico, que hoy se conoce como Modelo Atómico Mecano Cuántico y constituye el actual modelo atómico. En su modelo, Schrödinger describe la naturaleza dual del electrón y las características de todos los electrones que componen un átomo, por medio de “los números cuánticos”. De acuerdo a su modelo, los electrones se ubican en la corteza del átomo en zonas de probabilidad o “nubes” electrónicas las que pueden ser diagramadas como lo indica la figura: Erwin Schrödinger De acuerdo con esto, no es posible conocer un lugar exacto en donde se encuentre un electrón, pero sí una “zona probable” en donde se le pueda encontrar. Estas coordenadas son definidas por los números cuánticos. 3 Números Cuánticos Los números cuánticos se denominan con las letras n, m, l y s y nos indican la posición y energía del electrón. De acuerdo con los principios de la mecano cuántica y el modelo propuesto por Schödinger dos electrones de un mismo átomo NO pueden tener los mismos cuatro números cuánticos. Porque no pueden tener la misma energía y la misma posición al mismo tiempo. Dicho de otro modo, tú y tu compañero no pueden estar sentados en la misma silla. En la corteza, los electrones se sitúan siguiendo caminos determinados llamados orbitales. Cada orbital está definido por tres números cuánticos, que determinan el tamaño, la forma y la orientación del orbital. Además existe un cuarto número cuántico que describe “como gira el electrón” mientras se está desplazando. ¿Qué significan los números cuánticos? NÚMERO CUÁNTICO PRINCIPAL (n) El número cuántico principal, n, indica el nivel de energía donde se encuentra el electrón, en otras palabras, determina el tamaño. Puede tomar cualquier valor natural (entero, no decimal) distinto de cero: n = 1, 2, 3, 4, 5, 6, 7, etc. Varios orbitales pueden tener el mismo número cuántico principal, y de hecho lo tienen, agrupándose en capas. Los orbitales que tienen el mismo número cuántico principal forman una capa electrónica. Cuanto mayor sea el número cuántico principal, mayor será el tamaño del orbital y, a la vez, más lejos del núcleo estará situado. NÚMERO CUÁNTICO SECUNDARIO O AZIMUTAL (l) El número cuántico azimutal, l, indica la forma del orbital, que puede ser circular, si vale 0, o elíptica, si tiene otro valor. Además indica en qué orbital se ubica el electrón. El valor del número cuántico secundario depende del valor del número cuántico principal. Toma valores que van desde 0 a una unidad menos que n (l = n-1). Si el número cuántico principal vale 1, entonces n = 1. Como consecuencia, el número cuántico secundario sólo puede valer 0, ya que sus posibles valores van desde 0 hasta una unidad menos que n. Si por el contrario el número cuántico principal vale 4, n = 4, el número cuántico secundario puede tomar cuatro valores distintos, desde cero hasta tres: l = 0, 1, 2, 3 4 Números Cuánticos A cada valor del número cuántico secundario le corresponde una forma de orbital, que se identifica con una letra minúscula de acuerdo a lo que se muestra en la tabla: Número cuántico secundario l (azimutal) Letra 0 1 2 3 s p d f Cuando el número cuántico secundario vale cero, el orbital tiene forma circular y en la medida que va aumentando se va achatando, por lo tanto, cuando vale uno, es algo elíptica. Si dos, es más achatado… etc. n=1 n=2 n=3 n=4 NÚMERO CUÁNTICO MAGNÉTICO El número cuántico magnético, m, representa la orientación de los orbitales en el espacio. Dicho de otro modo representa el tipo de orbital dentro de un subnivel específico. Los valores que puede tomar dependen del valor del número cuántico secundario. Puesto que m, toma valores que van desde - l hasta + l. Si el número cuántico secundario vale 0, entonces l = 0. De este modo, el número cuántico magnético sólo puede tomar el valor 0. Y en este caso, sólo hay un orbital s. 5 Números Cuánticos Si el número cuántico secundario vale 1, l = 1, el número cuántico magnético puede tomar los valores -1, 0 y 1, ya que sus posibles valores van desde – l hasta l. Por lo tanto, existen tres orbitales p, ya que si l = 1 el orbital se llama p, como se describió anteriormente. En general, para un valor l, habrá 2·l + 1 orbitales: Número cuántico secundario ( l ) Número de orbitales 0 1 2 3 1 3 5 7 Como el valor de m depende del valor que tenga el número cuántico secundario, l, y éste toma valores dependiendo del número cuántico principal, n, y, por tanto, de la capa electrónica, el número de orbitales variará de una capa a otra. En la primera capa electrónica n = 1, por lo tanto l = 0 y, como consecuencia, m = 0. Sólo hay un único orbital, de tipo s. En la tercera capa electrónica n = 3, de forma que l puede tomar 3 valores: 0, 1, 2. Habrá orbitales s, p, d: El orbital s indica que l = 0, por lo que m = 0, sólo hay un orbital s. El orbital p significa que l = 1, de forma que m = -1, m = 0 o m = 1. Hay 3 orbitales p. Finalmente, si el orbital es d indica que forzosamente l = 2, y, por lo tanto, m = -2, m = -1, m = 0, m = 1 y m = 2. Hay 5 orbitales d. En la tercera capa, por tanto, hay 9 orbitales: 1 s, 3 p y 5 d. El número de orbitales de cada tipo viene determinado por los valores que puede tomar el número cuántico magnético, m, y será: 2·l+1. Si l = 0 hay un único orbital, si l = 4 habrá 9 Lo anterior puede representarse en la siguiente figura: 6 Números Cuánticos l=0 m=0 Hay un orbital l=1 m = -1, 0, 1 Hay tres orbitales. l=2 m = -2, -1, 0, 1, 2 Hay cinco orbitales. NÚMERO CUÁNTICO DE SPÍN Si consideramos el electrón como una pequeña esfera (lo que en rigor no es cierto) este podría girar en torno a un eje imaginario sobre sí mismo, de una manera similar a como la Tierra gira ocasionando la noche y el día. Dicho de esta manera, el electrón tendrá sólo dos posibles sentidos de giro, hacia la izquierda o hacia la derecha. Este giro del electrón sobre sí mismo está indicado por el número cuántico de espín, que se indica con la letra s. Dado que el spín puede tener dos sentidos de giro, el número de espín tomará dos valores: + ½ si gira hacia la derecha y - ½ si gira hacia la izquierda. Podemos sistematizar toda esta información indicando que los electrones dentro del átomo se organizan en la periferia y en capas, indicadas por el número cuántico principal, n, que indica su lejanía al núcleo. Dentro de las capas hay distintos orbitales, especificados por el número cuántico secundario, l, que además indica la forma del orbital. El número de orbitales de cada tipo está dado por el número cuántico magnético, m, que nos señala la orientación del orbital. Y finalmente hay otro número cuántico, de espín, s, que sólo puede tomar dos valores e indica el giro del electrón sobre sí mismo. Utilidad de los números cuánticos Los números cuánticos son una herramienta que además se relaciona con la configuración electrónica y la tabla periódica. Es posible obtener los números cuánticos sabiendo sólo el Z de cada elemento, su ubicación en la tabla periódica o su configuración electrónica. ¡Investiga más sobre estas relaciones! y ¡Profundiza tus conocimientos! 7 Números Cuánticos Organizador Gráfico Recapitulando lo que hemos visto dentro de este módulo tenemos que: NÚMEROS CUÁNTICOS Describen la posición relativa y nivel de energía de un electrón NÚMERO CUÁNTICO PRINCIPAL (n) Corresponde al nivel de energía Toma valores: 1, 2, 3, 4, 5, 6 … NÚMERO CUÁNTICO AZIMUTUAL (m) Corresponde a la forma del orbital Toma valores: s=0, p=1, d=2 y f=3 NÚMERO CUÁNTICO MAGNÉTICO(l) Corresponde a la orientación del orbital Toma valores: -l , 0, l NÚMERO CUÁNTICO SPÍN (s) Corresponde al giro que da el electrón sobre su eje Toma valores: -1 , +1 8 Números Cuánticos ¡Practica tus conocimientos! 1. En el modelo atómico moderno. El número cuántico l representa: a) b) c) d) e) La forma que toman los giros de los electrones. La posición exacta de encontrar un electrón. La disposición de los neutrones en un átomo. La zona de probabilidad de encontrar un electrón La posición de los protones en el átomo. 2. Si el valor de l es 3, ¿Qué tipo de subnivel está relacionado con dicho valor? a) b) c) d) e) S P D F G 3. Cuántos electrones pueden existir en un átomo que tiene completo hasta el nivel 2? a) b) c) d) e) 2 4 6 8 10 4. Si el número cuántico es n=5, ¿Cuál o cuáles son los valores del número cuántico l? a) b) c) d) e) 3 2y3 1, 2 y 3 0, 1, 2 y 3 0, 1, 2, 3 y 4 9 Números Cuánticos 5. ¿Cuántos subniveles tiene un átomo cuando el valor de n=2? a) b) c) d) e) 9 5 4 3 1 6. Si los valores de, n, m, l y s para un elemento desconocido son los siguientes 3, 2, -2, -1/2 ¿Qué información puedes obtener a partir de ella? ………………………………………………………..………………………………………………………………… ………………………………………………………..………………………………………………………………… ………………………………………………………..………………………………………………………………… ………………………………………………………..………………………………………………………………… ………………………………………………………..………………………………………………………………… ………………………………………………………..………………………………………………………………… 10