Curso arritmias - G. Zuelgaray: Taquicardias Supraventriculares
Anuncio

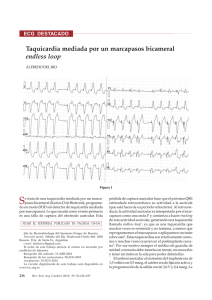
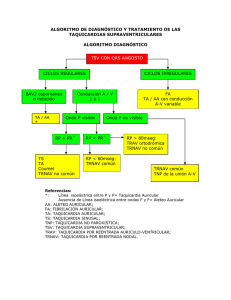
[ Scientific Activities - Actividades Científicas ] Primer Curso de Arritmias por Internet Directores Dr. Jorge González Zuelgaray Dr. Edgardo Schapachnik División Cardiología. Hospital General de Agudos Dr. Cosme Argerich Buenos Aires - Argentina Módulo Número 6 Taquicardias Supraventriculares Dr. Jorge González Zuelgaray Jefe de Electrocardiografía y Electrofisiología División Cardiología. Hospital General de Agudos Dr. Cosme Argerich Buenos Aires - Argentina Introducción Se entiende como taquicardias supraventriculares a aquellas en las que participan necesariamente estructuras ubicadas por encima de la bifurcación del haz de His. A su vez, estas arritmias se pueden dividir en dos grupos: taquicardias de la unión (cuando es componente imprescindible la unión A-V) o taquicardias auriculares (cuando la unión A-V no tiene una participación esencial). Así, la fibrilación auricular constituye una taquicardia auricular por excelencia; sin embargo, no será tratada en esta clase debido a que se abordó -junto con el aleteo auricular- en un módulo previo. Es importante analizar por qué el clínico debe ser capaz de di- lucidar el probable mecanismo implicado en la génesis de una taquicardia supraventricular. A nuestro entender, en la era de la ablación por catéter es más importante que nunca evaluar las posibilidades de éxito y las complicaciones específicas del método en relación con cada tipo de arritmia. En más del 95% de los casos de reentrada nodal, el procedimiento de ablación de la vía lenta es efectivo y todo puede realizarse a través de accesos venosos sin necesidad -en la mayoría de los centros- de anticoagulación. Sin embargo, aunque mínimo, el riesgo de bloqueo A-V iatrogénico existe y debe ser específicamente considerado. Cuando las evidencias electrocardiográficas sugieren una vía oculta (es decir, con conducción sólo en el sentido retrógrado o ventrículo-atrial) cuya localización es lateral izquierda, es viable considerar un trayecto oblicuo y la eventual necesidad de abordaje en la inserción auricular a través de una punción del septum interauricular. Esto conlleva riesgos y requiere un entrenamiento y una logística que son específicos. Si se trata de una taquicardia auricular cuyo probable origen se ubica en la aurícula izquierda, a menos que el paciente tenga un foramen oval permeable, será necesario recurrir a una punción transeptal. Igualmente, aunque existen fármacos que podríamos denominar "inespecíficos" (como la amiodarona), también determinados agentes tienen mecanismos de acción que los hacen particularmente indicados para determinadas arritmias (como la flecainida en el tratamiento de las taquicardias auriculares ectópicas) o poseen sitios particulares de acción (como los beta-bloqueantes, la digital o los antagonistas del calcio con respecto al nódulo A-V). Taquicardia sinusal Se deben excluir causas sistémicas o cardíacas para una frecuencia sinusal elevada (fiebre, anemia, hipertiroidismo, embarazo, feocromocitoma, pericarditis, insuficiencia cardíaca o respiratoria, entre otras causas). Taquicardia Sinusal Fisiológica (tono simpático aumentado) -Ejercicio -Ansiedad Patológica -Fiebre -Anemia -Hipovolemia -Hipertiroidismo -Falta de sueño -Abandono de beta-bloqueantes -Dolor -Insuficiencia cardíaca -Enfermedad pulmonar -Pericarditis -Miocarditis -Feocromocitoma Por drogas: -Catecolaminas -Vagolíticos -Alcohol -Cafeína -Nicotina -Marihuana -Cocaína La taquicardia sinusal fisiológica es atenuada por la adenosina administrada por vía endovenosa, con aceleración posterior de la frecuencia cardíaca en respuesta a la descarga adrenérgica que provoca la vasodilatación causada por el fármaco. Una aparente taquicardia sinusal puede en algunos casos corresponder a una taquicardia auricular ectópica cuyo origen esté próximo al nódulo sinusal. Cuando la taquicardia tiene comienzo y/o finalización bruscos, es más probable que se trate de una taquicardia auricular. En ciertos casos, la arritmia se debe en realidad a la deno- minada "reentrada sinoauricular", que es pasible de ablación por radiofrecuencia. Esta arritmia tiene comienzo y terminación bruscos, con una frecuencia de alrededor de 150 latidos por minuto. Finalmente, la taquicardia sinusal "inapropiada", que tiene una frecuencia de 110 a 130 latidos por minuto, con ondas P que sugieren un origen sinusal, se ve más frecuentemente en mujeres jóvenes y aparentemente se debería a una exagerada respuesta al estímulo adrenérgico. Su tratamiento se intenta habitualmente con beta-bloqueantes o con antagonistas del calcio. Reentrada nodal Es la taquicardia supraventricular más común, junto a las reentradas A-V por participación de vías anómalas. Típicamente, en el electrocardiograma se caracteriza por la ausencia de onda P visible o por su localización inmediatamente antes o después del complejo QRS. En este último caso, la onda P puede simular una "q" en las derivaciones de la cara inferior o una r' en V1. Debe destacarse que la polaridad de la onda P es siempre negativa en las derivaciones de la cara inferior. En niños menores de 5 años no se observa este tipo de taquicardia, presumiblemente debido a la falta de maduración de las estructuras involucradas. Cuando la reentrada nodal se presenta entre los 5 y los 10 años, es más frecuente observar la variedad "atípica" ("rápida-lenta", que analizaremos más adelante). Tradicionalmente se ha considerado que el sustrato estaba constituido por la denominada fisiología nodal doble: una vía "rápida" y otra "lenta" (habitualmente con menor período refractario que la rápida) (figura 1). Fig. 1: Representación esquemática del probable sustrato de la reentrada nodal. A: circuito confinado al nódulo A-V. B: participación de la aurícula. C: circuito en el nódulo A-V con sitios de entrada y salida diferenciados para una y otra vía (lenta y rápida) En la forma "común" o "típica" de reentrada nodal, el impulso avanza en el sentido anterógrado por la vía lenta y lo hace en el sentido retrógrado por la vía rápida (reentrada "lenta-rápida"). En el 5% de los pacientes el circuito puede invertirse (reentrada "rápida-lenta", "no común" o "atípica"). En el laboratorio de Electrofisiología es posible revertir el sentido de propagación del impulso mediante maniobras de estimulación. En la variedad común, la activación auricular más precoz se registra en las adyacencias del haz de His (figura 2), en tanto en la forma "rápida-lenta", la activación más temprana ocurre cerca del ostium del seno coronario. Fig. 2: Disociación A-V durante sobreestimulación ventricular en una reentrada nodal. La línea vertical en el último latido muestra que la activación auricular es concéntrica (antes en la zona tricuspídea que en el seno coronario) En la gran mayoría de los individuos a los que se practica un estudio electrofisiológico se observa el denominado "salto de vía" (figura 3 A y B). Fig. 3 A: Estimulación auricular programada. Con un intervalo de acoplamiento del extraestímulo de 321 mseg. el intervalo H1-H2 resultante mide 352 mseg. y no hay arritmias. Fig. 3 B: Estimulación auricular programada. Al aumentar la prematuridad del extraestímulo a 309 mseg. , el H1-H2 se prolonga a 493 mseg. ("salto de vía") y se inicia una reentrada nodal típica. Esto se caracteriza por un brusco alargamiento en el intervalo AH que supera los 50 mseg para un acortamiento en la prematuridad del extraestímulo auricular de sólo 10 mseg. Sin embargo, en el 15% de los individuos con reentrada nodal no es posible hallar "salto de vía". En ciertos casos, se puede demostrar fisiología nodal doble durante estimulación ventricular programada, lo que se asocia frecuentemente con la inducción de la variedad "atípica". Otras veces, la doble fisiología nodal se pone de manifiesto al agregar uno (o excepcionalmente, dos) extraestímulos, al marcapasear desde un segundo sitio, al reducir el ciclo del tren de estimulación basal (lo que acorta la refractariedad auricular y posibilita la captura con estímulos más precoces), o al administrar fármacos (isoproterenol o atropina y, raramente, esmolol o digoxina). Debe destacarse que hasta en el 2% de los pacientes con reentrada nodal dicha arritmia no es reproducible en el laboratorio. Frente a tal eventualidad, se deben integrar los datos epidemiológicos (sexo femenino, edad de comienzo de la arritmia) y electrocardiográficos disponibles de modo de lograr la mejor aproximación que sea posible. Una técnica particularmente valiosa consiste en el marcapaseo auricular con ciclos progresivamente decrecientes que, cuando se asocian con conducción 1 a 1 con un intervalo PR mayor que el RR, revelan conducción anterógrada por la vía lenta. En años recientes se ha instalado una polémica acerca de la participación auricular en la reentrada nodal, en contraposición a la existencia de un circuito confinado al nódulo A-V. Resulta sugestivo que la interrupción de la vía lenta se logra emitiendo energía de radiofrecuencia en las proximidades del ostium del seno coronario, que se encuentra notablemente alejado de la porción compacta del nódulo A-V. Además, al estimular desde determinados sitios del triángulo de Koch, se puede observar reciclado con un tiempo de circulación del impulso exactamente igual al ciclo de la taquicardia; esto indica que se ha marcapaseado desde el circuito y no desde un sitio adyacente al mismo. Sin embargo, también se puede observar -aunque es excepcional- la falta de activación auricular durante una reentrada nodal. Aunque esto sugiere la ausencia de participación de la aurícula en el circuito, puede argumentarse que sólo una porción extremadamente pequeña de la aurícula haya sido activada sin ser detectable por un catéter relativamente alejado. Más discutida aún es la participación imprescindible (o no) de una "vía final común inferior" ubicada por debajo del nódulo A-V. El bloqueo A-V de segundo grado que puede presentarse en una reentrada nodal asienta siempre por debajo del His, lo que sugiere un rol determinante de esta supuesta vía final común inferior (figura 4). Fig. 4: reentrada nodal con bloqueo 2 a 1 de localización infrahisiana. Arritmias asociadas La arritmia que más frecuentemente se asocia a la reentrada nodal ha sido -en nuestra experiencia- la taquicardia auricular automática con origen a todo lo largo de la crista terminalis. Esto sugiere una anomalía en el desarrollo de las estructuras que van desde el nódulo sinusal hasta la región posteroinferior del nódulo A-V (correspondiente a la vía lenta). También se ha observado asociación con aleteo auricular, lo que nuevamente da pie a un posible defecto en el desarrollo si se tiene en cuenta la localización de la zona con conducción lenta en el aleteo (suponiendo que aceptemos la existencia de dicha zona). En una paciente hemos llegado a observar la coexistencia de aleteo auricular típico, reentrada nodal y taquicardia auricular originada en la porción media de la crista terminalis. En cuanto a la coexistencia de la reentrada nodal con reentra- da A-V por participación de una vía accesoria, la regla es que recién se pone de manifiesto la reentrada nodal cuando se ha eliminado la conducción por el haz anómalo ya sea por medios farmacológicos o ablativos. Por este motivo, es importante evaluar la inducibilidad de reentrada nodal o la presencia de "doble fisiología nodal" una vez que se ha ablacionado una vía accesoria. Tratamiento El tratamiento agudo consiste en la realización de maniobras vagales (que actúan principalmente sobre la vía lenta) y, ante su fracaso, en la administración de verapamilo por vía endovenosa (asociado a las maniobras vagales). Para la prevención de las recurrencias el tratamiento actualmente recomendado es la ablación de la vía lenta mediante radiofrecuencia, con un éxito que supera el 95% y un índice de complicaciones notablemente bajo. Específicamente, la complicación más temida es el bloqueo A-V completo, que ocurre entre el 0,5 y el 3% de los casos, según diferentes autores. En nuestra casuística lo hemos observado en dos pacientes que requirieron marcapasos definitivo sobre un total de 386 reentradas nodales. En otros dos casos observamos bloqueo A-V transitorio que retrogradó por completo en menos de 5 minutos con total normalización de la conducción tanto en situación basal como durante estimulación auricular con frecuencias crecientes; en ambas pacientes el seguimiento alejado mostró conducción 1 a 1. Es frecuente observar taquicardia sinusal de 100-120 latidos por minuto en los 3 a 6 meses posteriores a la ablación de la vía lenta. Esto se atribuye a una denervación vagal causada por la radiofrecuencia, con lesión del panículo adiposo subepicárdico ubicado en las adyacencias de la cruz del corazón que contiene fibras vagales que se dirigen al nódulo sinusal. Este trastorno puede causar molestias en ciertos casos, lo que llega a hacer necesaria la administración de beta-bloqueantes durante algunos meses. Cuando la ablación no es el tratamiento elegido (o en el lapso que media hasta su realización) preferimos el diltiazem por vía oral, con un éxito del 60% para la prevención de las recurrencias. Aunque se ha establecido la dosis del fármaco en 3 a 5 mg/kg de peso, los resultados se obtienen con dosis menores. Es discutible la conveniencia de proceder a la ablación por radiofrecuencia luego de un único episodio de taquicardia. No hay en este sentido una recomendación universal para todos los pacientes y la decisión depende de la repercusión hemodinámica de la arritmia, la posibilidad de un embarazo en un futuro cercano, y la preferencia del paciente, entre otros aspectos. Reentrada A-V por vías accesorias Junto con la reentrada nodal, constituye la taquicardia supraventricular más frecuente. Típicamente, se observa por primera vez a menor edad que la reentrada nodal, con preferencia en varones (doble prevalencia con respecto a las mujeres). Aunque existen diferentes posibilidades para la ocurrencia de taquicardias supraventriculares relacionadas con vías accesorias, en el presente módulo sólo consideraremos la reentrada ortodrómica. Las demás serán consideradas en el apartado referente a "Síndromes de preexcitación". La reentrada ortodrómica se caracteriza por la propagación del impulso por el eje nódulo A-V/His en el sentido anterógrado y a través de la vía accesoria en el retrógrado. Debe aclararse que pueden participar dos o más vías anómalas, en forma sucesiva o, muy raramente, de manera simultánea. Esta reentrada se puede presentar tanto en individuos con preexcitación manifiesta (permanente o intermitente) como en ausencia de onda delta en el electrocardiograma (vías accesorias "ocultas"). Debido a que la conducción desde las aurículas a los ventrí- culos tiene lugar por el eje nódulo A-V/His, el QRS durante la taquicardia es angosto (a menos que haya bloqueos de rama preexistentes o dependientes de la frecuencia). Característicamente, el intervalo RP es menor que el PR aunque, a diferencia de la reentrada nodal, la onda P es más claramente discernible en el electrocardiograma ya que el RP mide 80 o más milisegundos. Esto obedece a una mayor demora desde el inicio de la activación ventricular hasta que el impulso llega hasta la base de los ventrículos para recién ser conducido hacia las aurículas a través de la vía accesoria. Es imposible que haya reentrada ortodrómica en presencia de bloqueo A-V de segundo grado o mayor, debido a que es imprescindible la participación de los ventrículos en el circuito de la arritmia. Otro rasgo llamativo está constituido por la "alternancia" de los complejos QRS que, cuando se observa en un número significativo de derivaciones y persiste minutos después del comienzo de la taquicardia, es fuertemente sugestivo de reentrada A-V por participación de una vía accesoria (figura 5). Fig. 5: Obsérvese la marcada alternancia de los complejos QRS. No conocemos el motivo de este fenómeno; aunque se podría postular que obedece a un trastorno de la conducción intraventricular 2 a 1, es un hecho que en un mismo paciente se puede observar taquicardia por reentrada A-V y por otro mecanismo (ambas con igual ciclo), y sin embargo, sólo en la primera hay una marcada alternancia. Con respecto a la inducción de estas arritmias, una de las técnicas consiste en estimular desde las aurículas -en especial en la proximidad de la vía accesoria- con una prematuridad creciente hasta que se alcanza el período refractario del haz anómalo. Tras ésto, si el impulso avanza por el eje nódulo A-V/His en forma suficientemente lenta como para permitir la recuperación de la vía anómala y de la aurícula, luego de la activación ventricular ocurre la retroconducción por el haz y así se produce la reentrada. Lo mismo ocurre en forma espontánea luego de una extrasístole auricular o con una frecuencia sinusal críticamente elevada. Desde los ventrículos, ya sea en forma espontánea (luego de extrasístoles) o en el laboratorio (mediante estimulación programada) es posible inducir reentrada ortodrómica luego del bloqueo del impulso en el His-Purkinje (con retroconducción por la vía anómala), por bloqueo retrógrado en el nódulo A-V y, finalmente, siguiendo a una reentrada entre ramas. El primer mecanismo es el que más frecuentemente observamos en la clínica. Localización de la vía accesoria En presencia de reentrada ortodrómica hay dos datos en el electrocardiograma que resultan de valor para localizar el haz anómalo: a) la polaridad de la onda P, y b) la presencia de un aumento en el ciclo de la taquicardia durante bloqueos de rama. El primer aspecto nos habla acerca de la inserción auricular de la vía. En cuanto a los bloqueos de rama, cuando ocurre una prolongación en el ciclo de 30 o más milisegundos con respecto a lo que se observa cuando el QRS es angosto, cabe considerar que se trata de una vía homolateral a la rama bloqueada. Esto es así como consecuencia de la necesidad de conducción transeptal para llegar al ventrículo que corresponde al fascículo bloqueado. Cuando hay hemibloqueo anterior izquierdo y la taquicardia es más lenta que en presencia de conducción intraventricular normal, estamos frente a una vía lateral izquierda ya que primero la activación ventricular ocurre en la zona correspondiente a la hemirrama pósteroinferior para recién entonces conducirse a la porción correspondiente al fascículo bloqueado. Dicha porción se encuentra adyacente a las vías laterales izquierdas. En presencia de vías septales o muy próximas al septum es posible observar un mínimo retardo o la ausencia de modificaciones en el ciclo durante QRS ancho. En realidad es más confiable analizar el intervalo RP (o el V-A en los registros endocavitarios) ya que un acortamiento en el PR puede compensar la modificación en la velocidad de propagación dentro de los ventrículos y determinar un ciclo igual al que se observa cuando el QRS es angosto. Tratamiento Al igual que en la reentrada nodal, el tratamiento agudo consiste en la realización de maniobras vagales y, ante su fracaso, en la administración de verapamilo o adenosina por vía endovenosa. Para la prevención de nuevos episodios cabe considerar en pri- mer término a la ablación por radiofrecuencia. De todas maneras, la indicación del método está sujeta a algunas consideraciones que se vinculan con la probable localización del haz anómalo: - Si este es izquierdo, puede llegar a requerirse una punción transeptal (que algunos realizan con apoyo ecocardiográfico, ya sea transtorácico o transesofágico, en tanto otros prescinden de dicha técnica). A nuestro entender, de hacerse una punción transeptal es necesario contar con cirugía "stand-by", lo que implica una planificación previa en tal sentido. - De tratarse de una vía anteroseptal o muy cercana al nódulo A-V, cuando la arritmia de presentación fue una taquicardia ortodrómica aceptablemente tolerada y si el período refractario anterógrado de la vía supera los 300 mseg (si la preexcitación es manifiesta), muchos prefieren reevaluar la conveniencia de emitir radiofrecuencia ante el riesgo de un bloqueo A-V iatrogénico. Estos aspectos deben ser explicados al paciente y a su familia al mencionar esta opción no farmacológica. En la era preablativa se analizaba el denominado "brazo débil" de la arritmia a través de la observación cuidadosa del modo de terminación de la arritmia (cuando esto ocurría en forma espon- tánea). Si la taquicardia se interrumpía con una secuencia R-P-R (es decir, fallaba la conducción retrógrada), se conside- raba a la vía accesoria como el componente vulnerable y se optaba por fármacos que actúan preferentemente sobre el haz anó- malo. Cuando, en cambio, había una onda P no seguida de un complejo QRS, el brazo débil era el nódulo A-V y se optaba por antagonistas del calcio o por beta-bloqueantes. Esto sigue teniendo validez cuando no se elige o si fracasa la ablación con catéter. Vías anómalas decrementales Constituyen una variante poco frecuente de los haces accesorios, caracterizada por conducción lenta sólo en el sentido retrógrado (ventrículo-auricular). Proveen el sutrato para la ocurrencia de arritmias incesantes denominadas "taquicardias de Coumel" o "PJRT" ("permanent junctional reciprocating tachycardia). Se caracterizan por tener un intervalo RP prolongado (RP mayor que el PR) (figura 6) Fig. 6: Taquicardia con RP largo debida a una vía accesoria retrógada con propiedades decrementales (PJRT). y, como consecuencia de la conducción decremental que posee la vía, por una progresiva prolongación del RP hasta que ocurre un QRS no seguido de onda P. La localización más frecuente de estos tractos asienta en la proximidad del ostium del seno coronario, aunque se los suele hallar también en otras localizaciones. Ocasionalmente, una ablación incompleta de una vía anómala clásica (con conducción "todo o nada") puede dar lugar a su transformación en una vía con propiedades decrementales. En cuanto a su presentación clínica, frecuentemente son detectadas en un examen de rutina por el pediatra o por el clínico. A pesar de la falta de síntomas, por su comportamiento incesante estas arritmias pueden dar lugar al desarrollo de una "taquicardiomiopatía". Debido a ésto, se recomienda su ablación mediante radiofrecuencia. El tratamiento farmacológico resulta difícil, con un resultado parcial de los betabloqueantes (que generalmente no interrumpen la arritmia aunque sí pueden aliviar los síntomas) y una cierta respuesta a la amiodarona. Taquicardias auriculares Si bien existen criterios valiosos para distinguir entre reentrada, automatismo y actividad gatillada, esto muchas veces resulta imposible aún tras una evaluación invasiva. Por tal motivo, algunos en la era de la ablación por catéter prefieren la denominación de taquicardias "focales" ya que es posible su eliminación mediante una lesión puntual. De todas maneras, es lógico suponer un mecanismo "gatillado" en presencia de intoxicación digitálica. Las taquicardias auriculares que se presentan en dicho contexto tienen una frecuencia de 130-160 latidos por minuto aproximadamente, con ondas P positivas en las derivaciones de la cara inferior (ya que la activación es típicamente craneo-caudal) y se asocian a conducción A-V variable. Si bien la extrasistolia ventricular es la arritmia más frecuente en la intoxicación digitálica, cabe destacar que la taquicardia auricular con conducción variable constituye una arritmia patognomónica. Su tratamiento específico consiste, además de la interrupción del fármaco, en la administración de difenilhidantoína. Cuando no hay patología estructural demostrable es razonable suponer un mecanismo automático, en especial si al comienzo se observa un acortamiento de los intervalos P-P ("calentamiento" o "warm-up") y hay un enlentecimiento de la arritmia precediendo a su terminación. En el estudio electrofisiológico no son inducibles mediante estimulación programada y, en cambio, suele verse su iniciación con isoproterenol. Los focos automáticos pueden asentar en cualquier sitio, aunque con más frecuencia se observan a lo largo de la "crista terminalis", en la desembocadura de las venas pulmonares (en especial la vena pulmonar superior izquierda) y en los apéndices auriculares. No es excepcional que haya más de un foco, lo que debe preverse y explicarse al paciente antes de un procedimiento de ablación. Las taquicardias auriculares automáticas no responden a la cardioversión eléctrica. Su tratamiento farmacológico puede intentarse con relativo éxito con flecainida, aunque en la actualidad se prefiere la ablación por radiofrecuencia del foco ectópico. Las taquicardias auriculares reentrantes se presentan más comúnmente en presencia de cardiopatía estructural y no es raro que haya antecedentes de reparación quirúrgica de comu- nicación interauricular o de transposición de los grandes vasos. Estas taquicardias, a diferencia de lo que ocurre con los focos automáticos, suelen tener la primera onda P distinta de las siguientes. Su inducción e interrupción mediante estimulación programada es reproducible (con mayor prematuridad de los extraestímulos cuando se marcapasea más lejos de la zona de conducción lenta). Se asocian con relativa frecuencia a un intervalo PR exageradamente prolongado durante la taquicardia, como manifestación de la afectación del sistema de conducción (e inclusive la onda P puede quedar superpuesta a la T precedente). Aunque se puede intentar el tratamiento con drogas de clase 1C, antagonistas del calcio, digital, betabloqueantes y amiodarona, es altamente efectiva la ablación con catéter. Taquicardia automática incesante de la unión Cuando se presenta en niños por debajo de 6 meses de edad se la considera "congénita" y en el 50% de los casos hay presencia de historia familiar. Tienen una frecuencia de 140 a 380 latidos por minuto, usualmente con disociación A-V. Su pronóstico es ominoso, con una elevada mortalidad. El tratamiento combinado con digoxina y propranolol puede contribuir a reducir la frecuencia cardíaca y ante su fracaso, se recurre a la amiodarona y, en última instancia, a la ablación del His con implante de un marcapasos definitivo. Aproximación al mecanismo de una taquicardia supraventricular Hay dos datos sumamente valiosos para distinguir entre reentrada nodal y reentrada A-V por una vía anómala: a) el sexo del paciente (más frecuente la reentrada nodal en mujeres y la reentrada A-V en varones), y b) la edad de comienzo de los episodios (cuando se iniciaron antes de los 15 años es altamente probable que se encuentre involucrado un haz anómalo). De este modo, una historia de taquicardia con QRS angosto que comenzó, por ejemplo, a los 25 años en una mujer, nos orienta fuertemente en favor de una reentrada nodal. La presencia de cardiopatía estructural asociada ayuda en gran medida, ya que en los adultos hay alteración órganica en el 80 al 90% de los pacientes con taquicardia auricular (en especial reentrante), lo que sólo ocurre en el 5 al 10% de las taquicardias de la unión. Sintetizaremos los criterios electrocardiográficos que nos ayudan a identificar el mecanismo más probable de una taquicardia supraventricular, a partir de cuatro preguntas: 1) ¿Hay bloqueo A-V de segundo grado o mayor (espontáneo o provocado)? (figura 7) Fig. 7: De arriba hacia abajo, derivaciones de superficie 1,2, y V1 y registros endocavitarios de la aurícula derecha alta (ADA), del seno coronario (SC) y del Haz de His (EHH). Se observa una taquicardia auricular con bloqueo 2 a 1 de localización suprahisiana (excepto en los últimos dos latidos, que son conducidos). Si la respuesta es afirmativa, puede excluirse definitivamente la participación de una vía accesoria y el mecanismo no puede ser una reentrada A-V. A su vez, cuando esto se observa fuera del laboratorio de Electrofisiología (es decir, cuando ha transcurrido un cierto tiempo desde el comienzo de la arritmia), prácticamente siempre se trata de una taquicardia auricular. Si hay bloqueo de segundo grado o mayor, podemos formular otro interrogante: 1b) ¿La frecuencia auricular es menor o mayor de 250 por minuto? Si es mayor de 250 por minuto, estaremos frente a un aleteo auricular. Debemos aclarar que este criterio tiene sus excepciones, ya que el diagnóstico de aleteo no se establece sólo a través de la frecuencia auricular (Katz publicó un caso de aleteo de 115 latidos por minuto en una paciente que recibía quinidina). Ni siquiera es posible excluir que se trate de un aleteo por la ausencia del típico "serrucho" ya que algunas "aparentes" fibrilaciones auriculares terminan siendo un flutter luego de una evaluación electrofisiológica. Sin embargo, el aleteo tiene un número "mágico" en lo relativo a la frecuencia auricular: 300 por minuto (y sus submúltiplos: 150,100,75, etc.), para la respuesta ventricular. 2) ¿Hay alternancia de los complejos QRS? Si bien ésto es discutido, no tiene una explicación racional y tiene limitaciones, cuando la alternancia persiste más allá de los primeros minutos de la arritmia en un número significativo de derivaciones del ECG de superficie, frecuentemente se encuentra involucrada una vía accesoria. 3) ¿Dónde está la P? (figura 8) Fig. 8: Ver texto. Aunque este criterio tiene gran valor, nos permitimos recomendar su empleo sólo si la onda P es claramente discernible. Para ello, resulta útil comparar el ECG durante la arritmia con trazados en ritmo sinusal, ya que determinadas deflexiones que parecen ondas q, r o melladuras en el segmento ST, por ejemplo, son la impronta que revela la presencia de la P. Cuando la actividad auricular y la ventricular coinciden, la onda P resulta enmascarada por el complejo QRS o bien ocurre inmediatamente antes o después (figura 8 A). Esto es característico de la reentrada nodal común. Si el RP es menor que el PR y, a su vez, el intervalo RP supera los 80 mseg, generalmente se trata de una reentrada A-V por participación de una vía anómala (figura 8 B). Finalmente, cuando la arritmia tiene RP mayor que el PR (taquicardias con RP prolongado) (figura 8 C), podemos encontrarnos frente a tres situaciones: a) Taquicardia auricular b) Reentrada A-V por una vía retrógrada decremental c) Reentrada nodal no común o atípica ("rápida-lenta") 4) ¿Cuál es el eje de P ? Si la onda P es positiva en las derivaciones II,III y aVF, podemos descartar con absoluta certeza a la reentrada nodal. A su vez, la polaridad de P ayuda a identificar el sitio de inserción auricular de una vía accesoria y el probable origen de una taquicardia auricular. Cabe destacar, de todas maneras, que alrededor del 5% de los pacientes tienen más de un mecanismo de taquicardia supraventricular (figura 9). Fig. 9: Se observa la interrupción de una taquicardia con QRS angosto mediante dos extraestímulos auriculares con un intervalo de de 330 mseg. (flechas), lo que demuestra la naturaleza reentrante de la arritmia. Al comparar con los dos últimos latidos (de origen sinusal), se aprecia que el ST durante la taquicardia está deformado por una P negativa. Los ciclos alternan entre dos valores: 370 y 480 mseg. Dado que estos cambios están determinados por el PR (ya que el intervalo RP es constante), es dable pensar que las variaciones resultan de conducción por una vía nodal rápida (ciclos más cortos) y por otra lenta (ciclos más prolongados) en forma alternante. El estudio endocavitario confirmó la presencia de una vía oculta de localización lateral izquierda asociada a doble fisiología nodal. El comportamiento "incesante" (adoptamos como definición a la presencia de arritmia durante más del 50% del tiempo en un Holter de 24 horas) orienta en favor de la existencia de una vía anómala con propiedades decrementales (PJRT o taquicardia "de Coumel") o bien de taquicardia auricular. Por tal motivo, estos mecanismos usualmente se detectan en un Holter. Otros mecanismos menos frecuentes 1) Taquicardia auricular multifocal Su presentación es típica en pacientes mayores de 50 años con insuficiencia cardíaca o enfermedad pulmonar aguda. Su alta mortalidad se debe a la gravedad de la enfermedad asociada y no a la arritmia per se. Se define por la existencia de 3 o más configuraciones diferentes de la onda P e intervalos P-P irregulares con una frecuencia auricular promedio de 120 a 200 latidos por minuto (en general la frecuencia es menor de 150 latidos por minuto) (figura 10). Fig. 10: Taquicardia auricular multifocal Predomina la conducción 1 a 1 debido al tono adrenérgico aumentado. Aunque no se comunicaron estudios electrofisiológicos en estas taquicardias debido a la gravedad de la situación clínica en la que se presentan, se cree que podrían deberse a actividad gatillada, como sugiere su respuesta al verapamilo y su relación causal con la digital y la hipopotasemia. El diagnóstico diferencial debe hacerse con la fibrilación auricular y con la existencia de ritmo sinusal con extrasístoles auriculares frecuentes. En este último caso existe un ritmo de base predominante, que es sinusal. La cardioversión eléctrica por lo común no resulta eficaz. El tratamiento consiste en : 1) Corrección del medio interno y eliminación de la causa que la provoca. 2) Verapamilo. 3) Aunque se ha informado el uso exitoso de metropolol, debe recordarse que los beta-bloqueantes pueden empeorar el cuadro dada la asociación frecuente de enfermedad broncopulmonar e insuficiencia cardíaca. 4) La digital puede disminuir la respuesta ventricular siempre que se excluya a la intoxicación digitálica como causa del trastorno. 2) Taquicardia de la unión no paroxística Esta taquicardia, en la que es común la disociación A-V, tiene una frecuencia mayor de 70 latidos por minuto, con aumento durante el ejercicio. Su duración puede oscilar entre horas y días y tiene comienzo y terminación graduales. La intoxicación digitálica constituye la causa en dos tercios de los pacientes, seguida por la cirugía cardíaca - especialmente valvular-, la miocarditis reumática aguda y el infarto agudo de miocardio. Probablemente se deba a actividad "gatillada" debida a la presencia de posdespolarizaciones tardías. En pacientes con fibrilación auricular previa, la intoxicación digitálica es frecuentemente diagnosticada frente a una inesperada regularidad del ritmo cardíaco en presencia de QRS angosto, lo que es debido a esta forma de taquicardia. En general, resulta efectivo el tratamiento de la intoxicación digitálica, pero cuando la arritmia se debe a cirugía cardíaca y causa deterioro hemodinámico por la existencia de retroconducción hacia las aurículas -con la consiguiente simultaneidad en las contracciones auricular y ventricular- puede ser necesaria la estimulación auricular con una frecuencia superior a la de la arritmia. Tope • Dr. Armando Pacher Presidente Comité Organizador [email protected] [email protected] • Dr. Emilio Kuschnir Presidente Comité Científico [email protected] [email protected] © CETIFAC Bioingeniería UNER Actualización