Reporte de un Caso de Mielinolisis Central Pontina
Anuncio

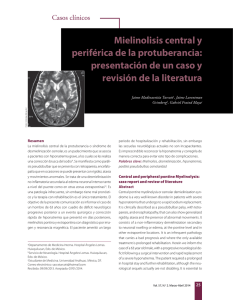
6 @ Imprenta Faroga, San José, 2005 Neuroeje, 2005, Vol. 19. N° 1 CASO CLÍNICO Reporte de un Caso de Mielinolisis Central Pontina Central Pontine Myelinolisis Raúl Bonilla Montero*, Kenneth Carazo Céspedes**, Ana Carolina Wang Zúñiga*** Neuropatólogo, Asistente de Patología, Hospital San Juan de Dios* Residente de Neurología, Hospital México** Médico General, Clínica de Pavas, COOPESALUD, R.L. *** Correspondencia: Kenneth Carazo Céspedes, Apartado Postal 11174-1000 San José - Correo Electrónico: [email protected] Artículo recibido: 01-02-2005 Aprobado: 02-02-2005 ABSTRACT Central Pontine Myelinolysis is a non inflammatory demyelinative disease that has been associated with the treatment for severe and symptomatic hiponatremia. However, there are many others factors that can alter the homeostasis and can generate myelinolysis; they should be known during the management of such patients. We review possible etiologies and discuss the case of a patient with polytrauma who developed recurrent infection, dysphagia and hyponatremia that generated a demonstrated myelínolysis. KEY WORDS: Central pontine myelinolysis hyponatremia malnutrition RESUMEN La Mielinolisis Central Pontina es una enfermedad desmielinizante no inflamatoria infreéuente que se ha asociado a reposición de sodio en hiponatremias severas y sintomáticas. No obstante existen otros factores que pueden alterar la homeostasis y así favorecer la mielinolisis; tales factores deben ser tomados en cuenta ante el manejo de una hiponatremia. Se plantean las diferentes causas que pueden contribuir a producir una mielinolisis pontina y se discute el caso de un paciente quien posterior a politrauma presenta múltiples complicaciones médicas incluyendo infecciones recurrentes, disfagia y culmina con un cuadro de hiponatremia que asociado a otros factores generan una mielinolisis pontina demostrada. PALABRAS CLAVES: Mielinolisis central pontina hiponatremia - desnutrición Introducción Mielinolisis Central Pontina (MCP), descrita por primera vez en 1959 por Adams et al1, se caracteriza por una desmielinización no inflamatoria que involucra la parte central de la base del puente. Los primeros casos fueron descritos en pacientes con historia de alcoholismo y desnutrición, en un momento en que la determinación sérica de electrolitos no estaba totalmente disponible para el clínico2; sin embargo en reportes posteriores se demuestra que la MCP ha ocurrido más frecuentemente en asociación con una rápida corrección de la hiponatremia3. Manifestaciones clínicas incluyen alteración de la conciencia, disfagia, disartria y otros signos de pares craneales caudales, parálisis pseudobulbar, para y tetraparesias (incluyendo el "síndrome de enclaustramiento"); además pueden presentarse convulsiones y manifestaciones psiquiátricas', en relación con la hiponatremia o la desmielinización extrapontina2. Revisión de Tema Las primeras descripciones postmorten de lesiones desmielinizantes en la base del puente fueron en pacientes con enfermedad de Wilson y datan de 1931. En 1950 el cuadro clínico fue por primera vez descrito en un paciente joven, alcohólico que rápidamente desarrolló una tetraplejía y parálisis pseudobulbar. No es sino hasta 1959, que Adams et al introducen el concepto de mielinolisis central pontina para este tipo de lesiones. La incidencia exacta de esta patología se desconoce, sin embargo algunos estudios han revelado lesiones típicas en un 0.25% de 3548 autopsias realizadas en adultos. El pico de incidencia se encuentra entre los 30-50 años con una pequeña preponderancia del sexo masculino'. Macroscópicamente en el tallo cerebral fijado se aprecia una decoloración grisácea de la parte central de la base del puente. El cuadro histológico muestra destrucción de las vainas de mielina a través de toda la lesión respetando relativamente el eje del cilindro de las células nerviosas de los núcleos pon tinos, con la presencia de macrófagos reactivos y sin signos de inflamación; aspectos que diferencian claramente la MPC del infarto y la desmielinización mediada por inflamación. Estos cambios inician siempre y son más severos en el centro geométrico del puente donde pueden producir franca necrosis, creando una típica imagen en alas de murciélago o de mariposa. En cuanto a la patogénesis se ha demostrado que el tejido nervioso utiliza diferentes mecanismos para evitar edema severo durante la hiponatremia. Fisiológicamente en el tejido nervioso se normaliza cualquier desbalance osmótico y por consiguiente de Vol. 19. N° 1, 2005 líquido y volumen, previniéndose así el edema cerebral. Inicialmente se varía el flujo del líquido cefalorraquídeo y concomitantemente el del líquido intersticial; luego en forma más tardía se da la salida de potasio y de otras sustancias orgánicas en la célula (taurina, fosfocreatina, mioinositol, glutamina y glutamato), para hacer una compensación con el medio hipoosmolar; mecanismo que se inicia a las 3 horas y hace un pico de efectividad a las 24 horas 2. En pacientes con hiponatremia aguda la compensación no puede llevarse a cabo lo suficientemente rápido, por lo que eventualmente se desarrolla el edema cerebral. Un cambio brusco en los niveles de sodio puede tener un papel más importante en el desarrollo de MCP que la hiponatremia por sí sola; aunque también se ha mencionado que variación en la osmolaridad sérica total por sí sola representa un factor de riesgo, sin embargo lo anterior es difícil de desligar del contexto debido al peso que ejerce la natremia sobre la osmolaridad. Las correcciones rápidas de niveles de sodio en la hiponatremia crónica llevan a una deshidratación significativa del cerebro, ya que el potasio y otras sustancias orgánicas no pueden ser reintroducidas en la célula lo suficientemente rápido para contrarrestar el cambio osmótico y la movilización de agua hacia afuera de la célula se da a una velocidad mayor; como resultado el axón se desmieliniza principalmente por separación mecánica y por último los oligodendrocitos se ven dañados y se necrosan. Una enfermedad caquectizante afecta los requerimientos del sistema para realizar todos éstos mecanismos, aunado a esto un estado de hipoxemia puede sumarse para lesionar la población de astrocitos y de ésta manera los cambios osmóticos que se están llevando a cabo en el intersticio ya no pueden ser balanceados por los mecanismos regulatorios de esta célula. También los cambios osmóticos en el espacio extracelular, conllevan a daño endotelial vascular resultando en edema vasogénico y por tanto la salida de sustancias mielinotóxicas de los vasos. Todos los mecanismos descritos llevan a la desmielinización6, pero aún queda por aclarar porqué estos cambios se dan principalmente a nivel pontino. El cuadro clínico de la MCP es muy variado pues otras, áreas del cerebro así como tractos ascendentes y descendentes pueden estar involucrados. Algunos pacientes se muestran con un curso silencioso mientras que en otros se han observado recaídas. Síntomas cardinales incluyen manifestaciones psiquiátricos, trastornos de la conciencia, alteración de los pares craneales caudales y signos de parálisis pseudobulbar con disartria y disfagia por la desmielinización del tracto corticobulbar, así como paraparesia espástica y tetraparesias de varios grados de severidad, ataxia, alteración de los reflejos, convulsiones e hipotensión. Muchas de estas manifestaciones son difíciles de discernir en pacientes críticamente enfermos, por lo cual muchas veces la patología es pasada por alto. El diagnóstico clínico es usualmente confirmado por la Resonancia Magnética (RM), la cual es superior a la Tomografía Computarizada (TC) especialmente en el diagnóstico temprano. Las lesiones son simétricas e hipointensas en las imágenes en TI en la fase aguda, mientras que en la fase subaguda son hiperintensas en T2. En las fases iniciales de la enfermedad los hallazgos en RM o TC pueden ser inespecíficos pues las áreas desmielinizadas no aparecen hasta una o dos semanas después. Anormalidades tempranas en RM o TC usualmente desaparecen, lo cual Mielinolisis Central 7 sugiere que pueden ser provocadas por edema de la parte central del puente, mientras las anormalidades posteriores pueden ser causadas por la desmielinización propia, lo cual sería irreversible. Estudios electroencefalográficos no muestran características específicas y no se consideran dentro de los métodos diagnósticos7. La MCP usualmente se manifiesta pocos días después de la corrección de la hiponatremia, por lo que una adecuada reposición es esencial en la prevención de ésta patología. Al inicio de la corrección el paciente presenta una franca mejoría al revertir la hiponatremia, pero los días siguientes presenta deterioro neurológico por la mielinolisis. Hiponatremia severa se define como concentraciones séricas de sodio menores a 115 mmol/l, principalmente porque los síntomas neurológicos severos se manifiestan generalmente a esas concentraciones. El término agudo-se refiere a una duración menor a 36-48 horas 8 o cuando la tasa de disminución del sodio sérico sobrepasa los 5mmol/l/h; ya que a ésta velocidad el tejido nervioso no logra realizar las medidas compensatorias. Hiponatremia severa se manifiesta por cambios en el sensorio y crisis convulsivas e involucra el riesgo de edema cerebral, herniación de tallo y déficit neurológico irreversible, por lo que debe ser tratada rápidamente, usualmente utilizándose solución de NaCl al 3%. La velocidad mínima de corrección de sodio debe ser 1mmol/l/h en la hiponatremia aguda; mientras que cuando se sospecha de un caso crónico el sodio debe ser repuesto a una velocidad menor de 0.5 mmol/l/h (8-12 mmol/l/día) ya que se han demostrado secuelas neurológicas en pacientes a quienes se les corrigió el sodio a velocidades mayores y por otro lado no hubo mayor incidencia de convulsiones por hiponatremia en quienes se corrigió a esa velocidad; debe tenerse en cuenta que la corrección del sodio no debe exceder el 10% del sodio total base. La rápida corrección de la hiponatremia se asoció con casi ninguna complicación neurológica cuando furosemida u otros diuréticos se administraron simultáneamente, principalmente porque favorecen la pérdida de agua libre. Lameta es alcanzar una hiponatremia leve (125mmol/1130mmol/l) que es cuando los síntomas severos ceden9 y luego manejarse con restricción de líquido o con soluciones isotónicas en días posteriores. Es importante mencionar que la hipokalemia debe ser corregida antes de tratar la hiponatremia. Se utiliza la siguiente fórmula para el manejo de la hiponatremia, la cual estima el cambio esperado del sodio sérico ante la infusión de un litro de cualquier solución de sodio: Cambio Na sér. = Total Na infundido- Na sér. Agua Corporal Total + 1 Deben de tomarse en cuenta las pérdidas de líquidos y electrolitos, tanto renales como extra renales; así como el estado nutricional y enfermedades concomitantes que pueden dificultar un resultado idóneo de la reposición. Igualmente debe definirse el tipo de hiponatremia, con sodio total depletado o normal o en un estado de hipo o hiperosmolaridad, para optimizar el manejo posterior. El Síndrome de Secreción Inapropiada de Hormona Antidiurética (SSIHAD), con sodio total normal y frecuente en trauma craneal debe considerarse ya que en el mismo la restricción de líquidos es de elección, sin embargo debe mencionarse que ésta medida produce una corrección lenta 8 R. Bonilla y en casos de emergencia el uso de soluciones hipertónicas y de diuréticos están indicados, permitiendo una corrección más controlada. No existe un tratamiento de elección para el manejo de la MCP, sin embargo en la literatura se describen cuatro diferentes. Estos incluyen la administración de TRH (factor liberador de tirotropina), plasmaféresis, la administración de corticoesteroides como monoterapia o la administración de plasmaféresis más inmunoglobulinas intravenosas 10. Debemos considerar que lo infrecuente de ésta patología impide contar con protocolos estandarizados de manejo en éste momento, así como de estudios comparativos, por lo que la prevención sigue siendo fundamental. Resumen del caso Masculino de 68 años de edad quien, previamente sano, sufre un accidente de tránsito al ser atropellado; produciéndose politrauma severo y fractura de base de cráneo, fractura expuesta del tercio medio de la tibia derecha y trauma de la rodilla izquierda. Manejado inicialmente en un Servicio de Ortopedia, al ingreso Glasgow 3 se describe pupila izquierda media no reactiva, sospechando un III par craneal compresivo se realiza TC que corrobora la fractura y demuestra una hemorragia subaracnoidea sin hematoma; se instaura tratamiento con fenitoína y diuréticos; se considera que presenta un III par craneal periférico traumático. En 12 horas Glasgow 7, es llevado a lavado quirúrgico y reducción cerrada de la fractura de tibia sin complicaciones; se inicia antibioticoterapia. A los 2 días movilizaba las 4 extremidades y abría los ojos al llamado, no acataba órdenes; posteriormente su sensorio mejoró manteniendo un Glasgow de 14. Durante la estancia el paciente recibió varios esquemas de antibióticos, debido a neumonía nosocomial asociada a ventilación mecánica la cual requirió los tres primeros días. Al mes de. estancia presenta progresivo descenso de la natremia con valores desde 126 mmol/l, hasta 108 a las dos semanas cuando se inició el tratamiento de reposición; concomitantemente el paciente tenía progresivo deterioro del sensorio. . La reposición de sodio se dio con NaCl al 3%, buscando una corrección no mayor a 0.5 mmol/l/h o de 15 mmol/l/ día hasta obtener un sodio de 125 mmol/l. Durante las primeras horas la corrección se logró llevar a un ritmo adecuado, pero no ocurrió así a las 12 horas de reposición que se pasó de un sodio de 116 a 125 mmol/l en 5 horas. A los 2 días el paciente nuevamente conciente pero se anota que presenta dificultad para la deglución; luego presenta un cuadro de diarrea asociada a antibióticos que lo hace llegar a una natremia de 138 mmol/l. A los 2 meses se extrae pin y el paciente es referido para continuar manejo médico en otro centro. Al ingreso se describen signos neumonía y úlcera sacra de III grado. En la exploración neurológica detallada del día siguiente se anota que abre los ojos al estímulo nociceptivo, hace sonidos guturales incomprensibles y realiza movimientos de retirada (Glasgow 8/15); la pupila derecha mide 2 mm y responde adecuadamente a la luz, pupila izquierda mide 8 mm y no responde a la luz; ojo izquierdo desviado lateralmente y con ptosis; fondo de ojo con vasoespasmo y exudados duros y blandos; reflejo nauseoso débil; hemiparesia faciobraquial izquierda; respuesta plantar flexora normal al lado derecho e indiferente al lado izquierdo. Los laboratorios de ingreso muestran azoemia prerrenal y discreta elevación del sodio en relación a deshidratación; albúmina en 1.7 g/ dl. Debido al antecedente traumático se plantea nuevamente la posibilidad de una lesión compresiva del III par craneal por lo que se solicitó una TC, la cual reveló fractura parietal izquierda, neumoencéfalo frontal pequeño y una lesión hipodensa frontoparietal derecha, sin efecto de masa que se consideró contusión cerebral. La valoración por neurocirugía anota que no es de manejo quirúrgico y se sugiere realizar una gastrostomía para evitar el uso de sonda nasogástrica y así disminuir el riesgo de sinusitis, tomando en cuenta que durante el internamiento el paciente había presentado un trastorno deglutorio sin encontrarse causa etiológica. No se describen posteriores exploraciones neurológicas detalladas que objetivasen el estado del paciente en ésta área. Durante los días posteriores se normaliza la azoemia, pero el paciente se mantiene con signos de infección pulmonar. El mal manejo de secreciones, así como el estado nutricional del paciente se convierten en la prioridad de tratamiento, haciéndose énfasis en la necesidad de realizar una gastrostomía percutánea, principalmente por la presencia de problemas deglutorios y encamamiento. La albúmina sérica mantenía niveles muy bajos que nunca pasaron los 2.5 g / dl Y la úlcera sacra tuvo mejoría ante las curaciones realizadas. A los tres meses del accidente se había estabilizado su patología infecciosa y tenía programada la gastrostomía, sin embargo presentó importante alteración del sensorio, con mínima respuesta al medio, y empeoramiento de la tos y secreciones por lo cual se suspendió el procedimiento. Tenía en ese momento un sodio en 108 mmol/l y una osmolaridad sérica de 221 mmol/l, por lo cual se inició corrección de sodio con solución NaCl al 3% a una tasa no mayor de 0.35 mmol/l/hora y se agregó mayor cantidad de sodio a la dieta. Al día siguiente el paciente se encuentra alerta. A los cuatro días de iniciada la reposición se suspende la misma ya que el sodio alcanzó un nivel de 126 mmol / dl y el paciente se encuentra en la condición basal de los días previos, alerta pero con mal estado general por sepsis. Se planteó la posibilidad de un SSIHAD el cual no fue corroborado. El paciente inicia en los días siguientes un cuadro de diarrea y se describe soporoso en días posteriores, cae en un choque séptico y presenta nuevamente azoemia prerrenal e hipernatremia, llegando a valores de nitrógeno ureico de 34 mg / dl con creatinina normal y de sodio de 162 mmol / dl, para una osmolaridad sérica de 326 mmol/l. Durante las dos semanas posteriores el paciente fue manejado con antibióticos, sin embargo empeoró el manejo de secreciones y así como su patrón respiratorio, posteriormente el paciente fallece. Se realizó la autopsia, la cual mostró en el cerebro evidencia de contusiones antiguas a nivel parietal derecho y en ambos lóbulos temporales. Además se observó un extenso reblandecimiento central sin afectación de los bordes, a nivel del puente de Varolio (Fig. 1). Microscópicamente dicha zona correspondió a una zona de desmielinización con abundantes macrófagos espumosos y preservación de cuerpos neuronales (Fig. 2) lo cual corrobora el diagnóstico de MPC; se descartan la isquemia o procesos inflamatorios como causales de la lesión. Se realizó además tinción para mielina (Luxol Fast Blue) la cual mostró la extensa desmielinización que formó la típica imagen en alas de mariposa (Fig. 3). El resto de la autopsia evidenció, básicamente, un proceso infeccioso bronconeumónico en ambos pulmones. Vol. 19. N° 1, 2005 Mielinolisis Central 9 Discusión La MPC es una patología desmielinizante no inflamatoria infrecuente, o al menos en su diagnóstico demostrado, que se ha relacionado a la corrección rápida de sodio en hiponatemias severas, sin embargo otros factores de riesgo son la desnutrición, infecciones bacterianas severas y la deshidratación concomitantes, los cuales se sumaron en éste caso; también los cambios de osmolaridad sérica fueron muy notorios. La semiológía es difícil de discernir en los pacientes críticos que generalmente son victimas de esta patología, pero los trastornos de deglución son muy constantes. La corrección de la hiponatremia severa con soluciones hipertónicas debe ser pronta y se recomienda a una tasa controlada hasta llegar a un nivel de hiponatremia leve, haciendo una vigilancia de la corrección horaria estricta; debe siempre tenerse en cuenta que hay otros factores asociados que pueden influir en forma aditiva sobre la génesis de la mielinolisis pontina sabiendo que pérdidas extra de electrolitos y líquidos pueden alterar los resultados esperados como en el caso de un cuadro diarreico. Se debe determinar en la forma más precisa la causa del desequilibrio electrolítico para optirnizar el tratamiento. El SSIHAD, en que la restricción de líquidos puede ser más apropiada, es un diagnóstico que debe ser tomado en cuenta ante un cuadro de hiponatremia en un politraumatizado. La morbimortalidad de pacientes con sintomatología bulbar depende en mucho de la atención brindada a los problemas deglutorios y el manejo de secreciones, que- deben ser resueltos con prontitud; teniendo en cuenta además que el aspecto nutricional es fundamental en pacientes críticos. Planteamos la posibilidad que la disfagia en este paciente se debió a algún grado de desmielinización generado durante la primera reposición de sodio y que esta fue la principal complicación que no permitió la optima recuperación del paciente a lo largo del internamiento, ya que con ella vinieron las repetidas infecciones nosocomiales. La presencia de un III par craneal completo no pudo ser precisada con exactitud en éste paciente, pero en vista de la normalidad del análisis del mesencéfalo y la ausencia de herniaciones se plantea que se haya debido a lesión periférica del nervio como se había sospechado. . Consideramos que el diagnóstico de mielinolisis pontina puede ser actualmente subdiagnósticado, primero por la falta de sospecha clínica debido principalmente a la poca. rigurosidad con que se realiza la exploración neurológica en muchos pacientes críticos, y segundo porque la confirmación anatomopatológica casi nunca se realiza debido a que a estos pacientes se les diagnostican causas de muerte en apariencia muy obvias por el proceso crítico que generalmente sufren. , Figura 1. Sección transversal de la parte caudal del puente de Varolio, que muestra una zona grisácea reblandecida en forma de "alas de mariposa". Figura 2. Microfotografía en la cual se observan abundantes macrófagos espumosos (flecha corta), un cuerpo neuronal íntegro (flecha larga) y restos de mielina. (Tinción de hematoxilina y eosina, 40X). Referencias Bibliográficas 1 2 3 Figura 3. Fotografía macro-micro que evidencia la zona de desmielinización central en el puente de Varolio. (Tinción de Luxol Fast Blue). 4 5 Victor M, Ropper AR. Adams and Victor's Principles of Neurology. 7th Ed. New York, NY.: Mc Graw-Hill Companies lnc, 2001: 1193-1195. Sterns, Richard. The Management of Symptomatic Hyponatremia. Seminars in Nephrology. 1990; 10: 503-514. Pirzada A, Miran l. Central Pontine Myelinolysis. Mayo Clinic Proc. 2001; 559-562. Lamp C, Yazzdi K. Central Pontine Myelinolysis. European Neurology. 2002; 3-10. Laurreno R, Illowsky Karp B. Myelinolysis after Correction of Hiponatremia. Annals of lnternal Medicine. 1997; 57-62. 10 6 7 8 R. Bonilla Lamp C, Yazzdi K. Central Pontine Myelinolysis. European Neurology. 2002; 3-10. Lawson A, Niedermeyer E. Central Pontine Myelinolysis. Am J END Tecnol. 2002; 151-158. Gross P. Treatment of severe hiponatremia. Kidney International. 2001; 2417-2427. 9 10 Adrogué HJ, Madias NE. Hyponatremia. New England Journal of Medicine. 2000; 1581-1569. Dietmar Bibl et al. Treatment of central pontine myelinolysis with therapeutic plasmapheresis. The Lancet. 1999; 1155.