CASO CLÍNICO ARRITMIAS VENTRICULARES
Anuncio

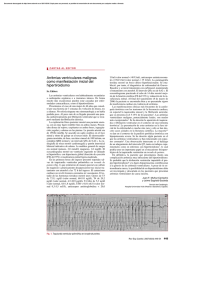
Gerardo Moreno Unidad de Arritmias Instituto de Cardiología y Cirugía Cardiovascular Mujer de 36 años de edad sin Factores de Riesgo ni antecedentes cardiovasculares familiares ni personales. Ingres a UTI por sepsis a punto de partida de lesión plantar: Antibiótico terapia vía parenteral con Vancomicina e Imipenem. Disnea en CF IV: asumen diagnóstico de Insuficiencia Cardiaca y se realiza Furosemida parenteral. 24 hs posteriores presentó TV Polimorfa y FV por lo que fue necesario CVE. Posterior a su reversión se registra en monitor y en ECG alta densidad de Extrasistolia Ventricular Polimorfa, duplas ventriculares y salvas autolimitadas de TV Polimorfa. Cómo controlaríamos sus arritmias ventriculares? Se administró Amiodarona endovenosa en dosis de carga y mantenimiento. Posteriormente la paciente presentó múltiples episodios de FV que requirieron CVE. Derivación a nuestro centro. Al ingreso, sintomática por palpitaciones, mareos, episodios pre-sincopales, y episodios sincopales. Ionograma de ingreso: hipopotasemia (K+ 2,7 mEq/L), hipomagnesemia (Mg++ 1,34 mEq/L) e hipocalcemia (Ca++ 7,65 mEq/L). Medicada con Amiodarona vía parenteral y antibióticoterapia. EV con R/T EV con R/T Inducción de Torsade de Pointes Cuál sería nuestra conducta a continuación? Al Ingreso al Servicio de UTI de nuestra institución se inició corrección parenteral de su Ionograma. Una vez iniciada esta corrección, pero sin que aún se alcanzara el objetivo, continuó presentando múltiples episodios de TdP y FV (tormenta arrítmica), que en ciertas ocasiones requirieron CVE. Qué conducta adoptaríamos? Se suspendió la administración de amiodarona y se implantó Marcapasos Transitorio para sobreestimulación, acortar y homogeneinzar la repolarización ventricular. Normalizado el medio interno, se interrumpió estimulación ventricular y se evidenció repolarización ventricular normal y ausencia de EV. Finalmente, tras la estabilización cardiovascular y la buena respuesta al tratamiento antibiótico, se decidió su alta institucional, sin datos patológicos en el electrocardiograma, con el medio interno corregido e indicación de seguimiento por consultorio externo. El electrocardiograma sigue siendo el método complementario más accesible, no invasivo, barato y útil de la práctica clínica en cardiología. La formación de las ondas en el electrocardiograma están íntimamente ligadas al desplazamiento de iones, en especial potasio y sodio, a través de la membrana celular de los miocitos. Por lo tanto, es lógico que las alteraciones electrolíticas y los fármacos antiarrítmicos que afectan el transporte transmembrana de dichos iones produzcan cambios en los trazados electrocardiográficos y fisiopatológicamente expliquen su relación en la inducción de arritmias ventriculares de alto riesgo. TRASTORNOS HIDROELECTROLÍTICOS AMIODARONA (CLASE III) Moreno, G, et al. REV ARGENT CARDIOL 2008;76:491-494 La duración del potencial de acción en el endocardio es 40-60 milisegundos mayor que en el epicardio, certificando de esta manera la presencia de un gradiente de voltaje entre ambas capas de la pared ventricular. Epi M Endo PAT Normal del Endocardio + + ECG – – PAT Normal del Epicardio También sabemos que existe una subpoblación de células en el espesor del miocardio ventricular (células M), que difieren en sus propiedades funcionales en lo que respecta a la repolarización. Tienen una tendencia a prolongar en forma desproporcionada el potencial de acción en respuesta a trastornos hidroelectrolíticos o a la acción de drogas antiarrítmicas, jugando un rol importante en el desarrollo del Sme. de QT prolongado adquirido. La interrelación entre las células endocárdicas, epicárdicas, y células M, durante la repolarización ventricular, determinan la morfología y duración del intervalo QT y onda T, tanto en condiciones normales como patológicas. Moreno, G, et al. REV ARGENT CARDIOL 2008;76:491-494 Las EV con R/T, representa la actividad eléctrica conducida transmuralmente durante las fases 2 o 3 del potencial de acción Las fases 2 y 3 del potencial de acción tienen expresión electrocardiográfica en la rampa de descenso de la onda T, la cual presenta una ventana de vulnerabilidad para las arritmias ventriculares, y se debe a la heterogeneidad de la repolarización de los miocitos. El mecanismo fisiopatológico más relacionado con las arritmias ventriculares complejas del síndrome de QT prolongado adquirido son las posdespolarizaciones precoces en fase 2 generadas en el endocardio y/o subendocardio en presencia de fármacos o trastornos electrolíticos que prolonguen la duración del potencial de acción. Moreno, G, et al. REV ARGENT CARDIOL 2008;76:491-494 En el caso clínico presentado hemos refrescado la memoria respecto de las alteraciones electrocardiográficas de la repolarización ventricular secundarias a la interacción de alteraciones del medio interno y a la administración de amiodarona, sus consecuencias clínicas en el desarrollo de arritmias ventriculares malignas y el mecanismo fisiopatológico involucrado. Debemos recordar analizar las posibles interacciones farmacológicas y el medio interno de los pacientes previo a la toma de conductas. El ECG sigue, y seguirá siendo, “la herramienta” cardiológica por excelencia para valoración de riesgo arrítmico. No lo subestimemos GRACIAS POR SU ATENCIÓN Y PARTICIPACIÓN Gerardo Moreno Unidad de Arritmias Instituto de Cardiología y Cirugía Cardiovascular