PMP Q10 1P 2014
Anuncio

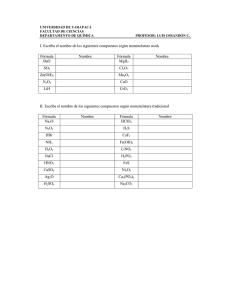
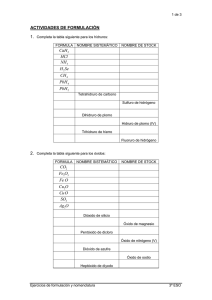
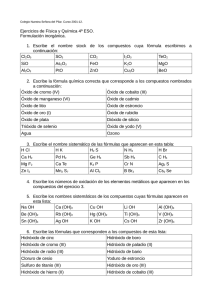
INSTITUCIÓN EDUCATIVA FEDERICO SIERRA ARANGO Área: Ciencias Naturales y Educación ambiental Docente: Grado: John Jairo Pérez M Décimo Plan de mejoramiento FI y Nomenclatura Fecha: Asignatura Química PLAN DE MEJORAMIENTO DEL PRIMER PERIODO DE 2014 Parámetros: Esta actividad debe resolverse y entregarse en un trabajo manuscrito, de forma individual, según fecha convenida con el docente, este será sustentado con una evaluación escrita, de no entregarse el trabajo escrito no se tendrá derecho a la presentación de la evaluación; los puntos de dicha evaluación se sacaran del mismo trabajo entregado. 1. Explicar cuál es la relación existente entre las 2. 3. 4. 5. fuerzas intermoleculares y la solubilidad de las sustancias Con base en los conceptos de las fuerzas intermoleculares explicar la diferencia de los puntos de ebullición del agua (H2O), 100 ºC y el tetracloruro de carbono (CCl4), 77 ºC ¿Qué son el punto de fusión y ebullición de una sustancia? Las fuerzas intermoleculares están directamente relacionadas con el punto de fusión o ebullición de las sustancias. ¿De qué manera? ¿Cómo influyen los puentes de hidrógeno en la diferencia de densidad del agua líquida y del agua sólida? Argumenta tu respuesta. Completa las siguientes ecuaciones a. b. c. d. e. f. g. h. i. j. ____ + ____ → VO2 Bi+5 + O2 → ______ HNO3 + Ca(OH)2 → _____ Ti2O3 + H2O → ______ ____ + ____ → H2Se I2O7 + H2O → ______ ____ + ____ → HBr N2O3 + H2O → ______ H2Se + Rh(OH)4 → _____ + _____ → Co(OH)3 7. Determina los números de oxidación de los siguientes compuestos: Compuesto a. Ácido hidrácido + hidróxido → _____ + _____ b. Hidróxido + ácido oxácido → ____ + ____ c. Óxido ácido + agua → _____ d. Metal + oxígeno → _____ e. No metal + oxígeno → _____ f. Óxido básico + agua → g. Metal + Hidrogeno → h. Halógeno + Hidrogeno → 6. Completar las siguientes reacciones con las Números de oxidación Óxido de cobre (II) Óxido arsenioso Hidróxido de radio Ácido sulfhídrico Ácido sulfuroso Hipoclorito de potasio Nitrato de cesio Carbonato de aluminio Fluoruro áurico fórmulas y los nombres tanto de reactivos como de productos 8. Completar la siguiente tabla Fórmula Pd(OH)2 Al2O3 CaF2 H2CO3 Br2O5 H2Te FeSO3 Números de oxidación Función química Stock Racional o sistemática Tradicional