Ferran Sanz, "Plataformas Tecnológicas, Innovative Medicines Initiative Medicamentos Innovadores"
Anuncio

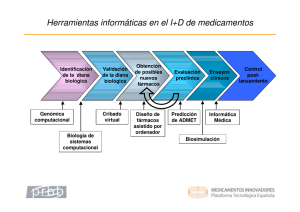
Plataformas Tecnológicas Innovative Medicines Initiative Medicamentos Innovadores Ferran Sanz Vicerrector de Política Científica - Universidad Pompeu Fabra Unidad de Investigación en Informática Biomédica (IMIM-UPF) Barcelona Crear un nuevo medicamento es un proceso largo e incierto 15 Medicamento Estudios en miles de pacientes para evaluar riesgos Aprobación para la comercialización 10 Estudios en 100-300 pacientes (Fase II) Estudios en voluntarios sanos (Fase I) Estudios intensivos de seguridad Candidato a medicamento 5 Desarrollo de formulaciones Cribado Síntesis de compuestos años Descubrimiento y validación de dianas Idea Adapted from a slide of EFPIA Estudios preliminares de seguridad … y extraordinariamente caro $M (in year 2000 dollars) Average R&D costs per NCE medicine launched Bain & Co 1700 Dec 03 1600 1400 R&D Heads 1400 @ IBC mtg 2003 1200 1000 Post-launch costs 800 95 802 600 400 200 0 54 1976 231 1987 2000 Year 2003 Evolución del I+D farmacéutico números índices (1992 = 100) 200 Ventas globales 180 Gasto en I+D global 160 140 120 Tiempo de desarrollo (media móvil 3 años) 100 80 Nuevas entidades químicas 60 0 1992 1993 1994 1995 1996 1997 1998 1999 2000 Fuente: CMR International Institute for Regulatory Science 2001 2002p Nuevos moléculas (NME) por área geográfica Fuente: SCRIP Publications - EFPIA calculations Reproducido de una presentación de Octavi Quintana. EC. 2006. Razones de fracaso en el desarrollo de nuevos medicamentos Actualmente, seguridad y eficacia son los dos principales cuellos de botella Agenda estratégica: cuellos de botella a superar Seguridad: Facilitar la obtención de medicamentos más seguros Generar nuevos métodos y herramientas para la predicción toxicológica y la evaluación de riesgos, incluyendo la identificación y validación de biomarcadores. Eficacia: Facilitar la obtención de medicamentos más efectivos Abordar nuevos métodos y herramientas para la predicción farmacológica, incluyendo la identificación y validación de biomarcadores, y nuevas estrategias para el reclutamiento de pacientes. Inicialmente los estudios se enfocarán hacia 5 enfermedades con grandes retos científicos: cáncer, enfermedades de SNC, enfermedades inflamatorias, diabetes y enfermedades infecciosas. Gestión del Conocimiento: Explotar el potencial de las nuevas tecnologías de la información para analizar grandes cantidades de información de manera integradora y predictiva Producir predicciones “in silico” de los beneficios y riesgos de posibles nuevos medicamentos. Educación y Formación: Generar los expertos requeridos para facilitar y mejorar la investigación biofarmacéutica y el proceso de desarrollo de medicamentos. El objetivo de IMI no es desarrollar nuevos medicamentos o vacunas Oportunidades actuales en I+D de medicamentos El descubrimiento y desarrollo de medicamentos tiene oportunidades de mejora en base a: 9 la comprensión de los mecanismos terapéuticos (y los de los efectos secundarios y la toxicología) desde el punto de vista molecular, estructural y sistémico, 9 la consideración de los nuevos conocimientos y tecnologías “ómicos”, 9 la explotación “inteligente” de la enorme diversidad molecular natural y sintética, y 9 el uso de las grandes capacidades actuales de las tecnologías de la información. Herramientas informáticas en el I+D de medicamentos Identificación de la diana biológica Genómica computacional Biología de sistemas computacional Validación de la diana biológica Cribado virtual Obtención de posibles nuevos fármacos Diseño de fármacos asistido por ordenador Evaluación preclínica Predicción de ADMET Ensayos clínicos Informática Médica Biosimulación Control postlanzamiento La predicción de actividades farmacológicas es factible n=64 VL=2 r2=0.94 q2=0.88 Modelado molecular en diseño de fármacos Agua extracelular ketanserina O H N O + N N F Membrana celular O h5HT2AR Agua intracelular Fenotipo = f (tratamiento), pero la “f” es muy complicada Treated Patient Treated Control Control no tratado Paciente no tratado Reproducido de una presentación de Scott Boyer (AstraZeneca) Fenotipo = f (tratamiento), pero la “f” es muy complicada Paciente tratado Treated Control Control no tratado Paciente no tratado Reproducido de una presentación de Scott Boyer (AstraZeneca) Fenotipo = f (tratamiento), pero la “f” es muy complicada Paciente tratado Control tratado Control no tratado Paciente no tratado Reproducido de una presentación de Scott Boyer (AstraZeneca) Herramientas informáticas en el I+D de medicamentos Identificación de la diana biológica Genómica computacional Biología de sistemas computacional Validación de la diana biológica Cribado virtual Obtención de posibles nuevos fármacos Diseño de fármacos asistido por ordenador Evaluación preclínica Predicción de ADMET Ensayos clínicos Informática Médica Biosimulación Necesidad de integración de datos y conocimiento Control postlanzamiento Oportunidades actuales en I+D de medicamentos ómica Imágen biomédica Datos de ensayos y historias clínicas Conocimiento previo Genómica Proteómica Química combinatoria Cribado de alto rendimiento (HTS) Quimiogenómica Integración/ análisis de datos Conocimiento Tecnologías de la información Eficacia y seguridad Gestión integrada del conocimiento en I+D de medicamentos Integración de información biomédica para obtener una visión más completa de una enfermedad, su tratamiento farmacológico y las reacciones adversas Enfermedad Información clínica Sistemas Dianas Fármacos Información “ómica” Información química Conceptos clave en Gestión de Conocimiento según IMI • Gestión traslacional del conocimiento (integración de información básica a la clínica) • Datos compartidos entre distintas organizaciones • Ontologías y estándares • Minería de textos • Representación del conocimiento científico (por ejemplo, en biología de sistemas o modelos de enfermedad) • Modelado y simulación (multi-escala) • Predicción in silico de la eficacia y de la seguridad Plataforma Tecnológica Española Medicamentos Innovadores Objetivos: • Crear un foro con la participación de todos los actores interesados en el progreso del I+D farmacéutico en España, potenciando la colaboración entre ellos. • Facilitar el dialogo bidireccional entre las iniciativas españolas y europeas. • Detectar áreas de investigación prioritarias según los capacidades e intereses de los actores españoles, con especial atención a las necesidades industriales. • Promover de proyectos de investigación que impliquen una amplia colaboración entre los actores. Actores del I+D farmacéutico • Industria farmacéutica • Compañías especializadas en el I+D farmacéutico (PYMEs biotecnológicas, CROs) • Instituciones académicas • Instituciones sanitarias • Autoridades sanitarias, industriales y de I+D, europeas, españolas y autonómicas. • Organizaciones de pacientes Plataforma Tecnológica Española Medicamentos Innovadores Grupos de trabajo: – Investigación clínica – Gestión del conocimiento – Educación y formación – Seguridad preclínica • 1ª Reunión Anual (Barcelona, Julio 2005) – Más de 150 participantes • 2ª Reunión Anual (Madrid, Julio 2006) – Más de 250 participantes • 3ª Reunión Anual (Barcelona, 3-4 Octubre 2007) Plataforma Tecnológica Española Medicamentos Innovadores www.medicamentos-innovadores.org – http://www.medicamentos-innovadores.org