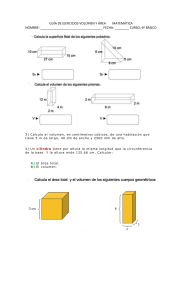
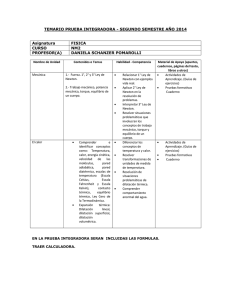
Calor y Temperatura Es Absorbido Liberado Produciendo Produciendo Aumento de temperatura Disminución de temperatura Puede producir Se propaga por CALOR Puede ser Se expresa mediante Sólidos Fahrenheit Escalas termométricas Mediante Celsius kelvin Mediante Mediante Puede producir Contracción Vacío Energía en tránsito Convección Conducción Dilatación Fluidos Radiación Calor y Temperatura2 Si es liberado produce Si es absorbido produce CALOR Se propaga por cuerpos Disminución de temperatura Lineales Superficiales Aumento de temperatura Volumétricos que produce que produce Contracción Excepto en el Agua entre 0[ºC] y 4[ºC] Excepto en el Dilatación Calor y Temperatura 3 CALOR Puede producir Cambio de temperatura Cambio de fase Calor específico Capacidad calórica Lleva al Equilibrio térmico Si se agrega calor Calor latente Fusión Solidificación Evaporación Ebullición Condensación Sublimación Sublimación inversa Si se extrae calor 1. Calor y Temperatura 1. Calor y temperatura 1.1 Definición Calor Se define como la energía en tránsito que fluye, natural y espontáneamente, desde un cuerpo o sistema más caliente hacia otro más frio. Es una magnitud escalar y se mide en: S.I.: [joule] = [J] C.G.S.: [ergio] = [erg] También se suele expresar en [calorías] = [cal]. Temperatura Se puede decir que es una medida de la energía cinética promedio de las partículas de un cuerpo o sistema. Mientras más se muevan (vibren) las partículas de un cuerpo, mayor será su “temperatura”. Es una magnitud escalar y se puede expresar en grados Celsius, Fahrenheit o kelvin. 1. Calor y temperatura 1.2 Escalas termométricas La temperatura de un cuerpo puede expresarse según diferentes escalas termométricas. Las más usadas son: Celsius, Fahrenheit y kelvin. Tº ebullición del agua Escala Fahrenheit Creada en 1724 por Gabriel Fahrenheit (alemán); en esta escala, la temperatura de fusión del hielo corresponde a 32 [ºF], y la temperatura de ebullición del agua corresponde a 212 [ºF]. Escala Celsius Creada en 1742 por el sueco Anders Celsius. En esta escala, a la temperatura de fusión del hielo se le asigna el 0 [ºC], y a la temperatura de ebullición del agua se le asigna el valor 100 [ºC]. Tº fusión del hielo 5 TC (TF 32) 9 1. Calor y temperatura 1.2 Escalas termométricas Escala kelvin o absoluta Creada en 1848 por el británico William Thomson (lord Kelvin). La escala absoluta incluye la temperatura teórica más baja posible, el cero absoluto o 0 [kelvin] . En esta escala, la temperatura de fusión del hielo corresponde, aproximadamente, al 273 [K], y la de ebullición del agua al 373 [K]. Tº ebullición del agua TK TC 273 Tº fusión del hielo Cero absoluto Ejercicios 3. ¿Cuál de los siguientes gráficos representa correctamente la relación entre las escalas Fahrenheit [F] y Celsius [ºC]? D Comprensión 2.Transmisión del calor 2. Transmisión del calor 2.1 Formas de transmisión del calor El calor puede transmitirse de tres formas distintas, que dependerá del medio por el cual se propague. Conducción El calor (energía) se transmite de una partícula a otra, avanzando paulatinamente por el material. Esta forma de propagación del calor ocurre solo en los sólidos. 2. Transmisión del calor 2.1 Formas de transmisión del calor En una lámpara de magma Convección Corresponde a la transmisión del calor en los fluidos (líquidos y gases), debido a corrientes cálidas ascendentes y frías descendentes. Corrientes cálidas ascendentes En la atmósfera En el interior de la Tierra Corrientes frías descendentes 2. Transmisión del calor 2.1 Formas de transmisión del calor Radiación Corresponde a la transmisión del calor por medio de ondas electromagnéticas (principalmente del espectro infrarrojo), pudiendo viajar grandes distancias a través del vacío, sin calentar el espacio intermedio. Fotografía térmica: los seres vivos irradiamos calor Ejercicios 4. Respecto de la transmisión del calor por convección, es correcto afirmar que I) se requiere de una fuente de calor para que se produzca. II) se produce en un medio material. III) se produce solo en los fluidos. A) B) C) D) E) Solo I Solo II Solo III Solo I y II I, II y III E Reconocimiento 3. Dilatación y contracción 3. Dilatación y contracción 3.1 Efectos de la variación de temperatura en los cuerpos Al variar la temperatura de un cuerpo son varios los efectos que este puede experimentar. Algunos de ellos son: los cambios de fase, la incandescencia, deformación, el aumento de tamaño (dilatación) o la disminución de tamaño (contracción). Cambios de fase Metal fundido incandescente Botellas deformadas por calor Chocolate fundido por calor Falla producida por dilatación 3. Dilatación y contracción 3.2 Cuerpos lineales, superficiales y volumétricos Dentro de los efectos mencionados, nos detendremos en los cambios de tamaño que experimentan los cuerpos cuando varía su temperatura, es decir, estudiaremos la dilatación y contracción. Cuerpos lineales En la naturaleza todos los cuerpos poseen 3 dimensiones: alto, largo y ancho. Sin embargo, en algunos cuerpos una (o dos) de esas dimensiones puede ser mucho menor y, por tanto, despreciable respecto de las demás. Por ejemplo, en un alambre delgado y largo, el alto y el ancho, comparados con su longitud, pueden llegar a ser dimensiones despreciables. Cuando un cuerpo posee una sola dimensión importante, siendo las otras dos despreciables respecto de la primera, se dice que es un cuerpo “lineal”. Un alambre es un cuerpo “lineal” En los cuerpos lineales, nos fijamos solo en su longitud. 3. Dilatación y contracción 3.2 Cuerpos lineales, superficiales y volumétricos Cuerpos superficiales En cambio, otros cuerpos poseen dos dimensiones importantes (largo y ancho), siendo la tercera (alto) despreciable respecto de las otras dos; en este caso se dice que el cuerpo es “superficial”. En los cuerpos superficiales, nos interesa solo la superficie del cuerpo. Una lámina, una hoja o una membrana, son cuerpos “superficiales” 3. Dilatación y contracción 3.2 Cuerpos lineales, superficiales y volumétricos Cuerpos volumétricos Cuando todas las dimensiones de un cuerpo son relevantes, no existiendo dimensiones despreciables respecto de las demás, entonces se dice que el cuerpo es “volumétrico”. En los objetos volumétricos, todas las dimensiones del cuerpo son relevantes y, por lo tanto, nos interesa su volumen. Un cubo, un cilindro, un balón de futbol y un microondas, son cuerpos “volumétricos”. 3. Dilatación y contracción 3.3 Dilatación – contracción de cuerpos lineales Dilatación - contracción lineal En general, al variar la temperatura de un cuerpo lineal, su longitud cambiará aumentando si esta se eleva, o disminuyendo si esta decrece. Así, el cuerpo se dilatará al calentarse, y se contraerá al enfriarse. Por ejemplo: en un riel de ferrocarril. Li L L i T L Juntas de dilatación: son espacios que permiten la dilatación y contracción en las estructuras. Ejercicios 5. El espacio, medido en centímetros, que debe existir entre dos rieles de acero de 6 [m] de longitud cada uno, si se prevé una variación de temperatura de 100 [ºC], es (Considere que el coeficiente de dilatación lineal del acero es 11 · 10-6 [ºC]-1) A) B) C) D) E) 0,33 0,66 0,99 1,32 1,88 B Aplicación 3. Dilatación y contracción 3.4 Dilatación – contracción de cuerpos superficiales Dilatación - contracción superficial En general, al variar la temperatura de un cuerpo superficial su área o superficie cambiará, dilatándose al calentarse o contrayéndose al enfriarse. Por ejemplo: en una lámina delgada de metal. S Si S Si T Las estructuras deben tener espacio suficiente para dilatarse, de lo contrario, pueden colapsar. 3. Dilatación y contracción 3.5 Dilatación – contracción de cuerpos volumétricos Dilatación volumétrica La dilatación o contracción afecta el volumen del cuerpo; todo el cuerpo “crece o se encoge” al variar su temperatura. Por ejemplo: en un cubo de metal. V ¿Sabías que la torre Eiffel crece 6 [cm] en los veranos? Vi V Vi T Ejercicios 6. Un líquido de coeficiente de dilatación volumétrica igual a 6,9 · 10-5 [°C]-1 se encuentra contenido en un recipiente de metal, cuyo coeficiente de dilatación lineal es 2,3 · 10-5 [°C]-1. Si el líquido llena completamente el recipiente y el conjunto es sometido a un aumento de temperatura de 40 [°C], es correcto afirmar que el líquido se dilatará A) B) C) D) E) el triple de lo que lo hará el recipiente. el doble que el recipiente. lo mismo que el recipiente. la mitad de lo que se dilatará el recipiente. la tercera parte de lo que se dilate el recipiente. C ASE 4. Anomalía del agua 4.1 El agua, una excepción Como acabamos de ver, en general los materiales se dilatan cuando se calientan y se contraen cuando se enfrían. Sin embargo, cuando enfriamos agua, a partir de los 4 [ºC] comienza a dilatarse, aún cuando su temperatura siga disminuyendo. Por otro lado, si tenemos agua a 0 [ºC], al aumentar su temperatura comenzará a contraerse, al contrario de lo esperado; esto sucederá así hasta los 4 [ºC]. A partir de esta temperatura, el agua comienza a comportarse de manera “normal”, es decir, se dilatará al calentarse y se contraerá al enfriarse. Densidad (g/mL) Recuerda, este comportamiento anómalo del agua solo se presenta entre los 0 [ºC] y los 4 [ºC]. Volumen v/s temperatura Densidad v/s temperatura Temperatura (ºC) 4. Anomalía del agua 4.2 Dos fenómenos curiosos Normalmente, un material en estado sólido es más denso que en estado líquido, por lo que un sólido se hunde en su propio líquido. Sin embargo, ¡el hielo flota en el agua!....¿por qué? Si ponemos agua en una botella y la dejamos en el congelador a 0 [ºC], veremos que todo el volumen de agua se congela. Sin embargo, en los lagos de zonas muy frías, aun cuando la temperatura en invierno puede alcanzar varias decenas de grados bajo cero, solo se congela la capa superior del agua. ¿Por qué no se congela el lago completo? ¿Qué importancia puede tener este fenómeno? Ejercicios 7. Si se tiene un líquido desconocido a 0 [°C] y se le aplica calor, esperaríamos que el líquido A) B) C) D) E) se dilate. se contraiga. mantenga su volumen. se dilate o se contraiga, nunca mantenga su volumen. se contraiga o mantenga su volumen, nunca se dilate. D Comprensión 5. Equilibrio Térmico 5. Equilibrio térmico 5.1 Definición Al aislar dos cuerpos a distinta temperatura, fluirá calor desde el cuerpo más caliente (quien cederá calor, enfriándose) hacia el cuerpo más frío (quien absorberá calor, calentándose) hasta que sus temperaturas se igualen; cuando esto suceda, el sistema se encontrará en equilibrio térmico. Calor 6. Capacidad calórica y calor específico 6. Capacidad calórica y calor específico 6.1 Definición Capacidad calórica Es la cantidad de calor que un cuerpo debe absorber o ceder para elevar o disminuir, respectivamente, su temperatura en 1 [ºC]. La capacidad calórica se designa por C y es característica de cada cuerpo. Mientras mayor sea la capacidad calórica del cuerpo, más costará calentarlo o enfriarlo. Se calcula como: Q C T Sus unidades son: calorías cal º Celsius º C 6. Capacidad calórica y calor específico 6.2 Definición Calor específico Se define como la capacidad calórica por unidad de masa. Es característica de cada material y se calcula como: Q C c m m T Sus unidades son: calorías cal gramo º C g º C El calor específico del agua es: 1 [cal/g °C] Q m c T ¿Quién posee mayor calor específico, el agua Ambasdeplovsaeseonoelemlaisgmuaodcaelolarpeisspceincaíf?ico,pues son el mismo material; agua. Ejercicios 8. La capacidad calórica de un cuerpo de 200 [g] de masa, que aumenta su temperatura en 40 [°C] cuando se le suministran 4.000 [cal], es A) 4.000 cal B) 2.000 cal ºC ºC cal ºC C) 200 D) 100 cal E) 0,5 ºC cal ºC D Aplicación Ejercicios 9. Si el calor específico del acero es 0,12 cal , la cantidad de calor g ºC necesaria para que 400 [g] de acero pasen de 20 [°C] a 100 [°C] es A) 3.840 [cal] B) 4.350 [cal] C) 4.520 [cal] D) 4.800 [cal] E) 5.500 [cal] A Aplicación 7. Principio calorimétrico de mezclas 7.1 Definición Al mezclar dos materiales a distinta temperatura en un sistema en donde el calor no pueda entrar ni escaparse hacia el exterior (sistema adiabático), todo el calor cedido por el material a mayor temperatura será completamente absorbido por aquel a menor temperatura. Q 2 m2 c2 T2 Q1 m 1 c 1 T1 Material más caliente. Material más frío. Q cedido Q absorbido 0 m1 c1 Teq T1 +m2 c2 Teq T2 0 Ejercicios 10. Un recipiente de capacidad térmica despreciable contiene 100 [g] de agua a una temperatura de 20 [°C]. Si al interior del mismo se vierten 200 [g] de agua a 80 [°C], la temperatura final de la mezcla es A) 40 [°C] B) 50 [°C] C) 60 [°C] D) 70 [°C] E) 80 [°C] C Aplicación 8. Cambios de fase 8.1 Fases de la materia 8. Cambios de fase 8.1 Fases de la materia Evaporación Ebullición Condensación Fusión Sublimación Solidificación 8. Cambios de fase 2. Leyes del cambio de fase – Calor latente de cambio de fase 1. A una determinada presión atmosférica, los cuerpos solo pueden cambiar de fase a una temperatura bien definida llamada “temperatura crítica” o “punto crítico”; en el caso del hielo, la temperatura a la cual logrará fundirse, es decir, su punto crítico de fusión, es 0 [ºC]. 2. Estando en su punto crítico, para que cada gramo de material pueda cambiar de fase se le debe ceder o extraer una cantidad de calor Q por unidad de masa m, llamada calor latente de cambio de fase “L”. El calor latente de cambio de fase se expresa como: L Q m 3. Durante un cambio de fase la temperatura del material permanece constante. En el caso del hielo, al fundirse (a 0 ºC), el agua que se obtiene está a 0 [ºC] ya que, durante todo el proceso de fusión, la temperatura se mantiene constante. 4. El calor latente absorbido o liberado por un cuerpo para cambiar de fase será el mismo que requiera liberar o absorber, respectivamente, para revertir dicho cambio. 9. Roce y calor 9.1 Definición Cada vez que frotamos dos superficies entre sí se produce fricción o roce entre ellas, disipándose calor. Esto se debe a que interactúan entre sí los electrones de cada una de las superficies en contacto, produciendo interacciones de tipo electromagnético. La energía así disipada se manifiesta en forma de calor. Ejercicios 11. Un trozo de azufre de 200 [g] de masa se encuentra a una temperatura de 119 [°C]. Si el punto de fusión del azufre es 119 [ºC] y se le suministran 650 [cal], ¿cuál es la masa de azufre que se fundirá? (Considere que el azufre posee un calor latente de fusión de 13 cal ). g A) 25 [g] B) 50 [g] C) 60 [g] D) 100 [g] E) 200 [g] B Aplicación