TP 3 2016 - Campus Virtual - Universidad Nacional de Tucumán
Anuncio

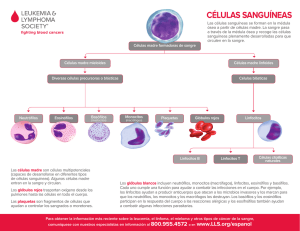
Facultad de Bioquímica, Química y Farmacia Universidad Nacional de Tucumán GUÍA DE TRABAJOS PRÁCTICOS Nº2 Hemograma. Recuento diferencial leucocitario. Trastornos leucocitarios. 1 RECUENTO DIFERENCIAL LEUCOCITARIO La fórmula leucocitaria o recuento diferencial leucocitario (RDL) actual es lo que antes se denominaba “Hemograma de Schilling”. Existen dos tipos: la porcentual o relativa y la absoluta. La primera expresa la cantidad de cada tipo leucocitario por 100 leucocitos; y la segunda la cantidad de cada uno por litro de sangre. Para el cálculo de la segunda es indispensable el conocimiento de la cifra de leucocitos por litro. Debe tenerse en cuenta que la relativa es sólo el paso indispensable para el cálculo de la absoluta, que es la que tiene valor clínico real. Cualquier aumento de la concentración absoluta es un incremento absoluto, mientras que una elevación sólo del porcentaje representa un aumento relativo. El RDL en condiciones de normalidad está constituido por 5 poblaciones de leucocitos: neutrófilos (segmentados y en cayado o en banda), linfocitos, monocitos, eosinófilos y basófilos. MÉTODO VISUAL O MANUAL: técnica para el examen del frotis sanguíneo Una vez confeccionado el extendido, éste se deja secar, se fija, colorea y examina sistemáticamente. Se cubre toda la superficie con una película fina de aceite de inmersión y se observa primero con poco aumento (con el objetivo de 40x), hasta encontrar un área donde los glóbulos rojos estén bien distribuidos y no distorsionados, la morfología de los leucocitos sea clara y los tamaños de ambos sean proporcionales (generalmente se encuentra en la zona intermedia entre el cuerpo y cola del extendido) (Figura N°1). FIGURA N°1: Elección de la zona para realizar el recuento diferencial leucocitario Varios sistemas se han propuesto para realizar el recuento diferencial. Existe el problema de la diferente distribución de las células en la extensión, que debe ser tenido en cuenta al realizar el recuento. El mismo se realiza con el aumento de 40x o 100x de acuerdo a la experiencia del operador o a la complejidad de las células del extendido. La técnica consiste en seguir una guarda griega y contar entre 100 o 200 elementos (Figura N°2). De esta manera el trayecto en la zona elegida incluirá un 50% de células de las zonas periféricas o bordes y el 50% restante de células pertenecientes a la zona central propiamente dicha. La distribución irregular de los leucocitos obedece al diferente tamaño de las células, de forma que las más pequeñas (linfocitos) tienen tendencia a situarse hacia el centro de la extensión y las de mayor tamaño (monocitos) en las regiones más periféricas. 2 FIGURA N°2: Técnica de recuento diferencial leucocitario 50 o 100 elementos en c/u Cálculo del número absoluto de cada leucocito Ejemplo: para el cálculo del valor absoluto de neutrófilos se utiliza una regla de tres simple Neutrófilos x 109/L = Número total de leucocitos x 109/L X % de neutrófilos 100 Se procede de igual manera para cada uno de los otros leucocitos. Causas de error en el RDL 1. Distribución irregular y no aleatoria de los leucocitos en la extensión 2. Realización del recuento en un lugar inadecuado de la extensión 3. Variaciones de la calidad y las características de la tinción 4. Observación de un número insuficiente de células 5. Pericia del observador en la identificación de determinados leucocitos: neutrófilos segmentados versus no segmentados (en bandas), monocitos versus linfocitos estimulados, formas inmaduras de granulocitos neutrófilos. Pese a todo ello y de momento, el RDL visual continúa siendo el método de referencia para la realización de la fórmula leucocitaria tanto para el NCCLS (National Committee for Clinical Laboratory Standards) como para el ICSH (International Comité for Standardization in Haematology). MÉTODO AUTOMÁTICO En la actualidad existen autoanalizadores hematológicos que realizan un RDL con gran precisión, exactitud y sobre todo rapidez. Un autoanalizador de fórmula leucocitaria debe cumplir siempre dos requisitos fundamentales: 1. Reconocer y cuantificar las poblaciones leucocitarias. 2. Identificar la presencia de anomalías morfológicas mediante alarmas con el objetivo de detectar la posible presencia de células atípicas o patológicas. Los métodos que utilizan los distintos contadores para la realización del RDL son los siguientes: VCS (Volumen, Conductivity, Scatter): Medición de volumen de cada célula por impedancia; conductividad que informa sobre la estructura interna de las células incluyendo el tamaño nuclear, densidad y razón núcleo/citoplasma; y dispersión, que informa sobre la granularidad y superficie celular. Empleado por Coulter STKS. 3 M.A.P.S.S.: Separación por dispersión polarizada con ángulos múltiples (0º, 90º, 10º, 90º despolarizado). Empleado por Abbott CELL-DYN 3500. CC y RF: Detección por CC (corriente continua), que mide volumen total celular y RF (radiofrecuencia), que informa sobre la relación núcleo/citoplasma, la complejidad y el volumen del núcleo celular y la granulación citoplasmática. Empleado por Sysmex SE-9000. Tinción con peroxidasa, dispersión óptica y absorción para neutrófilos, linfocitos, monocitos y eosinófilos; y lisis diferencial, contracción y dispersión con láser para basófilos. (Bayer ADVIA 120) El informe del autoanalizador incluye el recuento porcentual y absoluto de los distintos tipos leucocitarios. Lamentablemente, aunque se trata de instrumentos muy útiles para detectar la presencia de patología, carecen de garantía para la interpretación de muchas alteraciones, que generalmente son suministradas bajo la forma de alarmas. Por lo tanto siempre es obligada la observación microscópica de la extensión para poder determinar de qué anomalía se trata. VALORES DE REFERENCIA DE LA FÓRMULA LEUCOCITARIA (adultos) Fórmula absoluta [x109/L] Célula Fórmula relativa [%] Rango Promedio Rango Promedio 0,1-0,5 0,22 2-5 3,0 1,7-6,5 3,78 38-65 52,0 0,04-0,4 0,20 1-4 2,7 Basófilos 0-0,10 0,04 0-1 0,5 Linfocitos 1,0-4,0 2,50 22-40 34,0 Monocitos 0,1-0,8 0,30 2-10 4,0 Neutrófilos Cayados Neutrófilos segmentados Eosinófilos VARIACIONES DE LA FÓRMULA LEUCOCITARIA Las células hematopoyéticas se distribuyen en cuatro compartimientos: Compartimiento mitótico medular Compartimiento de maduración-depósito medular Compartimiento vascular, el cual en el caso de los neutrófilos se subdivide en: 1. un pool circulante 2. un pool marginal Compartimiento tisular Durante las infecciones las células centinelas tales como los macrófagos tisulares combaten los microbios invasores y liberan citoquinas tales como IL-1, IL-6 y TNF, 4 que activan las células estromales y los linfocitos T para producir factores de crecimiento adicionales. Como resultado, las células progenitoras tempranas en médula ósea son estimuladas para dividirse y diferenciarse, los precursores mieloides se mueven más rápidamente a través del pool de maduración; un número aumentado de células se libera a partir del compartimiento de depósito medular y los fagocitos circulantes se vuelven capaces de sufrir y aumentar el estallido respiratorio. Arneth clasifica a los neutrófilos en dos grupos fundamentales: neutrófilos no lobulados o incompletamente lobulados y neutrófilos completamente lobulados (2 o más lóbulos). Los primeros son los mielocitos, metamielocitos y cayados. Se habla de desviación a la izquierda del hemograma cuando aumentan las formas no segmentadas y/o inmaduras. Se dice que hay desviación a la derecha, cuando aumentan las células maduras o adultas de mayor lobularidad. Para valorar la intensidad de la desviación, se recurre al “Indice de desviación nuclear” (IDN), que consiste en establecer la relación entre las células neutrófilas no segmentadas y las segmentadas. IDN = Mielocitos + Metamielocitos + Cayados = 1 = 0,06 Segmentados 16 Se considera desviación a la izquierda cuando el IDN es superior a 1/10=0,1. Dentro de la desviación a la izquierda hay dos tipos: 1. De tipo regenerativo 2. De tipo degenerativo La primera está determinada por el aumento proporcional (y en general también absoluto) de las formas menos lobuladas de cromatina juvenil, más laxa y con funcionalismo perfecto. Reflejan por lo tanto una hiperactividad medular de carácter normal. En cambio, la desviación izquierda de tipo degenerativo consiste en el aumento del IDN pero sobre la base de elementos que aún cuando ostentan escasa lobulación presentan cromatina picnótica y desde el punto de vista citoplasmático, micropolivacuolización y granulación tóxica. Son verdaderos “piocitos circulantes”, con escasa funcionalidad. VARIACIONES DE LA FÓRMULA LEUCOCITARIA CON EL ESTRÉS Consta de las fases de: a) Alarma. Caracterizada por leucocitosis con neutrofília con desviación a la izquierda de tipo regenerativo; linfopenia y eosinopenia. b) Reacción o lucha: caracterizada por el incremento de la cifra de monocitos y descenso proporcional de la neutrofilia. c) Agotamiento o curación alternativamente. Fase de agotamiento: el organismo sucumbe ante la agresión. Se caracteriza por retrogradación a neutrofilia con desviación a la izquierda de tipo degenerativo. Fase de curación: caracterizada por linfocitosis y eosinofilia con regularización de los demás valores y desaparición de la desviación a la izquierda. En la mayoría de los procesos infecciosos y en muchos metabólicos y 5 necrotizantes se cumple estrictamente la regla del estrés. No obstante, hay infecciones que soslayan alguna etapa y otras que prolongan bastante algunas de ellas. TRASTORNOS LEUCOCITARIOS Las variaciones de la concentración de cada tipo leucocitario en la sangre resulta de: El flujo de células hacia la sangre La salida de células desde la sangre La distribución de las células dentro del sistema vascular Combinaciones de ellas Los trastornos de los leucocitos pueden ser clasificados en fisiológicos y patológicos. VARIACIÓN FISIOLÓGICA DE LOS LEUCOCITOS Se define como leucocitosis un aumento del número absoluto de leucocitos por encima del rango de referencia (mayor de 10,0 x 10 9/L). Se define leucopenia como una disminución del número absoluto de leucocitos por debajo de 4,5 X 109/L. Estos términos están definidos para la población adulta. La leucocitosis fisiológica consiste en un aumento de los leucocitos producido por factores o situaciones que no implican lesión hística y se observa en los siguientes casos: Edad: el recuento total al nacer y durante las primeras 24 horas de vida varía dentro de amplios márgenes: 9,0-30,0 x 109/L, siendo los neutrófilos las células predominantes (neutrofilia), con hasta un 15% de cayados. Los linfocitos se convierten en la célula predominante después de la segunda semana; esa linfocitosis alcanza su máximo al año y se mantiene hasta los cinco años cuando es superada por los neutrófilos. No es raro encontrar en los primeros meses linfocitos estimulados por contacto con los primeros antígenos. Actividad física: aumento de los leucocitos a expensas de los neutrófilos proporcional a la intensidad y persistencia del esfuerzo muscular. El aumento rápido y la falta de formas inmaduras sugiere un desplazamiento de los leucocitos de la reserva marginal a la circulatoria. 9 Embarazo: leucocitosis de hasta 15,0 x 10 /L. Ocurre casi completamente en el último trimestre. Hay aumento de los neutrófilos y algunos granulocitos inmaduros a veces, especialmente en hiperemesis y toxemia gravídica. En el parto hay neutrofilia progresiva y al iniciar el puerperio los leucocitos fluctúan entre 10,0-40,0 x 109/L, especialmente en las primíparas. Se normaliza en el séptimo día del puerperio. Tabaco: los fumadores de cigarrillos muestran un recuento leucocitario mayor que los no fumadores. 6 VARIACIONES PATOLÓGICAS DE LOS LEUCOCITOS Comprenden variaciones cuantitativas y cualitativas. VARIACIONES CUANTITATIVAS Un aumento en el número absoluto de neutrófilos, eosinófilos, basófilos, monocitos y linfocitos por encima del valor de referencia para la edad, se designa respectivamente como: neutrofilia, eosinofilia, basofilia, monocitosis y linfocitosis. Una disminución en el número absoluto por debajo del valor de referencia para la edad de neutrófilos, eosinófilos, monocitos y linfocitos se denomina: neutropenia, eosinopenia, monocitopenia y linfopenia respectivamente. Neutrofilia: indica aumento del número de neutrófilos por encima del valor de referencia absoluto para la edad. En un adulto se habla de neutrofilia cuando el valor de neutrófilos es mayor a 7 x 109/L. Reacción leucemoide: significa leucemio: leucemia y eidos: aspecto, tiene aspecto de leucemia, por lo tanto son aquellos cuadros donde aparecen células inmaduras (metamielocitos, mielocitos, promielocitos y algunos blastos). Puede ir acompañada de leucocitosis tan altas como de 50,0 x 10 9/L, como así también hay raros casos de leucopenia. Las siguientes características de la reacción leucemoide ayudan a distinguirla de la leucemia mieloide crónica: 1. Los neutrófilos podrían mostrar granulación tóxica 2. Los recuentos de eosinófilos y de basófilos no están aumentados 3. El score de la fosfatasa alcalina leucocitaria está aumentado. Reacción leucoeritroblástica: el hallazgo característico es la presencia de glóbulos rojos nucleados (eritroblastos) y de glóbulos blancos inmaduros (principalmente mielocitos) en sangre periférica. El recuento de leucocitos puede o no estar elevado. Este cuadro se encuentra cuando la médula ósea está infiltrada con células malignas (carcinoma, linfoma, mieloma, leucemia), con tejido fibroso (mielofibrosis primaria o secundaria) o células de depósito (enfermedad de Gaucher). La aspiración o biopsia de medula ósea ayudan a establecer el diagnóstico. Neutropenia: indica disminución del número de neutrófilos por debajo del valor de referencia absoluto para la edad. La neutropenia se puede clasificar como: 1. Leve, si el recuento de neutrófilos es de 1,0-1,5 x109/L 2. Moderada, si el recuento es de 0,5-1,0 x109/L 3. Severa, si el recuento es menor a 0,5 x109/L 4. Agranulocitosis, si el recuento es menor de 0,2 x109/L Esta estratificación es útil para predecir el riesgo de infecciones piógenas, ya que sólo los pacientes con neutropenia severa tienen susceptibilidad aumentada a infecciones con riesgo de muerte, especialmente si la neutropenia persiste por más de unos pocos días. Las bacterias endógenas son los invasores más frecuentes, pero la colonización con una variedad de organismos de origen nosocomial también es común. La neutropenia se acompaña de monocitosis, pero los monocitos son más lentos para ejecutar las funciones del neutrófilo. 7 La neutropenia también forma parte de la pancitopenia cuyas principales causas son: 1. Falla en la producción de las células 2. Destrucción periférica de las células aumentada Eosinofilia: Causas: enfermedades alérgicas, infecciones parasitarias, síndrome de Loëffler, leucemia mieloide crónica. Basofilia: Causas: síndromes mieloproliferativos crónicos, reacciones de hipersensibilidad. Monocitosis: Causas: infecciones bacterianas, síndromes mielodisplásicos, leucemias mielomonocíticas Linfocitosis: Se considera linfocitosis cuando el número absoluto de linfocitos se encuentra por encima del valor de referencia con respecto a la edad: 9 En la infancia: el número de linfocitos es > 9,0 x10 /L 9 En adultos: el número de linfocitos > 4,0 x10 /L Más importante que la cifra absoluta o relativa de linfocitos, es el análisis cuidadoso de sus características morfológicas, en busca de. A) linfocitos estimulados, reactivos o inmunocitos: suelen presentarse en mayor o menor grado en las distintas linfocitosis de origen infeccioso (mononucleosis, citomegalovirus, rubéola, varicela y otras). En general son más grandes que los normales, con núcleos situados a veces excéntricamente y puede haber nucleolo. Citoplasma hiperbasófilo, siendo más marcada la basofilia en la periferia de la célula. Los inmunocitos se agrupan bajo tres aspectos: Plasmocitoides: semejantes a células plasmáticas. Monocitoides: semejantes a un monocito. Pseudoblásticos: semejantes a blastos. Los linfocitos reactivos se informan en porcentaje incluyéndolos dentro de la fórmula leucocitaria relativa. La mononucleosis infecciosa es una enfermedad aguda y generalmente benigna producida en adolescentes y adultos jóvenes causada por la infección con el virus de Epstein-Barr. Se presenta en la primera semana con una linfocitosis relativa y absoluta de más de un 50%, con más de un 10 % de inmunocitos. Estos inmunocitos son linfocitos T citotóxicos y supresores, que reaccionan contra los linfocitos B, que son los infectados por el virus. Los síntomas principales son la fiebre, dolor de garganta y las adenopatías. La prueba diferencial para MNI detecta anticuerpos heterófilos (Reacción de Paul-Bunell-Davidsohn) adsorbibles por eritrocitos de buey. También se podrían detectar anticuerpos contra el virus de Epstein-Barr B) linfocitos atípicos: se presentan en patologías oncohematológicas. Linfopenia: Se presenta cuando el recuento absoluto de linfocitos está por debajo del valor de referencia para la edad. Ejemplos: SIDA, tratamiento con corticoides y quimioterápicos 8 VARIACIONES CUALITATIVAS ALTERACIONES CITOPLASMÁTICAS ADQUIRIDAS Granulaciones gruesas, granulaciones tóxicas o exceso de granulación primaria: se trata de una abundante granulación primaria, inespecífica y azurófila, la cual es densa y más voluminosa que la específica. Tiene como enzima marcadora la peroxidasa y corresponde a lisosomas. Aparecen en cuadros infecciosos o inflamatorios, intoxicaciones, en tratamientos con drogas antineoplásicas, corticoides o factores estimulantes de colonias. Vacuolización: las vacuolas fagocíticas se encuentran en los neutrófilos en diversas situaciones (quemaduras, infecciones severas y drogas antineoplásicas) y pueden ser únicas o múltiples, en cuyo caso se habla de micropolivacuolización. Cuerpos de Dhöle: son inclusiones ovaladas que se sitúan hacia la periferia del citoplasma del neutrófilo. Están compuestos fundamentalmente por ARN y adquieren un color azul pálido con la tinción panóptica. Aparecen en el curso de infecciones graves (por ejemplo la escarlatina) y en quemados. Desgranulación de los polimorfonucleares neutrófilos: puede deberse a una disminución del número de gránulos específicos o a un defecto en su tinción. Es un fenómeno que se observa con relativa frecuencia en las enfermedades hematológicas con afectación de la célula madre pluripotente o de la serie mieloide (leucemia agudas, mielodisplasias y síndromes mieloproliferativos crónicos). Bastones de Aüer: estructuras citoplasmáticas presentes en la progenie granulocítica en forma de barras gruesas o palillos que resulta de la fusión de lisosomas. Se tienen de color fucsia con la tinción de May Grünwld Giemsa. Son peroxidasa positiva. Se presentan en las leucemias mieloides agudas y en los síndromes mielodisplásicos. ALTERACIONES CITOPLASMÁTICAS HEREDITARIAS Anomalía de Alder-Reilly: de transmisión autosómica recesiva, consiste en la aparición de gruesas granulaciones azurófilas, muy visibles y que suelen ocasionar algunas enfermedades tesaurismóticas como la mucopolisacaridosis. Son coloreables metacromáticamente por el azul Alcián, peroxidasa negativa y PAS positiva. Anomalía de Chediak-Higashi: de transmisión autosómica recesiva, se asocia a un síndrome clínico peculiar (albinismo óculo-cutáneo) y consiste en la aparición de inclusiones citoplasmáticas azurófilas gigantes, peroxidasa positiva y PAS negativo. La granulación no se limita al neutrófilo, sino que se extiende a toda la progenie leucocitaria. Los neutrófilos son no funcionantes o hipofuncionantes, por lo que son frecuentes las infecciones. Anomalía de May-Hegglin-Rebuck: de transmisión autosómica dominante, consiste en la presencia de inclusiones color celeste, Feulgen y PAS negativas. Son residuos ribosómicos de ARN. El defecto comprende a los leucocitos y las plaquetas, siendo característica la aparición de macroplaquetas, cuya función no es normal; también se acompaña de trastornos de la coagulación. 9 ALTERACIONES NUCLEARES ADQUIRIDAS Hipersegmentación nuclear: son neutrófilos de cinco o más lóbulos, que aparecen en la anemia megaloblástica y en síndromes mielodisplásicos. Seudomaduración degenerativa: consiste en un asincronismo morfoestructural de maduración demostrado por: a) lobulación del núcleo; b) cromatina inmadura para ese grado de lobulación; y c) masa nuclear total francamente aumentada respecto de la citoplasmática. El hallazgo de estos elementos coincidente con la presencia de blastos permite clasificar la leucemia como mieloide. Neutrófilos pelgeroides: es un leucocito de núcleo bilobulado que acompaña a los elementos inmaduros de las leucemias mieloides sobre todo las agudas e infecciones graves ALTERACIONES NUCLEARES HEREDADAS Anomalía de Pelger-Huet: se transmite con carácter autosómico dominante, y consiste en la disminución o ausencia de segmentación nuclear en los neutrófilos. Las claves para identificarla son: a) núcleos esféricos, ovalados o bilobulados, b) heterocromatina muy densa, y c) la mayoría de las células tiene una apariencia similar. La cromatina de los núcleos Pelger-Huet se caracteriza por su concentración grosera formando masas que han determinado su designación de “núcleo en escarapela”. Los leucocitos de la malformación de Pelger-Huet conservan intacto su funcionalismo. Presenta una falsa desviación a la izquierda, pues los elementos no son inmaduros. Hipersegmentación de los neutrófilos de Undritz: de carácter autosómico dominante, no entraña patología. El 80% o más de los neutrófilos tiene 4 o 5 lóbulos. EJEMPLOS DE HISTOGRAMAS NEUTROFILIA 10 LINFOCITOSIS EOSINOFILIA BIBLIOGRAFIA Diagnóstico citológico de las hemopatías. Grignaschi. Ed. Panamericana. 1991. Dacie and Lewis Practical Haematology. Tenth edition. Churchill y Livingstone. 2006. Hematología Clínica de Wintrobe. R. Lee y colaboradores. Ed. Lea and Febiger. London. 1.993. Manual de técnicas de laboratorio en hematología. Vives J y Aguilar J. 2ª edición. Ed. Masson. 2006. Hematología. Fundamentos y Aplicaciones Clínicas. Rodak. 2ª edición. 2004. Informe automatización del hemograma: entre la ayuda, la confusión y la controversia. Carbia C, Fink N, Lazarowski A. XIX Congreso Argentino de Hematología. 2009. Manual de histogramas Sysmex. Autoanalizador hematológico KX-21/KX21N. Edición 2002.