- Ninguna Categoria
Nutrientes y Fisicoquímica en Tilapia (Oreochromis niloticus)
Anuncio
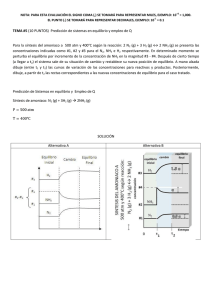
UNIVERSIDAD DEL MAR Campus Puerto Ángel ACUMULACIÓN DE NUTRIENTES Y PARÁMETROS FISICOQUÍMICOS DEL AGUA EN UN SISTEMA CERRADO DE TILAPIA (Oreochromis niloticus) Mayoral Noriega Denise E. Ing. En Acuicultura Quinto Semestre. 503 Puerto Ángel, Oaxaca, Oax. a 27 de Noviembre de 2009. INTRODUCCIÓN La calidad del agua está determinada por la hidrología, la fisicoquímica y la biología de la masa de agua a que se refiera. Las características hidrológicas son importantes ya que indican el origen, cantidad del agua y el tiempo de permanevncia, entre otros datos ("Calidad del agua." Microsoft® Student 2009 [DVD]. Microsoft Corporation, 2008). La cantidad y la temperatura también son importantes a la hora de analizar las causas que concurren para que el agua presente una calidad u otra. Lógicamente, para una cantidad de contaminantes dada, cuanto mayor sea la cantidad de agua receptora mayor será la dilución de los mismos, y la pérdida de calidad será menor. Por otra parte, la temperatura tiene relevancia, ya que los procesos de putrefacción y algunas reacciones químicas de degradación de residuos potencialmente tóxicos se pueden ver acelerados por el aumento de la temperatura ("Calidad del agua." Microsoft® Student 2009 [DVD]. Microsoft Corporation, 2008). Los parámetros más comúnmente utilizados para establecer la calidad de las aguas son los siguientes: oxígeno disuelto, pH, sólidos en suspensión, DBO (Demanda bioquímica de oxígeno), fósforo, nitratos, nitritos, amonio, amoníaco, compuestos fenólicos, hidrocarburos derivados del petróleo, cloro residual, cinc total y cobre soluble ("Calidad del agua." Microsoft® Student 2009 [DVD]. Microsoft Corporation, 2008). En el caso particular de la Tilapia, éstas realizan todas sus funciones con aguas que contengan temperaturas de 22 a 26°C durante la mayor parte del año y mínima de 18°C en el invierno (Morales Díaz, 1991). Toleran concentraciones de oxígeno disuelto entre 2 a 3 mg/L por periodos prolongados (Cuevas Fuentes y Delgado Vidal, 2007), para aguas cálidas deberá tener no menos de 5ppm (Morales Díaz, 1991). El pH está entre los rangos de 6.5 y 8.5, siendo el ideal de 7.5, el amonio debe ser menor a 0.1 ppm/l y nitritos menor a 4.6 mg/l(Morales Díaz, 1991). La mayoría de los organismos toleran cambios de pH dentro del intervalo de 6 a 9 que normalmente se presentan en ambientes acuáticos. Otra repercusión importante en la variación del pH en estanques de peces, está asociada a los niveles tóxicos del amoniaco (NH3), que en periodos cortos oscilan entre 0.6 y 2.0 mg/L y para efectos subletales entre 0.1 a 0.3 mg/L. un incremento de de una unidad de pH aumenta 10 veces el contenido de amonio no ionizado (amoniaco) (Martínez Córdova, 1998). El agua deberá contar con los elementos minerales necesarios como sales de calcio, nitrógeno, fósforo y potasio. Si éstas no están presentes, deben de adicionarse por medio de abonos o fertilizantes (Morales Díaz, 1991). Las actividades acuícolas que requieren adiciones de fertilizantes y alimentos, pueden llegar al sedimento del 10 al 30%, consecuencia de diferentes factores: comportamiento alimentario, estabilidad del alimento método de distribución y la frecuencia; a esta actividad hay que adicionarle también la producción fecal que puede representar hasta el 26% del alimento consumido y que puede llegar al sedimento (Martínez Córdova, 1998). Existen diversas formas nitrogenadas disueltas en el agua: a) orgánicas como aminoácidos, aminoazúcares de bajo peso molecular, hasta sustancias húmicas de diverso graso de refractabilidad; b) nitrógeno molecular (sólo asimilables para bacterias y algas cianofitas) y c) sales inorgánicas que predominan en concentración como amonio (NH4+), nitritos (NO2-) e incluso, bajo ciertos pH alcalinos, el amoniaco (NH3) (Martínez Córdova, 1998). La materia orgánica está constituida por proteínas y éstas a su vez por aminoácidos, que al descomponerse producen amoniaco (NH3) (el cual en el medio acuático reacciona y produce amonio (NH4)), proceso que se conoce como amonificación y que se lleva a cabo tanto en condiciones aeróbicas como en anaeróbicas. Este amonio (NH4) es asimilado por el fitoplancton y la macrovegetación directamente (sin cambio químico y gasto de energía) (Martínez Córdova, 1998). Amonificación CHON CO2 + H2O + NH3 NH3 + H NH4 + OH El amoniaco (NH3) y el amonio (NH4) se pueden encontrar simultáneamente ya que se establece una reacción de equilibrio que depende del pH, por arriba del 7.0 hay mayor contenido de amoniaco (NH3) y tiene efectos tóxicos, letales y subletales; en ambientes dulces con pH entre 6.5 y 7.5 representan menor riesgo que los salobres o marinos con pH de 7.0 a 8.5 (Martínez Córdova, 1998). En aguas naturales y bajo condiciones aeróbicas, el amonio (NH4) puede oxidarse a nitritos (NO2) o nitratos (NO3), proceso conocido como nitrificación; la última forma es preferencial por los productores primarios o fotosintetizadores en la asimilación biológica a pesar de que representa un gasto de energía para transformarla a amonio (NH4), que es utilizado para la elaboración de aminoácidos y proteínas. La reducción de nitrato (NO3) a nitrito (NO2), amonio (NH4) e incluso nitrógeno se define como desnitrificación y se lleva a cabo en condiciones de baja concentración de oxígeno (Martínez Córdova, 1998). Nitrificación N2 NH4 NO2 NO3 Desnitrificación OBJETIVO Comparar los nutrientes y parámetros fisicoquímicos del agua de un sistema abierto y uno cerrado. MATERIAL Y MÉTODO En el laboratorio de Acuicultura a las 8:30 de la mañana se alimentó a tilapias de dos estanques, los cuales fueron denominados uno el control y otro el experimental, siendo el control un sistema abierto, porque tenía recirculación de agua y el experimental un sistema cerrado, ya que no tenía recirculación de agua y se midieron los parámetros principales del agua, los cuales fueron: amoniaco, amonio, nitritos, nitratos, temperatura, unidades prácticas de salinidad, total de sólidos disueltos y oxígeno disuelto con un multiparámetro, después se realizaron mediciones de los mismos a las diez, once, doce, una y dos de la tarde, los cuales se registraron en una bitácora. RESULTADOS En las siguientes tablas se muestran las mediciones de cada uno de los parámetros de los estanques: Experimental Hora 08:30 10:00 11:00 12:00 13:00 14:00 NH3 0.15 0.01 0.01 0.01 0.01 0.01 NH4 2.47 0.87 1 0.96 0.97 0.92 Nitritos Nitratos 0.98 169.97 0.66 172.3 0.33 176.01 0.33 179.04 0.49 176.36 0.56 178.45 °T 27.1 27.1 27.2 27.2 27.2 27.3 UPS 0.87 0.88 0.88 0.88 0.88 0.88 TDS 1131 1131 1137.5 1137.5 1137.5 1137.5 OD 5.01 4.5 4.43 4.56 4.7 5.27 Tabla 1. Datos del estanque experimental Control Hora 08:30 10:00 11:00 12:00 13:00 14:00 NH3 0.13 0.01 0.01 0.01 0.01 0.01 NH4 2.29 0.84 0.9 0.86 0.85 0.81 Nitritos 0.66 0.49 0.66 0.33 0.49 0.32 Nitratos 167.32 174.2 175.3 174.2 180.55 173.15 °T 27.3 27.6 27.8 28.1 28.3 28.6 UPS 0.87 0.88 0.88 0.88 0.88 0.88 Tabla 2. Datos del estanque control TDS 1131 1131 1137.5 1137.5 1137.5 1137.5 OD 5.01 5.1 5.21 5.44 4.7 4.59 A continuación las gráficas obtenidas de cada uno de los parámetros de los estanques en las cuales el tiempo es la variable independiente y la variable dependiente cada uno de los parámetros: NH3 Hora Experimental Control 08:30 0.15 0.13 10:00 0.01 0.01 11:00 0.01 0.01 12:00 0.01 0.01 13:00 0.01 0.01 14:00 0.01 0.01 NH3 0,2 0,15 0,1 experimental control 0,05 0 08:30 10:00 11:00 12:00 13:00 14:00 -0,05 Tabla 3 y Gráfica 1. Amoniaco de los estanques. NH4 Hora Experimental Control 08:30 2.47 2.29 10:00 0.87 0.84 11:00 1 0.9 12:00 0.96 0.86 13:00 0.97 0.85 14:00 0.92 0.81 NH4 3 2,5 2 experimental 1,5 control 1 0,5 0 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 4 y Gráfica 2. Amonio de los estanques. NO2 Hora Experimental Control 08:30 0.98 0.66 10:00 0.66 0.49 11:00 0.33 0.66 12:00 0.33 0.33 13:00 0.49 0.49 14:00 0.56 0.32 NO2 1,2 1 0,8 0,6 experimental 0,4 control 0,2 0 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 5 y Gráfica 3. Nitritos de los estanques. NO3 NO3 Hora Experimental Control 08:30 169.97 167.32 185 10:00 172.3 174.2 180 11:00 176.01 175.3 12:00 179.04 174.2 13:00 176.36 180.55 170 14:00 178.45 173.15 165 175 experimental control 160 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 6 y Gráfica 4. Nitratos de los estanques. °T Hora Experimental Control 08:30 27.1 27.3 10:00 27.1 27.6 11:00 27.2 27.8 12:00 27.2 28.1 13:00 27.2 28.3 14:00 27.3 28.6 °T 29 28,5 28 experimental 27,5 control 27 26,5 26 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 7 y Gráfica 5. Temperaturas de los estanques. UPS Hora Experimental Control 08:30 0.87 0.87 10:00 0.88 0.88 11:00 0.88 0.88 12:00 0.88 0.88 13:00 0.88 0.88 14:00 0.88 0.88 UPS 0,882 0,88 0,878 0,876 0,874 0,872 0,87 0,868 0,866 0,864 experimental control 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 8 y Gráfica 6. Unidades Prácticas de Salinidad de los estanques. TDS TDS Hora Experimental Control 08:30 1131 1131 1138 10:00 1131 1131 1136 11:00 1137.5 1137.5 12:00 1137.5 1137.5 13:00 1137.5 1137.5 14:00 1137.5 1137.5 1134 1132 experimental 1130 control 1128 1126 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 9 y Gráfica 7. Total de sólidos disueltos de los estanques. OD OD Hora Experimental Control 08:30 5.01 5.01 6 10:00 4.5 5.1 5 11:00 4.43 5.21 4 12:00 4.56 5.44 3 experimental 13:00 4.7 4.7 control 14:00 5.27 4.59 2 1 0 08:30 10:00 11:00 12:00 13:00 14:00 Tabla 10 y Gráfica 8. Oxígeno disuelto de los estanques. DISCUSIONES Según Martínez Córdova: bajo condiciones de cultivo en los estanques, la fertilización inorgánica, el alimento no consumido, el plancton muerto y el excremento de los organismo en cultivo, constituyen material rico en Nitrógeno que se degrada rápidamente. El incremento de materia orgánica además de conducir a la anaerobiosis y a una mineralización incompleta con formación de ácidos orgánicos e inorgánicos, pueden generar las formas no ionizadas de nitrógeno o amoniaco NH3, tóxico para peces en un intervalo entre 0.6 y 2.0 mg/l; la tasa de liberación de amonio en estanques se ha estimado entre 2.6 a 3.3 veces, además de la liberación de sedimentos tóxicos no perturbados. El amoniaco se disuelve en el agua y reacciona para producir amonio: NH3 + H2O NH4 + OH y el pH del ambiente es responsable de las proporciones de las dos formas, cuando el pH decrece el cociente NH4 /NH3 se incrementa. Aunque se desconoce el mecanismo de la toxicosis del amoniaco, tiene efectos fisiológicos visibles en los peces como reducción en la excreción, incremento del pH en la sangre, inactivación de enzimas, afectación de la permeabilidad, daño a las agallas, incremento del consumo de O 2 por células y cambios histológicos en los riñones, bazo y tiroides, entre otros. En condiciones anóxicas o de bajo contenido de oxígeno, propiciadas por la fertilización o la adición de alimento que producen desnitrificación, la generación de NO2 puede ser significativa (con predominio selectivo entre Nitrobacter y Nitrosomonas) y ciertas condiciones de luminosidad, que se traducen en niveles tóxicos para los organismos en cultivo. Por lo que en la gráfica de amonio NH4, se observa que el estanque experimental hay más cantidad del mismo que en el control, por lo que al parecer el que el sistema no tenga una recirculación del agua hace que se produzca más amonio. De igual forma con el amoniaco NH3, ya que a la primera hora se cuantificó más en el estanque experimental que en el control, sin embargo en las siguientes mediciones se mantienen igual en ambos estanques. De la cantidad de amoniaco que haya en el agua se producirá amonio, por lo que al comparar ambas gráficas, en la primera (amoniaco) desciende la concentración y de igual forma en la segunda (amonio), por lo que se confirma que están correlacionadas. Y no se llegó a un nivel de toxicidad. En cuanto los nitritos y nitratos, debido a la nitrificación, los resultados del estanque control demuestran que la cantidad de amonio que hay, tienen una oscilación parecida con los dos anteriores. En el estanque experimental solo se dio una oscilación semejante entre el amonio y los nitritos, sin embargo con los nitratos no fue así ya que cuando disminuyeron la concentración de nitritos aumento la de los nitratos. Todo lo anterior está muy relacionado con la temperatura y el oxígeno disuelto, ya que son los dos factores de mayor importancia que se deben de controlar en un estanque de cultivo, así que al haber un aumento de temperatura, el oxígeno disminuye y esto se puedo ver en las gráficas ya que la temperatura fue aumentando y el oxígeno en el experimental fue disminuyendo y después volvió a subir, en cambio en el control debido a la circulación del agua primero subió y después bajo pero esto podría ser debido al lugar de donde se hacía la captación ya que era de un tinaco localizado en la azotea del laboratorio, además que dependiendo de la hora del día también aumenta la temperatura ambiental provocando que el agua del tinaco tenga una mayor temperatura. El total de sedimentos disueltos, se dio en aumento, debido a la alimentación de los organismos, que en sus heces liberan amoniaco. CONCLUSIONES Tanto en la columna de agua como en el sedimento, la materia orgánica requiere de oxígeno para su descomposición, debido a la penetración de este gas en el estanque, origina diferencias en las condiciones de óxido-reducción que a su vez influyen en la velocidad de descomposición y en la formación de compuestos refractarios, que favorecen la disolución de metales pesados con el incremento de toxicidad; lo que ponen en riesgo a los organismos en cultivo. Esto último es una buena razón para limpiar o acondicionar el fondo de los estanques acuícolas regularmente. La degradación de la materia orgánica en el sedimento es la fuente de energía biológica y química; este proceso consume oxígeno, por lo que se debe tener el control del oxígeno en un rango óptimo de acuerdo al organismo que se esté cultivando. Debido a que la dieta que se les proporciona a las tilapias de los estanques contienen proteínas, carbohidratos y grasas, los productos de desecho contienen carbono, nitrógeno orgánico, amonio, bicarbonato y fosfatos entre otros, que junto con las heces se hunden y llegan al sedimento. Por lo que la materia orgánica en el sedimento no sólo es fuente importante de nitrogenados y fosfarados, sino que su presencia acelera los cambios diagenéticos (formación de una roca a partir de sedimentos sueltos y sostiene a una población heterótrofa que a su vez es consumida por una comunidad béntica, contribuyente con sus excretas que contiene estos nutrientes y los difunde por su acción excavadora. Diversos autores han determinado un intervalo de 10 a 30% de alimento que no es consumido y se pierde, puede depositarse en el fondo y en consecuencia, permanecer hasta la cosecha de los organismos cultivados, con un incremento sustancial de nutrientes en el agua desalojada, e incluso en el sedimento (Martínez Córdova, 1998). REFERENCIAS Microsoft ® Encarta ® 2009. © 1993-2008 Microsoft Corporation. Reservados todos los derechos. Ecología de los Sistemas Acuícolas. Martínez Córdova, Luis R. 1998. AGT EDITOR, S.A. México. La Tilapia en México biología, cultivo y pesquerías. Morales Díaz, Armando. 1991. AGT EDITOR, S.A. México. http://www.sra.gob.mx/internet/informacion_general/programas/fondo_tierras/manu ales/Cultivo__tilapia_estanques__r_sticos.pdf
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados