5.- Razonar y justificar si el amoniaco se emplea como uno de los
Anuncio

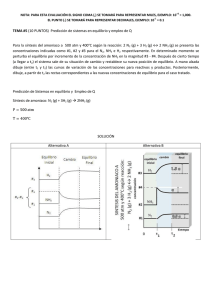
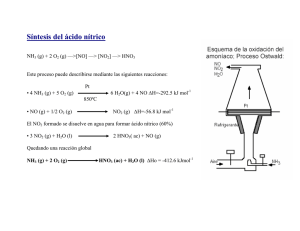
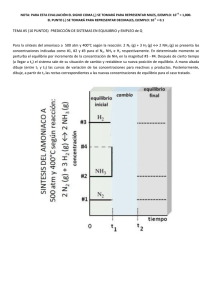
CASTILLA LEÓN / JUNIO 99. LOGSE / QUÍMICA / DESCRIPTIVA / OPCIÓN A / Nº 5 5.- Razonar y justificar si el amoniaco se emplea como uno de los reactivos a utilizar: a) En la industria de la obtención del ácido nítrico. b) En la obtención industrial de abonos para la agricultura. c) En la obtención de ácidos débiles previa disolución del mismo en agua. d) Como producto de limpieza. Solución. a) El amoniaco se utiliza en la obtención del ácido nítrico mediante la combinación del método de Haber y del método de Ostwald. El ácido nítrico se obtiene por la siguiente secuencia de reacciones: 500º C 800º C N2 + 3 H2 à 2 NH3 à NO + H2O Fe, Mg Pt, Rh O2 H2O NO à NO2 à N2O4 à HNO3 + HNO2 à NO + HNO3 b) El amoniaco se utiliza para fabricar fertilizantes ya que se puede transformar en el ión amonio NH4+ : NH3 + H+ à NH4+ Este ión puede ser asimilado por los vegetales que lo utilizan para formar sus proteínas. Así, como fertilizante se utiliza por ejemplo el fosfato amónico: NH4H2PO4 c) En disolución acuosa el amoniaco se comporta como base débil según el equilibrio: NH3 + H2O à NH4+ + OHEl ión amonio ( NH4+ ) , el ácido conjugado del amoniaco, es un ácido débil. d) El amoniaco se utiliza como producto de limpieza por su capacidad de autoionizarse: 2 NH3 ⇔ NH4+ + NH2Se trata de un disolvente ionizante no acuoso. Además, tiene poder bactericida y germicida. Sirve para limpiar la superficie ennegrecida de los metales, ya que es capaz de disolver las partículas de óxido, sulfuro o carbonato que están depositadas. Esto se debe a la capacidad del amoniaco para formar complejos de coordinación solubles en agua con muchos cationes metálicos. Por otra parte, una disolución acuosa amoniacal es una fuente de iones OH-, como ya hemos afirmado. Este ión transforma muchos compuestos orgánicos hidrófobos (aceites, grasas) en otros compuestos solubles en agua , y elimina las largas moléculas orgánicas apolares que poseen facilidad para adherir partículas de polvo. Finalmente, las disoluciones amoniacales se secan con cierta rapidez. www.profes.net es un servicio gratuito de Ediciones SM