Subido por
ANTONIO EMILIANO ARIAS CARRASCO
Examen Fisicoquímica: Lixiviación, Cementación y Remediación
Anuncio

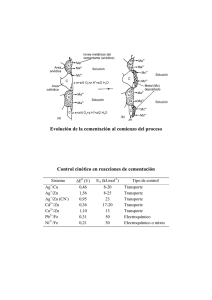
EXAMEN FINAL DE LABORATORIO GRUPO CALCITA CURSO: Fisicoquímica DOCENTE: Lovera Dávila, Daniel Florencio INTEGRANTES: Aguilar Duran, Jarol Andherson (21160057) Alferez Pacco, Jack Jhuller (21160070) Arias Carrasco, Antonio Emiliano (21160049) Baquerizo Revollar, Giovani Maicol (21160008) Masgo Flores, Vickler (21160011) 2022 BLOQUE TEÓRICO 1.- Explicar la base teórica de la Práctica de Lixiviación de minerales sulfurados de Zinc. Factores y variables que intervienen en la lixiviación La lixiviación es una operación extractiva primaria en el procesamiento hidrometalúrgico, mediante la cual un metal de interés se transfiere de minerales naturales a una solución acuosa, mediante una solución química activa conocida como solución de lixiviante. La lixiviación del zinc se realiza simultáneamente a la oxidación y la neutralización de forma que se pueda precipitar el hierro con el que coprecipitan impurezas como el As, Sb y Ge. También se coprecipitan sílice coloidal e hidróxido de aluminio. Esta precipitación de Fe3+ se efectúa actualmente haciendo uso de las precipitaciones jarosítica, goetítica o hematítica. 2.-Escriba las reacciones Redox de la Cementación de soluciones lixiviadas de Cobre. La cementación es un proceso de precipitación química que permite retirar iones en solución agregando un reactivo precipitante. En el caso de iones metálicos disueltos la reacción se favorece agregando un metal más activo, según la serie electroquímica, como reactivo para formar un precipitado conocido como cemento. Este proceso es aplica en el tratamiento de efluentes de operaciones metalúrgicas Reacciones de Cementación Mostramos las siguientes reacciones de cementación en el sistema Sulfatante: ● ● ● El cemento de cobre de alta calidad tiene la ventaja de oxidarse rápidamente, mediante la formación de una película de óxido de cobre en la superficie, favorable para su disolución en medio ácido. La presencia de iones Fe++ y aire producen iones Fe+++ que ayudan a disolver el cobre metálico La cinética de lixiviación de Cu° es incrementada sustancialmente con el aumento de temperatura. 3.- Escriba la Ecuación cinética de Cristalización del NiSO4.7H2O. 4.- Explicar el fundamento teórico de la Electrodeposición de soluciones lixiviadas. Antes de comenzar, se dará una breve definición de soluciones lixiviantes, la cual los lixiviantes son soluciones químicas utilizadas en la extracción de lixiviación para mejorar la disolución de metales en minerales. La electrodeposición de un metal se basa en la electrólisis de soluciones acuosas o sales fundidas con ánodos insolubles. Mayoritariamente se realiza en una solución acuosa de los sulfatos de un metal en ácido sulfúrico, para así evitar la deposición de los hidróxidos del metal. Debido a un precio relativamente bajo, se selecciona el ácido sulfúrico. Las reacciones básicas durante la electrodeposición de soluciones acuosas son: - La deposición del metal deseado en el cátodo - La evolución del oxígeno en el ánodo Desde que el oxígeno se desprende en el ánodo, la concentración de los iones metálicos disminuye y la acidez del electrolito aumenta, lo cual puede originar una evolución del hidrógeno junto con la deposición del metal en el cátodo. 5.- Explique la remediación de efluentes de minas (DAM y RAM). DAM Para el proceso de remedición de drenaje ácido se usan Carbonato de Calcio (CaCo3) de aserrín, arena gruesa y estiércol de cuy. El drenaje ácido de la mina constituye una fuente de contaminación de aguas superficiales y subterráneas. Para el tratamiento del drenaje ácido de mina, existen métodos activos y pasivos, estos últimos comprenden los humedales artificiales, los cuales vienen siendo usados en países industrializados, obteniéndose resultados interesantes. RAM La resistencia a los antimicrobianos es una amenaza cada vez mayor para la salud y requiere medidas por parte de todos los sectores tanto del gobierno como de la sociedad, es por ello que como métodos para remediar se debe de reforzar la investigación; optimizar el uso de medicamentos antimicrobianos; y asegurar que se realicen inversiones sostenibles en la lucha contra la resistencia a los antimicrobianos BLOQUE EXPERIMENTAL 1.- Comentar la Participación de Ingeniería Geológica en la Feria de CIENTEC 2022. La feria realizada por CIENTEC 2022, fue un evento muy interesante debido a la aglomeración de personas de diferentes países para hacer un reconocimiento de un nuevo proyecto, como a su vez también para la escuela de Ingeniería Geológica debido a que recientemente se estaba realizando una investigación al respecto sobre los Humedales de Puerto viejo. Dentro ya del evento, los encargados de la divulgación, la exposición de la investigación realizada fue muy buena y reconocida por la personas que tenían el interés de escucharlas y conocerlas, es por ello que la ganadora a mejor trabajo de investigación se la llevó nuestra escuela. 2.- Escriba los datos experimentales de la Cementación de soluciones de Sulfato de Cobre pentahidratado. Tiempo (min) Altura (cm) Voltaje inicial (V) 0 0 -66 5 7,3 -29,4 10 7,4 -40 15 7,2 -54 20 7,2 -68,3 25 7,3 -17 30 7,1 -34,2 35 7,3 -45,6 40 6,8 -75 3.- Mostrar el procesamiento de los datos experimentales de la Lixiviación de minerales sulfurados. 1. 2. 3. 4. 5. 6. 7. Se utiliza 500mL de agua clorurada en un matraz de la misma cantidad, se acidifica con HCl a un pH de 1.5 Se da una agitación de la solución lixiviante durante unos 30 min a temperatura ambiente. Se pesa 5 gr de mineral sulfurado de cobre. Se agrega a la solución lixiviante y se empieza a contar el tiempo de reacción. Sacar muestras cada 15 min, hasta obtener 6 muestras. Se filtran las soluciones muestreadas (3ml). Repetir los pasos anteriores para 30, 40, 60 y 70 °C. 4.- Explicar la Visita de Campo con su grupo de investigación del Humedal de Puerto Viejo. El grupo Calcita se dedicó al sector de estudio denominado "Formación de los humedales de Puerto Viejo" por lo que nos dividimos en diferentes partes. En primer lugar hicimos un pre campo determinando las formaciones geológicas del lugar e información de anteriores estudios en la zona. En segundo lugar de forma presencial se hizo la visita a los humedales junto a mis compañeros de grupo por lo que esperamos a ver si realmente coincidía con el área y perímetro del lugar. En tercer lugar observamos la geología de la zona junto con muestras de mano para saber en qué tipo de suelo y sobre qué tipo de roca está ubicado los humedales de Puerto Viejo. 5.- Comentar la velocidad de cristalización del sulfato de cobre pentahidratado. Velocidad de cristalización:Solo puede ocurrir en soluciones sobresaturadas. Este factor es crítico porque las diferencias en la velocidad hacen que los cristales adopten diferentes formas y estructuras. Por ejemplo, en la región inestable, la nucleación ocurre debido a varios factores, como la fricción, lo que da como resultado una nucleación secundaria, lo que significa que los cristales ya formados se destruyen. En cuanto al enfriamiento es a partir de La temperatura de cristalización es de 70 °C y la solución se enfría. Según el estudio, la tasa de cristalización del sulfato de cobre pentahidratado se mide y analiza en función de la temperatura de evaporación de 70 °C. BLOQUE ANALÍTICO 1.- Explicar y mostrar los cálculos de los datos experimentales de lixiviación de minerales sulfurados. Cálculo de cementación: Trabajo a unos 20°C Gráfica de concentración y tiempo 2.- Mostrar los gráficos de la práctica de cementación de la solución de sulfato de cobre. fig.1 Cementación del cobre fig.2 Cinética de Cementación del Cobre y otros Iones presentes sin agitación fig.3 Efectos de la temperatura en la cinética de cementación Cu(+2) fig.4 Efecto de la agitación en la cinética de cementación Cu(+2) fig.5 Efectos del pH con el tiempo de cementación Cu(+2) fig.6 Simulación de la cementación a diversas temperaturas fig.6 Recuperación de Iones Cu en Lixiviación 3.- Explicar con fotos toda la secuencia de la práctica de Cristalización de soluciones de CuSO4.5H2O. 1. Pesar 1.4 g del mineral sulfurado, para su posterior uso. 2. Agregar 10 ml de agua a la probeta, para su posterior mezcla con el mineral. 3. Luego de haber realizado los pasos anteriores, realizar la mezcla de ambos tal como se muestra en la figura adjunta. 4. Colocar la probeta en un baño maría, en la cual con el pasar de los minutos se cambiara un poco su tonalidad. 5. Extracción de las muestras durante los tiempos considerados en el proceso de 10, 20, 30 y 40 minutos para hallar su variación de ph. 6. Finalmente, se observa cómo poco a poco se va cristalizando hasta volverse más sólido . 4.- Mostrar las gráficas de simulación de los resultados a distintas condiciones en la remediación de efluentes de mina. 5.- Explicar el cuestionario referido a la Remediación de Pulpas Metalúrgicas. 1.- Encontrar la ecuación de sedimentación de los datos experimentales obtenidos. Las siguientes gráficas están en función a dos variables: la altura en cm (ubicada en el eje X) y el tiempo de sedimentación en minutos (ubicado en el eje Y). Con dichas variables se puede hallar la velocidad de sedimentación (Vs). Cabe aclarar que se usó un floculante (sustancia química que precipita sólidos) para constatar la variación de las gráficas cuando se aplicaba y cuando no.