Regla de Fases: Reporte de Laboratorio de Fisicoquímica
Anuncio

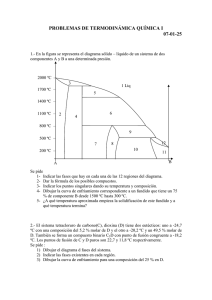
Universidad Nacional Mayor de San Marcos Facultad de Química e Ingeniería Química Reporte Nº 4 : Regla de fases Grupo 5 Escuela de Ingeniería Química Alumnos: Becerra Alarcon, Osias Alonso - 21070064 De la Cruz Escalante, Smith Antony - 21070091 Duran Bustamante, Anthony Bryan - 21070074 Huaman Yrigoin, Franz Cristopher - 21070146 Profesor Giraldo Acero, Yovani Curso Laboratorio de Fisicoquímica II 2022 TABLA DE CONTENIDO RESUMEN 3 1. INTRODUCCIÓN 4 2. OBJETIVOS 5 3. PARTE TEÓRICA 6 4. PARTE EXPERIMENTAL 9 5. TABLA DE DATOS 16 6. CÁLCULOS Y GRÁFICOS 20 7. TABLA DE RESULTADOS 26 8. DISCUSIÓN DE RESULTADOS 27 9. CONCLUSIONES 28 10. CUESTIONARIO 29 11. REFERENCIAS 30 12. ANEXOS 31 RESUMEN En el presente informe tiene como objetivo determinar experimentalmente el diagrama de fases y la curva de enfriamiento de una mezcla binaria cuyos componentes no son miscibles en estado sólido, pero sí en estado líquido. Por lo cual, para alcanzar un mejor resultado la práctica de laboratorio se dividió en dos partes, donde en la primera se tuvo que determinar las temperaturas de cristalización experimental para cada muestra en ocho tubos diferentes y con los datos obtenidos realizar el diagrama de fases. De manera similar, se realizó para la segunda parte, puesto que se tuvo que calcular la temperatura mediante un intervalo de diez segundos para luego determinar las curvas de enfriamiento para la mezcla binaria y un compuesto puro con los datos obtenidos. Asimismo, se pudo comprobar en el diagrama de fases que el punto eutéctico va depender tanto de la temperatura y de la composición de las sustancias. 3 1. INTRODUCCIÓN Los diagramas de fases representan un equilibrio termodinámico de un determinado sistema permitiendo predecir todas las fases presentes junto a sus propiedades, por lo cual resultan ser de suma importancia en el campo de la ingeniería, ya que a partir de la manipulación y procesamiento de materiales se puede relacionar los procesos de obtención con las propiedades de diseño, con el objetivo de optimizar estos procesos para la adquisición de un producto deseado. Durante las aplicaciones que se le pueda brindar a los diagramas de fase posibilitan determinar la solubilidad en un estado sólido y en equilibrio de una sustancia en otra. Por otro lado, también facilita conocer las fases que se encuentran presentes a diferentes composiciones y temperaturas bajo condiciones de enfriamiento lento. De esta manera, los diagramas de equilibrio de fases son ampliamente utilizados porque facilitan entender como tal el comportamiento de un sistema en equilibrio, evidenciándose ello en el control de la operación de diversos procesos, como el de cristalización o el mismo diseño de estos. Al mismo tiempo, son de gran aporte en los estudios de solidificación, microestructura, metalúrgica física y en el diseño de nuevos materiales. Por tal razón, también son muy empleados en el campo de la ingeniería, debido a que proporcionan los materiales necesarios en la composición de máquinas u objetos a partir de distintas materias primas. 4 2. OBJETIVOS 2.1. Objetivos generales ➢ Determinar experimentalmente el diagrama de fases y la curva de enfriamiento de una mezcla binaria. 2.2. Objetivos específicos ➢ Distinguir el equilibrio entre las diferentes fases. ➢ Interpretar el diagrama de fases a partir de su temperatura obtenida. 5 3. PARTE TEÓRICA Fase. Porción de un sistema que es macroscópicamente homogéneo en cuanto a sus propiedades fisicoquímicas , es decir, son cada una de las “capas” o “superficies” que se pueden distinguir dentro de un sistema material; además de encontrarse separada de otras porciones similares por regiones límites bien definidas, llamadas interfases. Por otro lado, en el ámbito fisicoquímico el término fase es simbolizado por la letra P. Componente. Es el número mínimo de especies químicas y variables independientes necesarias para describir la composición de cada fase; asimismo, el término en mención se simboliza se forma fisicoquímica por la letra C. Figura 1. Ejemplo de fases y componentes. Nota. Imagen tomada de http://nosotrosyciencia.blogspot.com/2011/10/fases-y-componentes-de-un-sistema.html 6 Grados de libertad. Es el número de parámetros termodinámicos que se pueden variar o cambiar sin generar una alteración en el número de fases del sistema; se simboliza de forma fisicoquímica por la letra F. Regla de fases. Es una relación que describe el número de grados de libertad (F) en términos del número de fases separadas (P) y el número de componentes (C) del sistema; teniendo en consideración que la regla en mención solo aplica a estados de equilibrio de un determinado sistema el cual debe encontrarse en equilibrio homogéneo en cada fase por la cual este compuesto el sistema, además de presentar un equilibrio heterogéneo entre las fases coexistentes. F=C–P+2 Diagrama de fases. Diagrama en el que se muestran las fases estables en función de dos variables, normalmente la composición y la temperatura. Se construyen para enfriamientos muy lentos, por lo tanto, nos indicará las fases de equilibrio cuando se somete a una aleación del diagrama de fases a un enfriamiento muy lento. Si se realiza un enfriamiento rápido, puede ser necesario recurrir a otra serie de diagramas en que aparecen fases de no equilibrio, es decir fases metaestables, cuya tendencia a formar las fases estables para lo que se requerirá un cierto tiempo. 7 Figura 2. Diagrama de fases Nota. Imagen adaptada de https://www.cartagena99.com/recursos/alumnos/apuntes/Manual%20Tema%208%20Diagram as%20de%20fase%20FORMATO2.pdf 8 4. PARTE EXPERIMENTAL MATERIALES ➢ 8 tubos de prueba grandes Figura 3. Tubos de prueba Nota. Imagen tomada de https://tecfresh.com/producto/tubo-de-ensayo-de-vidrio-13-x-100mm-con-tapa-rosca-cja-x-2 50-1230-100t/ 9 ➢ Agitador metálico pequeño y grande Figura 4. Agitador metálico de laboratorio Nota. Imagen tomada de https://tecfresh.com/producto/tubo-de-ensayo-de-vidrio-13-x-100mm-con-tapa-rosca-cja-x-2 50-1230-100t/ ➢ Termómetro de -10 a 110°C Figura 5. Termómetro digital Nota. Imagen tomada de https://mspinstruments.com/product/termometro-digital/ 10 ➢ Vasos de 400 y 600 mL Figura 6. Vasos de precipitado Nota. Imagen tomada de https://www.labolan.es/es/producto/vaso-precipitado-forma-baja-simax-600ml-90x125mm-c10uds.html ➢ Cocina electrica Figura 7. Cocina calefactora Nota. Imagen tomada de https://www.alquimialab.com/cocinilla-calefactora-multiusos/ 11 REACTIVOS ➢ Naftaleno QP Figura 8. Bolas de naftaleno Nota. Imagen tomada de https://www.freepik.es/fotos-premium/bolas-naftalina-naftaleno-sobre-fondo-amarillo_16436 915.htm 12 ➢ p-diclorobenceno QP Figura 9. p-diclorobenceno sólido Nota. Imagen tomada de https://es.made-in-china.com/co_huaronggroup/product_Paradichlorobenzene-P-Dichloroben zene-Santochlor_erggyggeg.html 13 4.1. a) Determinación del diagrama de fases Prepare el montaje que se observa en la siguiente imagen. Figura 10. Montaje para la regla de fases Nota. Elaboración propia. b) En el vaso de 600 mL, caliente agua de caño hasta cerca de la temperatura de ebullición (95 – 96° C). c) Sumerja los tubos numerados de dos en dos, comenzando por los de mayor temperatura de fusión (ver Tabla 1) para fundir las muestras. Destape ligeramente los tubos, sin retirarles los tapones de corcho. d) En el vaso de 400 mL, caliente agua de caño hasta unos 3° C por encima de la temperatura de cristalización aproximada, más alta de su set. e) Cambie el tubo de temperatura de fusión más alto al vaso de 400 mL, coloque dentro del tubo el agitador pequeño y el termómetro. Dentro del baño coloque el agitador 14 grande y otro termómetro (Figura 10.3). La muestra y el baño de agua no deben diferir en más de 2 – 3° C. f) Dejar enfriar lentamente la muestra agitándose al igual que el baño exterior hasta obtener la temperatura de cristalización, la cual reconocerá por la aparición de un escarchado en el interior del tubo. g) Repita los pasos e) y f), con las muestras restantes de su set en orden decreciente de temperaturas de cristalización. h) No lave los tubos al terminar la práctica y déjelos con sus tapones correctamente numerados. 4.2. Determinación de las curvas de enfriamiento a) Seleccione un tubo que contenga un solo componente (1 u 8). b) Elija una temperatura inicial mayor en 3 – 5° C a la de solidificación observada, y tome datos de temperatura cada 10 segundos, diferentes a los de cristalización. c) Repita a) y b) en una muestra de dos componentes. 15 5. TABLA DE DATOS Tabla 1 Condiciones de laboratorio P (mmHg) 759 mmHg T (°C) 20°C HR (%) 94% Nota. Elaboración propia Tabla 2 Datos teóricos de las muestras. Punto de fusión Muestras Masa molecular C10H8 (A) 128.1705 80 p-C6H4Cl2 (B) 147.01 53 Nota. Elaboración propia 16 teórico (°C) Tabla 3 Temperatura de cristalización experimental del Sistema C10H8 (A); p-C6H4Cl2 (B) Tubo N° C10H8 (A) (g) p-C6H4Cl2 (B) (g) Temp. Crist. (ºC) aproximada Temp. Crist. (ºC ) Experimental 1 0 15 52-56 52 2 1,5 12,5 45-49 46 3 2,5 12,5 41-45 44 4 6 12,5 30-34 31 5 10 10 46-50 47 6 12,5 7 56-60 58 7 15 3 70-74 72 8 15 0 78-82 79 Nota. Elaboración propia 17 Tabla 4 Variación de temperatura de la muestra pura (tubo 1) con respecto al tiempo. Tubo N°1 Tiempo (s) Temperatura (°C) Tiempo (s) Temperatura (°C) 0 57 90 54 10 56 100 53 20 55 110 53 30 54 120 53 40 54 130 53 50 54 140 53 60 54 150 53 70 54 160 53 80 54 170 53 Nota. Elaboración propia 18 Tabla 5 Variación de temperatura de la muestra mixta (tubo 2) con respecto al tiempo. Tubo N°2 Tiempo (s) Temperatura (°C) Tiempo (s) Temperatura (°C) 0 51 130 48 10 50 140 48 20 50 150 47 30 50 160 47 40 50 170 47 50 49 180 47 60 49 190 46 70 49 200 46 80 49 210 46 90 48 220 46 100 48 230 46 110 48 240 46 120 48 250 46 19 6. CÁLCULOS Y GRÁFICOS a) Mediante la composición de cada una de las muestras (Tabla 3), calcule la fracción molar experimental de cada componente en cada mezcla. Se siguen los cálculos hasta el tubo N°4, los resultados obtenidos se observarán en la Tabla N°6 de resultados. 20 b) Con los datos de a) y de 4.1, construya el diagrama de fases. Analícelo. Figura N°11 Diagrama de fases de un sistema binario (naftaleno / p-diclorobenceno) Nota. Elaboración propia. Análisis de la gráfica: Al mezclarse el naftaleno y el p-diclorobenceno, cambia el punto de fusión y el equilibrio entre las fases. En la gráfica se observan 4 regiones que están divididas por el punto eutéctico. En la parte superior del punto eutéctico se observa que los compuestos están en fase líquida, en la superior izquierda una composición de naftaleno sólido y p-diclorobenceno líquido, en la parte superior derecha se tiene al componente p-diclorobenceno sólido y naftaleno líquido y, finalmente, se tiene en la parte inferior una composición de naftaleno y p-diclorobenceno en estado sólido. 21 c) Construya las curvas de enfriamiento del componente puro y de la mezcla elegida. La elaboración de esta gráfica fue en base a los datos de la Tabla N°4 con respecto a el p-diclorobenceno puro durante un tiempo determinado Figura N°12 Curva de enfriamiento del componente puro (p-diclorobenceno) Nota. Elaboración propia 22 La elaboración de esta gráfica fue en base a los datos de la Tabla N°5 con respecto a el tubo 4 puro durante un tiempo determinado Figura N°13 Curva de enfriamiento del la mezcla (naftaleno - p-diclorobenceno) Nota. Elaboración propia. 23 d) Del diagrama de fases, determine el punto eutéctico, igualmente determine la temperatura y composición de dicho punto. Figura 14. Punto eutéctico, temperatura y composición. Nota. Elaboración propia. En la gráfica mostrada anteriormente, se observa qué el punto eutéctico posee una temperatura de 31°C <> 304.15 K, una fracción molar de p-diclorobenceno y naftaleno de 0.645 y 0.355 respectivamente. 24 e) Mediante la Ec. (10.7), calcule la solubilidad del naftaleno (fracción molar teórica en la mezcla), para el rango de temperaturas observadas, entre el punto de cristalización del naftaleno y el punto eutéctico. ❖ Para T=79 ºC=352,15K ❖ Para T=72 ºC=345,15K ❖ Para T=58 ºC=345,15K f) Repita el cálculo anterior para el p-diclorobenceno, en el rango de temperaturas desde su punto de cristalización hasta el punto eutéctico, mediante la Ec. (10.6). ❖ Para T=52 ºC=325,15K 25 ❖ Para T=46 ºC=319,15K ❖ Para T=44 ºC=317,15K ❖ Para T=31 ºC=304,15K g) Calcule el calor latente de fusión de los componentes puros en sus puntos de fusión observados. Calcule también los valores teóricos correspondientes. ❖ Para 𝐶10𝐻8 Para T=79 ºC=352,15K (experimental) Para T=80 ºC=353,15K (teórico) ❖ Para p-diclorobenceno 26 Para T=52 ºC=325,15K (experimental) Para T=54 ºC=327,15K (teórico) h) Determine el número de grados de libertad en el punto eutéctico usando las ecuaciones (10.1) ó (10.2). i) Compare los valores teóricos con los experimentales. % 𝑒𝑟𝑟𝑜𝑟 = ( 𝑉𝑎𝑙𝑜𝑟𝑇𝑒ó𝑟𝑖𝑐𝑜 − 𝑉𝑎𝑙𝑜𝑟𝐸𝑥𝑝. 𝑉𝑎𝑙𝑜𝑟𝑇𝑒ó𝑟𝑖𝑐𝑜 ) 𝑥 100% ❖ Para el Naftaleno: % 𝑒𝑟𝑟𝑜𝑟 = ( 4630.99 − 4629.41 4630.99 ) 𝑥 100% % 𝑒𝑟𝑟𝑜𝑟 = 0.03% ❖ Para el Diclorobenceno: 27 % 𝑒𝑟𝑟𝑜𝑟 = ( 4353.20 − 4362.18 4353.20 ) 𝑥 100% % 𝑒𝑟𝑟𝑜𝑟 = 0.02% 28 7. TABLA DE RESULTADOS Tabla 6 Fracción molar de los tubos de ensayo Fracción Tubo N° C10H8 p-C6H4Cl2 molar exp del C10H8 Fracción molar exp del p-C6H4Cl2 Temp. Temp. Crist. (ºC) Crist. (ºC) aprox. exp. 1 0 15 0,000 1,000 52-56 52 2 1.5 12.5 0,121 0,879 45-49 46 3 2.5 12.5 0,187 0,813 41-45 44 4 6 12.5 0,355 0,645 30-34 31 5 12 10 0,534 0,466 46-50 47 6 12.5 7 0,672 0,328 56-60 58 7 15 3 0,852 0,148 70-74 72 8 15 0 0,852 0,000 78-82 79 Nota. Elaboración propia Tabla 7 Datos del punto eutéctico Fracción molar del Fracción molar del Temperatura del naftaleno p-diclorobenceno punto eutéctico (°C) 0.355 0.645 31°C Nota. Elaboración propia 29 Tabla 8 Calor latente de fusión de los componentes puros con su respectivo error porcentual. Componentes Calor latente Calor latente Pto. fusión Pto. fusión teórico de experimental teórico experimental fusión de fusión (cal/mol) (cal/mol) C10H8 353.15 K 79 4630,99 4629,41 p-C6H4Cl2 326.15 K 52 4353,20 4362,18 Nota. Elaboración propia Tabla 9 Error porcentual del punto de fusión y calor latente de fusión de los componentes. % Error Pto. de fusión Calor latente de fusión C10H8 1,25% 0,03% p-C6H4Cl2 3,7% 0,02% Nota. Elaboración propia Tabla 10 Error porcentual del punto de fusión y calor latente de fusión de los componentes. Compuesto % Error C10H8 0.03% p-C6H4Cl2 0.02% Nota. Elaboración propia 30 8. DISCUSIÓN DE RESULTADOS El elaborar el diagrama de fases con las temperaturas halladas para cada fracción molar de los compuestos otorgó información y comportamiento importante al mezclarse los dos compuestos estudiados, con el gráfico realizado se determina el punto eutéctico de la mezcla y este determina las fases que se observan en el gráfico. Con respecto al punto eutéctico; se nota que dicho punto no corresponde a ninguna fase como tal, sino que se trata de una mezcla de tres fases conformada por naftaleno sólido, p-diclorobenceno sólido y solución líquida que contenía una fracción molar igual a 0.355 de naftaleno, mientras que el p-diclorobenceno poseía una fracción molar igual a 0.645. Haciendo un análisis en el punto eutéctico, se llegó a un valor de cero referido al número de grados de libertad, esto debido a que dicho punto se encuentra en equilibrio entre tres fases; además que por otro lado el punto de solidificación depende de la composición de la mezcla. Mediante la curva de enfriamiento de mezcla de composición definida, es posible obtener el punto de solidificación así como su temperatura eutéctica. Con respecto a los grados de libertad; mientras más grande es el número de componentes del sistema, mayor es el número de grados de libertad. Asimismo, cuanto más grande es el número de fases, menor es el número de grados de libertad. Finalmente, con respecto al porcentaje de error se notaron valores muy bajos que no llegaban ni al 1%; a excepción de los valores de punto de fusión del naftaleno y del p-diclorobenceno los cuales tuvieron resultados de 1.25% y 3.7%, esto podría deberse a un deficiente control de las temperaturas tomadas en pequeños intervalos de tiempo, o problemas en los equipos de medición, principalmente el termómetro. 31 9. CONCLUSIONES ● Se pudo observar que mientras mayor sea el número de componentes en un sistema, mayor será el número de grados de libertad; asimismo, cuando más grande sea el número de fases habrá un menor número de grados de libertad. ● Al obtener los datos de las variaciones de temperatura con dos compuestos cuya fracción molar varía se realizó el diagrama de fases respectivo y con ello, determinar el punto eutéctico de esta mezcla. Este punto eutéctico se encuentra a una temperatura de 31°C con las fracciones molares del naftaleno y p-diclorobenceno son 0.355 y 0.645 respectivamente. ● Se pudo comprobar que el punto eutéctico depende tanto de la temperatura y de la composición de las sustancias. Además, de que el sólido depositado en la parte inferior del tubo es una mezcla heterogénea constituida por microcristales de cada compuesto. ● El tiempo necesario para que la temperatura sea constante en una curva de enfriamiento va depender de la composición de la mezcla, por lo que si dicha composición está más próxima a la composición eutéctica, el tiempo será mucho mayor. 32 10. CUESTIONARIO 1) ¿Que es un diagrama de fases? ¿Cuál es su importancia? Los diagramas de fase son gráficos que proporcionan información acerca de las condiciones de P y T en las cuales una sustancia puede existir en alguna de sus tres fases, sólido, líquido o gas. Todo diagrama de fases presenta las siguientes características: ● Es un diagrama presión vs temperatura. ● Presenta un punto triple, A, donde las tres fases sólido, líquido y gas se encuentran en equilibrio. ● Presenta un punto crítico, B, que es el extremo de la curva de presión de vapor. La temperatura en este punto se llama temperatura crítica y la presión se denomina presión crítica. A temperaturas mayores a la temperatura crítica una sustancia no se puede licuar (pasar de gas a líquido), independientemente de lo elevada que sea la presión. El aspecto general del diagrama de fases es el siguiente: 33 Los diagramas de fase permiten predecir los cambios presentes en el punto de fusión, punto de ebullición y punto de sublimación de una sustancia debido a sus variaciones de la presión externa. 2) ¿Qué entiende usted por un sistema de punto eutéctico simple? El punto eutéctico es un punto el cual se encuentra dentro del diagrama de fases de una mezcla binaria, el cual se encuentra definido por una temperatura y composición determinadas. Gracias a este punto se puede apreciar que la fase líquida solidifica, generando 2 fases sólidas que están en composiciones diferentes. 3) En un diagrama de punto eutéctico simple, explique la aplicación de la regla de la palanca. Se tiene el siguiente diagrama de fases Se puede apreciar que faltan 3 puntos, solubilidad a temperatura ambiente de A en B, solubilidad a la temperatura eutéctica de A en B y la composición del punto eutéctico. Para determinar la composición del eutéctico se debe aplicar la regla de la palanca sabiendo que la aleación de un contenido del 30% de B contiene un 75% de fase sólida a 401ºC, es decir de fase alfa proeutectica y por tanto lo tanto se sabe 100-75=25% de liquido a 401ºC, 34 por tanto para obtener la composición del eutéctico podemos aplicar la regla de la palanca con el contenido de sólido alfa a 401ºC. 35 11. REFERENCIAS ● Chang, R. (2005). Química. Colombia: McGraw-Hill ● De Paula, A. (2006) Química física. Editorial médica panamericana https://www.academia.edu/31503242/Quimica_Fisica_Atkins_and_de_Paula_8va_Edi cion_Español ● Dingrando, L. et al. (2003) Química Materia y Cambio. Colombia: McGraw-Hill. ● García, H.; Irazoque, G. y Talanquer, V. (1996). Introducción a la Física y a la Química. México: Fondo de Cultura Económica. ● Levine, I. (2004) Fisicoquímica. Mc Grall Hill https://www.academia.edu/28151329/_FQ_Levine_Fisicoquímica_Vol_1_5ta_Ed 36 12. ANEXOS Hoja de seguridad del Naftaleno 37 38 39 40 41 42 43 44 Hoja de seguridad del diclorobenceno 45 46 47 48 49 50 51