LIPIDOS LAS BIOMOLECULAS DE LA VIDA : Bioquímica
Anuncio

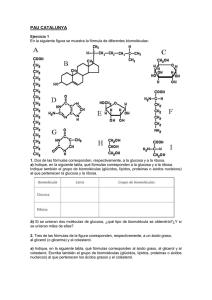
UNIVERSIDAD MAYOR DE SAN SIMÓN FACULTAD DE MEDICINA “AURELIO MELEAN” PROGRAMA DE LICENCIATURA EN NUTRICIÓN Y DIETÉTICA LAS BIOMOLECULAS DE LA VIDA LIPIDOS ASIGNATURA: Bioquímica DOCENTE: Dra. Miriam Rosario Arnez Camacho INTEGRANTES: Coca Callejas Maricel Flores Illanes Tahiz Shahuri Macias Fernández Natalia Torrico Aguilar Maria Selene Villarroel Sarmiento Carlos COCHABAMBA-BOLIVIA OCTUBRE 2013 LAS BIOMOLECULAS DE LA VIDA LIPIDOS 1. DEFINICIÓN Los lípidos son biomoléculas orgánicas formadas básicamente por carbono e hidrógeno y generalmente también oxígeno; pero en porcentajes mucho más bajos. Además pueden contener también fósforo, nitrógeno y azufre, como se observa en las siguientes estructuras (Figura 1). Figura 1. 2. CARACTERÍSTICAS Entre ellas se indican que son: Insolubles en agua Solubles en disolventes orgánicos, como éter, cloroformo, benceno, etc. Hidrofobicidad. La baja solubilidad de los lípidos se debe a que su estructura química es fundamentalmente hidrocarbonada (alifática, alicíclica o aromática), con gran cantidad de enlaces C-H y C-C) en un 100% covalente y su momento dipolar es mínimo. El agua, al ser una molécula muy polar, con gran facilidad para formar puentes de hidrógeno, no es capaz de interaccionar con estas moléculas. En presencia de moléculas lipídicas, el agua adopta en torno a ellas una estructura muy ordenada que maximiza las interacciones entre las propias moléculas de agua, forzando a la molécula hidrofóbica al interior de una estructura en forma de jaula, que también reduce la movilidad del lípido como se puede notar en Figura 2. Todo ello supone una configuración de baja entropía, que resulta energéticamente desfavorable. Esta disminución de entropía es mínima si las moléculas lipídicas se agregan entre sí, e interaccionan mediante fuerzas de corto alcance, como las fuerzas de Van der Waals. Este fenómeno recibe el nombre de efecto hidrofóbico. Figura 2. En presencia de moléculas lipídicas, el agua adopta en torno a ellas una estructura muy ordenada, en forma de jaula, reduciendo la movilidad del lípido. 3. FUNCIONES DE LOS LÍPIDOS Función de reserva. Son la principal reserva energética del organismo. Un gramo de grasa produce 9,4 kilocalorías en las reacciones metabólicas de oxidación, mientras que proteínas y glúcidos sólo producen 4,1 kilocaloría/gr. Función estructural. Forman las bicapas lipídicas de las membranas. Recubren órganos y le dan consistencia, o protegen mecánicamente como el tejido adiposo de pies y manos. Función biocatalizadora. En este papel los lípidos favorecen o facilitan las reacciones químicas que se producen en los seres vivos. Cumplen esta función las vitaminas lipídicas, las hormonas esteroideas y las prostaglandinas. Función transportadora. El transporte de lípidos desde el intestino hasta su lugar de destino se realiza mediante su emulsión gracias a los ácidos biliares y a los proteo lípidos. Y el transporte de proteínas liposolubles. Sabor y textura de los alimentos. Los lípidos resultan indispensables para lograr preparaciones de cocción con agradable sabor. Por otra parte, las grasas retardan el vaciado gástrico, por lo que aumentan la sensación de saciedad después de la ingesta. 4. CLASIFICACIÓN DE LOS LÍPIDOS a. LÍPIDOS SAPONIFICABLES Los lípidos saponificables agrupan a los derivados por esterificación u otras modificaciones de ácidos grasos, y se sintetizan en los organismos a partir de la aposición sucesiva de unidades de dos átomos de carbono. En este grupo se incluyen: ÁCIDOS GRASOS Y SUS DERIVADOS: Los ácidos grasos son ácidos monocarboxílicos de cadena larga, como se indica a continuación. Por lo general, contienen un número par de átomos de carbono, normalmente entre 12 y 24. Ello se debe a que su síntesis biológica tiene lugar mediante la aposición sucesiva de unidades de dos átomos de carbono. Sin embargo también existen ácidos grasos con un número impar de átomos de carbono, que probablemente derivan de la metilación de un ácido graso de cadena par. Ácido mono carboxílicos de cadena larga Las propiedades químicas de los ácidos grasos derivan por una parte, de la presencia de un grupo carboxilo, y por otra parte de la existencia de una cadena hidrocarbonada. La coexistencia de ambos componentes en la misma molécula, convierte a los ácidos grasos en moléculas débilmente anfipáticas. El grupo -COOH es capaz de formar puentes de hidrógeno, de forma que los puntos de fusión de los ácidos grasos son mayores que los de los hidrocarburos correspondientes. Según la naturaleza de la cadena hidrocarbonada, distinguimos tres grandes grupos de ácidos grasos: ÁCIDOS GRASOS SATURADOS Desde el punto de vista químico, son muy poco reactivos. Por lo general, contienen un número par de átomos de carbono. Los ácidos grasos saturados más abundantes son el palmítico (hexadecanoico) y el esteárico (octadecanoico). Los ácidos grasos saturados de menos de 10 átomos de C son líquidos a temperatura ambiente y parcialmente solubles en agua. A partir de 12 C, son sólidos y prácticamente insolubles en agua. En estado sólido, los ácidos grasos saturados adoptan la conformación alternada todo-anti, que da un máximo de simetría al cristal, por lo que los puntos de fusión son elevados. El punto de fusión aumenta con la longitud de la cadena. Acido palmítico (C16:0) Acido esteárico (C18:0) Los ácidos grasos de cadena impar probablemente derivan de la metilación de un ácido graso de cadena par. En ellos, la simetría del cristal no es tan perfecta, y los puntos de fusión son menores. Ejemplos son el ácido propiónico (C3:0), valeriánico (pentanoico, o C5:0) y pelargónico (nonanoico, o C9:0). Los lípidos ricos en ácidos grasos saturados constituyen las grasas. Conviene en este punto hacer una distinción entre los términos lípidos, grasas y aceites. Grasas son aquellos lípidos que son sólidos a temperatura ambiente, mientras que aceites son aquellos lípidos que son líquidos a temperatura ambiente. Tanto los aceites como las grasas son lípidos. ÁCIDOS GRASOS INSATURADOS Con mucha frecuencia, aparecen instauraciones en los ácidos grasos, mayoritariamente en forma de dobles enlaces, aunque se han encontrado algunos con triples enlaces. Cuando hay varios dobles enlaces en la misma cadena, estos no aparecen conjugados (alternados), sino cada tres átomos de carbono. En el siguiente cuadro (1) se muestra algunos ejemplos de ácidos grasos insaturados y poli saturados. Familia ω-9 Ácido Oleico (C 18:1;19) ω-6 Ácido Linoléico (C 18:2; 9,12) ω-3 Ácido Linolénico (C 18:3,9,12,15) ω-6 Acido Araquidónico (C 20:4; 5,8,11,14) Cuadro 1. Estructura química de acido grasos. En esta tabla se observa la estructura química de ácidos grasos saturados como el oleico y ácidos grasos polinsaturados como el linoléico, linolénico y araquidónico, indicándose además el nombre de la familia omega al que pertenecen. Siendo los ácidos poliinsaturados escenciales para el ser humano. EICOSANOIDES Este término agrupa a una serie de compuestos derivados de ácidos grasos poliinsaturados de 20 átomos de carbono (de donde deriva su nombre), como el ácido araquidónico. Como la diversidad de los eicosanoides es grande, estos compuestos se clasifican en función de las enzimas que intervienen en su síntesis: Si son productos de la ruta de la ciclooxigenasa: prostaglandinas y tromboxanos Si son productos de la ruta de la lipoxigenasa: leucotrienos Acido Araquidónico, ácido graso esencial ω-6 Tienen una amplia gama de actividades biológicas: intervienen en procesos alérgicos, inflamatorios, provocan la contracción del músculo liso (en la menstruación y en el parto). Son el prototipo de mediadores locales, liberados in situ ante diversos estímulos. Aunque son compuestos que funcionan como señales químicas, difieren de las hormonas en dos aspectos: Se sintetizan prácticamente en todos los tejidos, no en una glándula endocrina. Químicamente son muy inestables y, por tanto, sólo actúan a nivel local. PROSTAGLANDINAS Las prostaglandinas (PG) se consideran derivados de un hipotético ácido prostanoico (no existe como tal en la naturaleza), de 20 átomos de C, con un anillo pentagonal entre los carbonos 8 y 12. Existen varias familias de PG, que se denominan con una letra adicional (PGA, PGB, PGC, PGD, PGE, PGF, etc.), en función de los sustituyentes del anillo ciclo pentano de su estructura. A menudo, la letra mayúscula va seguida de un subíndice que indica el número de dobles enlaces presentes en la molécula, sin incluir el anillo. Se conocen unas 20 PG, cuya función es la de regular la acción hormonal. Las PGE y PGF provocan la contracción de la musculatura lisa, en especial en el aparato reproductivo, de ahí que sean utilizadas para inducir el aborto. Prostaglandina E1 Prostaglandina E2 La PGI2 (también llamada prostaciclina) es un vasodilatador que actúa principalmente sobre las arterias coronarias y que impide la agregación plaquetaria. Las PGG y PGH son mediadores de la reacción inflamatoria. Compuestos como el ácido acetilsalicílico (aspirina) y los glucocorticoides (cortisol, dexametasona) inhiben la síntesis de estas PG, y de ahí sus efectos antiinflamatorios. LEUCOTRIENOS Son derivados eicosanoides que deben su nombre a la presencia de tres dobles enlaces conjugados. Se sintetizan a partir de la ruta de la lipoxigenasa, que es especialmente activa en los leucocitos. Son mediadores locales que intervienen en reacciones de tipo alérgico, asmático o inflamatorio. Aparecen frecuentemente combinados con el tripéptido glutatión, como en el caso del leucotrieno C4 (LTC4). CÉRIDOS También llamados ceras, se forman por la unión de un ácido graso de cadena larga (de 14 a 36 átomos de carbono) con un mono alcohol, también de cadena larga (de 16 a 30 átomos de carbono), mediante un enlace éster. Sólidos a temperatura ambiente, poseen sus dos extremos hidrófobos, lo que determina su función impermeabilizar y proteger. Los céridos, sirve de revestimiento de las hojas, frutos, flores o talos jóvenes, así como los tegumentos de muchos animales, el pelo o las plumas está recubierto de una capa cérea para impedir la pérdida o entrada (en animales pequeños) de agua. Entre las más conocidas se encuentran la de abeja (esteres del ácido palmítico con alcoholes de cadena larga), la lanolina (grasa de lana de oveja), el aceite de espermaceti (producido por el cachalote) y la cera de carnauba (extraído de una palmera de Brasil). En general en los animales se encuentran en la piel, recubriendo el pelo, plumas y exoesqueleto de insectos. En los vegetales forman películas que recubren hojas, flores y frutos. Las ceras se utilizan en cremas y lociones, para lustrar muebles y automóviles, en grasas para zapatos y velas y cosméticos. FOSFOLIPIDOS Los fosfolípidos en general son aquellos lípidos que contienen ácido fosfórico. En el campo de la ciencia y la tecnología de los alimentos, la expresión suele limitarse a los derivados del ácido glicerofosfórico, que están formados por una molécula de glicerol esterificada en las posiciones 1 y 2 por dos ácidos grasos, con la posición 3 esterificada por un ácido fosfórico que lleva unidas además otras estructuras, dependiendo del fosfolípido de que se trate. De forma genérica se denominan "lecitinas", aunque se considera que la lecitina propiamente dicha es la fosfatidilcolina. Según la estructura unida al ácido fosfórico, podremos hablar de fosfatidiletanolamina, fosfatidilcolina, fosfatidilserina,y fosfatidilinositol, que son los fosfolípidos más frecuentes en los alimentos. Figura 4. Estructura de la molécula de fosfoglicerido La estructura de los ácidos grasos unidos también varía entre los fosfolípidos. Es frecuente que el ocupa la posición 2 sea insaturado, mientras que el que ocupa la posición 1 suele ser saturado. Son lípidos polares, ya que tienen una región hidrofílica formada por el grupo cargado del fosfato y la zona hidrófina de la etanolamina, colina, serina o inositol. Los fosfolípidos son los principales constituyentes lipídicos de las membranas biológicas, donde forman estructuras en bicapa, con las zonas no polares de los constituyentes de cada capa orientados hacia el interior. Consecuentemente, los fosfolípidos se van a encontrar presentes en la mayoría de los alimentos complejos, en los que exista material celular. Los fosfolípidos son también capaces de producir estructuras artificiales del tipo de bicapa (liposomas). Su interés en el campo de los alimentos radica en que al ser lípidos polares se orientan en las superficies de contacto entre el agua y los materiales hidrófobos, y reducen la tensión superficial. Es decir, reducen la energía necesaria para crear superficie de contacto y la tendencia minimizarla, facilitando la producción de emulsiones y estabilizándolas. Los fosfolípidos son un componente importante de los lípidos de la yema de huevo, lo que explica su buena capacidad como emulsionante. También se encuentra en la membrana del glóbulo graso de la leche (y consecuentemente, en la mantequilla). Los fosfolípidos utilizados como emulsionantes en la industria (lecitinas) suelen proceder del refinado del aceite de soja. Los fosfolípidos también pueden reducir la energía de superficie en el contacto de interfaces con aire. En una interface aire-agua, los fosfolípidos se sitúan con la región hidrofóbica hacia el aire, facilitando la formación de espumas. Aunque la gran mayoría de espumas alimentarias se obtienen con proteínas, esta propiedad de los fosfolípidos se ha utilizado en "cocina creativa" para la formación de espumas muy ligeras, los llamados "aires". En las interfaces aceite-aire, los fosfolípidos se orientan con la zona hidrófila hacia el aire, facilitando la formación de espumas. Esto resulta extremadamente perjudicial, ya que aumenta muchísimo la superficie de contacto entre el oxígeno del aire y la grasa, facilitando las reacciones de oxidación. En el caso de los aceites que contienen proporciones significativas de fosfolípidos tras su extracción, como el aceite de soja, éstos se eliminan en el refinado, en el proceso conocido como "desgomado" GLUCOLÍPIDO O glucoesfingolípidos son esfingolípidos compuestos por una ceramida (esfingosina + ácido graso) y un glúcido de cadena corta; carecen de grupo fosfato. Los glucolípidos forman parte de la bicapa lipídica de la membrana celular; la parte glucídica de la molécula está orientada hacia el exterior de la membrana plasmática y es un componente fundamental del glicocálix, donde actúa en el reconocimiento celular y como receptor antigénico. Entre los principales glúcidos que forman parte de los glucolípidos encontramos la galactosa, la manosa, la fructosa, la glucosa, la N-acetilglucosamina, la N-acetilgalactosamina y el ácido siálico. Dependiendo del glucolípido, la cadena glucídica puede contener, en cualquier lugar, entre uno y quince monómeros de monosacárido. Al igual que la cabeza de fosfato de un fosfolípido, la cabeza de carbohidrato de un glucolípido es hidrofílica, y las colas de ácidos grasos son hidrofóbicas. En disolución acuosa, los glucolípidos se comportan de manera similar a los fosfolípidos. Estructura química de un glucolipido CEREBRÓSIDOS Los cerebrósidos tienen un azúcar unido mediante enlace β-glucosídico al grupo hidroxilo de la ceramida; los que tienen galactosa se denominan galactocerebrósidos (como la frenosina) y se encuentran de manera característica en las membranas plasmáticas de células del tejido nervioso; los que contienen glucosa (glucocerebrósidos) se hallan en las membranas plasmáticas de células de tejidos no nerviosos. Los sulfátidos poseen una galactosa esterificada con sulfato en el carbono 3. β-D-Galactosilceramida, un galactocerebrósido; R es la cadena alquílica del ácido graso. Estructura química de β-D-Galactosilceramida GLOBÓSIDOS Los globósidos son glucoesfingolípidos con oligosacáridos neutros unidos a la ceramida. Estructura química de un globósido GANGLIÓSIDOS Son los esfingolípidos más complejos en virtud de contener cabezas polares muy grandes formadas por unidades de oligosacáridos cargadas negativamente ya que poseen una o más unidades de ácido N-acetilneuramínico o ácido siálico que tiene una carga negativa a pH 7. Los gangliósidos se diferencian de los anteriores por poseer este ácido. Están concentrados en gran cantidad en las células ganglionares del sistema nervioso central, especialmente en las terminaciones nerviosas. Los gangliósidos constituyen el 6% de los lípidos de membrana de la materia gris del cerebro humano y se hallan en menor cantidad en las membranas de la mayoría de los tejidos animales no nerviosos. Se presentan en la zona externa de la membrana y sirven para reconocer las células, por lo tanto se les considera receptores de membrana. Su nombre se debe a que se aislaron por primera vez de la membrana de las mitocondrias de las células ganglionares. Estructura química de un ganglilósido b. LÍPIDOS NO SAPONIFICABLES Los lípidos insaponificables son derivados por aposición varias unidades isoprénicas, y se sintetizan a partir de una unidad básica de 5 átomos de carbono: el isoprenol. TERPENOS Se denomina así a un grupo de compuestos isoprenoides, pertenecientes al grupo de los lípidos prenoles de Fahy y col. Se biosintetizan por conjugación de moléculas de isopreno, y su estructura, que puede ser lineal o cíclica, así lo refleja. Los terpenos se clasifican según el número de dímeros de isopreno que forman su estructura, considerando que la unidad terpénica consta de dos isoprenos. Se habla así de: Hemiterpenos (Media Unidad Terpénica, C5 ) Mono terpenos (Una, C10) Sesquiterpenos (Una Y Media, C15) Diterpenos (Dos, C20) Sesterterpenos (Dos Y Media, C25) Triterpenos (tres, C30) Tetraterpenos (cuatro, C40) y si hay más de cuatro unidades terpénicas (8 isoprenos) se habla de politerpenos. En ocasiones, los terpenos se pueden denominar también en función del número de unidades de isopreno que constituyen la molécula; en este caso se hablará de monoprenoides (hemiterpenos), diprenoides (monoterpenos), triprenoides (sesquiterpenos), tetraprenoides (diterpenos), etc. ESTEROIDES Son lípidos que derivan del ciclopentano perhidrofenantreno, denominado gonano (antiguamente esterano). Su estructura la forman cuatro anillos de carbono (A, B, C y D). Los esteroides se diferencian entre sí por el nº y localización de sustituyentes. ESTEROLES De todos ellos, el colesterol es el de mayor interés biológico (Cuadro 2). Forma parte de las membranas biológicas a las que confiere resistencia, por otra parte es el precursor de casi todos los demás esteroides. Cuadro 2. Estructura química de hormonas suprarrenales, sexuales, esteroles como el colesterol, estradiol, vitaminas y otros derivados del ciclo pentano perhidrofenantreno. Otros esteroles constituyen el grupo de la vitamina D o calciferol, imprescindible en la absorción intestinal del calcio y su metabolización. ÁCIDOS BILIARES Derivan de los ácidos cólico, desoxicólico y quenodesoxicólico, cuyas sales emulsionan las grasas por lo que favorecen su digestión y absorción intestinal. HORMONAS ESTEROIDEAS Incluyen las de la corteza suprarrenal, que estimulan la síntesis del glucógeno y la degradación de grasas y proteínas (cortisol) y las que regulan la excreción de agua y sales minerales por las nefronas del riñón (aldosterona). También son de la misma naturaleza las hormonas sexuales masculinas y femeninas (andrógenos como la testosterona, estrógenos y progesterona) que controla la maduración sexual, comportamiento y capacidad reproductora. 5. DIGESTION El proceso de digestión de los lípidos comienza en la boca, en primera instancia, a través de un proceso mecánico: la masticación. Las glándulas de von ebner, alojadas en la parte posterior de la lengua, por debajo de las papilas, segregan una lipasa conocida como lipasa lingual, que tiene un pH optimo de acción de 4,5. La lipasa lingual actúa como todas las lipasas hidrolizando los ácidos grasos en las posiciones 1 y 3 de los triacilgliceridos, teniendo especifidad sobre los ácidos grasos de cadena corta y media. Su actividad se da en el estomago, donde continua siendo activa hasta un pH de 2. La liberación de algunos ácidos grasos en el estomago sirve para estabilizar la superficie de emulsión de los triglicéridos y ayuda a la liberación de colecistoquininapancreocimina (CCk-PZ) desde la mucosa duodenal. Alrededor de un 10 a 20% del total ingerido de ácidos grasos puede encontrarse como ácidos grasos libres en el estomago veinte minutos después de la ingestión de grasas.la mayor parte de la hidrólisis de los triglicéridos se produce en el duodeno, donde se mezclan con las secreciones pancreáticas, especialmente bicarbonato y agua, que aumentan el pH duodenal a 6 o 6,5. La principal acción hidrolitica es llevada a cabo por la lipasa pancreática, que digiere por lo menos el 90% de las grasas consumidas, tiene un pH optimo de acción que varía entre 7 y 9 y se secreta en forma activa. Hidroliza los enlaces esteres externos en las posiciones 1 y 3 dando como producto final 2 monogliceridos, digliceridos y ácidos grasos libres. El proceso de digestión de los lípidos requiere además sustancias de características antipáticas: las sales biliares. Las mismas son necesarias para la actividad óptima de la lipasa y para producir la solubilizacion de los productos lipidicos a través de la formación de micelas. Las sales biliares están formadas por ácidos biliares que se combinan con glicina o taurina. La molécula de sal biliar, formada por partes hidrofobica e hidrofilica, interactúa con los lípidos en un ambiente acuoso y los solubiliza, formando micelas. La micela es una estructura molecular que se codifica a gran velocidad. Alrededor de ella se encuentran los di y triglicéridos, siendo la afinidad por el interior de la micela proporcional a la insolubilidad. Este proceso de formación de micelas facilita la digestión química de los lípidos al proporcionar una mayor superficie de contacto entre las moléculas de grasa. Cada día el hígado sintetiza aproximadamente 600 a 800 mg de ácidos biliares, cantidad igual a la que se pierde en las deposiciones. Mediante la circulación enterohepatica, las sales biliares se absorben activamente en el íleon terminal y retornan al hígado por el sistema venoso portal. Con el fin de satisfacer las necesidades de absorción de lípidos, la reserva de ácidos biliares puede ser reciclada varias veces en el curso de una sola comida. La mínima cantidad de sales biliares necesarias para la formación de micelas se denomina concentración micelar crítica. Otras enzimas que completan la digestión de los lípidos son la colesterolesterasa, que actúa sobre los esteres del colesterol hidrolizando las uniones con los ácidos grasos, dando colesterol libre y un acido graso. En forma similar hidroliza los esteres de las vitaminas liposolubles. Las fosfolipasas son producidas por el páncreas como profosfolipasas y son activadas por la tripsina. 6. METABOLISMO DEGRADACIÓN DE LOS TRIGLICÉRIDOS. Se produce fundamentalmente en el tejido adiposo, y comienza con la acción de la lipasa hormona sensible (LHS). Esta hormona produce la hidrolisis de los triglicéridos dando como productos ácidos grasos libres y glicerol. El glicerol no tiene actividad en el tejido adiposo, por lo que pasa a la circulación, metabolizándose en el hígado, donde puede oxidarse para producir energía. Los ácidos grasos libres son transportados en el plasma por la albúmina. La LHS se encuentra inicialmente inactiva, y debe ser activada por una proteína quinasa, la cual a su vez es estimulada por el AMP cíclico, como los glucocorticoides, adrenalina, somatotrofina y glucagón, favorecen la degradación de los triglicéridos. SÍNTESIS DE TRIGLICÉRIDOS. Los triglicéridos se sintetizan a partir del glicerol, que debe ser activado a glicerol P. en el hígado existe una gliceroquinasa que activa directamente al glicerol P. en el tejido no se encuentra esta quinasa, por lo que el glicerol que se utiliza para la síntesis de los triglicéridos proviene de la dihidroxiacetona P, producto intermedio de la glucolisis. El origen de los ácidos grasos también es doble, por un lado provienen de la degradación de los quilomicrones y las VLDL, o bien pueden obtenerse de la síntesis endógena a partir del acetilCoA. Para la síntesis de los triglicéridos los ácidos grasos deben ser activados a acil-CoA. SÍNTESIS DE ÁCIDOS GRASOS. La síntesis endógena de ácidos grasos se realiza en el citoplasma a partir del acetil -CoA. El acetil-CoA que proviene del metabolismo de los carbohidratos, los aminoácidos o los ácidos grasos se encuentra en la mitocondria, y debe salir al citoplasma; como la mitocondria no es permeable a su pasaje, forma ácido cítrico junto con el oxalecetato. El ácido cítrico pasa al citoplasma y origina nuevamente acetil-CoA. Este acetil-CoA se une al malonil-CoA, primer paso de la síntesis que está regulada por un sistema multienzimático denominado “ácido graso sintetasa”. El proceso de síntesis produce principalmente palmitato (C16:0); posteriormente, mediante sistemas de elongación, se adicionan carbonos para obtener ácidos de 18 y 20 carbonos. DEGRADACIÓN DE LOS ÁCIDOS GRASOS O BETA-OXIDACIÓN. Cerca del 50% de las necesidades energéticas del hígado, riñón, musculo cardiaco y esquelético en reposo es aportado por la oxidación de las grasas. Este porcentaje aumenta a casi el 100% en situaciones de ayuno. A diferencia de estos tejidos, las células cerebrales no utilizan los lípidos y dependen casi exclusivamente de la glucosa. Los ácidos para degradarse deben ser activados, para lo cual requieren energía. En presencia de ATP y CoA, el ácido graso se activa a acil-CoA. Una vez activado debe entrar en la mitocondria, proceso que es facilitado por la carnitina, compuesto derivado del aminoácido lisina. Dentro de la mitocondria, se oxida liberando sucesivamente acetil-CoA y un ácido graso en dos carbonos menos, que reanuda el ciclo. El acetil-CoA se oxida en el ciclo de Krebs. Este proceso se denomina beta-oxidación, debido a que la misma se produce en el carbono beta, el segundo a partir del grupo carboxilo terminal del ácido graso. METABOLISMO DE LOS CUERPOS CETÓGENOS. Los cuerpos cetógenos (aceto-acetato, betahidroxibutirato y acetona) se forman en el hígado y se oxidan en los tejidos periféricos, principalmente el musculo cardiaco, esquelético y riñón. La cetogénesis es un proceso fisiológico, por lo que se considera normal la presencia de cuerpos cetógenos en sangre (hasta 1mg%) y en orina (hasta 20mg en diuresis de 24 horas). La beta-oxidación de los ácidos grasos en el hígado, si es completa finaliza con la producción de acetil-CoA, origina acetoacetato, parte del mismo se convierte en acido beta-hidroxibutirico y en acetona. El principal mecanismo de producción de cuerpos cetógenos es a partir de un exceso de acetilCoA, el cual se produce cuando se consumen dietas ricas en grasas y pobres en carbohidratos, en situaciones de ayuno prolongado, en la diabetes, o en cualquier situación que condicione un déficit de glucosa en los tejidos. La glucosa provee glicerol P, que en el tejido adiposo es utilizado para la síntesis de triglicéridos y en el hígado provee piruvato que se transforma en oxalecetato permitiendo consumir el acetil-CoA. La falta de glucosa en el tejido adiposo impide la síntesis de triglicéridos, por lo que los ácidos grasos llegan al hígado, donde se oxidan acumulándose acetilCoA. La falta de glucosa en el hígado origina un déficit de piruvato y oxalacetato, situación que impide la oxidación del acetil-CoA que se produce en exceso. Esta producción aumentada de acetil-CoA permite la formación de aceto-acetil-CoA (dos moléculas de acetil-CoA). Sobre este compuesto se une otra molécula de acetil-CoA, formándose el beta-hidroximiel glutaril-CoA. Esta sustancia es intermediaria en la cetogénesis y la síntesis de colesterol, y a partir de ella se sintetizan el beta-hidroxibutirato y la acetona. CETÓLISIS. Se lleva a cabo en el musculo cardiaco, esquelético y riñón. El acetoacetato debe activarse a acetato acetil-CoA, el cual se tioliza dando dos moléculas de acetil-CoA, que se oxidan en el ciclo de Krebs. Cuando la producción es exagerada y se supera la capacidad de oxidación por los tejidos periféricos, los cuerpos cetónicos se acumulan en sangre y se eliminan en mayor cantidad por orina o por vía respiratoria. Esta situación se denomina cetosis, que lleva a una disminución del pH, pudiendo desarrollar como consecuencia una alteración del equilibrio acidobase del medio interno a través de una acidosis metabólica. COLESTEROL. La mayor `parte del colesterol corporal se sintetiza endógenamente, y una menor cantidad es aportada por la alimentación, en promedio 300 a 500 mg/día. Los principales órganos de síntesis son el hígado, intestino, piel y glándulas suprarrenales. La síntesis e realiza a partir del acetil-CoA en varias etapas: tras varios pasos se forman mevalonato, el cual origina unidades isoprenoides, de la condensación de seis de las mismas se forma el escualeno, que se transforma en lanosterol y luego en colesterol. La enzima clave de la síntesis en la BOH metilglutaril-CoA reductasa, que es inhibida por el colesterol sintetizado a modo de autorregulación endógena. La insulina y la hormona tiroidea estimulan su síntesis, mientras que el glucagón, las catecolaminas y los glucocorticoides la inhiben. 7. ABSORCION Los productos finales de la digestión de los lípidos son ácidos grasos, mono glicéridos, lisofosfoglicéridos, colesterol libre y vitaminas liposolubles. La captación de estos productos a través de la membrana micro vellosa se realiza por un proceso pasivo, los 2 monogliceridos y aun triglicéridos podrían atravesar la membrana del enterocito. La hidrólisis de estos productos incorporados sin una completa degradación seria llevada a cabo por lipasas intracelulares. Una proteína citológica de bajo peso molécula, denominada proteína transportadora de ácidos grasos, se liga a los mismos y funciona como proteína de transporte intracelular digiriendo los ácidos grasos de cadena larga hacia el retículo endoplasmático liso, lugar de la resíntesis de triglicéridos, fosfolípidos y esteres de colesterol. El glicerol y los ácidos grasos de cadena de 10 carbonos o menos atraviesan las membranas del enterocito y pasan directamente a los capilares del sistema porta. La absorción de los lípidos depende de ciertas características bioquímicas como: la longitud de la cadena, el grado de saturación y la estructura molecular. La mayor solubilidad de los ácidos grasos de cadena corta y media facilita su absorción. Los mismos no requieren de la formación de micelas, y por consiguiente tampoco de la presencia de sales biliares. Su pasaje directo al sistema venoso portal se realiza sin re esterificación intramucosal ni formación de quilomicrones. En relación a los ácidos grasos de cadena larga se sugiere una disminución del 10% en la absorción por cada incremento de dos átomos de carbono en la cadena de los ácidos grasos, lo que estaría relacionado con la menor solubilidad de los mismos a mayor longitud de la cadena. El grado de saturación afecta la absorción, de manera que los ácidos grasos insaturados se absorben mejor que los saturados. 8. TRANSPORTE DE LÍPIDOS Debido a la insolubilidad de los lípidos en el medio acuoso de la sangre, las proteínas proporcionan el mecanismo para su transporte mediante la formación de lipoproteínas. Las mismas están conformadas por una fracción proteica denominada apoproteína y una fracción lipídica con contenidos variables de colesterol, triglicéridos y fosfolípidos. Las apoproteínas tienen tres funciones principales: solubilizar a los compuestos lipídicos de las lipoproteínas, regular la acción de estos lípidos con las enzimas relacionadas con el metabolismo de las lipoproteínas y unirse a los receptores de las membranas celulares determinando los sitios y grados de degradación de las lipoproteínas. Las principales apoproteinas son la AI, AII, B48, B100, CII y E. Existen 5 clases de lipoproteínas: - quilomicrones, VLDL (very low-density lipoproteins: lipoproteínas de muy baja densidad), IDL (intermédiate-density lipoproteins: lipoproteínas de baja densidad)y HDL (lipoproteínas de alta densidad. Los quilomicrones son las lipoproteínas de mayor tamaño, están constituidas especialmente por triglicéridos de origen exógeno. Los quilomicrones nacientes contienen apolipoproteinas. Nacen en las vellosidades intestinales y son transportados por la circulación hacia el conducto torácico. En la circulación adquieren apolipoproteínas C y E que provienen de las HDL. La apoproteina CII es el cofactor necesario para la actividad de la lipoproteína lipasa, enzima que se encuentra en los capilares del endotelio y que hidroliza los triglicéridos de los quilomicrones. La apoproteína E es reconocida por un receptor hepático permitiendo la internalización del quilomicrón en el hígado, donde sus remanentes lipídicos y proteicos son catalizados. El transporte de lípidos oncogénicos se lleva a cabo por medio de las VLDL y LDL. La VLDL es una lipoproteína rica en triglicéridos de origen endogénico con una estructura y composición similar a los quilomicrones pero de menor tamaño. Es sintetizada en el hígado, aunque una muy pequeña proporción puede sintetizarse también en el intestino. Las apoproteínas constitutivas son la B-100, E y C. Su contenido lipídico es en parte hidrolizado por la LPL, con la cual se transforma en una nueva lipoproteína: la IDL. Parte de esta lipoproteína es removida del plasma por medio de receptores hepáticos que reconocen a la apolipoproteína E. El resto continua la lipolisis de su contenido lipídico y todas las apoproteínas excepto la B-100. Esta apoproteína es reconocida por receptores hepáticos y extrahepaticos con gran afinidad para la LDL. Alrededor del 70 % de la LDL es removida del plasma por este mecanismo, principalmente por el hígado. El resto es modificado en el plasma y removido por otros receptores que se encuentran en los macrófagos y células endoteliales. La cantidad de LDL en plasma esta en directa relación con el numero de receptores de LDL, el que a su vez esta regulado por las necesidades de colesterol. Cuando esta necesidades son bajas, las células sintetizan pocos receptores, reduciéndola remoción de las LDL. A su vez existen otros factores que afectan el número y la actividad de estos receptores de LDL, el principal es un determinante genético para la síntesis de los mismos. Entre los factores externos, el consumo elevado de grasas saturadas y colesterol disminuye la actividad de estos receptores. Una cantidad elevada de LDL en plasma condiciona un mayor riesgo de aterogénesis La HDL son las lipoproteínas encargadas del transporte reverso del colesterol, mecanismo por el cual el colesterol de los tejidos periféricos puede ser excretado. Las HDL naciente se sintetizan en el hígado e intestino y recogen el colesterol libre de las células. Este colesterol es esterificado por la enzima LCAT que utiliza a la lipoproteína A-I como cofactor. Las HDL maduras se forman con la adicción de los foslípidos y triglicéridos derivados del catabolismo de los quilomicrones y las VLDL a su vez el colesterol esterificado de las HDL puede ser transferido a las VLDL y LDL. En el hígado las HDL son degradas totalmente. Tabla 2 Esquema Conceptual Del Transporte De Los Lípidos Tabla 3. Contenido de lípidos en alimentos CONTENIDO EN ALIMENTOS (g/100 g DE ALIMENTO) >90 89 – 50 49 – 10 <10 ALIMENTOS Aceites Grasa de cerdo o vacuna Manteca Margarinas Mayonesa Fiambres Almendras Quesos Vísceras Carnes Huevo Crema de leche Chocolates Aceituna Coco Leche Algunos pescados: merluza, pejerrey, salmón. Tabla 4. Contenido Porcentual En Ácidos Grasos Sobre El Total De Grasas ALIMENTO GRASAS SATURADAS Carne de vaca Carne de pollo Pescados (merluza) Huevo Leche entera Aceite de maíz Aceite de girasol Aceite de oliva Manteca Frutas secas Palta 53 40 19 35 65 10 11 15 64 10 17 GRASAS MONOINSTURADAS 44 44 27 50 31 36 19 73 33 25 70 GRASAS POLIINSATURADAS 3 14 54 15 4 54 70 13 3 65 13 Tabla 5. Contenido de colesterol en algunos alimentos CONTENIDO EN COLESTEROL (mg/100g DE ALIMENTO) 500 – 300 290 – 100 90 – 60 <60 ALIMENTOS Hígado Riñón Caviar Huevo de gallina y codorniz Manteca Piel de pollo Calamar Camarón Menudos Sardinas Quesos con más del 30% de grasas Carne de cerdo Carne vacuna Carne de pollo Salchichas tipo Viena Fiambres Quesos con 20 al 30% de grasas Leche Merluza Salmon Quesos con menos del 20% de grasas Tabla 6. Efecto De Los Diferentes Ácidos Grasos En Las Fracciones Del Colesterol Sérico TIPO DE ÁCIDO GRASO SATURADOS MONOINSATURADOS POLIINSATURADOS OMEGA-3 ISÓMEROS TRANS EFECTO ELEVA EL COLESTEROL LDL. Anteriormente se consideraba que poseían un efecto neutro sobre la concentración del colesterol sérico; en la actualidad se postula que disminuye la fracción LDL y no afectan la fracción HDL. Disminuyen el colesterol LDL cuando reemplazan a las grasas saturadas en la dieta. Recientemente se ha demostrado que también disminuyen el colesterol HDL. Por otro lado, se ha sugerido que ingestas elevadas de AGPI pueden asociarse a un mayor riesgo de cáncer probablemente por su elevada susceptibilidad a la peroxidacion. Disminuyen los niveles de triglicéridos y colesterol LDL sin afectar al colesterol HDL. Otros efectos beneficiosos que se le atribuyen son la reducción en el riesgo de trombosis para disminuir la inflamación y la tendencia a la coagulación. Con respecto a sus efectos sobre los lípidos sanguíneos se ha sugerido que serían equivalentes a los de los AGS, elevan el colesterol LDL y disminuyendo el HDL. Experimentalmente se ha demostrado que compiten con el metabolismo de los ácidos grasos esenciales disminuyendo la conversión de estos a sus respectivos eicosanoides. 9. INGESTAS RECOMENDADAS DE LÍPIDOS Según recientes reuniones de expertos sobre grasas y aceites en la alimentación humana; la FAO ha establecido las siguientes recomendaciones acerca del consumo de lípidos en la alimentación. Ingestas Mínimas deseables Las grasas dietéticas deben aportar en las personas adultas un mínimo del 15% del consumo energético diario. En las mujeres en edad reproductiva, el mínimo aconsejado es el 20% del consumo energético. Ingestas límites para el consumo de grasas Los individuos activos que se encuentran en un balance energético en equilibrio pueden consumir hasta un 35% de su aporte diario en forma de grasas, si su ingesta de ácidos grasosa esenciales y demás nutrientes es adecuada y si el nivel de ácidos grasos saturados no excede el 10% del consumo calórico diario. Las personas con vida sedentaria no deben consumir más del 30% del aporte energético diario en forma de grasa. Consumos recomendados de grasa saturados, insaturadas y colesterol La ingesta de ácidos grasos saturados no debe proporcionar un porcentaje mayor al 10% del consumo energético. Las ingestas deseables de ácido linoleico establecen de un 4 a 10% de4l aporte energético, siendo el rango superior aconsejado cuando las ingestas de grasas saturadas y colesterol son relativamente elevadas. Se considera apropiada una reducción en la ingesta de colesterol, con un valor menor a 300mg diarios. Consumo de ácidos grasos esenciales La relación ácido linoleico-linoleico en la dieta debe mantenerse entre 5:1 a 10:1. Las personas que consuman dietas con una relación superior a 10:1, deben ser estimuladas a aumentar el consumo de alimentos ricos en ácidos omega-3. 10. PRUEBAS DE LABORATORIO PARA IDENTIFICAR LIPIDOS a. MÉTODOS DE EXTRACCIÓN DIRECTA DE LOS LÍPIDOS MÉTODO DE SOXHLET El método consiste en una extracción de lípidos semi-continua con el solvente o mezcla de solventes orgánicos adecuado según el tipo de grasa a extraer. PREPARACIÓN DE LA MUESTRA Y EXTRACCIÓN DE LOS LÍPIDOS En un cartucho de papel de filtro colocar la muestra seca y pesada (conviene utilizar lo proveniente de la determinación de humedad por el método indirecto), y ponerla en el tubo extractor. Tarar el balón del aparato y conectarlo al mismo. Por la parte superior del tubo extractor agregar el solvente adecuado (éter etílico, éter de petróleo, mezcla de ambos, etc.) hasta que descargue el sifón, agregando además alrededor de la mitad del contenido del tubo extractor. Calentar para que se produzcan al menos 7 ciclos de llenado y sifonado del tubo extractor (durante 2 horas aproximadamente). RECUPERACIÓN Y ELIMINACIÓN DEL SOLVENTE Quitar el cartucho del tubo extractor con el resto de la muestra. Volver a armar el equipo y recuperar el solvente limpio que se va acumulando en el tubo extractor. Una vez que queda un pequeño volumen en el balón separar el solvente de los lípidos por evaporación a baño María o en baño de arena caliente. Colocar el balón con los lípidos unos 10 minutos en estufa y pesar. Cálculos: una vez conocida la masa de lípidos libre de solvente orgánico, calcular el porcentaje de grasa en la muestra teniendo en cuanta la masa inicial de muestra colocada en el cartucho de extracción. Nota: Esta determinación suele denominarse extracto etéreo (si se utiliza éter), pues además de los lípidos se extraen otros compuestos solubles en el solvente. b. Métodos de extracción de los lípidos previa liberación de la fase grasa MÉTODO DE SCHMID-BONDZYNSKI-RATZLAFF Es un método muy empleado para determinar los lípidos en queso y en leche en polvo. En vaso de precipitado de 100 ml colocar la cantidad adecuada de BM hasta que las proteínas se hayan disuelto. Dejar enfriar, transferir el contenido a una probeta graduada con tapa esmerilada, lavando el vaso de precipitado con unos 10 ml de alcohol etílico en dos porciones y luego agregar 50-60 ml de éter. Dejar en reposo 24 horas y leer el volumen de la fase etérea. Tomar una alícuota exactamente medida y evaporar el éter en un vaso de precipitado pequeño previamente tarado. Una vez evaporado el éter pesar nuevamente y determinar el contenido de lípidos por diferencia, teniendo en cuenta la alícuota tomada para realizar los cálculos. MÉTODO DE GERBER MATERIA GRASA EN LECHE FLUIDA Se utilizará un butirómetro para leche y ácido sulfúrico Gerber El H2SO4 g/ml, se prepara con 94,2 ml de ácido sulfúrico concentrado (d = 1,84) y 5,8 ml de agua destilada (no agregar NUNCA agua sobre ácido sino ácido sobre agua). Medir con pipeta 10 ml de H2SO4 Gerber e introducirlos en un butirómetro para leche, cuidando no mojar las paredes internas del cuello. Agregar con rapidez 11 ml de leche medidos con pipeta de doble aforo, de manera que forme una capa sobre el ácido sin mezclarse con éste. Agregar inmediatamente 1 ml de alcohol amílico y tapar con el tapón correspondiente. Tomar el butirómetro con un paño seco sujetando el tapón y agitar por inversión suave pero efectiva. Verificar que esté bien tapado y colocarlo en un baño de agua a 65-70 °C durante 5 a 10 minutos con el tapón hacia abajo. Retirar del baño, secarlo y centrifugarlo en la centrífuga especial con los tapones hacia afuera. Llevar nuevamente a baño de agua durante aproximadamente 5 minutos hasta que alcance la temperatura del agua (65-70 °C) y leer de inmediato el volumen de fase grasa separada en la parte superior graduada del butirómetro. El volumen leído corresponde directamente al porcentaje de grasa en la leche. MATERIA GRASA EN CREMA O MANTECA Se utiliza un butirómetro similar al utilizado para leche, pero abierto en sus dos extremos y con una copita de vidrio en el tapón que obtura la base, en la que se pesa la muestra. La graduación del vástago es de 0 a 70. Se pesan en la copita 4 a 5 g de muestra (algo menos en el caso de la manteca), se la coloca en el butirómetro, se ajusta bien el tapón y por la otra boca se agregan 10 ml de agua destilada, 10 ml de H2SO4 hasta disolución total. Se coloca luego durante 5 min en baño María a 60-70 °C con el bulbo hacia abajo. Conviene atar los tapones, pues sino se corre el riesgo de que salten y se pierda la determinación. Una vez cumplido el tiempo de calentamiento, se centrifuga 5 min en la centrífuga Gerber con el ápice hacia adentro. Cálculo: Se aplica la fórmula siguiente: Lx5 materia grasa = --------- - 0,5 = g% p L: lectura en el butirómetro 5: porque el butirómetro está graduado para 5 gr de muestra p: gramos de muestra pesados. 0, 5: factor de corrección MÉTODO DE ROSE GOTTLIEB REACTIVOS: NH4OHconcentrado Etanol Eter etílico Eter de petróleo Pesar la muestra en papel satinado previamente tarado. Encerrarla parcialmente para que pueda entrar en contacto con los reactivos e introducirla hasta el fondo en una probeta de 50 ml con tapa. Agregar 5 ml de agua destilada y agitar hasta que se la muestra se disperse totalmente, calentando si es necesario a 60 °C en baño de agua. Enfriar y agregar 1 ml de NH4OH concentrado. Agitar y agregar 5 ml de etanol. Agitar y agregar con pipeta aforada 10 ml de éter etílico. Agitar durante 30 s y agregar con pipeta aforada 10 ml de éter de petróleo. Volver a agitar y leer bien el volumen total de la mezcla. Dejar reposar entre 4 y 24 horas en lugar fresco de modo de evitar la evaporación de solventes. Con pipeta aforada tomar 10 ml de la fase superior etérea y evaporarlos en un pequeño cristalizador tarado. Dejar enfriar en desecador, pesar y expresar como porcentaje de grasa en la muestra. a. MÉTODOS DE EXTRACCIÓN DE LÍPIDOS TOTALES EN FRÍO EXTRACCIÓN DE FOLCH. Pesar la masa deseada de muestra. Agregar 20 partes de una mezcla de metanol: cloroformo (2:1) por cada parte de muestra. Agregar 20 % del volumen de agua. Dejar overnight para lograr la separación de fases. Separar la fase acuosa de la orgánica EXTRACCIÓN DE BLIGH AND DYER (aplicada a la extracción de lípidos de músculos) Pesar 5 g de músculo. Agregar 10,0 ml de metanol (agitar) y 5,0 ml de cloroformo (relación metanol: Cl3CH:H2O = 2:1:0.8, incluyendo el agua contenida en la muestra). Agitar durante 30 min (4°C). Agregar 5,0 ml de Cl3CH y agitar. Agregar 5 ml de agua (relación metanol: Cl3CH:H2O = 2:2:1.8). Centrifugar a 5000 rpm, 10 min. Separar la fase acuosa de la orgánica. Pasar la fase orgánica a través de papel de filtro. A partir de la fase clorofórmica de cualquiera de estas extracciones se podrán realizar las siguientes determinaciones: Lípidos totales (por pesada luego de la evaporación del solvente) Cromatografía en capa fina (TLC) para evaluar las distintas fracciones lipídicas presentes. Cuantificación de colesterol y triglicéridos. Perfil de ácidos grasos REFERENCIAS BIBLIOGRÁFICAS BIOQUÍMICA DE HARPER, BIOQUÍMICA ILUSTRADA - MURRAY ROBERT K Ed. 28ª, Editorial Mcgraw-Hill, 2010. QUÍMICA - CHANG R. ED. MCGRAW-HILL 1998. BIOQUÍMICA - HORTON, H. ROBERT; MORAN, LAURENCE A; OCHS RAYMOND S; RAWN, J. DAVID; SCRIMGEOUR K. GRAY. México, D.F: Prentice-Hall Hispanoamericana, 1995. QUÍMICA - SIENKO, MICHELL J; PLANE, ROBERT A. Madrid: Aguilar, 1967. FUNDAMENTOS DE LA NUTRICIÓN NORMAL - LAURA B LÓPEZ; MARTHA MARÍA SUAREZ Edición 3ra, Reimpresión 2008. “Las Biomoléculas de la Vida “ Lípidos