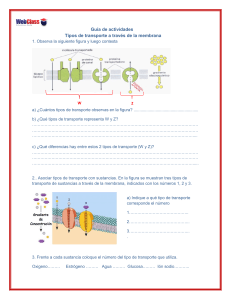
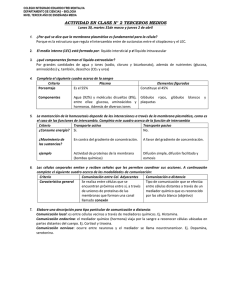
La base molecular de la vida LOS SERES VIVOS Para ser considerado un ser vivo debe satisfacer siete características: - Organización y complejidad: En niveles jerárquicos→principio de emergencia (cada nivel superior es generado por niveles preexistentes pero tiene unas propiedades emergentes, que son la suma de las anteriores) - Homeostasis: Mantener constantes sus condiciones internas. Debido a la Entropía→tendencia física natural al desorden de las moléculas. Es complejo mantener estructura organizada y compleja. Mucha energía se destina a los límites homeostáticos. - Irritabilidad: Capacidad de reacción ante los estímulos internos y externos. - Metabolismo: Intercambio de materia y energía con el medio mediante reacciones químicas. Esto hace posible que se mantenga su grado de complejidad y organización. - Crecimiento y desarrollo: Aumento de tamaño y conjunto de cambios. - reproducción y herencia: Capacidad de reproducirse→GeneracIon de copias de si mismos de forma asexual o forma sexual. Ácidos nucleicos soporte de la información→ desarrollo→ funcionamiento→ mantenimiento propia vida y descendientes. - evolución: La información genética de un ser vivo es la misma durante toda su vida→ mutaciones y recombinación entre genes→ conjunto de la especie cambie. LOS ENLACES QUÍMICOS Enlaces intramoleculares: Enlaces que mantienen unidos los átomos→ misma molécula. Enlaces intermoleculares: Enlaces que permiten la unión o interacción→ diferentes moléculas. Enlaces intramoleculares: Unión para conseguir una configuración electrónica estable: - Covalente: no metal y no metal. Comparten pares de electrones de su última capa. 1 Polar: Átomos de diferente electronegatividad. En estos casos la molécula es un dipolo ya que presenta una zona de mayor carga negativa y otra de menor. apolar: átomos de idéntica electronegatividad. - Iónico: metal y no metal. El metal pierde electrones→catión y el no metal gana electrones→anión. Ambos iones se unen debido a la carga electrostática. Enlaces intermoleculares: - fuerzas electrostáticas/puentes salinos: Atracción entre dos grupos ionizados con carga opuesta. - Fuerzas de solvatación: Interacción entre un ión y una molécula covalente polar. NaCl se disuelve en agua, cada ión Na+ o Cl- rodeado por una “capa de solvatación” formada por moléculas de agua. Muchas proteínas se disuelven de esta forma. - Interacciones hidrofóbicas: Tendencia natural de las moléculas hidrofóbicas a agruparse con el fin de evitar su interacción con el agua. - Fuerzas de van der waals: fuerzas de atracción débiles y de corto alcance entre moléculas eléctricamente neutras que se encuentran muy próximas.Pequeños desplazamientos de cargas que generan pequeños dipolos. Enlaces de hidrógeno: atracción electrostática entre polo positivo y negativo de dos moléculas dipolares formadas por átomos de hidrógeno unidos a pequeños elementos electronegativos→agua imprescindible para la vida→ estructura espacial de las proteínas y ácidos nucleicos→ procesos fundamentales de los seres vivos→ interacciones entre biomoléculas. LOS BIOELEMENTOS Son los elementos químicos que constituyen la materia viva. Son comunes a la materia viva e inerte. Se pueden encontrar unos 70 elementos de la tabla periódica en las moléculas de los seres vivos. - Bioelementos primarios: Son los más abundantes en el organismo. Constituyen un 98% del peso en un organismo. Resultan indispensables en la formación de las biomoléculas orgánicas e inorgánicas. C, N, O, H, P, S 2 - Bioelementos secundarios: Aparecen en menor proporción que los bioelementos 2%. Forman las sales minerales generalmente disociadas en sus cationes y aniones. Realizan funciones indispensables(5) como: →Formación de estructuras esqueléticas. →Generación de gradientes iónicos esenciales en la conducción del impulso nervioso. →contracción muscular. →Mantenimiento del equilibrio osmótico. →Neutralización de cargas en las macromoléculas. Mg, Ca, Na, K, CL - Oligoelementos: Aparecen en cantidades ínfimas 0,1% pero desempeñan funciones catalíticas que las convierten indispensables para la vida. 14 comunes en todos ellos. Mn, Fe, Cu, Zn, F, B, I, Sn... I→ función reguladora de las hormonas (tiroides). Fe→Transporte de oxígeno (glóbulos rojos). F→Protege el esmalte de los dientes. EL CARBONO: Elemento más adecuado para constituir la estructura básica de las biomoléculas orgánicas. Propiedades: - Capacidad de unirse mediante enlace covalente a más de un elemento (H, O, N). - Dar lugar a estructuras de gran complejidad. - Abunda en la corteza terrestre, la atmósfera y la hidrosfera. Esto facilita que los seres vivos lo asimilen. - Capacidad de unirse tanto al hidrógeno y oxígeno→ reacciones redox→ base metabolismo. LAS BIOMOLÉCULAS Son las moléculas que forman la materia viva. Están constituidas por bioelementos. - Biomoléculas orgánicas: Son exclusivas de la materia viva. Están formadas por cadenas de carbono. Se denominan también principios activos. Glúcidos, Lípidos, Proteínas y ácidos nucleicos 3 - Biomoléculas inorgánicas: Forman la materia viva y la inerte aunque en diferentes proporciones. Agua y sales minerales EL AGUA Es la molécula más abundante de la materia viva→75% masa celular total. varía en los organismos. Aparece de distintas formas: - Estructural: forma parte de las estructuras citoplasmáticas. Se pierde→deshidratación y se gana→hidratación. - Circulante: Lleva nutrientes y deshechos en disolución. - Metabólica: forma parte de las estructuras moleculares y no se puede perder. ESTRUCTURA DE LA MOLÉCULA DEL AGUA: - Formada por 2 átomos hidrógeno y 1 oxígeno unidos mediante enlace covalente polar. - Molécula angular→ dos átomos de hidrógeno separados por 104’5º - Comportamiento como dipolo→ los electrones compartidos se encuentran más cerca del oxígeno ( densidad de carga negativa) que del hidrógeno (densidad de carga positiva). ESTRUCTURA DEL AGUA LÍQUIDA: moléculas de agua unidas mediante enlaces de hidrógeno, el hidrógeno con densidad de carga positiva es atraído por el oxígeno con densidad de carga negativa→ estructura flexible y red extensa→ seno: agrupamientos transitorios y reorganización continua→ pesos moleculares elevados. líquido→temperaturas donde se desarrolla la vida. PROPIEDADES Y FUNCIONES DEL AGUA EN LOS SERES VIVOS(7): 4 5 LAS SALES MINERALES Se genera a partir de la neutralización de un ácido y una base. Se desprende agua. Una cantidad conocida de átomos de hidrógeno se reemplaza por átomos de un metal de la base. Se pueden encontrar en los seres vivos de dos formas: - Precipitadas: - Insolubles en agua→ funciones estructurales, protección o sostén. - Ejemplo: Exoesqueletos de crustáceos CaCo3. - Endoesqueletos de vertebrados CaCo3. - Disueltas: Aparecen disociadas en iones: cationes-base. Aniones-ácido. Enorme importancia biológica. Funciones: Catalítica Fe²⁺, Mn²⁺, cofactores enzimáticos necesarios para el funcionamiento. Fe²+ forma arte grupo hemo→ hemoglobina Mg²*→ clorofila→ fotosíntesis electroquímica Na⁺, K⁺, Cl⁻ generación gradientes electroquímicos→ potencial membrana y necesario acción → contracción muscular impulso nervioso osmótica Regulan equilibrio osmótico→ trasiego agua en células. tamponadora Regulan Ph celular monofosfato-bifosfato y carbonato-bicarbonato DISPERSIONES ACUOSAS: DISPERSIONES COLOIDALES (8): → Tamaño: 0,001 micras y 0’01 mcras → Polares→ estables (clara de huevo) 6 → Apolares→ Inestables→ aceite y agua. → Traslúcidas → elevada viscosidad y poder absorbente → Estados: Sol(fluido) y gel(viscoso) el cambio de uno a otro se debe a cambio de temperatura o ph. Cambio gradual y reversible siempre que no haya condiciones extremas. → capacidad de sedimentación de sus partículas- ultracentrifugación. → separación de partículas en función de carga eléctrica fase dispersa- electroforesis. - suspensiones: partículas fase dispersa sólidas. - Emulsiones: partículas fase dispersa líquida. DISPERSIONES MOLECULARES (6): → tamaño inferior a 0’001 micras hidrófilas→ dispersiones estables. → transparentes → viscosidad baja → no absorbentes → nunca presentan estado gel → no sedimentan por ultrafugación en la fase dispersa ni pueden separar por electroforesis. La ósmosis, difusión y diálisis son procesos físicos espontáneos sin gasto energético en sistemas dispersos cuando se ponen en contacto. DIFUSIÓN: Es la distribución homogénea de las partículas de soluto en un disolvente. Si se colocan dos disoluciones separadas por una membrana permeable se produce el paso por difusión de soluto y de disolvente siempre a favor del gradiente de concentración hasta que se igualan las concentraciones. Es una forma de intercambio celular. DIÁLISIS: Proceso que permite separar las partículas coloidales de las moleculares mediante una membrana permeable las moléculas e impermeables las coloidales. Las partículas dializables pasan de la disolución más concentrada a la más diluida. La hemodiálisis se utiliza para suplir la función renal deteriorada. ÓSMOSIS: Fenómeno por el cual entre dos disoluciones acuosas de diferente concentración separadas por una membrana semipermeable que sólo deja pasar disolvente y no soluto se 7 da trasiego de agua desde la más diluida (hipotónica) a la más concentrada (hipertónica) hast alcanzar la misma concentración (isotónica). La membrana plasmática es una membrana semipermeable, la célula debe vivir en un medio isotónico con ella para evitar fenómenos osmóticos desfavorables. - En un medio hipertónico las células perderían agua hasta deshidratarse→ plasmólisis. - En un medio hipotónico las células captarán agua por ósmosis hasta explotar→ turgencia. En las células vegetales la pared celular protege a las células de la variación de presión osmótica del medio, evitando que se produzca la explosión de la célula. comparación: DIFUSIÓN - membrana permeable. - pasa agua y solutos. - disolución más concentrada a la más diluida. DIÁLISIS ÓSMOSIS - membrana permeable para el agua y las partículas no coloidales. - Membrana semipermeable que no permite el paso de solutos. - pasa sólo agua. - pasan agua y soluto no coloidales. - - paso de la disolución más concentrada a la más diluida. de la disolución más diluida a la más concentrada. 8 Los glúcidos LOS GLÚCIDOS ¿Qué son?: Son biomoléculas orgánicas formadas por C,H, O, (P y S en menor proporción) en proporciones Cn H2n y On. Estructura química: Polihidroxialdehído o polihidroxicetona. Clasificación: OSAS El monómero de los glúcidos 3-7 átomos de carbono monosacárid os ribosa, galactosa, glucosa, desoxirribosa ÓSIDOS Formado por un conjunto de osas o monosacáridos mediante enlace o-glucosídico HOLÓSIDOS Formados por monoçsacáridos exclusivamente OLIGOSACÁRIDO S Formados de entre 2-10 monosacáridos POLISACÁRIDOS Formados por más de diez monosacáridos DISACÁRIDOS Formados por 2 monosacáridos (Lactosa, Maltosa, Sacarosa y celobiosa) HOMOPOLI SACÁRIDOS compuestos por el mismo monosacári do. almidón, celulosa, glucógeno. HETERÓSIDOS formados por monosacáridos y otros compuestos no glucídicos. glucoproteínas glucolípidos y peptidoglucano. HETEROPOLI SACÁRIDOS compuestos por diferentes monosacárid os. pectinas, ácido hialurónico, hemicelulosa . enlace: o-glucosídico o n-glucosídico. 9 Propiedades: Los monosacáridos son: - Solubles en agua (polares) y no solubles en disolventes orgánicos (apolares). - Sólidos blancos cristalinos. - Tienen sabor dulce. - Tienen poder reductor. - Forman enlaces glucosídicos. Los disacáridos son: - Solubles en agua (polar) pero no en disolventes apolares. - Sólidos cristalinos de color blanco. - Tienen sabor dulce. - Algunos tienen carácter reductor y otros no. - Son hidrolizables en presencia de ácidos o mediante la enzima glucosidasa. - Solo poseen poder reductor aquellos que se unen mediante enlace o-glucosídico monocarbonílico. Los polisacáridos son: - Son sólidos no cristalinos de color blanco. - no son solubles en agua (dispersiones coloidales en suspensión). - No tienen sabor dulce pero pueden generar sustancias dulces mediante hidrólisis. - No tienen poder reductor ya que la práctica totalidad de los carbonos anoméricos de su larga cadena de carbonos están implicados en enlaces o-glucosídicos. - Son hidrolizables en presencia de enzimas glucosidasas y ácidos. Poder Reductor: Tienen poder reductor gracias a las características reductoras del grupo carbonilo. Los aldehídos y cetonas reaccionan fácilmente con alcoholes formando unos compuestos llamados hemiacetales (aldehído) y hemicetales (cetona). En el curso de la reacción el grupo carbonilo se oxida y se desprenden electrones. CICLACIÓN DE LOS MONOSACÁRIDOS: El carácter reductor de grupo carbonilo permite que en disolución acuosa los monosacáridos de más de cinco átomos de carbono formen heterociclos. Estos se mantienen cerrados por el enlace hemiacetal intramolecular o el enlace hemicetal intramolecular. carbono carbonílico→ carbono asimétrico→ carbono anomérico que conserva su poder reductor. Su presencia da lugar a dos nuevos epímeros: 10 - Anómero Ⲁ (alfa)→ posición tans (diferente posición que el grupo CH2OH) - Anómero 𝛃 (beta)→ posición cis (misma posición que el grupo CH2OH) Piranosa→ seis vértices (hexágono) Furanosa→ cinco vértices (Pentágono) LOS ÓSIDOS: Los ósidos surgen mediante la unión de monosacáridos mediante enlaces glucosídicos. Los enlaces glucosídicos se producen por la unión de un -oh del carbono anomérico con un grupo hidroxilo o amino. En esta reacción se pierde una molécula de agua. Partes en un enlace glucosídico: - Glicona-componente glucídico. - Aglicona- componente no glucídico. Si la glicona y la aglicona son monosacáridos se forma un enlace holósido y si la aglicona es un compuesto no glucídico es un heterósido. EL ENLACE SE PUEDE ROMPER MEDIANTE HIDRÓLISIS ÁCIDA O ENZIMAS LLAMADAS ENZIMAS GLUCOSIDASAS QUE PUEDEN SER α GLUCOSIDASAS o 𝛃 GLUCOSIDASAS DEPENDIENDO DEL TIPO DE ENLACE QUE PUEDAN ROMPER. ENLACES GLUCOSÍDICOS: - Monocarbonílicos: Se une un carbono anomérico de un monosacárido con un grupo hidrófilo de otro monosacárido. El carbono anomérico pierde el poder reductor pero el carbono anomérico del segundo monosacárido sigue teniendo poder reductor siendo posible que se unan más monosacáridos y así formar cadenas de polisacáridos lineales o ramificadas. 11 - Dicarbonílicos: Se unen los carbonos anoméricos de los dos monosacáridos, por lo tanto ninguno de los dos monosacáridos tendrá poder reductor y no podrá unirse ninguna monosacárido más- estos enlaces solo se encuentran en los disacáridos. HOLÓSIDOS: OLIGOSACÁRIDOS: DISACÁRIDOS. Son cadenas formadas por el mismo monosacárido, uniones de monosacáridos (entre dos y diez) mediante enlaces o-glucosídicos. Sus funciones son estructurales y de reconocimiento de la superficie celular. Sus propiedades son (6): - Solubles en agua (polar) pero no en disolventes apolares. - Sólidos cristalinos de color blanco. - Tienen sabor dulce. - Algunos tienen carácter reductor y otros no. - Son hidrolizables en presencia de ácidos o mediante la enzima glucosidasa. - Solo poseen poder reductor aquellos que se unen mediante enlace o-glucosídico monocarbonílico. disacáridos de interés biológico: Maltosa e isomaltosa Glucosa y glucosa α-d.Glucopiranosa- α-d glucopiranosa Enlace α(1-4) maltosa y α(1-6) isomaltosa Enlace o-glucosídico Mono carbonílico (carácter reductor) Constituye el almidón y el glucógeno por lo que se obtienen a partir de ellos mediante hidrólisis ácida. Sacarosa Azúcar común Glucosa y Fructosa α-d-Glucopiranosa y beta d 12 fructofuranosa Enlace α- 𝛃 (1-2) Enlace o-glucosídico dicarbonílico (no tiene poder reductor) Origen vegetal: producto directo de la fotosíntesis Lactosa Galactosa y glucosa beta d galactopiranosa- beta d glucosa o alfa d glucosa. Enlace 𝛃 (1-4) Enlace o glucosídico monocarbonílico (poder reductor) Se encuentra en la leche de los mamíferos. No forma polímeros. Celobiosa Glucosa-glucosa Beta d glucopiranosa y beta d glucopiranosa Enlace 𝛃 ( 1-4) Enlace o glucosídico monocarbonílico (poder reductor) Se obtiene a partir de la hidrólisis ácida de la celulosa. 13 HOLÓSIDOS: POLISACÁRIDOS. Están compuestos por la unión de más de diez monosacáridos mediante enlaces o-glucosídicos. los que tienen enlaces de tipo α suelen tener función de reserva energética mientras que los de enlace tipo 𝛃 función estructural. Propiedades: - Son sólidos no cristalinos de color blanco. - no son solubles en agua (dispersiones coloidales en suspensión). - No tienen sabor dulce pero pueden generar sustancias dulces mediante hidrólisis. - No tienen poder reductor ya que la práctica totalidad de los carbonos anoméricos de su larga cadena de carbonos están implicados en enlaces o-glucosídicos. - Son hidrolizables en presencia de enzimas glucosidasas y ácidos. POLISACÁRIDOS DE INTERÉS BIOLÓGICO: ALMIDÓN - - Es un α-glucano formado por moléculas de α-d-glucopiranosa con enlaces tipo α(1-4) y α(1-6). Se encuentran en los amiloplastos de las células vegetales donde constituyen la principal fuente de reserva energética. El almidón está formado por dos polisacáridos: - Amilosa: (Situada en el interior de los granos de almidón) Formada por maltosas en forma lineal y helicoidal no ramificada unidas mediante enlaces o-glucosídicos α(1-4) - Amilopectina: (Situada exterior de los granos de almidón) Polímero helicoidal formado por maltosas en forma lineal mediante enlaces α(1-4) y ramificaciones laterales en posiciones α(1-6). GLUCÓGENO - Es un α-glucano constituido por una gran cantidad de moléculas de α-d-glucopiranosa unidas mediante enlaces α(1-4) y α(1-6). - El enlace α(1-6) permite las ramificaciones que permiten la hidrólisis del polímero en moléculas de glucosa para un mayor aporte energético que se requiera en algunas situaciones. Se encuentra en las células musculares y hepáticas de los animales en los que constituye una fuente de reserva energética. El almidón y glucógeno fácil hidrolizable por enzimas α-glucosidasas - 14 presentes en las secreciones salivales, pancreáticas y lisosomas celulares. CELULOSA - - Es un 𝛃-glucano formado por moléculas de 𝛃-d-glucopiranosa unida mediante enlace tipo 𝛃(1-4). Polimerización lineal no ramificada. Estas cadenas se unen entre sí mediante enlaces de hidrógeno y forman microfibrillas que se reúnen y forman fibrillas. Esta estructura confiere a la celulosa una gran rigidez, resistencia e insolubilidad en el agua. Tienen función estructural y constituyen el principal componente de las paredes celulares. QUITINA - Es un 𝛃-glucano formado por moléculas de n-acetil-𝛃-d-glucosamina unido mediante enlaces 𝛃(1-4). Es un polímero lineal no ramificado. Función estructural y se encuentra en los exoesqueletos de los artrópodos y las paredes celulares de los hongos. 𝛃-glucosidasas las tienen cierto tipo de hongos y bacterias. Los herbívoros para poder descomponer los enlaces establecen relaciones simbióticas en sus tractos digestivos con microorganismos descomponedores. HOLÓSIDOS:POLISACÁRIDOS:HETEROPOLISACÁRIDOS Los polisacáridos están formados por distintos tipos de monosacáridos unidos mediante un enlace o-glucosídico monocarbonílico. Funciones estructurales y lubricantes. Glucosaminoglucanos: Polímeros lineales no ramificados formados por ácido urónico y un aminoderivado. Ácido hialurónico→ tejido conjuntivo de los animales. 15 Pectinas y hemicelulosas: - Pectinas: Polímeros lineales no ramificados que se encuentran en las paredes celulares en menor proporción que la celulosa para que las células se mantengan unidas. α-d-galacturónico. - Hemicelulosas: Polímeros ramificados formados por grupos heterogéneos de α-d-monosacáridos. Forman parte de las paredes celulares de las células vegetales. HETERÓSIDOS: Asociación mediante enlaces glucosídicos de gluconas (componentes glucídicos) con aglicona(componentes no glucídicos). Principios activos de plantas medicinales. GLUCOLÍPIDOS: -Asociaciones covalentes glucosídicas de cadenas de oligosacáridos con lípidos. -Forman Membranas celulares. -Gangliósidos y Cerebrósidos: Galactocerebrósidos (llevan galactosa) y glucocerebrósidos (llevan glucosa). GLUCOPROTEÍNAS: -Asociaciones covalentes glucosídicas de cadenas de oligosacáridos con proteínas. -Las glucoproteínas de la parte externa de las membranas actúan como antígenos o receptores. Inmunoglobulinas→ cumplen función defensiva. PEPTIDOGLUCANO: Polímeros lineales no ramificados de residuos alternados de n-acetil-𝛃-d-glucosamina y 𝛃-d-n-acetilmurámico. Estos polímeros se disponen en paralelo y se unen transversalmente entre sí mediante cadenas cortas de aminoácidos. Base molecular de las paredes celulares de las bacterias. Protección y forma a las bacterias. 16 Los lípidos ¿Qué son?: Son biomoléculas orgánicas formadas por C, H y O. (S y N en menor proporción) CLASIFICACIÓN: SAPONIFICABLES Poseen ácidos grasos en su composición y por lo tanto pueden dar lugar a jabones. NO SAPONIFICABLES Carecen de ácidos grasos y por lo tanto no forman jabones. -Acilglicéridos: grasas. -Céridos: ceras. -Fosfolípidos: glicerofosfolípidos y esfingofosfolípidos. -Glucolípidos: cerebrósidos y gangliósidos. -Terpenos:Vitamina A, carotenoides, xantofilas. -Esteroides: Colesterol, hormonas sexuales, corticoides.. ENLACE: Enlace tipo éster / éster-fosfórico PROPIEDADES:(4) - No son solubles en agua pero sí son solubles en disolventes orgánicos apolares: Cloroformo y benceno. - Son untuosos al tacto. - Poseen un aspecto brillante (graso). - Baja densidad. FUNCIONES: - Reserva energética (acilglicéridos). - Estructural: Glicerofosfolípidos. - Metabólica: Hormonas lipídicas y vitaminas liposolubles. LOS ÁCIDOS GRASOS Y SUS DERIVADOS: Están compuestos por una cadena lineal hidrocarbonada con un número par de átomos de carbono que presentan un grupo carboxilo en un extremo. SATURADOS: - enlaces covalentes simples. - químicamente estables. - sólidos a temperatura ambiente. - Presentes en grasa animales, aceite de palma, coco y cacahuete. - Ácido palmítico (16 carbonos) ácido esteárico (18 carbonos). 17 INSATURADOS: - Poseen uno o más dobles enlaces en su cadena. - Son líquidos a temperatura ambiente. - Aceite de pescado azul y en aceites vegetales. Según el número de insaturaciones se clasifican en monoinsaturados o poliinsaturados: MONOINSATURADOS: -Químicamente estables. -Solo tienen un doble enlace en la cadena. -Ácido oleico (18 carbonos) (Omega 3) en el aceite de oliva. POLIINSATURADOS: -Tienen más de un doble enlace. -Químicamente Muy inestables. Los dobles enlaces se oxidan en contacto con el oxígeno atmosférico dando lugar a aldehídos y por eso es que se enrancian y huelen. -Ácido linoleico (18 carbonos) en el aceite de girasol. -Los ácidos grasos son esenciales para los mamíferos pero al no poder fabricarlos debemos ingerirlos obligatoriamente en la dieta. PROPIEDADES FÍSICAS DE LOS ÁCIDOS GRASOS: Se determinan por la longitud del ácido graso y el número de insaturaciones que tenga. SOLUBILIDAD: Son componentes anfipáticos→ se distinguen dos zonas de polaridad opuesta: - Cabeza polar: Formada por el grupo carboxilo, es hidrófila. - Cola apolar: Formada por la cadena de carbonos, es hidrófoba. debido a esta propiedad los ácidos en una disolución acuosa se disponen en las siguientes estructuras: - Monocapas de superficie. - Micelas: Esferas cuyas colas hidrófobas se dirigen al interior y las cabezas hidrófilas hacia el interior. - Bicapa: Formada por dos capas de ácidos grasos. Las cabezas polares se encuentran dispuestas hacia el exterior mientras 18 que las colas hidrófobas se juntan hacia el interior, formando así con las cabezas una barrera protectora. PUNTO DE FUSIÓN: El estado en el que se encuentran los ácidos saturados a temperatura ambiente depende del punto de fusión. Cuanta más larga y saturada es la cadena de carbonos más fuerzas de van der waals se establecen entre ellas y por lo tanto, más energía (calor) es destinada a romper estas fuerzas y el punto de fusión es mayor (paso de sólido a líquido). PROPIEDADES QUÍMICAS DE LOS ÁCIDOS GRASOS: Se deben al grupo carboxilo. ESTERIFICACIÓN: Se produce entre un grupo carboxilo de un ácido orgánico y un alcohol y produce una molécula de agua originando un éster carboxilo. SAPONIFICACIÓN: La reacción entre un ácido orgánico y una base fuerte. Se obtiene una sal sódica y agua. CÉRIDOS: Las ceras son ésteres entre un ácido graso y un alcohol monohidroxílico de cadena larga y con un número par de carbonos. - Altamente insolubles: crean películas protectoras de tejidos de animales (plumas y pelos) y plantas (recubren hojas y frutos). - Cera de abeja o cerumen conducto auditivo. 19 ACILGLICÉRIDOS o GLICEROLÍPIDOS: Son ésteres de una molécula de glicerina con uno, dos o tres ácidos grasos. Los glicerolípidos son moléculas saponificables ya que se pueden formar jabones a partir de ellas. Su hidrólisis en presencia de bases fuertes se utiliza para obtener jabones. Pueden formarse monoacilglicéridos, diacilglicéridos y triacilglicéridos. Esterificación de un acilglicérido(entre ácidos grasos y glicerina-se obtiene un acilglicérido): Saponificación de un acilglicérido (se obtienen jabones): GRASAS: Las grasas son triacilglicéridos que se consideran grasas neutras porque son apolares y por lo tanto, insolubles en agua. Esto las diferencia de los monoacilglicéridos y los diacilglicéridos ya que estos tienen cierta polaridad debido a los grupos hidroxilos libres de la glicerina. - Tienen función de reserva energética y además de aislante térmicos y mecánicos. Se clasifican según su consistencia a temperatura ambiente: -Aceites: Son líquidos a temperatura ambiente. En su composición abundan los ácidos grasos insaturados o de cadena corta. Aceite de oliva o girasol. 20 -Mantecas: Pastosas a temperatura ambiente. Formadas por ácidos grasos saturados con un número no demasiado alto de carbonos. Mantequilla y Margarina. -Sebos: Sólidos a temperatura ambiente. Formado por ácidos grasos saponificados con cadenas de un elevado número de átomos. Tocino. GLICEROFOSFOLÍPIDOS o FOSFOGLICÉRIDOS: Son ésteres entre un ácido fosfatídico y un aminoalcohol unidos mediante enlace fosfodiéster. ÁCIDO FOSFATÍDICO: Está formado por glicerina unida a un diacilglicérido ( un ácido graso saturado y otro insaturado) y unida a un ácido fosfórico mediante enlaces tipo éster (éster carboxílico y éster fosfórico). 21 TIPOS DE FOSFOGLICÉRIDOS: - Ácido fosfatídico + etanolamina→Cefalina: Fosfatidiletanolamina (cefalina) - Ácido fosfatídico + Colina→ Fosfatidilcolina (Lecina) - Ácido fosfatídico + Serina→ Fosfatidilserina (cefalina) Las más importantes son las cefalinas ya que se encuentran en los tejidos cerebrales y las lectinas en la yema de huevo. Funciones: Son moléculas anfipáticas ya que en su molécula se encuentran dos regiones: -Polar: Cabezas hidrofílicas- donde se encuentra el aminoalcohol y el ácido fosfórico. Suele presentar carga eléctrica. -Apolar:Colas hidrofóbicas. Formada por las dos cadenas largas de ácidos grasos. Esta anfipaticidad es responsable de que en medio acuoso los fosfoglicéridos creen bicapas. Estas bicapas constituyen la base molecular de la arquitectura de las membranas biológicas. ESFINGOLÍPIDOS: Aparecen en las membranas de las células animales y vegetales. Abundan en el tejido nervioso. Tienen ceramida (unión mediante enlace amida, de esfingosina (aminoalcohol insaturado de 18 carbonos) y un ácido graso de cadena larga). 22 ESFINGOFOSFOLÍPIDOS: - Se forman por la esterificación de la ceramida con un ácido fosfórico y a su vez otra esterificación con un aminoalcohol (colina o etanolamina). - Son constituyentes de las membranas celulares. - Las más importantes son la esfingomielinas que contienen colina y que protegen los axones de las fibras mielínicas de los mamíferos. ESFINGOGLUCOLÍPIDOS: - Unión de ceramida con un glúcido mediante enlace o-glucosídico. - Sin constituyentes de las membranas celulares y abundan en las neuronas. - Cerebrósidos (Parte glicona formada por glucosa o galactosa) y gangliósidos (cadena oligosacárida). Los gangliósidos exponen sus cadenas oligosacáridas hacia el exterior celular actuando como antígeno y diferenciando diferentes tipos de células. Son lugares de anclaje de microorganismos y regulan el proceso de crecimiento y diferenciación celular. LÍPIDOS ESTERÓLICOS: Derivan de un anillo tetracíclico con nombre: ciclopentanoperhidrofenantreno. Incluye dos grupos: Esteroles: Poseen un grupo hidrófilo -oh en el C3 y una cadena hidrocarbonada alifática (de cadena abierta) en el C17. - Colesterol: forma parte de las membranas celulares animales regulando la fluidez para hacerlas más estables y resistentes. - Ácidos biliares: se sintetizan en el hígado a partir del colesterol. Derivan de ellos las sales biliares- emulsión de las grasas en la digestión. - Vitamina D: Varias formas químicas más abundante la d3. Regula el metabolismo del calcio y fósforo y su absorción intestinal. - Estradiol: hormona sexual femenina es responsable de los caracteres sexuales secundarios y maduración del óvulo. Esteroides: En el c3 del ciclopentanoperhidrofenantreno tiene un doble enlace con el oxígeno. - Hormonas sexuales: Influyen en la madurez sexual y en la función reproductiva. -Testosterona (Hormona sexual masculina) -Progesterona (Hormona del embarazo) 23 - Hormonas de la corteza suprarrenal: Cortisol Glucocorticoide que regula el metabolismo de los glúcidos y aldosterona Mineralocorticoide que regula la absorción de agua y sales minerales. LÍPIDOS PRENÓLICOS Formados a partir del isopreno. - Terpenos: Fitol- forma principalmente la clorofila. Vitamina A- Imprescindible en el proceso de percepción lumínica. - Quinonas: Coenzima Q que actúa como transportadora de electrones en la respiración celular. 24 Las proteínas ¿Qué son?: Son biomoléculas orgánicas formadas por carbono, hidrógeno, oxígeno y a menudo llevan azufre y nitrógeno así como hierro y cobre. Son polímeros lineales no ramificados formados por aminoácidos unidos por enlaces peptídicos. CLASIFICACIÓN: Según el número de aminoácidos que forman la proteínas se dividen en: PÉPTIDOS Son cadenas de entre dos y cien aminoácidos. PROTEÍNAS Cadenas de más de cien aminoácidos. OLIGOPÉPTIDOS: Son de entre dos y diez aminoácidos. Se llaman dipéptidos, tripéptidos…. HEMOPROTEÍNAS: También llamadas proteínas simples están formadas únicamente por aminoácidos. Queratina, colágeno e histonas. POLIPÉPTIDOS: Entre diez y cien péptidos. insulina humana. Cadena a y b de 21 y 30 aminoácidos. HETEROPROTEÍNAS: Proteínas conjugadas Tienen parte proteica (apoproteina, formada por aminoácidos) y parte no proteica (Grupo prostético). hemoglobina, glucoproteínas y lipoproteínas. ENLACES: Peptídicos-amida PROPIEDADES: LOS AMINOÁCIDOS: Unidades o monómeros constituyentes de las proteínas. Formado por un carbono alfa unido a un grupo amino (-NH2) unido a un grupo carboxilo y a un radical. El radical establece las diferencias entre los diferentes tipos de aminoácidos. 25 CLASIFICACIÓN DE LOS AMINOÁCIDOS SEGÚN LA POLARIDAD DE SU RADICAL: APOLARES: Alanina TRIPTÓFANO: POLARES: - Neutros: Carecen de carga eléctrica o ph fisiológico. Glicina: Cisteína: - Polares ácidos. ácido aspártico: Ácido glutámico: PROPIEDADES FíSICAS DE LOS AMINOÁCIDOS: - Son sólidos cristalinos e incoloros. - Son solubles en agua gracias a los grupos hidroxilos unidos al carbono alfa y al grupo amino. - Algunos tienen sabor dulce. - Presentan estereoisomería, por ello existen dos enantiómeros de cada aminoácido, el D y el L - Presentan isomería óptica. Son capaces de rotar el plano de la luz polarizada cuando atraviesa una disolución de estos. Si el plano de luz polarizada giran hacia la derecha son dextrógiros y si giran hacia la izquierda levógiro. PROPIEDADES FÍSICAS DE LOS AMINOÁCIDOS: - Cada aminoácido tiene un ph determinado, esto se llama punto isoeléctrico o pI. En estos puntos los aminoácidos son iones dipolos neutros o zwitterion, el grupo amino y el grupo hidroxilo están ionizados pero sus cargas se equilibran y su carga neta es 0. Los aminoácidos tienen poder anfótero, es decir, que se pueden comportar como ácidos o bases. - PH<Pi el aminoácido se comporta como base y coge protones. - Ph>Pi El aminoácido se comporta como ácido y pierde protones. EL ENLACE PEPTÍDICO: Los aminoácidos se enlazan entre ellos mediante enlaces peptídicos. Es un enlace amida entre el grupo alfa carboxilo y el grupo alfa amino liberando una molécula de agua. El resultado es un dipéptido. 26 Extremo n-terminal y extremo c-terminal. CARACTERÍSTICAS DEL ENLACE PEPTÍDICO: 1. Son enlaces covalentes muy estables y más cortos que otros tipos de enlaces c-n. 2. Posee cierto carácter de doble enlace por lo que carece de libertad de giro y es plano y rígido. 3. Solo existe libertad de giro en los enlaces c-C alfa y N-C alfa. 4. Los cuatro átomos situados en el enlace C-o N-h se sitúan en el mismo plano. LOS NIVELES DE LAS PROTEÍNAS: Las proteínas son macromoléculas de gran complejidad estructural por lo que se estudian cuatro niveles: Estructura primaria: -Es la secuencia lineal concreta de aminoácidos que forman su cadena. De ella dependen los siguientes niveles estructurales y su funcionalidad. -Cada proteína tiene una cadena única ya que la información necesaria para construirla viene determinada por el ADN. -La alteración de la estructura primaria por eliminación, adición o intercambio da lugar a otra proteína con otra función biológica o incluso la pérdida de la actividad biológica. - La estructura primaria es mantenida por el enlace peptídico tan estable que solo se puede romper por hidrólisis ácida o enzimática. Supone la liberación de la proteína y los aminoácidos que la integran. 27 ESTRUCTURA SECUNDARIA: Es el modo en el que las cadenas polipeptídicas se disponen alrededor de un eje. Vienen determinadas por las características de los radicales y el enlace peptídico. Es la estructura superior que alcanzan las proteínas fibrosas. Hélice α: -La cadena polipeptídica se enrolla sobre sí misma en forma de espiral de forma dextrógira, en sentido de las agujas del reloj. -Habiendo 3’6 aminoácidos por vuelta. -La hélice queda estabilizada por puentes de hidrógeno entre el grupo -Nh del aminoácido y el grupo C=0 del cuarto aminoácido que le sigue. -Los radicales de los aminoácidos y los hidrógenos quedan colocados hacia el exterior de la hélice. -Un ejemplo de proteínas con esta estructura son las α-queratinas abundantes en las células epidérmicas que forman los pelos, plumas, uñas, cuernos y lana en los animales. Lámina β plegada: -Las cadenas polipeptídicas adoptan una forma en zig zag y varias cadenas se sitúan en paralelo. -Se estabiliza la lámina plegada mediante puentes de hidrógeno de grupos -NH y -C=o de las cadenas paralelas. -El carbono alfa queda situado en las aristas mientras que los enlaces peptídicos en los planos entre dos aristas y los radicales por encima y debajo de la lámina plegada alternativamente. - β-Queratina: fibras que fabrican los gusanos de seda y arañas. Hélice de colágeno: -Está formada por la glicina, Prolina e hidroxiprolina. -Se enrolla de forma levógira formando una hélice más estirada que la hélice alfa ya que solo hay tres aminoácidos por vuelta. -La hélice de colágeno está formada por tres hélices levógiras enrolladas unas con otras en sentido dextrógiro y se mantienen unidas mediante enlaces de hidrógeno. -El colágeno se sintetiza en los fibroblastos y es una parte importante de los huesos, tendones, vasos sanguíneos, cartílagos y huesos. -Fabricación de gelatina. ESTRUCTURA TERCIARIA: -La estructura secundaria se pliega y se repliega. Adoptando una disposición espacial más o menos estática mediante enlaces covalentes: Disulfuro y puentes de hidrógeno. 28 -Las proteínas globulares alternan pliegues de hélice alfa y lámina beta hasta adquirir una estructura esférica y compacta. -Las estructuras terciarias se pliegan de una forma concreta, compacta y estable y a estas formas se llaman dominios estructurales. Son tan concretos que desempeñan funciones específicas como los centros activos en las enzimas. ESTRUCTURA CUATERNARIA: -La unión de cadenas polipeptídicas, cada una de ellas con estructura terciaria. -Oligoméricas. Cada cadena se llama subunidad. -Cómo se distribuyen en el espacio las subunidades con respecto a otras. Enlaces similares a los de la estructura terciaria. -Número par de subunidades, todas necesarias para que cumpla la función. -Hemoglobina. Inmunoglobulina. CONFORMACIÓN NATIVA: La conformación nativa resulta de la combinación de las estructuras secundaria, terciaria y cuaternaria de la proteína. Cada proteína necesita un Ph, temperatura y salinidad del medio en los cuales adopta la conformación más estable posible que corresponde a su conformación nativa. Las proteínas sólo manifiestan su actividad biológica cuando se encuentran en su estructura nativa. La información para que una proteína alcance su estructura nativa se encuentran en los mismos aminoácidos (estructura primaria) sin embargo, hay algunas proteínas que requieren de otras proteínas llamadas chaperonas para un plegamiento adecuado. INTERACCIONES EN LA ESTRUCTURA TERCIARIA Y CUATERNARIA DE LAS PROTEÍNAS: Fuerzas intermoleculares Débiles: -Fuerzas de van der waals. -Puentes de hidrógeno. -Puentes salinos -Interacciones hidrofóbicas. Enlaces disulfúricos: Cuando dos cisteínas quedan próximas se establecen enlaces disulfúricos en las estructuras terciarias y cuaternarias. -SH 29 PROPIEDADES DE LAS PROTEÍNAS: Especificidad, Solubilidad,Capacidad tamponadora y Desnaturalización. Especificidad: La especificidad radica en la secuencia de aminoácidos. - Especificidad de especie: Cada especie tiene sus propias proteínas que son diferentes a las de otra especie en sus secuencia de aminoácidos. Las proteínas similares que desempeñan la misma función en especies diferentes es llamada proteína homóloga. Cambio en la secuencia de aminoácidos. resultado de la evolución. - Especificidad de función: Cada proteína al tener una secuencia específica de aminoácidos realiza una única función. Interacción selectiva con otras moléculas con una secuencia específica y una conformación espacial concreta. solubilidad: La solubilidad de las proteínas depende del Ph, del medio, la concentración de sales… Capacidad tamponadora: Las proteínas tienen un carácter anfótero, pueden neutralizar las variaciones de ph del medio liberando captando protones (básico) o liberando protones (ácido). Desnaturalización: Proceso por el cual debido a cambios en el muy extremos en el ph, la temperatura o presencia de determinadas sustancias (urea y detergentes) las proteínas pierden su conformación nativa, sus estructuras y por lo tanto su actividad biológica. No implica la ruptura de enlaces peptídicos ni pérdida de la estructura primaria pero sí cambios en la solubilidad. Suele ir acompañado de precipitado la desnaturalización. Puede ser reversible e irreversible: Irreversible: Es incapaz de recuperar su conformación nativa y por lo tanto su funcionalidad. Reversible: Recupera la conformación nativa y funcionalidad al recuperar las condiciones fisiológicas iniciales. Renaturalización. FUNCIONES DE LAS PROTEÍNAS: 30 -Estructural: Aporta fuerza y protección a las estructuras biológicas→glucoproteínas de las membranas de las bacterias, queratina del pelo y las uñas, y fibroína de la seda y las telas de araña. -Nutritiva y de reserva: Almacenan aminoácidos como elementos nutritivos como el gluten del trigo y la caseína de la leche. -Transportadora: Se unen a elementos para transportarlos→ hemoglobina- transporta O2 y en la fase lumínica de la fotosíntesis los citocromos transportan electrones (cloroplastos). -Contráctil: Permiten al organismo recombinarse y cambiar de forma. Miosina y actina. -Catalizadora: Es la función principal de las proteínas. Aumenta la velocidad de los procesos y la llevan a cabo las enzimas interviniendo en las reacciones metabólicas. -Reguladora: Se encargan de integrar y coordinar todos los procesos del organismo→ hormona del crecimiento e insulina. -Inmunológica: Los anticuerpos o inmunoglobulinas se ocupan de la defensa inmunológica. CLASIFICACIÓN DE LAS PROTEÍNAS: HOMOPOLISACÁRIDOS Se dividen en: -Fibrosos: Tienen estructura secundaria Forma de fibra Muy resistentes e insolubles en agua Colágeno: Tejido óseo, y conjuntivo. alfa queratina: Pelo, lana, piel, plumas... Beta Queratina: Fibras de gusano de seda y arañas. -Globulares: Estructura terciaria y cuaternaria. Forma esférica. Solubles en agua y disoluciones salinas. Albúminas: Principal reserva del organismo. Lactoalbúmina leche y ovoalbúmina huevo. Globulinas: Inmunoglobulinas forman anticuerpos. Histonas y Protaminas: Proteínas básicas en el adn. Protaminas solo en el adn. Prolaminas y gluteninas: Proteínas de reserva en semillas vegetales como el trigo. HETEROPOLISACÁRIDOS: La parte prostética está formada por una parte no proteica: -Cromoproteínas: Sustancias coloreadas. 31 Hemoglobinas: función de transporte de dióxido y o2. Principal parte de los eritrocitos→color rojo. Citocromos: Transportan electrones y se encuentran en células aeróbicas. -Glucoproteínas: Grupo prostético formado por oligosacáridos. Algunas proteínas forman las membranas. Inmunoglobulina. -Lipoproteínas: Parte prostética formada por lípidos. macromoléculas esféricas con lípidos neutros en su interior y en sus superficie colesterol, fosfolípidos, parte proteica. Los lipoproteínas de la sangre transportan lípidos entre el intestino, hígado y tejido adiposo. -Nucleoproteínas: Grupo prostético un ácido nucleico. Ribonucleoproteinas que forman los ribosomas. HEMOGLOBINA: - Es una cromoproteína conjugada. -Apoproteína: Cuatro cadenas polipeptídicas globulares: 2 α-globina de 141 aminoácidos y 2 β globina de 146 aminoácidos. -Cada una de las cadenas de la proteína lleva en su interior un grupo prostético llamado grupo hemo. Cada protoporfirina (anillo tetrapirrólico) tiene en su interior un Fe 2+. Este se puede unir a un 02 así cada molécula de hemoglobina puede transportar cuatro moléculas de o2 desde los alvéolos pulmonares hasta las células. O de Co2 desde las células a los alvéolos para poder expulsarlos. LAS ENZIMAS: Son biocatalizadores específicos que tienen la función de participar en las reacciones metabólicas aumentando su velocidad. Mayoría naturaleza proteica aunque se ha descubierto moléculas de arn catalíticas. Ribozimas. Las enzimas aceleran las reacciones químicas ya que rebajan la energía de activación de la reacción química, favoreciendo la adquisición del estado de transición. Una vez alcanzado este estado las reacciones suceden de forma espontánea y rápida. -Moléculas enzimas ejercen acción específica: SUSTRATO. La actuación de las enzimas: 32 1-.Centro activo: El sustrato se une a una zona específica de la enzima con una geometría y grupos funcionales definidos. 2.- Se forma un compuesto temporal: Compuesto enzima-sustrato. 3.- El sustrato se transforma químicamente y forma los productos de la reacción. Se forma el compuesto enzima-producto transitorio. 4.-Los productos se liberan al separarse del centro activo de la enzima. 5.-La enzima que en el transcurso de la reacción no se gasta ni cambia queda libre para unirse a otra molécula de sustrato. TIPOS DE ENZIMAS SEGÚN SU ESTRUCTURA: Simples: Están formadas por una fracción proteica y no requieren de ninguna interacción química con otra molécula para realizar su función. Conjugadas o Holoenzimas: Fracción proteica: Apoenzima y fracción no proteica: Cofactor. - Cofactores: Iones o moléculas no proteicas de bajo peso molecular que en muchos casos son indispensables para el funcionamiento de la enzima conjugada ya que son responsables de la actividad química. - Inorgánicos: Iones metálicos como Fe2+, Mg 2+, Zn2+ - Orgánicos: - Coenzimas: Cofactores orgánicos unidos mediante enlaces débiles no covalentes a la apoenzima. NAD+, FAD y coenzima a. -Grupos prostéticos: Cofactores orgánicos unidos a la apoenzima por enlace covalente. Grupo hemo. 33 Los ácidos nucleicos ¿QUÉ SON?: Son biomoléculas orgánicas formadas por C, H, N, O y P. En los seres vivos existen dos tipos de ácidos nucleicos: Ácido desoxirribonucleico (ADN) y ácido ribonucleico (ARN). Químicamente son polímeros lineales no ramificados construidos por unas unidades llamadas nucleótidos. Nucleótidos: Base nitrogenada Monosacárido. Nucleótido: Monosacárido (Ribosa o desoxirribosa)+ base nitrogenada + Ácido fosfórico (H3Po4). MONOSACÁRIDOS: 𝛃-d-ribofuranosa -Aldopentosa -Nucleótidos de arn y otros nucleótidos de gran importancia biológica como el atp y vitaminas y complejo b. 𝛃-d-desoxirribofuranosa -Aldopentosa. -derivado del arn solo que ha perdido el grupo hidroxilo en el carbono 2. -forma nucleótidos de adn. BASE NITROGENADA: Compuestos cíclicos aromáticos con nitrógeno en su estructura: 34 -Púricas: Adenina, guanina -Pirimidínicas: citosina timina y uracilo. Timina solo en el adn y uracilo sólo en el arn. Formación de un nucleósido: Enlace n-glucosídico de la aldopentosa con la base nitrogenada. El enlace n glucosídico se establece entre el carbono anomérico de la aldopentosas (carbono 1) y uno de los grupos amino de las bases nitrogenadas (púricas nitrógeno 9 y pirimidínicas nitrógeno 1) liberándose una molécula de agua. ARN púrica: osina Pirimidínica: idina ADN desoxsiFORMACIÓN DE UN NUCLEÓTIDO: Esterificación de un nucleósido con un ácido fosfórico. Enlace éster fosfórico. Se establece con el carbono número 5 del nucleósido y el ácido fosfórico con liberación de una molécula de agua. Si se unen más de un grupo fosfato el nucleósido se unen mediante un enlace anhídrido fosfórico. adenosín difosfato o monofosfato o trifosfato. LOS NUCLEÓTIDOS NO NUCLEICOS: Son aquellos nucleótidos que no forman parte de los ácidos nucleicos que se encuentran en el citoplasma y realizan funciones metabólicas. importantes son los trifosfato (atp, gtp) el AMP cíclico y las coenzimas Fad, nad+ fmp, nadp+ y la coenzima A. - Los trifosfatos: son los vectores energéticos en las células. Los enlaces anhídridos fosfatos al romperse o formarse pueden producir o captar energía, actúan como intermediarios entre las reacciones metabólicas. la energía se conserva. ATP y GTP. - AMP cíclico: se forma en el interior de las células a partir del atp y la enzima adenilatociclasa en respuesta a la unión específica de hormonas a los receptores de la superficie celular. Se considera uno de los transmisores hormonales ya que el amp cíclico actua en el interior activando enzimas para dar respuestas a la señal hormonal recibida en el exterior. - Coenzimas: Son cofactores imprescindibles para el funcionamiento de las holoenzimas. Principalmente son nucleótidos o derivados de estos. 35 - Coenzimas oxidoreductasas: Actúan en las reacciones de óxido-reducción intervienen como aceptores de electrones. Nucleótidos de nicotinamida. -Coenzima a: deriva de la vitamina b5 y de adp y se enlaza a los ácidos grasos activandolos para intervenir en reacciones metabólicas. POLINUCLEÓTIDOS: Los polinucleótidos son cadenas lineales no ramificadas formadas por nucleótidos unidos mediante enlaces nucleotídicos que es un enlace de tipo fosfodiéster. polirribonucleótido y desoxirribonucleótido. EL ENLACE NUCLEOTÍDICO: El enlace nucleotídico o diésterfosfórico Se produce entre el grupo fosfórico situado en el carbono 5’ y el grupo hidroxilo situado en el carbono 3’. Puede ser una cadena infinita. Lo que le da la especificidad son las bases nitrogenadas que quedan colocadas perpendicularmente al eje en donde están los monosacáridos y los ácidos. Las cadenas tienen polaridad: Empiezan por el ácido 5’ y terminan por el grupo hidroxilo 3’. ÁCIDO DESOXIRRIBONUCLEICO: Está formado por desoxirribonucleótidos unidos mediante enlaces nucleotídicos. Las bases nitrogenadas que los componen son adenina, guanina, citosina, timina. Estructura primaria: Está determinada por la secuencia específica de desoxinucleótidos que mantienen los enlaces nucleotídicos. Estructura secundaria: Las cadenas de nucleótidos forman estructuras de doble hélice a partir de la estructura primaria. Estructura terciaria: Empaquetamiento y enrollamiento de la doble hélice sobre sí misma para ocupar el menor espacio en el interior celular. ESTRUCTURA PRIMARIA DEL ADN: INCOMPLETo 36 La célula. Membrana y cubiertas celulares La célula es la unidad de vida elemental: Unidad estructural: Es la unidad básica de todo ser vivo. Unidad reproductiva: Toda célula se origina a través de la división de otra ya existente. Unidad funcional: La célula es capaz de intercambiar materia viva y energía con su medio; es capaz de mantener su existencia mediante sus funciones vitales. Unidad genética: Posee la información genética necesaria para realizar su propio ciclo celular, desarrollo y funcionamiento, además puede transmitir información a sus células hijas. LA CÉLULA: La célula es un conjunto altamente organizado de biomoléculas, macromoléculas y orgánulos celulares con capacidad para desarrollar todas las características asociadas a la vida. Cada célula debe poseer tres componentes básicos que la definen como ser vivo: membrana celular, material genético y citoplasma. - Membrana celular: Componente muy activo que además de comunicar la célula con el exterior la delimita e individualiza, evitando que sus componentes salgan del sistema y se pierdan, y que la célula deje de existir como tal. Regula el trasiego de sustancias entre el interior y el exterior. - Material genético: Biomoléculas que pueden duplicarse y, a su vez, controlar el funcionamiento y el crecimiento celular. Esto permite a la célula vivir y reproducirse. - Citoplasma: Contenido interno de la célula. Tiene una matriz fluida, químicamente activa llamada citosol o hialoplasma. Mediante reacciones metabólicas catalizadas mediante enzimas esta matriz usa nutrientes de alto contenido energético con el objetivo de fabricar y reponer los componentes celulares y reaccionar a los cambios externos e internos. Tipos de organización celular: Atendiendo a su grado de complejidad se pueden distinguir dos tipos: Eucariota (Hongos, plantas, animales, protoctistas) y Procariota (Bacterias). 37 Estructura o proceso procariota eucariota envoltura nuclear no si adn Circular, no asociado a histonas (desnudo). Cromosoma bacteriano. Lineal, asociado a histonas. Forma la cromatina del interior del núcleo celular. Nucleolos No Sí División celular Fisión binaria Mitosis y meiosis Ribosomas 70S 80 S Mitocondrias no Si con ribosomas 70 S y adn circular. Cloroplastos No. La función equivalente ocurre en la membrana plasmática. Si, en las células vegetales con ribosomas 70 S y con adn circular Orgánulos delimitados por membrana No Si Pared celular Siempre. De peptidoglucano Solo en las células vegetales (celulosa) y hongos (quitina) Membrana plasmática Crece por inserción directa de proteínas y lípidos Crece por fusión de vesículas de exocitosis Estructuras de locomoción Flagelos de flagelina Cilios o flagelos de tubulina Número de células Unicelulares o pluricelulares Siempre unicelulares 38 La célula procariota: En una célula procariota bacteriana se distinguen los siguientes componentes: Cápsula bacteriana: Una envoltura externa y viscosa, fuertemente adherida a la pared bacteriana. La propia célula la fabrica y la excreta; está formada por proteínas y polisacáridos (N-acetilglucosamina, ácido urónico, ácido glucurónico…) Presencia especialmente importante en las bacterias patógenas. Desempeña tres funciones: - Interviene en la adherencia y fija la bacteria patógena a su huésped. - Confiere resistencia frente a la acción fagocitaria de las células del sistema inmunitario. - Proteger de la desecación y de la acción de agentes antibacterianos. Pared bacteriana: Se trata de una envoltura rígida situada alrededor de la membrana plasmática y situada debajo de la cápsula, cuando ésta existe. Está constituida por peptidoglucano. Su función es mantener la forma de la bacteria y proteger de los cambios de presión osmótica. Membrana plasmática bacteriana: Tiene una estructura similar a la de las células eucariotas: Bicapa lipídica compuesta fundamentalmente de fosfolípidos, en la que se insertan de forma irregular y asimétrica moléculas de proteínas. No contiene esteroles pero si hopanoides que regulan su fluidez. Sus funciones son: - Actuar como barrera osmótica. - Realizar funciones de transporte, biosíntesis, transducción de energía y punto de anclaje para los flagelos. - En las bacterias fotosintéticas, contiene los pigmentos fotosintéticos, responsables de la fase luminosa de la fotosíntesis. Citoplasma bacteriano: Se trata de una matriz fluida, químicamente activa llamada citosol donde se encuentran las estructuras celulares: ribosomas, plásmidos, inclusiones y vesículas. Mesosomas: Es una invaginación de la membrana plasmática. Interviene en la respiración celulares, replicación del ADN y formación del tabique que separa las células hijas durante la división celular. Nucleoide: Es una región del citoplasma (más o menos central) desprovista de ribosomas y transparente a los electrones. En esta zona se localiza el cromosoma bacteriano, que está constituido por una única molécula de ADN duplehelicoidal, circular y desnudo. Empaquetamiento mediante superenrollamiento o retorcimiento de la molécula sobre sí misma. 39 Ribosoma bacteriano: Partícula ribonucleoproteica (70 S ), responsable de la síntesis de proteínas. Formada por dos subunidades (30 S y 50 S ). Plásmido: Pequeña molécula de ADN circular disperso por el citoplasma. Se replica con independencia del cromosoma bacteriano. Inclusiones: Acúmulos de sustancias rodeados o no por una envoltura proteica. Gránulos intracelulares de glucógeno y polifosfato, empleados como fuente de energía y materia, o los formados por desechos metabólicos. Vesículas: Formaciones más o menos esféricas rodeadas por membrana. - Vesículas gaseosas: Típicas en las cianobacterias. Rellenas de gas e intervienen en la regulación de flotabilidad, necesaria para alcanzar la profundidad con una óptima intensidad de luz. - Carboxisomas: Contienen enzimas para la fijación de carbono. Pilis: Prolongaciones celulares de naturaleza proteica. Flagelos: Apéndice filamentoso, extremadamente largo y fino, dotado de movimiento giratorio, cuya localización es muy variable. Existen distintos tipos de bacterias: Cocos, bacilos y espirilos. 40 La célula eucariota: Animal: Centrosoma:Organiza microtúbulos, interviene en la división celular y forma cilios y flagelos. Lisosoma: Digestión celular, Membrana plasmática:Limita la célula y controla el intercambio de sustancias con el medio. Flagelo: Permite el movimiento. La membrana plasmática o celular: Es una membrana biológica de entre 7’5 nm y 10 nm de grosor, visible solo a microscopio electrónico, que define la célula. Químicamente la membrana plasmática está formada por un mosaico fluido de fosfolípidos que en el que se disponen proteínas de forma irregular, cantidades variables de colesterol y, sobre su superficie, restos de oligosacáridos que están unidos a los lípidos y a las proteínas. Lípidos de la membrana plasmática: - Fosfolípidos: Base estructural de la membrana plasmática es una bicapa formada por fosfolípidos, tanto glicerofosfolípidos como esfingofosfolípidos. Al tratarse de moléculas anfipáticas, en agua, de forma espontánea se disponen en bicapas: las cabezas polares hacia el exterior, en contacto con el medio acuoso y las colas apolares hacia el interior, unidas mediante interacciones hidrofóbicas. - Glucolípidos: Están representados principalmente por los esfingoglucolípidos (cerebrósidos y gangliósidos) y se sitúan en la monocapa externa, con los restos de azúcares (oligosacáridos) proyectados hacia el exterior celular. - Colesterol: Un lípido esterólico que solo se encuentra en las membranas de las células animales. Proteínas de la membrana plasmática: - Proteínas integrales: Son proteínas hidrofóbicas que se encuentran integradas en la bicapa de lípidos y muy unidas a las colas apolares de los fosfolípidos. - Proteína integral transmembrana: Atraviesan por completo la bicapa, dejando sus extremos, de carácter hidrofílico, expuestos al medio acuoso. Glucoproteínas. (Glúcidos-hidrofílos-expuestos) 41 - Proteína periférica: Tienen carácter hidrofílico por lo que están adheridas a la superficie de las membranas a través de interacciones con las proteínas integrales y con las cabezas polares de los lípidos de la membrana. Estructura de la membrana plasmática: Modelo del mosaico fluido - La estructura de la membrana está formada por una bicapa lipídica de carácter anfipático, mayormente fosfolípidos. Unida a ella en mayor o menor proporción y de forma irregular hay colesterol (solo en membranas animales) y proteínas. Las proteínas hidrofóbicas (integrales) se insertan en la bicapa lipídica y las hidrófilas (periféricas) se localizan en posiciones superficiales. - Se llama fluida porque los lípidos y proteínas integrales se desplazan mediante movimientos de traslación y rotación e incluso, saltando de la capa interna a la externa y a la inversa (flip-flop). La fluidez está regulada por el colesterol y los fosfolípidos. - Las membranas biológicas son asimétricas en cuanto a la disposición de sus componentes moleculares. Los restos de glucoproteínas y glucolípidos siempre se localizan en el exterior de la monocapa formando el glucocáliz. Función de los componentes de la membrana plasmática: Lípidos: - Regulan la resistencia y la fluidez: La fluidez es regulada por la longitud y el grado de saturación de las cadenas hidrocarbonadas de los ácidos grasos que forman los fosfolípidos. Cuanto más saturada y más larga sea la cadena, mayor será las fuerzas de Van der Waals entre ellas y el punto de fusión será mayor por lo tanto habrá menor fluidez. El colesterol actúa de diferente forma: Cuando las temperaturas son bajas, mantiene la fluidez ya que evita las interacciones de Van der Waals entre los fosfolípidos. Con temperaturas altas, la fluidez es menor ya que interviene con el movimiento de los fosfolípidos, lo que disminuye la fluidez. - Regulan la permeabilidad: El interior de la bicapa resulta impermeable a las moléculas hidrosolubles como iones y la mayoría de las biomoléculas. Proteínas: - Transporte: Permiten el paso de nutrientes u otras sustancias que por su tamaño o carga no podrían pasar a través de la bicapa lipídica. Proteínas canal y permeasas. - Comunicación: Reciben y transmiten señales eléctricas o químicas del exterior o procedentes de otras células. - Enzimática: Intervienen en la catálisis de las reacciones químicas. Enzimas de la cadena respiratoria 42 Oligosacáridos: - Reconocimiento: Actúan como marcadores que identifican los distintos tipos celulares y como antígenos de la superficie celular. - Receptores de superficie: Anclaje e interacción específica de moléculas, virus, bacterias y otros tipos celulares con la membrana plasmática. Funciones de la membrana plasmática: Las funciones de la membrana plasmática derivan de las funciones de sus componentes. - Mantiene constante la forma celular mediante los anclajes específicos que ofrecen los filamentos del citoesqueleto o los componentes de la matriz extracelular. - Permiten la transferencia de señales entre el medio externo e interno de la célula. - Reconocimiento e identificación celular. - Permeabilidad selectiva, gracias a la cual protege la célula y aísla el contenido celular del exterior. - Intercambio de sustancias entre el medio interior y exterior. - Favorece la adherencia o la comunicación entre células adyacentes a través de las uniones intercelulares. El transporte a través de las membranas: Las células disponen de mecanismos de transporte a través de su membrana que les permiten incorporar sustancias necesarias para su funcionamiento así como eliminar los desechos que se generan en el metabolismo. Transporte pasivo: Se produce de manera espontánea, sin gasto energético por parte de la célula. A favor del gradiente electroquímico; las moléculas se desplazan por difusión desde la zona de mayor concentración a la de menor. La velocidad de difusión es más rápida cuando la diferencia de gradiente entre las dos zonas sea mayor. El transporte pasivo se puede llevar a cabo mediante dos mecanismos: - Difusión simple: Las moléculas atraviesan libremente la membrana plasmática. Moléculas solubles en lípidos, oxígeno, dióxido. - Difusión facilitada: Los iones o las moléculas polares o cargadas no pueden atravesar el entorno hidrofóbico de la bicapa por lo que intervienen las siguientes proteínas sin gasto energético: - Permeasas: Las moléculas se unen a las proteínas a un lado de la membrana. Estas sufren un cambio de conformación reversible que permiten que liberen las moléculas al otro lado. azúcares, aminoácidos y nucleósidos. 43 -Proteínas canal: Se trata de aberturas en forma de poros regulables en la membrana. Transporta iones y agua (ósmosis). Transporte activo: No se produce de forma espontánea ya que se produce en contra del gradiente electroquímico. Requiere de un gasto energético por parte de las células. Las moléculas son bombardeadas con la intervención de proteínas transmembrana: ATPasas (consumen atp) desde la zona de mayor concentración a la de menor. Consiguen la energía para poder realizar el transporte mediante la hidrólisis del ATP. Bombas iónicas: La bomba Na⁺-K⁺ Las bombas iónicas son ATPasas especializadas en el transporte activo de iones a través de la membrana.La más importante es la bomba Na⁺-K⁺. Esta bomba mantiene la concentración de Na⁺ mayor en el exterior y la de K⁺ mayor en el interior ya que por cada ATP hidrolizado expulsa tres cationes Na⁺ e introduce dos cationes K⁺ al interior celular. Fosforilación y desfosforilación. Principales funciones: - Conservar un equilibrio osmótico y un volumen celular. El citoplasma de la célula contiene una gran cantidad de moléculas orgánicas que se compensa gracias al bombardeo de Na⁺ hacia el exterior. Baja la concentración intracelular de iones e impide la entrada masiva de agua por ósmosis. - Genera y mantiene el potencial eléctrico de la membrana. En el exterior es positivo y en el interior es negativo. Fundamental en propagación de señales eléctricas de los nervios y músculos. El transporte mediado por vesículas: El transporte de macromoléculas o partículas grandes se produce a través de vesículas y deformaciones en la membrana que se pueden ver al microscopio electrónico. Las vesículas son rodeadas por la membrana plasmática que en su interior tienen las sustancias que entran o salen de la célula. Exocitosis y endocitosis. Endocitosis: Es la entrada de sustancias al medio celular mediante la vesícula formada por la membrana plasmática. Fagocitosis, Pinocitosis y endocitosis medida por receptor. Exocitosis: Es la expulsión de partículas al exterior por medio de vesículas. Estas partículas pueden ser de desecho o metabolitos. Cuando las sustancias se han incluido en una vesícla de exocitosis esta migra hacia el exterior donde, cuando está en contacto con la membrana 44 plasmática, la membrana de la vesícula se fusionan de modo que el contenido queda en el exterior. Cubiertas celulares: Pared celular bacteriana: Envoltura rígida que rodea la membrana plasmática de la célula. Está formada por un glúcido heterósido llamado peptidoglucano o mureína. Estructura formada por polímeros lineales no ramificados de residuos alternantes de beta-d-n-acetilmurámico y n-acetil-beta-d-glucosamina que se disponen en paralelo y se unen transversalmente entre sí mediante cadenas cortas de aminoácidos. Se distinguen en el peptidoglucano aminoácidos d que protegen la pared. - Pared bacteriana Gram positiva: Se tiñe con el colorante de Gram. Grusa red de capas superpuestas de peptidoglucano que protegen la bacteria de la deshidratación. Lleva asociados polímeros lineales de glicerol fosfato denominados ácido teicoicos. - Pared bacteriana Gram negativa: No se tiñe con el colorante Gram. Se estructura en dos capas: El periplasma, interna de peptidoglucano y una externa de fosfolípidos donde se internan lipopolisacáridos y proteínas canal que aumentan su permeabilidad. Pared celular vegetal: Cubierta gruesa y rígida que rodea las células vegetales. Adosada a la membrana plasmática. Formada por celulosa. Matriz amorfa formada por agua, heteropolisacáridos y minerales. Lámina media: Más extensa y antigua (primera en formarse), adherencia entre células adyacentes. Aspecto homogéneo. Pared Primaria: Pegada a la lámina media. Permite a la célula crecer. Más celulosa y menos matriz amorfa. Pared secundaria: Se desarrolla cuando el crecimiento de las células vegetales ha cesado.En contacto con la membrana plasmática. Resistencia celular. Fibras en diferentes orientaciones. Funciones: Dar forma y consistencia. Protección y soporte. Protección frente a los cambios de presión osmótica. Barrera ante determinados patógenos. Reconocimiento celular. 45 El citoplasma celular El citoplasma: Se trata de la región de la célula que se encuentra entre el núcleo y la membrana plasmática. En él se distinguen el citosol y los orgánulos celulares. Se relaciona con el nucleoplasma a través de los polos nucleares de la envoltura nuclear. El citosol es una matriz fluida en la que se encuentran los orgánulos. El citosol constituye entre el 50% y el 80% del volumen total de la célula. Al tratarse de un líquido se puede separar del resto de componentes celulares mediante la centrifugación. Composición del citosol: - El agua compone de entre un 70 a un 75% del citosol. (dispersión coloidal acuosa) - Sales minerales. - Biomoléculas orgánicas (aminoácidos, monosacáridos, nucleótidos…) - ARNt y ARNm - Proteínas enzimáticas y estructurales. - Desechos metabólicos, moléculas solubles como polisacáridos, triglicéridos y terpenos. Funciones: - Contiene los orgánulos celulares. - Interviene en los desplazamientos intracelulares, forma el huso mitótico y la división del citoplasma además de la formación de la formación del citoesqueleto mediante sus proteínas estructurales. - Regula la fluidez y la consistencia del citoplasma pasando de sol a gel. - La mayoría de las reacciones metabólicas suceden en el citoplasma.Reguladas por las enzimas. - Actúa como tampón, regulando el Ph citoplasmático de sus sales minerales y aminoácidos disueltos. Los orgánulos celulares: Se clasifican según tengan membrana o no que los delimitan: Delimitados por membrana: Núcleo Retículo endoplasmático liso y rugoso. Lisosomas Glioxisomas 46 Vacuolas Peroxisomas Aparato de golgi Mitocondria Plastos No delimitados por membrana: Centrosomas Ribosomas El citoesqueleto: Es una estructura tridimensional de filamentos proteicos que se encuentra en el citosol de todas las células eucariotas. Se trata de una estructura dinámica, se ensambla y reorganiza continuamente en función de las necesidades celulares. Está constituido por tres tipos de filamentos proteicos que se mantienen unidos a la membrana plasmática y a los orgánulos celulares. Microfilamentos de actina: (5-7 nm) Son los componentes más delgados del citoesqueleto y están compuestos de actina (proteína globular) en doble hélice dextrógira. Esta doble hélice está formada por dos hebras 3 en las que hay una clara polaridad: uno de los extremos se alarga (positivo) y otro se acorta (negativo). Funciones: - Forman el córtex celular que es una estructura densa situada debajo de la membrana plasmática. Es responsable del mantenimiento de la forma celular y de la ordenación y el desplazamiento de las proteínas de la membrana. - Junto con la proteína miosina son responsables de la contracción muscular. - Forman el anillo contráctil durante la citocinesis de las células animales. - Intervienen en procesos de fagocitosis. Filamentos intermedios: (12nm) Son exclusivos de las células animales y están formados por diferentes tipos de proteínas fibrosas. Son los componentes más estables del citoesqueleto. Su principal función consiste en dar soporte a los orgánulos celulares y proporcionar resistencia mecánica a la célula. 47 Microtúbulos de tubulina:(25nm) Son estructuras tubulares huecas cuya pared está formada por la polimerización de una proteína tubular llamada tubulina. Tubulina alfa + Heterodímeros- Protofilamentos 13 protofilamentos- microtúbulo Tubulina Beta Presentan una polaridad: Se alargan y se acortan. Funciones: - Son el conjunto de microtúbulos que forman el huso mitótico y, a su vez, es responsable del transporte de cromosomas. - Constituyen el centro de las estructuras del flagelo, los cilios y el centrosoma. - Intervienen en la forma celular. - Transporte intracelular de sustancias y distribución de orgánulos y vesículas. El retículo endoplasmático: Es el orgánulo más grande y más desarrollado en la mayoría de las células eucariotas. Está formado por un sistema de endomembranas en forma de túbulos o sacos aplanados llamados cisternas. Estas cisternas se comunican entre ellas formando una red continua que se extiende desde la envoltura nuclear hasta la membrana. La membrana del retículo endoplasmático está formada por una bicapa lipoproteica. Delimita un espacio llamado cavidad luminal. Es un órgano primordial en procesos de síntesis. Ss cavidades luminales constituyen importantes vías de comunicación intracelular, en estrecha relación con el aparato de golgi. Retículo endoplasmático rugoso: Estructura: Está formado por sacos aplanados unidos a la membrana nuclear. Lleva adosados ribosomas que son los que le dan el aspecto rugoso en la parte en contacto con el citosol mediante los riboforinas, unas proteínas de anclaje que unen los ribosomas a los sacos. Funciones: - Síntesis de proteínas de membrana o de secreción: Esta acción es posible gracias a los ribosomas adosados a sus membranas. Tienen dos destinos: -Si son proteínas de membrana, permanecen unidas a la membrana del retículo. -Si son proteínas de secreción atraviesan completamente la membrana y se liberan en las cavidades del retículo. 48 - Glicosilaciones: de las proteínas fabricadas anteriormente. Así se fabrican glucoproteínas. Finaliza en el aparato de golgi. Retículo endoplasmático liso: Estructura: Está formado por túbulos de superficie lisa debido a la ausencia de ribosomas en su cara hialoplasmática. Se encuentra relacionado con el rel. Funciones: - Metabolismo de lípidos: Sintetiza lípidos de membrana, como los fosfolípidos y el colesterol e interviene en la desaturación de ácidos grasos. - Detoxificación: En sus membranas existen enzimas encargadas de metabolizar toxinas, a las que transforman en sustancias menos tóxicas y fácilmente eliminables. - Regulación de la concentración de calcio en el citosol: Capata calcio del citosol para liberarlo en respuesta a señales extracelulares (estímulos nerviosos). - Producción de vesículas de transporte: de proteínas y lípidos recién fabricados para enviarlos hacia el golgi. El aparato de golgi: Está presente en las células eucariotas, particularmente en las que tienen función excretora. Una característica típica del aparato de Golgi es su polaridad. Estructura: Está formado por dictiosomas. El número de dictiosomas varía dependiendo de las células, de dos hasta varias decenas. Cada dictiosoma está formado por un número variable de sacos aplanados, llamados cisternas., delimitados por una membrana lisa y aplanados unos sobre otros sin que las membranas lleguen a tocarse. Con frecuencia, las cisternas aparecen perforadas por poros. Se distinguen dos caras: - Cara proximal: Esta cara se localiza hacia el núcleo. Por ella se incorporan a las cisternas compuestas procedentes del retículo endoplasmático. Vesículas de transición en la cara proximal. - Cara distal: Se orienta hacia la superficie celular. En la periferia existe una población de vesículas de mayor tamaño que las vesículas de transición denominadas vesículas de secreción que contienen los productos de la actividad del aparato de golgi. Función: Embalaje de productos de secreción: 1. Síntesis de proteinas poteen los ribosomas del rer. 49 2. Transferencia de las proteínas al interior del rer. 3. Paso de las proteínas a los elementos transicionales del retículo endoplasmático, sin ribosomas. 4. Inclusión de las proteínas en vesículas de transición que se dirigirán a la cara proximal del aparato dictiosoma. 5. Fusión de las vesículas con la membrana de las cisternas de la cara proximal y liberación de su contenido en el interior de estas. 6. Transporte de las proteínas a través de las cisternas del dictiosoma hasta que llegan a la cara distal. Son modificadas ya que se les añaden glúcidos, grupos fosforilo o ácidos grasos. 7. Clasificación y empaquetamiento de las proteínas en la cara distal en vesículas de secreción. 8. Mediante exocitosis expulsión del contenido de la vesícula al medio extracelular. Fusión de la membrana plasmática con la vesícula. Biogénesis de membranas: Mediante la fusión de membranas de las vesículas de secreción con la membrana plasmática. Formación de orgánulos intracelulares: A partir de orgánulos que permanecen en el citosol, como los lisosomas. LISOSOMAS: Vacuola: Se trata de un orgánulo rodeado por una membrana simple llamada tonoplasto. Se encuentra en las células vegetales en gran abundancia. Cuando un acélula vegetal es juven se encuentran muchas vacuolas diminutas esparcidas pot rl votplasma pero a medida que crecen y se diferencian, las vacuolas se unen hasta construir una gran vacuola central que puede ocupar casi todo el citoplasma, El núcleo queda desplazado a una parte de la célula. La totalidad de las vacuolas se llama vacuoma. Función: Almacenar productos de desecho, sustancias de reserva, sales minerales, sustancias aromáticas o tóxicas, pigmentos hidrosolubles, grandes cantidades de agua. Por ósmosis entra en agua proporcionando turgencia. Los ribosomas: Son orgánulos formados por sustancias ribonucleoproteicas compactas y no delimitadas por membrana formadas por arn ribosómico y proteínas estructurales. Están presentes en el citoplasma de células eucariotas y procariotas. Están formados por dos subunidades, la subunidad grande y la subunidad pequeña. 50 Estructura Localización Ribosomas 70 S Ribosomas 80 S Subunidad 50 S (grande) Subunidad 30 S (pequeña) Subunidad 60 S (grande) Subunidad 40 S (pequeña) - Función citoplasma de las células procariotas matriz de mitocondrias estroma de cloroplastos - - citoplasma de las células eucariotas adosado a la cara citoplasmática del rer adosados a la cara citoplasmática de la membrana nuclear externa Biosíntesis de proteínas o traducción de una secuencia de nucleótidos de una cadena de ARNm en una secuencia de aminoácidos concreta. Polirribosoma (conjunto de ribosomas unidos a una cadena de ARNm) Centrosoma: Solo existe en las células animales y debe estar situado junto al núcleo. Estructura: - Diplosoma: Está formado por dos centríolos dispuestos perpendicularmente uno del otro. - Material pericentriolar: Es la región de aspecto amorfo que rodea el diplosoma. - Fibras de áster: Microtúbulos que irradian a partir del material pericentriolar. El centriolo Funciones: Son centros organizadores de microtúbulos. En consecuencia se encargan de la formación del huso mitótico, los cilios y flagelos y los componentes microtúbulos del citoesqueleto. Cilios y flagelos: Son digitaciones móviles de la superficie celular que están delimitados por la membrana plasmática.Gracias a su movimiento, las células se pueden desplazar en el medio en el que están. Cilios: Son cortos y numerosos, se disponen en hileras sucesivas llamadas cinétidas. Flagelos: Son largos y escasos. Están presentes en los espermatozoides. Mitocondria: conjunto de mitocondrias es llamado condrioma. 51 Existen en el citoplasma de todas las células eucariotas aerobias. Es mayor en células que requieren de altos requerimientos energéticos como las musculares ya que necesitan más ATP. Estructura: Matriz mitocondrial: Es la parte central de la mitocondria. Está delimitada por la membrana mitocondrial interna. En ella se distinguen estos elementos: Adn mitocondrial, mitorribosomas, iones, metabolitos y enzimas responsables de: La carboxilación oxidativa del piruvato, el ciclo de Krebs, síntesis proteica, beta oxidación de los ácidos grasos. Espacio intermembrana: Es el espacio que separa la membrana interna de la externa. Debido a que la membrana externa es semipermeable su composición es muy parecida al citosol. Membrana mitocondrial externa: Es una membrana continua, en contacto con el citosol. Está formada por varias proteínas entre las que destacan las porinas que la hacen completamente permeable al agua. aminoácidos… Membrana mitocondrial interna: Es una membrana continua rodeada por la membrana mitocondrial externa que está orientada hacia la luz de la mitocondria, las crestas mitocondriales. Es impermeable para metabolitos e iones, que solo pueden entrar en ella a través de un transporte específico. Elevada cantidad de proteínas entre las que destecan: -Proteínas de la cadena respiratoria. - Proteínas de transporte de metabolitos entre la matriz y el citosol. - ATPasa mitocondrial, responsable de la fosforilación oxidativa. Mitorribosomas: Son los ribosomas mitocondriales de coeficiente 70 S. Las proteínas de estos ribosomas proceden del citosol. ADN mitocondrial: Es un ADN circular y desnudo, similar al ADN bacterial y cloroplasto, Codifica la síntesis de aprox 5% de las proteínas mitocondriales, concediendoles a las mitocondrias cierta autonomía con respecto al núcleo celular. ATPasa mitocondrial: Es un complejo proteico que incluye dos componentes: Componente F1 y componente F0: Componente f1: Está formado por proteínas periféricas que se disponen en forma de gajo alrededor de un eje. Es el responsable directo de la síntesis de ATP acoplada al transporte de electrones en la cadena respiratoria (fosforilación oxidativa). 52 Componente F0: Formado por proteínas transmembrana que forman un poro por el que fluyen los protones que estimulan la síntesis acoplada de ATP en el F1. Función: Generan ATP mediante procesos metabólicos conocidos como respiración celular. - Oxidación de metabolitos: A través de la descarboxilación oxidativa, el ciclo de Krebs y la beta- oxidación de los ácidos grasos. - Obtención de ATP mediante la fosforilación oxidativa que es dependiente de la cadena de transporte de electrones. - Formación de precursores de las principales rutas anabólicas. En sus ribosomas sintetizan una gran parte de sus proteínas. 53 El metabolismo: catabolismo La nutrición celular y el metabolismo: La nutrición es el proceso global de intercambio y transformación de materia y energía en un organismo y cada una de sus células. Comprende tres procesos: Ingestión, metabolismo y excreción. El metabolismo es la suma de todas las transformaciones químicas que se dan en el interior de un organismo. Es una actividad celular muy coordinada, construida por series de reacciones químicas que se acoplan perfectamente→ llamadas rutas metabólicas. Rutas metabólicas Una ruta metabólica es una secuencia ordenada de reacciones consecutivas que están catalizadas y reguladas por enzimas específicas. El producto de la primera reacción se transforma en el sustrato de la segunda y así sucesivamente. El sustrato inicial, el precursor, se convierte en el producto final, los compuestos intermediarios de la ruta son los intermediarios metabólicos o metabolitos. - Rutas lineales: Son secuencias de reacciones en cadena, el producto de una reacción→ reactivo de la siguiente. - Rutas ramificadas: En ellas se forman varios productos a partir de un precursor→ un metabolito participa a la vez en dos o más reacciones. - Rutas cíclicas: Los intermediarios metabólicos no se consumen durante la transformación del precursor en producto. CARACTERÍSTICAS DE LAS REACCIONES DE LAS RUTAS METABÓLICAS: - Son globalmente irreversibles y están reguladas. - Se producen en un medio acuoso. - Sus reacciones ocurren de forma encadenada y acoplada. - Si liberan energía→ exergónicas y si la consumen→ endergónicas. - En las células eucariotas se localizan en compartimentos celulares específicos lo que facilita su regulación. - Cada reacción está catalizada por una enzima específica, estrictamente regulada. 54 PROCESOS METABÓLICOS: En la célula se diferencian dos procesos metabólicos que ocurren simultáneamente en el interior de la célula y se encuentran interconectados a través de rutas catabólicas y anabólicas. Muchas veces el límite entre el anabolismo y el catabolismo no es claro por lo que existen rutas anfibólicas, que pertenecen a los dos procesos. - Catabolismo: Es la fase de la degradación del metabolismo: las moléculas complejas se oxidan y forman moléculas sencillas. El catabolismo genera energía , que se emplea en el trabajo celular y en las reacciones del anabolismo. Rutas catabólicas: - Son rutas oxidativas. - Liberan energía en forma de ATP. - Generan poder reductor en forma de coenzimas reducidas NADH y FADH2. - Son rutas convergentes que a partir de varios precursores obtienen los mismos productos. - Glucólisis y beta-oxidación. - Anabolismo: Es la fase de la biosíntesis del metabolismo: las moléculas sencillas se reducen y dan lugar a moléculas complejas. Las moléculas sintetizadas en el anabolismo se utilizan para el crecimiento y la renovación celular, también se almacenan en modo de reserva para su posterior uso en el catabolismo. Rutas anabólicas: - Son rutas reductoras. - Requieren energía en forma de ATP. - Necesitan una fuente de poder reductor que aportan los electrones de las coenzimas reducidas nadh, nadph y fadh2. - Son rutas divergentes: A partir de unos cuantos precursores se forman una gran cantidad de productos. - Ciclo de Calvin. Rutas anfibólicas: - Son rutas mixtas, anabólicas y catabólicas. - Poseen reacciones oxidativas en las que se produce energía (ATP) y poder reductor (NADH y FADH2) - Generan precursores para la biosíntesis de moléculas en las rutas anabólicas. - Ciclo de krebs y ciclo de la urea. 55 Procesos energéticos del metabolismo: Las rutas metabólicas son impulsadas por la energía química que proporcionan dos grupos de biomoléculas esenciales en el metabolismo: - Las coenzimas Nadh, nadph y Fadh2, que suministran la energía de óxido-reducción. - ATP (y en menor medida GTP) que almacenan energía en su enlace anhídrido fosfórico entre grupos fosfatos. Transferencia de electrones en el metabolismo: Se oxida: pierde electrones. Se reduce: Gana electrones. Transferencia de grupos fosfato: Fosforilación-desfosforilación. Enlaces anhídrido fosfórico del ATP. Los nucleótidos trifosfato entre los que destaca el ATP almacenan una gran cantidad de energía en los enlaces anhídrido fosfórico que se establecen entre sus grupos fosfato. Las reservas de ATP en el organismo duran pocos segundos por lo que es necesaria su síntesis continua. Esto es posible gracias a la energía que aportan las reacciones catabólicas. Mecanismos de síntesis de ATP en la célula: -Fosforilación oxidativa: Se trata de la síntesis de ATP que se produce acoplada a la cadena de transporte de electrones de la mitocondria y la fase luminosa de la fotosíntesis. Es la ruta más importante de síntesis de ATP en condiciones aeróbicas. 56 Las enzimas que catalizan esta reacción son las ATPasas o ATP sintasas que aprovechan la energía que se libera cuando las atraviesa un flujo el gradiente de protones H+ a favor para fosforilar ADP transformándolo en ATP. -Fosforilación a nivel de sustrato: La síntesis de ATP se produce acoplada a ciertas reacciones catabólicas, altamente exergónicas. Glucólisis y ciclo de Krebs. Representa la única forma posible de síntesis de ATP en condiciones anaeróbicas. Las enzimas que catalizan esta síntesis son las quinasas. El catabolismo: Comprende reacciones degradativas y de oxidación que requieren de compuestos orgánicos de partida y un aceptor final de los electrones que se liberan en las oxidaciones catabólicas. Glúcidos→Glucólisis→ Citoplasma/Estroma de los cloroplastos Piruvato→Fermentación→Citoplasma Ciclo de Krebs→ Matriz mitocondrial Cadena respiratoria y fosforilación oxidativa→ Crestas mitocondriales - Respiración Aeróbica: Se usa el oxígeno como aceptor final de los electrones. Se obtiene atp a través de la fosforilación oxidativa y la fosforilación a nivel de sustrato. Es el catabolismo más extendido y el de mayor eficiencia energética. En células eucariotas y en protoctistas y mayoría de hongos y bacterias. - Respiración Anaeróbica: Su aceptor final son compuestos inorgánicos pero nunca el oxígeno. Produce síntesis de atp mediante los procesos de fosforilación oxidativa y fosforilación a nivel de sustrato. Solo existe en algunas bacterias y tiene mayoe eficiencia energética que la respiración aeróbica→ Ciclos biogeoquímicos. - Fermentación: Se usa un compuesto orgánico (piruvato) como aceptor de los electrones. La reducción del piruvato origina diversos compuestos orgánicos como el etanol y el ácido láctico. Solo produce Atp mediante fosforilación a nivel de sustrato. Posee mucho menor rendimiento energético que la respiración. Algunos grupos de bacterias, hongos y células musculares esqueléticas de los animales vertebrados. 57 El catabolismo de los glúcidos: La Glucosa es el glúcido que más se emplea para obtener energía. Cualquier otro glúcido debe convertirse en glucosa para su catabolización. Se obtiene energía a través de la glucosa mediante la respiración celular o la fermentación. Ambos procesos comparten la misma ruta metabólica inicial: La glucólisis pero siguen rutas metabólicas diferentes. El catabolismo de la glucosa por respiración: Consiste en un flujo de electrones desde la molécula a la glucosa (elevado contenido energético) hasta co2 y h2o (bajo contenido energético), en un proceso acoplado a la síntesis de atp. FÓRMULA: C6H12O6 + O2→ H2O+ CO2+ 38 (36) atp La degradación de la glucosa por respiración aeróbica comprende tres rutas metabólicas consecutivas: - La glucólisis: Es la oxidación citoplasmática de la glucosa para obtener piruvato, atp y nadh. - El ciclo de Krebs: Es la oxidación del Acetil-CoA que se obtiene de la descarboxilación oxidativa del piruvato para obtener CO2, NADH, FADH2 y ATP. En las células eucariotas se produce en la matriz mitocondrial y en las procariotas en el citosol. - La cadena respiratoria: Es la reoxidación de los NADH y los FADH que ceden sus electrones al oxígeno molecular. Este oxígeno se reduce formando agua. Esto se produce mediante una serie de reacciones de óxido-reducción en las que participan los transportadores de electrones de la membrana mitocondrial interna (eucariotas) o de la membrana plasmática (células procariotas). La energía que se libera en este transporte electrónico está acoplada a la síntesis de atp. La glucólisis: Es una ruta catabólica lineal y anaerobia (Se desarrolla en ausencia de oxígeno). Ocurre en todas las células tanto en eucariotas como procariotas en el hialoplasma celular por lo que se trata de una ruta citoplasmática. Excepción→ células vegetales fotosintéticas en el que la glucólisis se da en el estroma de los cloroplastos. La glucosa se oxida para obtener piruvato, atp y nadh. 58 Procedencia de la glucosa: En las células eucariotas animales: - Difusión facilitada a través de la membrana celular. - Degradación del glucógeno de reserva intracelular. - Hidrólisis digestiva de los glúcidos que se ingieren en la dieta (almidón, lactosa, sacarosa) Los monosacáridos resultantes (fructosa, galactosa y glucosa) se incorporan a la glucólisis. - Gluconeogénesis o síntesis a partir de precursores no glucídicos. En los animales los precursores de la glucosa son compuestos de tres carbonos: piruvato, lactato, glicerol, intermediarios del ciclo de krebs y aminoácidos. No glioxisomas→ no sintetizan glucosa a partir de compuestos de dos carbonos (acetil-coA). En las células eucariotas vegetales: - Degradación del almidón que se obtiene de la fotosíntesis.→ cloroplastos de las células fotosintéticas. - Hidrólisis de la sacarosa fabricada en la fotosíntesis→ hialoplasma de las células no fotosintéticas. - Gluconeogénesis a partir de precursores no glucídicos. Las plantas pueden sintetizar glucosa a partir del acetil-coA que resulta de la degradación de los ácidos grasos gracias a la ruta del ciclo glioxilato que tiene lugar en los glioxisomas. Acetil-coA→ intermediario ciclo de Krebs→ sacarosa se forma mediante gluconeogénesis. Se divide en: 1 Fase preparatoria de la glucólisis: A partir de una glucosa se obtienen 2 moléculas de gliceraldehido 3-fosfato. Se consume la energía de 2 atp. 2 fase de beneficios de la glucólisis: Por cada molécula de gliceraldehido 3-fosfato se obtienen: 1 piruvatos 1 molécula de coenzima reducida Nadh dos moléculas de ATP sintetizadas mediante fosforilación a nivel de sustrato. Balance neto: glucosa+ ADP+ pi+nad+→ 2piruvatos+2atp+2nadh+ 2h+ +2h20 59 El ciclo de krebs: - Es una ruta metabólica cíclica mediante la cual el piruvato que se genera en la glucólisis se oxida completamente en condiciones aeróbicas produciendo co2 y energía química. - En ella confluyen las rutas catabólicas de ácidos grasos y aminoácidos. - Se considera una ruta anfibólica. Ingreso del piruvato en el ciclo de krebs: descarboxilación oxidativa: El piruvato se origina en el citoplasma mediante la glucólisis, atraviesa las membranas mitocondriales externa e interna hasta llegar a la matriz mitocondrial. Antes de ingresar en el ciclo de krebs, el piruvato debe experimentar una etapa previa, la descarboxilación oxidativa, que cataliza el complejo multienzimático piruvato deshidrogenasa . Este se usa como coenzima del pirofosfato de tiamina. Ocurren estas reacciones: - El grupo carboxilo se elimina como dióxido de carbono (descarboxilación) - El grupo carbonilo se oxida simultáneamente (descarboxilación oxidativa) cediendo sus electrones a una molécula de Nad+ que se reduce a nadh y forma un grupo acetilo. - El grupo acetilo recién creado se esterifica, por formación de un enlace tioéster con el grupo -SH de la coenzima A. El resultado es una molécula de Acetil coenzima a que ingresará directamente al ciclo de krebs. - Se obtiene 2 Fadh2, 6 nadh, 4 co2 y 2 gtp La cadena respiratoria y la fosforilación oxidativa: Son procesos perfectamente acoplados, la primera se paralizaría si no se verificara la segunda. Ambos procesos se sitúan en la membrana plasmática de las células procariotas o en la membrana mitocondrial interna de las células eucariotas. Su función es doble: - Regenerar las formas oxidadas de las coenzimas reducidas. Esto es imprescindible para que se vuelvan a usar en las correspondientes reacciones glucolíticas o en el ciclo de krebs. - Sintetizar Atp de forma acoplada al transporte electrónico de la cadena respiratoria. Así la energía química que contienen las formas reducidas de las coenzimas se recupera mediante energía química, útil para la célula. La cadena respiratoria: Está formada por una serie de transportadores de electrones. En su mayoría proteínas integrales o transmembrana con grupos prostéticos portadores de elementos metálicos (Fe o Cu). Estos transportadores captan o ceden electrones secuencialmente por lo que se origina una cascada de óxido-reducción. Esta cascada se inicia en las coenzimas 60 reducidas NADH y FADH2 que proceden de la glucólisis y el ciclo de krebs, y culmina en el aceptor final: que se reduce y da agua. En la mitocondria de los animales se localizan cuatro complejos: - Complejo I o NADH deshidrogenasa: Contiene grupos prostéticos FNM. Transfiere los electrones desde el NADH a la ubiquinona (coenzima q) que difunde libremente por la bicapa. Sólo recoge los electrones de los NADH de la matriz mitocondrial. - Complejo II o succinato deshidrogenasa: Cataliza el paso 6 del ciclo de Krebs. Sus prostéticos son FAD y transfiere los electrones del FADH2 a la ubiquinona. - Complejo III o complejo ubiquinol-citocromo-c-oxidoreductasa: Contiene como grupo prostético el grupo hemo. Transfiere los electrones desde la ubiquinona al citocromo c en el espacio intermembranal. - Complejo IV o citocromo oxidasa: Contiene como grupo prostético el grupo hemo, además de átomos de Cu que son los responsables del transporte de electrones desde el citocromo c al O2, el cual se reduce y da agua. LA FOSFORILACIÓN OXIDATIVA: HIPÓTESIS QUIMIOSMÓTICA DE MITCHELL: Es la síntesis de ATP mediante la fosforilación de adp de forma acoplada a la oxidación de componentes de la cadena de transporte de electrones. La hipótesis quimiosmótica establece que la fosforilación ocurre según dos fases acopladas: - Formación del gradiente de electrones: El transporte electrónico de la cadena respiratoria (desde el Nadh y fadh2 hasta el oxígeno) provoca un bombeo de protones hacia el espacio intermembranal a través de la membrana mitocondrial interna. Los puntos de bombeo de protones son los complejos I, III y IV. La acumulación de los h + en el espacio intermembrana genera un gradiente electroquímico de protones muy enérgico entre el espacio intermembrana y la matriz: el espacio intermembrana se hace más positivo y más ácido que la matriz. - Uso del gradiente de electrones para sintetizar ATP: El equilibrio quimioeléctrico se consigue mediante el regreso de los protones a la matriz a través del complejo atp sintasa de las crestas mitocondriales. La energía que se libera la usa el propio complejo V o ATP sintasa para sintetizar ATP a partir de ADP y Pi. El gradiente protónico que ha generado el transporte electrónico acopla la fosforilación con la oxidación. 61 - Balance energético de la fosforilación oxidativa: Por cada NADH se obtienen 3 atp aunque aquellas células que utilizan la lanzadera 3-p reduce el rendimiento de estos 2 nadh a 4 atp. La reoxidación del FADH2 que transfiere sus electrones al complejo II da lugar a 2 atp por cada fadh2 que se reoxida. Rendimiento neto del atp→ 36 a 38 atp. EL CATABOLISMO DE LA GLUCOSA POR FERMENTACIÓN: La fermentación es una ruta metabólica lineal citoplasmática y anaeróbica que implica dos rutas consecutivas: Glucólisis y fermentación. La fermentación permite regenerar el Nad+ (imprescindible para que la glucólisis suceda) mediante la reoxidación de los nadh al transferir sus electrones una molécula orgánica, que normalmente es el piruvato que se ha generado la glucólisis. Fermentación alcohólica y láctica. Fermentación alcohólica: (el ser humano no la hace). El piruvato se transforma en etanol, con desprendimiento de CO2 en una secuencia de dos reacciones: 1. Descarboxilación del piruvato con lo que se produce el acetaldehído. 2. Reducción del acetaldehído a etanol a expensas de los electrones que cede el NADH glucolítico. Las levaduras saccharomyces originan este tipo de fermentaciones. Fermentación Láctica: El piruvato se convierte en lactato (ácido láctico), mediante su reducción a partir de los electrones que cede el Nadh glucolítico. Producen esta fermentación las bacterias streptococcus y lactobacillus; las células musculares de los vertebrados, cuando se les somete a una actividad física tan intensa que no reciben suficiente aporte de oxígeno y los eritrocitos que no tienen mitocondrias. El catabolismo de los lípidos: Los triacilglicéridos→ principal reserva energética de los animales. Para su uso como fuente energética las enzimas lipasas deben hidrolizar las grasas previamente: de esta hidrólisis resultan el glicerol y ácidos grasos: 62 - El glicerol sufre una fosforilación a expensas de un atp y se origina glicerol 3-fosfato. El glicerol 3-P se oxida y forma NADH y dihidroxiacetona fosfato que se incorporan a la glucólisis. - Los ácidos grasos se activan y se introducen en las mitocondrias o en los peroxisomas, ruta metabólica cíclica→ beta oxidación o hélice lynen. La degradación de los ácidos grasos: Se realiza en cinco etapas: activación, transporte, beta oxidación, ciclo de krebs y cadena respiratoria. Beta-oxidación: Sucede en los peroxisomas de las células vegetales y en los peroxisomas y la matriz mitocondrial de las células animales. Los tres primeros pasos implican la oxidación del carbono beta (segundo carbono a partir del grupo carboxilo) del acil-CoA a través de un proceso similar a la conversión de succinato en oxalacetato durante el ciclo de Krebs. La división del carbono alfa y beta genera acetil-coA que tiene dos carbonos menos que el acil-CoA. El proceso se repite hasta que todo el Acil-coA se divide en Acetil-CoA. Balance neto: 63 El metabolismo: anabolismo El anabolismo comprende reacciones biosintéticas que requieren: - Una fuente de materia como punto de partida. - Una fuente de energía para que se lleven a cabo reacciones endergónicas. - Una fuente de electrones para reducir los precursores metabólicos. Seres vivos fotoautótrofos: Para sintetizar sus biomoléculas utilizan: - El CO2 como fuente de carbono. - La luz solar como fuente de energía. - Compuestos inorgánicos (H20, H2, S….) como fuente de electrones. Plantas, algas, algunas bacterias y las bacterias rojas y verdes del azufre. Anabolismo fotoautótrofo: La fotosíntesis: La fotosíntesis es el proceso mediante el cual los organismos fotoautótrofos captan la luz solar y la utilizan como fuente de energía para la síntesis de compuestos orgánicos a expensas de contenidos inorgánicos de bajo contenido energético presentes en el medio: CO2… Fases de la fotosíntesis: - Fase luminosa: La energía luminosa se transforma en energía química (ATP Y NADPH) que se empleará en la fase oscura. Las características son: - Se produce en la membrana de los tilacoides en las eucariotas y en las cianobacterias en los tilacoides intracitoplasmáticos. - Depende de la luz solar para producirse. - Convierte la energía luminosa en química en forma de atp y nadph. - Usa h2o como fuente de electrones, esto hace que se libere o2 a la atmósfera. - Fase oscura: la energía química fabricada en la fase luminosa se usa para reducir el co2, NO3- y SO₄²-. en compuestos orgánicos. La ruta metabólica más destacada es el ciclo de calvin. Las características son: - Suceden en el estroma de las células eucariotas y en el citoplasma de las células procariotas. - No dependen directamente de la luz para producirse. 64 - Utiliza el atp y el nadph de la fase luminosa para reducir el co2 en hexosas y el NO3- y el SO₄²- en grupos amino (-hn2) y tiol (-sh) componentes de los aminoácidos o nucleótidos. - Restituye el adp y el nadp+ a las reacciones de la fase luminosa. La fase luminosa o fotoquímica: La transformación de la energía luminosa en nadph y atp requiere de los siguientes componentes y procesos: fotosistemas, transporte electrónico fotoinducido y fotofosforilación. Los fotosistemas: Es una agrupación funcional de pigmentos (clorofilas e isoprenoides) capaces de captar fotones de la luz solar. Se localizan en las membranas tilacoidales de las células eucariotas y cianobacterias y en la membrana plasmática del resto de células procariotas. Componentes: - Antena: Está formada por una gran variedad de pigmentos especializados en absorber energía luminosa, que será transferida rápidamente al centro de reacción fotoquímico. Los pigmentos más abundantes en las células eucariotas son los isoprenoides: el beta-caroteno (naranja) y las xantofilas (amarillo). - Centro de reacción fotoquímico: Está integrado por moléculas de clorofila diana. El tipo de clorofila en las plantas, algas y cianobacterias es la clorofila a que capta la luz roja y azul y refleja la verde (de ahí su color). Al recibir la energía captada por los pigmentos de la antena, las moléculas de clorofila se oxidan y pierden un electrón por cada fotón (hv) que reciben. Este electrón, rico en energía es captado por el primer miembro de una cadena transportadora de electrones, así, la energía luminosa se convierte en química. Tipos de fotosistemas: Fotosistema I (PS i) o p700 : Está localizado en unas partículas pequeñas y esféricas, situadas principalmente en los tilacoides del estroma. La clorofila diana capta fotones con una longitud igual o menor a 700 nm. Fotosistema ii (PS ii) o p680: Está localizado en pequeñas partículas ovoides, situados en los tilacoides apilados en granas. La clorofila diana capta fotones con una longitud de onda igual o menor a 680 nm. 65 TRANSPORTE DE ELECTRONES FOTOINDUCIDO: Proceso clave de la fotosíntesis→ fotólisis del agua. Consiste en la rotura de moléculas de h20 por la luz y la cesión de sus electrones a algún aceptor, el nadp+. Proceso global expresado a través de la ecuación de hill: 2h2o + 2nadp+ → o2 + 2nadph + 2 h+ El flujo de electrones de h2o hasta el nadp+ necesita la intervención de diversos transportadores de electrones de la membrana tilacoidal y lo impulsa la energía solar→ transporte de electrones fotoinducidos. Tipos: - Transporte acíclico (en z): En este fotosistema ocurren una serie de reacciones de óxido-reducción en las que intervienen los fotosistemas I y II y en las que el dador de electrones es la molécula del agua. - Transporte electrónico fotoinducido en el PS I: La molécula de clorofila a diana del centro de reacción del ps I es excitada por dos fotones, como resultado la clorofila se oxida y pierde dos electrones. Estos fotones son captados por la ferredoxina (Fd), pequeña proteína soluble del estroma, que a su vez, los transfiere al nadp+, el cual se reduce y forma el nadph. La oxidación de la ferredoxina para ceder sus electrones al nadp+ está catalizada por la ferredoxina NAD+ oxidorreductasa (FNR). - Transporte electrónico fotoinducido en el PS II: La molécula de clorofila a diana del centro de reacción del ps II es excitada por dos fotones, oxidándose y dando lugar a dos electrones. Estos electrones ingresan en una cadena transportadora de electrones cuyo último paso será la reducción de la molécula de clorofila a del PS I que quedó oxidada al ceder dos electrones a la ferredoxina. Así la clorofila a I es reducida y está en condiciones de volver a ser excitada por nuevos fotones. La cadena de conexión entre PS I y PS II implica, de forma secuencial, la oxidación-reducción de los siguientes componentes de la membrana tilacoidal: plastoquinona, complejo b6f, plastocianina y PS I. En la transferencia de la plastoquinona hasta la plastocianina se bombean a través del complejo B6F dos protones al espacio intratilacoidal por cada electrón transportado. - Fotólisis del agua: La clorofila a II se reduce y vuelve a su estado inicial a expensas de dos electrones liberados de una molécula de agua, que representa el dador inicial de electrones. 66 La oxidación de la molécula está catalizada por la deshidrogenasa, que contiene magnesio y genera ½ o2, 2 e-, 2 h+. El oxígeno se libera a la atmósfera y los protones se acumulan en el espacio intratilacoidal. Producción de oxígeno a expensas del agua→ oxigénico. - Transporte cíclico (en d) Ocurre en una serie de etapas de óxido-reducción secuenciales en las que solo está implicado el fotosistema i. No produce oxígeno por lo que se llama anoxigénico. Durante el transporte cíclico, un electrón de la clorofila a del ps i, excitado por un fotón, es transportado por la ferredoxina directamente al complejo b6f, de forma que la clorofila i recupera su electrón a través de la plastocianina. El resultado neto es el bombeo de 2 protones extra al espacio intratilacoidal. Supone una fuente extra de atp para la célula ya que se genera un déficit de atp en la fase luminosa. LA FOTOFOSFORILACIÓN: Es la síntesis de atp, se produce mediante la fosforilación de adp, de forma acoplada al transporte de electrones fotoinducido durante la fotosíntesis. Se divide en dos etapas: - Generación del gradiente de protones: El transporte de electrones fotoinducido, desde el h2o hasta el nad+ genera 14 h + por cada nueve fotones de luz. Gracias al transporte de electrones de la membrana intratilacoidal. Se genera un gradiente electroquímico de protones entre el espacio intratilacoidal y el estroma, debido a la diferencia de ph y carga eléctrica entre ambos compartimentos. - Utilización del gradiente para sintetizar ATP: Un flujo a favor del gradiente de regreso al estroma a través de un complejo atp sintasa orientado hacia el estroma libera energía suficiente para sintetizar 3 tap por cada 14 h+. Balance neto de la fase luminosa: 9hv+ 2h2o+2nadp++adp+pi→o2+2nadph +3atp + 2h+ 67 La fase oscura o biosintética: el ciclo de calvin. La reducción de Co2 se realiza a través de una ruta cíclica en la que los organismos fotoautótrofos o fotosintetizadores fijan el dióxido de carbono. El Co2 es reducido en una hexosa, usando la energía química Nadph y atp que se fabrica durante la fase luminosa. Este ciclo se realiza en el estroma de los cloroplastos de las células eucariotas vegetales y en el citoplasma de las células procariotas fotosintéticas. Se divide en tres fases: Fase de fijación o carboxilación: El co2 entra en el ciclo mediante la condensación con una molécula de 5 carbonos: ribulosa 1, 5-bifosfato (RuBiP) Se forma un intermediario inestable de seis carbonos que rápidamente se hidroliza formando dos moléculas de 3-fosfoglicerato por cada co2. La enzima que cataliza este proceso es la ribulosa 1, 3-bifosfato carboxilasa/oxigenasa (RiBisCO) ribulosa 1, 3-bifosfato → 3- fosfoglicerato Fase de reducción: Cada 3-fosfoglicerato formado en la primera fase sufre dos fases consecutivas que requieren gasto energético en forma de ATP y NADPH: - Fosforilación: a expensas de 1 atp que da 1,3-fosfoglicerato. - Reducción: gliceraldehido 3-fosfato mediante el poder reductor del nadph. Fase de regeneración: Se regenera la ribulosa 1, 5-bifosfato consumida en la fase de reducción. De cada doce moléculas de triosa fosfato producidas , 10 se convierten en 6 de ribulosa. Las dos molécula restantres de triosa fosfato pueden seguir dos destinos: - Permanecer en el estroma→ biosíntesis del almidón para almacenar energía en el cloroplasto (reserva energética)→ Fructosa 1-bifosfato. - Pasar al citoplasma donde se transformará en glucosa 6-fosfato o fructosa 6-fosfato para su posterior conversión en sacarosa que se transporta a los tejidos de crecimiento o serán degradadas como fuente de energía. Ecuación global de la fotosíntesis: 54hv+ 3co + 6 h2o→ c6h12o6+ 6 o2 Ecuación global del ciclo de Calvin: 6 RuBiP + 6 Co2+12 NAPDH+ 18 ATP+ 12H+→ 6 RuBiP+ C6H12o6+H2O+12 nadp+ 18 adp+ 18 pi Fase oscura o biosintética: la fijación del nitrógeno, azufre y fósforo. 68 Genética molecular La genética molecular estudia los mecanismos de la transmisión y expresión de la información genética que determinan las funciones y estructuras celulares. La expresión génica: Es la decodificación de la información contenida en una secuencia de ADN, es decir en un gen, en un polipéptido concreto. El proceso de la expresión génica implica dos pasos consecutivos: La transcripción y la traducción. El gen como unidad de transcripción: Los genes que llevan información para producir proteínas se transcriben y forman arn mensajero que se traduce formando polipéptidos. Hay algunos genes que no se traducen, que sólo se transcriben. Como el ARN ribosómico, los transferentes o los pequeños nucleares. Realiza funciones estructurales y catalíticas. Regiones del gen: Región promotora: Es una secuencia no codificante que posee unas secuencias consenso de bases específicas que señalizan el inicio del gen y el nucleótido de la secuencia donde se debe realizar la transcripción. Región codificante: Es una secuencia de bases que tiene la información necesaria para la síntesis de una cadena de arn específica. Comienza en el primer nucleótido que se transcribe y acaba en el último. La posición de estos nucleótidos viene marcada por la región promotora y la terminadora. Región terminadora: Son una región no codificante. Son unas secuencias terminadoras específicas que marcan el final del gen y de la transcripción. Al terminar la secuencia de terminación se desembala el complejo transcripcional y se libera el arn transcrito. La transcripción: j 69 Ingeniería Genética El ADN recombinante: La ingeniería genética es la rama de la genética que se dedica a manipular o transferir material genético de un organismo a otro, con el fin de obtener, a través de su expresión, productos específicos e innovadores de utilidad para el ser humano. Tecnología del adn recombinante: El conjunto de técnicas y procedimientos de la ingeniería genética que permiten analizar y modificar el ADN. ADN recombinante: nuevas combinaciones de segmentos o moléculas de ADN que no se encuentran juntas de manera natural, moléculas mixtas obtenidas mediante la unión de secuencias de ADN que provienen de diferentes fuentes biológicas. Tecnología del adn recombinante: Herramientas moleculares: - Materias primas moleculares: Para manipular las moléculas de ADN en el laboratorio → Materiales moleculares de partida: ADN que interesa desoxinucleótidos oligonucleótidos sintéticos ARNmensjero producto del gen de interés Los oligonucleótidos sintéticos son fragmentos de ADN de cadena simple que se sintetizan en el laboratorio por adición de nucleótidos en el orden deseado por el investigador. A través de ellos es posible fabricar genes artificiales o fragmentos de un gen, así como cebadores para la síntesis o secuencia de otros fragmentos de ADN. - Enzimas: La ingeniería genética se sirve de las mismas enzimas que usa la célula para duplicar y transferir la información genética: polimerasas, primasas, ligasas y nucleasas. Polimerasas: transcriptasa inversa (descubierta en el retrovirus) y permite sintetizar ADN bicatenario a partir de ARNm. El ADN codificado de este modo se llama ADN complementario y está desprovisto de intrones. 70 Nucleasas: Endonucleasas de restricción: Pueden cortar el ADN en secuencias específicas y se descubrió en el bacteriófago lambda. - Vectores de clonación: Son moléculas en las que se inserta el ADN de interés para su posterior introducción en células hospedadoras que se encarguen de que este ADN se replique. Los tipos de vectores empleados dependen de si los hospedadores son eucariotas o procariotas: Hospedadores procariotas: Se usan como vectores los plásmidos, bacteriófagos o fagos y cósmidos. Hospedadores eucariotas: Se usan como vectores ADN virales que proceden de virus infectivos. - Células hospedadoras: Son las células en las que se insertará el gen que se va a manipular. Se elige el hospedador según: -Facilidad de manipulación de la célula hospedadora mediante las técnicas de ingeniería genética. -Posibilidad de multiplicación en el laboratorio. -Características del producto que se desea obtener. -Procariotas: Escherichia coli. -Eucariotas: Levaduras. Técnicas de manipulación del ADN: - Hibridación: Localización de genes: Se basa en el apareamiento específico entre los pares de bases.Permite localizar el fragmento de ADN o ARNm de interés entre todos los ácidos nucleicos que posee la célula. - Secuenciación del ADN: Se determina la secuencia de nucleótidos de un fragmento de ADN e incluso la secuencia de un genoma completo. Se consigue integrando las secuencias parciales de los fragmentos obtenidos por escisión enzimática. Se consiguen de esta forma mapas genéticos completos. - Reacción en cadena de la polimerasa: Permite amplificar una secuencia de ADN dada, a partir de una pequeña muestra de ADN se generan millones de copias idénticas en pocas horas y sin necesidad de células vivas. Termocicadores. La clonación molecular: 1. Creación de bibliotecas genómicas: Genotecas. 2. Expresión de proteínas recombinantes. 3. Realización de estudios de filiación en medicina forense. 71 4. Obtención de organismos transgénicos. 5. Diagnóstico de enfermedades genéticas y terapia génica. 6. Secuenciación de genomas. HERRAMIENTAS MOLECULARES: Actualmente se tiene una gran cantidad de enzimas y componentes moleculares que permiten manipular y transferir el material genético. Endonucleasas de restricción o Restrictasas: 1. Tienen actividad endonucleasa, es decir, pueden hacer cortes en el interior de las moléculas de ADN. 2. No escinden el ADN al azar, sino que lo hacen en secuencias específicas de nucleótidos, de entre cuatro a ocho pares de bases. Esas secuencias se denominan secuencias diana de restricción que son palindrómicas. Las secuencias palindrómicas son iguales en las dos hebras y simétricas según la complementariedad de bases. 3. Las restrictasas que más se emplean en ingeniería genética escinden el adn en cada cadena por lugares separados del centro geométrico de la secuencia diana , se generan extremos cohesivos que pueden ser 5’ o 3’. Los extremos cohesivos se suelen aparear entre sí. VECTORES DE CLONACIÓN: Son molécula de ADN que se usan como vehículo para introducir el ADN que interesa en la célula hospedadora, en la cual se replicará y se expresará. Características: 1. Son de pequeño tamaño, esto facilita su manipulación y aislamiento. 2. Poseen un origen de replicación que les permite replicarse dentro de la célula hospedadora. 3. Cuentan con marcadores de selección que permiten verificar su presencia en las células hospedadoras. Estos marcadores son genes que confieren resistencia a algún antibiótico, de tal manera que en presencia de este antibiótico, sólo sobreviven las bacterias que hayan incorporado este vector. 4. Presencian secuencias diana únicas para al menos una enzima de restricción. De esta manera, cuando se le inserta el fragmento, el vector se vuelve a armar con la nueva secuencia introducida. 5. Tienen genes con funciones indicadoras en los que se sitúan las secuencias diana. Debido a esto, cuando el gen deseado se introduce en las secuencias diana, el gen 72 indicador queda interrumpido y como resultado, hay un cambio fenotípico en las bacterias. PRINCIPALES TIPOS DE VECTORES: Vectores en organismos procariotas: - plásmidos - Bacteriófago lambda. - Cósmidos. Vectores en organismos eucariotas: - Vectores en levaduras - Vectores en plantas - Vectores en animales 73