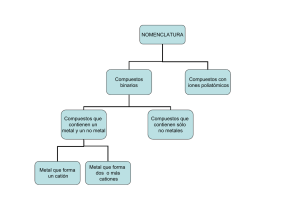
Nomenclatura Química Inorgánica II NOMENCLATURA INORGANICA (RESUMEN) 1. Cationes 1.1. Elementales: no cambia el nombre del elemento. Ej.: Na+ ión sodio O2+ ión dioxígeno Hg2+2 catión dimercurio (2+) ó (I) 1.2. Derivados de hidruros más protón: raíz del anión y terminan en -onio. Ej.: H3O+ oxonio NH4+ amonio H2F+ fluoronio PH4+ fosfonio 1.3. Derivados de ácidos: agregan la terminación -io al nombre del ácido o del anión. Ej.: H4PO4+ tetrahidrogenotetraoxofosfatio CH3COOH2+ etanoico acidio 1.4. Radicales catiónicos: conservan su nombre anteponiendo la palabra "catión" o con desinencia -io. Ej.: NO+ catión nitrosilo NO2+ catión nitroílo OH catión hidroxilo (hidroxilo) CH3+ catión metanilo (metilo) ClO+ catión clorosilo ClO2+ catión cloroílo (clorilo) + 1.5. Cationes heteroatómicos en general: siguen las reglas de coordinación. Ej.: ICl2+ dicloroiodo (+) VF4+ [Al(H2O)6] tetrafluorovanadio (+) +3 hexaacuoaluminio (3+) 2. Aniones 2.1. Homoatómicos: raíz del nombre del elemento y desinencia -uro. Ej.: VI Nomenclatura Cl cloruro I3 triioduro 3 N nitruro N3 azoturo (trinitruro 1-) 2 S sulfuro S22 disulfuro Sn52 pentaestannuro (2-) C22 acetiluro (dicarburo) 2.1.1. Excepción: los derivados del oxígeno se nombran usando la desinencia -ido. Ej.: O2 O3 óxido ozónido (trióxido 1-) O22 peróxido (dióxido 2-) O2 hiperóxido (super) (dióxido 1-) 2.2. Heteroatómicos: usan la desinencia -ato. Ej.: NO3 nitrato (trioxonitrato) SO42 sulfato (tetraoxosulfato) FeO42 ferrato (tetraoxoferrato) ClO3 clorato (trioxoclorato) ICl4 tetracloroiodato Excepciones: 2.2.1. Alguno heteroatómicos por excepción terminan en -uro Ej.: NH2 amiduro NH2 imiduro N2H3 hidrazinuro (diazanuro) CN cianuro HS hidrógenosulfuro 2.2.2. Los derivados del oxígeno: Ej.: terminan en -ido. HO hidróxido HO2 hidrogenodióxido (1) (hidrogenperóxido) 2.2.3. Algunos oxoaniones de valencia menor todavía mantienen la desinencia -ito. Ej.: NO2 nitrito (dioxonitrato) SO32 sulfito (trioxosulfato) ClO hipoclorito (monoxoclorato) VII Nomenclatura 2.3. Oxoaniones con hidrógeno "ácido": usan el prefijo -hidrógeno. Ej.: HSO4 hidrogenosulfato HCO3 hidrogenocarbonato H2PO4 dihidrogenofosfato 2.4. Aniones con otros ligandos: usan el nombre del ligando (cloro-, hidruro-, tio-, etc.). Ej.: [PtCl6]2 hexacloroplatinato 2 [AuF4] tetrafluoroaurato 1 [BH4] tetrahidruroborato S2O82 peroxodisulfato 2 S2O32 tiosulfato (trioxotiosulfato) 3. Acidos En las fórmulas, se escribe primero el hidrógeno, luego el átomo central o característico y luego los ligandos (oxo, cloro, etc.). 3.1. Acidos muy comunes: usan el nombre "ácido". Ej.: HNO3 ácido nítrico H2SO4 ácido sulfúrico H3PO4 ácido fosfórico 3.2. Los menos comunes: se nombran como sales de hidrógeno. Ej.: H[AuCl4] tetracloroaurato de hidrógeno H4[Fe(CN)6] hexacianoferrato (II) de hidrógeno HN3 azoturo de hidrógeno 4. Sales En las fórmulas se escribe en primer término el componente electropositivo seguido del electronegativo. Si hay más de un componente (de una o ambas clases) van en el orden alfabético de sus símbolos químicos. Ej.: NaCl Na2O CaSO4 CaH2 AlCa4O7 AlLiMn2O4(OH)4 En los nombres, va adelante el componente electronegativo seguido del electropositivo. Si hay más de un componente, se nombran en el orden en que figuran en la fórmula (alfabético de símbolos). VIII Nomenclatura Ej.: Na2CO3 carbonato de sodio KMgF3 trifluoruro de potasio y magnesio MgNH4PO4 fosfato de magnesio y amonio AlK(SO4)2.12H2O sulfato de aluminio y potasio, doce de agua Na(UO2)3Zn(CH3COO)9 nonaacetato de sodio, dioxouranio y zinc Ca5F(PO4)3 fluorurotris(fosfato) de pentacalcio MgCl(OH) clorurohidróxido de magnesio BiClO cloruroóxido de bismuto VO(SO4) óxidosulfato de vanadio (IV), si el oxígeno formara parte del catión sería sulfato de oxovanadio (2+) 5. Elementos Símbolos: internacionales Nombres: varían en cada idioma Los símbolos derivan del nombre latino o griego latinizado del elemento. Los nombres propios no se alteran. Debe mantenerse la correspondencia entre nombre y símbolo. Ej.: Na natrium K kalium Cu cuprum Fe ferrum I iodo Y ytrio Yb yterbio Zn zinc Zr zirconio W wolframio (tungsteno en lengua sajona) 6. Elementos superpesados: Nombre y símbolo tienen nomenclatura racional derivada del número atómico. El símbolo está formado por tres letras, la primera en mayúscula, que derivan de prefijos numéricos ad-hoc. 0 nil 5 pent 1 un 6 hex 2 bi 7 sept 3 tri 8 oct 4 quad 9 enn El nombre se forma poniendo en órden de los dígitos del número atómico y con la desinencia -io. Ej.: IX Nomenclatura 105 unnilpentio Unp 109 unnilennio Une 112 ununbio Uub Alrededor del símbolo pueden ubicarse cuatro números: Nro. de masa (arriba a la izquierda) Carga (arriba a la derecha) Nro. atómico (abajo a la derecha) Atomicidad (abajo a la izquierda) Ej.: 32S162- X