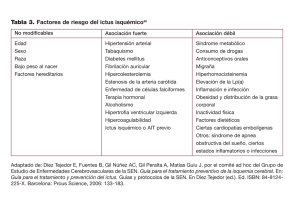
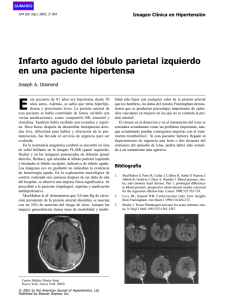
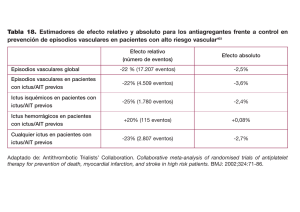
TEMA 1: PATOLOGÍA CEREBROVASCULAR DR. JOSÉ DÍAZ PÉREZ TERMINOLOGÍA Y CLASIFICACIÓN ECV: lesiones del SN que se producen a consecuencia de una alteración en los vasos cerebrales. o Agudas = ICTUS. o Crónicas. Ej: demencia o parkinsonismo vascular. ICTUS: o Isquémicos (85%) o Hemorrágicos (15%) Un ictus es un síndrome o término genérico que requiere precisar todos sus aspectos: etiopatogenia, localización, naturaleza (isquémica o hemorrágica), gravedad o posibilidades terapéuticas. ICTUS ISQUÉMICO 1. IMPACTO - Proceso médico que más estancias hospitalarias, invalidez y mortalidad causa. - La incidencia aumenta de forma progresiva con la edad. - Atención médico-sanitaria escalonada: 1. Prevención primaria de los principales factores predisponentes 2. Diagnóstico y tratamiento urgente del ictus agudo 3. Prevención secundaria 4. Rehabilitación. Un ictus isquémico es un síndrome o término genérico que requiere precisar todos sus aspectos: etiopatogenia, localización, naturaleza (isquémica o hemorrágica), gravedad o posibilidades terapéuticas. 2. FACTORES PREDISPONENTES 2.1 FACTORES NO MODIFICABLES: Edad: La incidencia aumenta con la edad. En > 55 años la incidencia se duplica cada década. Sexo: Más frecuentes en hombres, sobre todo los de patología ateroesclerótica. En mujer es más frecuente entre los 35-44 y > 85 años. Raza: por sí sola no es un factor, existen diferencias incluso dentro de la misma raza así como influencia de otros factores. Más frecuente en raza caucásica, africanos y asiáticos. Genética: No influyen en epidemiología global. Una razón fundamental es el agrupamiento familiar de los 3 principales factores (HTA, DM, DLP). Enfermedades arteriales, hemstológicas, ApoE4. PATOLOGÍA CEREBROVASCULAR 1 2.2 FACTORES MODIFICABLES: Son los más importantes y donde va enfocado las estrategias de prevención primaria y secundaria. HTA: Es el factor más perjudicial. Tanto la TAS como la TAD. Hasta en un 70 % de los pacientes con ictus. La HTA incrementa de 2 a 4 veces el riesgo de ictus y su control disminuye de un 38 a 42 % la incidencia. DM: Su verdadero peso es difícil ya que influye en la DLP, HTA y cardiopatía. Empeora el pronóstico. Control más estricto de la HTA. DLP: Niveles altos de LDL y bajos de HDL, aumentan el riesgo. Tabaco: Produce daño directo endotelial, aumenta agregabilidad plaquetaria y eleva el hematocrito. Aumenta el riesgo de 2-3 veces. Es necesario 5 años de abstinencia para que desaparezca el riesgo. Etanol: Perfil en J. Un consumo regular y muy moderado de vino (< 30 g/d) disminuye incidencia de infarto. El consumo excesivo predispone a ictus cerebrales de distintas maneras: Aumento de arritmias cardiacas y miocardiopatías. Aumento de incidencia de HTA e hipertrigliceridemia. Facilita agregación plaquetaria y activa cascada de coagulación. Disminuye el flujo sanguíneo cerebral. Aumenta el riesgo de Hemorragias por alteraciones de la fibrinólisis y HTA. Anticonceptivos orales: Alteran factores de coagulación. Mayor riesgo de tromboembolismo venoso que arterial. Otros: Obesidad, sedentarismo, SAHS, migraña con aura, simpaticomiméticos 3. FISIOPATOLOGÍA ISQUEMIA CEREBRAL 1. FSC (flujo sanguíneo cerebral) = cte (autorregulación cerebral) = 50 ml /100 gr cerebro/ min. 2. Descenso de FSC = Isquemia 3. Autorregulación eficaz TA 50- 150 mm Hg. 4. Zona necrosis (FSC < 10) y zona penumbra isquémica ( FSC 10- 20 ). 5. Circulación colateral 4. ETIOPATOGENIA Arteriosclerosis Lacunar: Lipohialinosis. Disección arterial Causa infrecuente Cardioembólico Hemodinámico Trombosis senos venosos Desconocida PATOLOGÍA CEREBROVASCULAR 2 4.1 TROMBOSIS ARTERIAL: ARTERIOSCLEROSIS Afecta a tronco supraaórtico y grandes arterias intracraneales. Todas las capas están involucradas. HTA, flujo turbulento, DLP, DM y tabaquismo contribuyen al desarrollo de la placa de ateroma. La ulceración de la placa de ateroma y la presencia de trombos adheridos son las principales complicaciones relacionadas con la isquemia cerebral ya que son fuente embolígena y de trombosis arterial. Se localiza preferencialmente en bifurcaciones carotideas (la + frecuente en bifurcaciones carotideas). En territorio posterior sobretodo en ambos extremos de la Arteria Basilar. La ateromatosis intracraneal es más frecuente en raza negra y asiáticas. 4.2 TROMBOSIS ARTERIAL: LIPOHIALINOSIS/NECROSIS FIBRINOIDE La lipohialinosis es una lesión segmentaria y focal de arterias de pequeños tamaño (capilares, arteriolas) siendo las arterias predominantemente afectadas las arteriolas perforantes (lenticuloestriadas, talamogeniculadas, talamoperforantes, paramedianas pontinas) siendo causa de los infartos lacunares. La HTA crónica es la causa más frecuente PATOLOGÍA CEREBROVASCULAR 3 4.3 TROMBOSIS ARTERIAL: DISECCIÓN ARTERIAL - Disección de la íntima de la AC con formación de un hematoma intramural asociado. - Antecedente traumático o de malformación vascular, variable. - Clínica: 1. Sd. Horner ipsilateral 2. Cervicalgia 3. AIT o ictus carotídeos Es la rotura de la capa íntima de la pared arterial. Las disecciones pueden ser subintimales o internas, medias y subadventiciales o externas (pueden producir dilatación aneurismática). La isquemia se puede deber a émbolos distales u oclusión arterial en punto de disección. La mayoría ocurren en adultos de 25-45 años. Pueden suceder espontáneamente, sobretodo en pacientes con antecedentes de conectivopatías o displasia fibromuscular y ante traumatismos directos o maniobra de Valsalva potentes. La localización más frecuente es la de la carótida interna extracraneal pudiendo existir dolor cervical lateral (carotidinia), cefalea frontoorbitaria, síndrome de Horner y sintomatología isquémica. Diagnostico mediante eco-Doppler y /o angioRM o arteriografía. Las disecciones intracraneales suelen ser supraclinoideas y tienen un peor pronóstico. En el caso de disecciones vertebrales se suelen asociar a tracciones quiroprácticas, torsión cervical inusual etc 4.4 TROMBOSIS ARTERIAL: CAUSAS INFRECUENTES Migraña: Infarto de migrañoso (uno o más síntomas del aura no totalmente reversibles en 7 días con confirmación del infarto en neuroimagen). Relación incuestionable. Fisiopatología: Oligohemia durante la fase de depresión propagada que ocurre durante el aura, aumento del K extracelular y liberación de glutamato, liberación de sustancias vasoactivas. Arteritis: o Infecciosas: Sífilis meningovascular fue la primera causa históricamente (actualmente muy raro), micosis (aspergilosis), cisticercosis, TBC, Herpes Zoster… Lo habitual es que primero debuten como una meningoencefalitis y posteriormente se compliquen con una arteritis. o No infecciosas: Arteritis de células gigantes, Takayasu, PAN o vasculitis aislada del SNC (esta última es un diagnóstico de exclusión, patrón angiográfico caracteristico-Arrosariado, LCR inflamatorio o no, diagnostico por biopsia). Otras: LES, Sd Sjogren, Bechet… Pensar en una vasculitis sistémica cuando además de la alteración neurológica exista afectación a otro nivel (renal, cutáneo, intestinal, artralgias, Raynaud, síntomas generales, aumento de VSG. Displasia fibromuscular: Infrecuente y rara. Pueden presentar herencia autosómica dominante. Macroscópicamente existe una alteración segmentaria no ateroesclerotica de las arterias de mediano calibre (“pila de monedas”). Existe PATOLOGÍA CEREBROVASCULAR 4 una transformación de las células musculares lisas en fibroblastos con proliferación de tejido conectivo. Tres tipos histológicos: medial (la + frecuente, más frecuente en mujeres y en ACI y AV), adventicial e intimal. Enfermedad de Moya-Moya: Es una artropatía progresiva, oclusiva y crónica que afecta a porción terminal de ACI y bifurcación. Se debe a una proliferación de células musculares lisas. Esta oclusión progresiva se asocia a la formación de una red colateral en la base del cerebro (“patrón angiográfico en humo”). Hay que descartar que estas alteraciones se deban a vasculitis, infecciones, trombosis, traumatismos, neurofibromatosis, meningitis crónicas, radioterapia… en cuyo caso se consideraría un síndrome de Moya-Moya. Síndrome de Sneddon: Livedo reticularias + lesiones cerebrovasculares. Pueden presentar anticuerpos antifosfolípido. Síndrome de Susac: Arteriopatía de pequeños vasos. Afectación coclear (sordera), retiniana (ceguera) y cerebro (infartos múltiples). Posible origen autoinmune. Citopatías mitocondriales Angiopatía cerebral amiloidea. Arteriopatías hereditarias: CADASIL (AD, mutación gen Notch3), CARASIL (AR, mut gen HTRA1), HERNS, HANA y enfermedad de Fabry (déficit de alfa glicosilasa A, AR ligada a X, clínica: angioqueratomas cutáneos, opacidad corneal, insuficiencia renal, cardiopatia, cocleo-vestibulopatía e ictus de perfil lacunar, dolicoectasias, PNP fibra fina; Tratamiento sustitutivo enzimático) Alteraciones hematológicas: o Depranocitosis: Niños-adolescentes de origen africano. o Estados de activación de la coagulación: Mutación de factor V Leiden (+ frecuente, se produce una resistencia a la activación de proteína C), defectos proteína C, proteína S o Antitrombina III. o Hiperfibrinogenemia y disminución de actividad fibrinolítica. o Trastornos mieloproliferativos: Policitemia Vera y trombocitemia esencial. o Anticuerpos antifosfolípidos: Anticoagulante lúpico y anticardiolipina. Se asocian a trombosis, abortos y trombocitopenia. o Niveles elevados de homocisteína. o El embarazo y las primeras 4 semanas de puerperio existe un estado de hipercoagulabilidad junto con un aumento de esteroides (favorecen hiperplasia intimal) que aumentan el riesgo de ictus isquémicos. Drogas. Vasoespasmo. 4.5 EMBOLISMO ARTERIAL En pacientes jóvenes el mecanismo embolico es el más representativo. Los émbolos suelen tener un componente mayor en fibrina con menor adhesión a la pared por lo que suelen fragmentarse y migrar a ramas distales multiterritoriales, cuando el tejido en riesgo se necrosa si existe una revascularización puede existir una PATOLOGÍA CEREBROVASCULAR 5 transformación hemorrágica. Los émbolos cardiacos suelen ser de mayor tamaño de ahí que produzcan un infarto de mayor tamaño. Particularidades (composición, localización, transformación hemorrágica…) Embolismo arterio-arterial: Origen diverso desde enfermedad ateromatosa de grandes vasos, disección arterial, estenosis intracraneales o aneurismas saculares no rotos. Cardiopatías embolígenas (15-20 % de los ictus isquémicos): o Fibrilación auricular (Flutter) valvular (Estenosis Mitral) y no valvular. o IAM (< 4 semanas y acinesia apical) o Otras: valvulopatías, prótesis, endocarditis infecciosas o no infecciosas (Libman-Sachs, marántica), tumores (mixoma, fibroelastoma), miocardiopatía (FEVI < 30-35%), cirugía, FOP (aneurisma del septo), síndrome del seno enfermo. Embolismos menos frecuentes: Paradójica (origen venoso con paso a sistema arterial por comunicaciones interauriculares o fístulas AV pulmonar), grasa (fracturas de hueso largo), gaseosa (maniobras quirúrgicas-toracocentesis, bypass-, neumotórax/peritoneo, submarinismo, idiopáticos). 4.6 MECANISMO HEMODINÁMICO Estenosis arterias extracerebrales de grado avanzado. Descenso de perfusión sanguínea: o Gasto cardiaco disminuido o Hipotensión arterial o Inversión flujo (síndrome de robo) Infartos en territorio frontera. 4.7 TROMBOSIS SENOS VENOSOS - Situaciones de hipercoagulabilidad (deshidratación, embarazo, puerperio, déficit proteínas coagulación, infecciones, Cáncer,...). - Infartos congestivos y/o hemorrágicos - Clínica: Según localización trombosis: o Venas corticales: cefalea, crisis epiléptica y déficits focales o Seno Longitudinal Superior: HIC +/- signos focales o Seno lateral/sigma/vena yugular: Empastamiento retromastoideo, dolor, torticolis, pares bajos. o Seno cavernoso: Dolor ocular, congestión conjuntival, exoftalmos y parálisis oculomotora. o Vena de Galeno: Necrosis hemorrágica diencefálica bilateral - Dx y tto específico. PATOLOGÍA CEREBROVASCULAR 6 5. CLÍNICA Signo del delta vacío en secuencias T1 PERFIL TEMPORAL o ACCIDENTE ISQUEMICO TRANSITORIO (A.I.T.): Episodio de alteración neurológica focal de < 1 hora de evolución (la descripción clásica era hasta 24 horas, pero en estudios de neuroimagen se ha visto que déficits de 1-24 horas existen más lesiones isquémicas). Principal causa: Aterosclerosis, seguido de la cardiopatía embolígena mientras que los AIT vertebrobsilares suelen ser hemodinámicos. Tras un AIT el riesgo de infarto es de 24-30 % en los siguientes 5 años, 4-8 % en el primer mes y 12-13 % en el primer año. o ICTUS ESTABLECIDO TERRITORIO CEREBRAL o CIRCULACION ANTERIOR (CAROTIDEA) o CIRCULACION POSTERIOR (VERTEBROBASILAR) PATOLOGÍA CEREBROVASCULAR 7 5.1 SÍNDROMES CAROTIDEOS La arteria carótida interna presenta dos segmentos: Segmento Cervical. Segmento Intracraneal. Ramas básicas: o Oftálmica. o Coroidea Anterior. o Comunicante Posterior o Cerebral Anterior. o Cerebral Media. La oclusión de la arteria carótida común puede ser asintomática mientras que la obstrucción de la arteria carótida interna puede ser desde asintomática (si existe adecuada compensación intracraneal por el polígono de Willis) hasta infarto cerebral masivo que afecta al territorio de ACM y ACA. Lo habitual es que la sintomatología sea similar a la de la oclusión de la arteria cerebral media (ya que el territorio de la arteria cerebral anterior suele estar compensado desde la AComA). ISQUEMIA A. OFTÁLMICA Rama ACI que irriga la retina y otras estructuras del ojo. Clínica: pérdida de visión. Presentación como A.I.T. muy frecuente (amaurosis fugax). Indica patología carotídea. ISQUEMIA A. CEREBRAL MEDIA Es el sd. vascular más frecuente. Puede ser completo (todo territorio ACM) o incompleto (ramas). Morbimortalidad elevada Vasculariza corteza M-S de MS y cara contralateral, radiaciones ópticas, áreas de lenguaje (h. dominante) o áreas de reconocimiento visuoespacial (h. no dominante). Clínica o Hemiparesia CL predominio faciobraquial o Hemihipoestesia CL o Hemianopsia homónima CL o Trs. lenguaje tipo afásico (HD) o Heminegligencia, anosognosia (HND) PATOLOGÍA CEREBROVASCULAR 8 ISQUEMIA A. CEREBRAL ANTERIOR Vasculariza corteza M-S de MI contralateral, y áreas prefrontales. Variabilidad anatómica. Clínica: Hemiparesia y hemihipoestesia de presdominio crural, síntomas cognitivos. Bilateral: paraparesia, mutismo acinético e incontinencia urinaria. Poco frecuente. Causas: vasoespasmo post HSA, embólico (A-A), no trombótico. 5.2 SD. VERTEBROBASILARES ISQUEMIA A. CEREBRAL POSTERIOR Vasculariza: corteza occipital, corteza temporal medial, tálamos (A. Talamoperforantes y talamogeniculadas), mesencéfalo (A. Interpedunculares y paramedianas). Clínica: Variabilidad. Déficit campimétrico contralateral, ceguera, agnosias visuales, alexia (HD), alteración memoria visual/verbal, síndromes mesencefálicos y talámicos. PATOLOGÍA CEREBROVASCULAR 9 ISQUEMIA VERTEBROBASILAR Síntomas “cruzados”: déficit PPCC ipsilateral y déficit motor/sensitivo contralateral. Afectación precoz nivel conciencia (sustancia reticular). Alteración en los movimientos oculares (núcleos pares oculomotores). Vértigo, sordera (núcleos vestibulares). Disfagia, disfonía (núcleos pares bajos). 5.3 SD. LACUNARES Pequeños infartos en territorios arterias perforantes. Origen enfermedad pequeño vaso o embolia. Clínica: déficits motores o sensitivos sin afectación asociada del nivel de conciencia ni síntomas corticales. Ejemplos: o Sd. Motor puro (+ frecuente). o Sd. Sensitivo puro. o Sd. Sensitivomotor puro o Disartria- mano torpe o Ataxia- hemiparesia 5.4 COMPLICACIONES FASE AGUDA Son la principal causa de morbi-mortalidad. 1. Deterioro neurológico y/o progresivo: Fundamentalmente en relación con la progresión de la isquemia, sobre todo durante las primeras 72 horas. Se define por un empeoramiento > 4 puntos en la escala NIHSS. A partir de las 72 horas suelen estar en relación con complicaciones sistémicas. El principal responsable es el edema cerebral. Existen varios marcadores clínicos (Edad avanzada, afectación grave, hipotensión arterial, fiebre, hiperglucemia…) y radiológicos (signos precoces de isquemia, peor colateralidad, peor missmatch). PATOLOGÍA CEREBROVASCULAR 10 2. Transformación hemorrágica: 30 % de ictus isquémicos (+ en cardioembólicos). Mecanismo por reperfusión de tejido necrótico donde la BHE está muy afectada. 3. Convulsiones: 7-20% de pacientes con ictus isquémico. 1/3 en las primeras 2 semanas (predominantemente el primer día). Es más frecuente en paciente con lesiones corticales amplias y suelen ser de inicio focal. 4. Depresión: suele ser más complicación a largo plazo e influye en la recuperación funcional de los pacientes. 5. Alteraciones CV: Muchas veces supone un continuum con la patología cerebral. Los ictus pueden provocar alteraciones del ritmo por elevación de catecolaminas y ECG. 6. Fiebre e infecciones: Fiebre en un 40 % de los pacientes con ictus agudas. Suele deberse a infección urinaria o respiratoria, aunque en ocasiones es central. 7. Otras (TVP/TEP, úlceras por decúbito, estreñimiento, alteraciones nutricionales). 6. ATENCIÓN DEL ICTUS AGUDO: CÓDIGO ICTUS 6.1 PROTOCOLO ATENCIÓN INICIAL • Reposo absoluto. Cabecero a 30-45º. • Monitorización (TA, Tª, Fc, SatO2) y soporte ventilatorio. • ECG 12 derivaciones • Dos vías venosas • Glucemia capilar • Analítica urgente: Bioquímica, Hemograma y Coagulación 6.2 ANAMNESIS INICIAL • Edad • Enfermedad Actual • Hora de inicio de los síntomas • ¿Sospecha de TCE? • Antecedentes personales • Factores de riesgo vascular • Cardiopatía/Arritmia embolígena (FA) • Patología cerebrovascular previa • SITUACIÓN BASAL: Escala de Rankin modificada, deterioro cognitivo… • Tratamiento crónico: ANTICOAGULACIÓN/ANTIAGREGACIÓN PATOLOGÍA CEREBROVASCULAR 11 Escala NIHSS (National Institutes of Health Stroke Scale) de valoración del ictus isquémico. 6.3 PRUEBAS DE IMAGEN • TC cráneo simple: 1. Descartar simuladores de infarto 2. Signos precoces de infarto 3. Escala ASPECTS PATOLOGÍA CEREBROVASCULAR 12 • • AngioTC: 1. Punto de oclusión arterial 2. Colaterales 3. Posible etiología 4. Imágenes fuente de angioTC TC perfusión: 1. Tejido hipoperfundido (isquemia) 2. Core (infarto) 3. Penumbra (salvable) 7. MEDIDAS GENERALES INICIALES FLUIDOTERAPIA • Fluidoterapia: evitar perfusiones hipotónicas y un balance excesivamente positivo (medidas antiedema cerebral). • Si hay disfagia o deterioro de conciencia: 1000 fisológico/24horas con ajuste si es que aumentan las pérdidas. VÍA AÉREA • En casos seleccionados de compromiso de la vía aérea (coma o ictus vertebrobasilar) podría estar indicada la intubación orotraqueal. PATOLOGÍA CEREBROVASCULAR 13 • • • Oxigenoterapia las primeras 24 horas. Asegurar saturaciones > 94% Evitar broncoaspiración: o Elevación cabecera de la cama (30-45º) o Sonda nasogástrica si precisa Aspiración de secreciones y tto broncodilatador TENSIÓN ARTERIAL • En pacientes con Ictus Isquémico la TA deberá mantenerse por debajo de 220/120. • En pacientes candidatos o que reciban tratamiento trombolítico se deben mantener cifras de TA menores de 185/105. • En pacientes con Hemorragia cerebral, o en situaciones especiales como IAM, Insuficiencia Renal o ICC la TA deberá mantenerse por debajo de 185/105. • En caso de que la TA sea mayor de 220/120 o 185/105 o menor de 100/60 se medirá cada 15 minutos hasta que se normalice dentro de estos límites. • Fármacos Intravenosos: Labetalol, Urapidil, Nicardipino Nitroprusiato sódico i.v en bomba 0,5-10 mgr/kg/ min. No deben usarse fármacos que produzcan un descenso rápido e impredecible de la TA, como el nifedipino sublingual. HIPERTERMIA • La hipertermia indica daño cerebral extenso y tiene un efecto negativo sobre el pronóstico • Si fiebre > 37,5 C: • Metamizol ½ o 1 amp. en 100 ml en 15 min/8horas o paracetamol oral/iv más medidas físicas si alta Tª • Investigar la causa de la fiebre y tto antibiótico si procede. GLUCEMIA • La hiperglucemia inicial se relaciona con peor pronóstico. • Objetivo: 140-180 mg/dL. • Tratamiento con insulina rápida • Glucemias 180-250 mg/dL: Subcutánea • Glucemias > 250 mg/dL: Intravenosa • Evitar las soluciones glucosadas a no ser que haya hipoglucemia • Tratar la hipoglucemia (< 60 mg/dL) PATOLOGÍA CEREBROVASCULAR 14 8. TRATAMIENTO TROMBOLÍTICO: DECISIÓN 8.1 FIBRINÓLISIS INTRAVENOSA CRITERIOS DE INCLUSIÓN: Pacientes con ictus isquémico de < 4.5 h de evolución SIN criterios de exclusión CRITERIOS DE EXCLUSIÓN 1. Hemorragia intracraneal en TC 2. Evolución de los síntomas de más de 4.5 horas o desconocimiento de la hora de inicio 3. Síntomas menores o mejoría franca antes del inicio de la infusión. 4. Síntomas sugestivos de HSA aunque TC sea normal 5. Diátesis hemorrágica conocida 6. Tratamiento con Heparina Sódica las 48 horas previas y TTPa elevado o HBPM a dosis anticoagulantes en las 12 horas previas 7. Tratamiento con anticoagulantes orales dicumarínicos. Puede considerarse el tratamiento si INR ≤ 1.7. Si tratamiento con nuevos ACO (dabigatran, rivaroxaban, apixaban) no se recomienda tratamiento con rt-PA a no ser que los test de laboratorio específicos (Tiempo trombina, ecarina o test de actividad factor X) sean normales o no se haya tomado la dosis correspondiente en los últimos dos días. 8. Plaquetas < 100.000 9. Glucemia < 50 mg/dl o > 400 mg/dl que no se corrigen 10. Tensión arterial > 185/105 mmHg o necesidad de medidas agresivas para controlarla 11. Traumatismo craneoencefálico o ictus en los 3 meses previos 12. Historia de hemorragia intracraneal previa 13. Antecedentes de HSA por rotura aneurismática 14. Historia de lesión del SNC (aneurismas > 10 mm, neoplasias, cirugía intracraneal o espinal) 15. Retinopatía hemorrágica 16. Antecedentes de masaje cardiaco, parto o punción en vaso sanguíneo no accesible en los 10 días previos. 17. Endocarditis bacteriana, pericarditis, pancreatitis aguda 18. Enfermedad ulcerativa gastrointestinal documentada en los 3 meses previos. Varices esofágicas, malformaciones vasculares intestinales conocidas. 19. Neoplasia con aumento de riesgo de sangrado (Metastásicos, CID, fármacos antiangiogénicos). Individualizar. 20. Enfermedad hepática severa 21. Cirugía mayor o trauma significativo en los 3 meses previos CARACTERÍSTICAS DEL TRATAMIENTO • DOSIS: 0.9 mg/Kg. Máximo 90 mg. Administrar 10 % en bolo en 1 min y el resto en perfusión (1 hora). PATOLOGÍA CEREBROVASCULAR 15 • CONSIDERACIONES TRAS INICIO DEL TRATAMIENTO: • Vigilancia y monitorización: Si cefalea brusca, nauseas/vómitos, hipertensión brusca y/o deterioro neurológico. DETENER PERFUSIÓN Y REALIZAR TC DE CRÁNEO. • Control estricto de cifras de TA (< 185/105) y Glucemias • Exploración Neurológica y control de constantes cada 15 minutos durante la infusión. • Vigilancia de angioedema. 8.2 TROMBECTOMÍA MECÁNICA INTRAARTERIAL (TIAM) CRITERIOS DE INCLUSIÓN: • > 18 años • mRS previo 0-2 • ASPECTS > 6 • Oclusión de gran vaso • Perfusión favorable • < 8-16 h En aquellos pacientes que no cumplan estos criterios habría que individualizar la posibilidad de tratamiento. CRITERIOS DE EXCLUSIÓN 1. Hemorragia intracraneal en la neuroimagen 2. Síntomas sugestivos de HSA aunque TC sea normal 3. Síntomas menores o mejoría franca antes del inicio de la infusión. Sospecha de infarto lacunar. 4. Glucemia < 50 mg/dl o > 400 mg/dl que no se corrigen 5. Tensión arterial > 185/105 mmHg o necesidad de medidas agresivas para controlarla 6. Existencia de diátesis hemorrágica: - < 30000 plaquetas - Heparina Sódica en las 48 horas previas y TTPa 2 veces lo normal - Anticoagulantes orales dicumarínicos con INR > 3. En caso de nuevos ACO, mismas consideraciones que con el rt-PA - Heparina de bajo peso molecular a dosis anticoagulantes en las últimas 12 horas - TTPA > 39 seg, ratio TTPA > 1.5, TP > 15 seg o INR 1.4-1.7 por trastornos hereditarios o adquiridos de la coagulación. 7. Infarto subagudo en TC/RM que ocupa > 1/3 del territorio de la ACM o > 100 cc de tejido cerebral. 8. No oclusión arterial 9. Sospecha de disección aortica 10. Contraindicaciones relativas - Estenosis > 50 % proximal al vaso ocluido (contraindicación relativa, se puede plantear realización de angioplastia previamente) PATOLOGÍA CEREBROVASCULAR 16 - Cirugía intracraneal o espinal, TCE o ictus en los 3 meses previos Historia de hemorragia intracraneal Enfermedad terminal con poca esperanza de vida o comorbilidad muy importante Endocarditis bacteriana conocida con o sin aneurisma micóticos e ictus Embarazo ALGORTIMO 9. TRATAMIENTO DE LAS COMPLICACIONES Edema cerebral: o Hemicraniectomía descompresiva: a valorar en menores de 65 años con ictus extensos de la ACM. o Diuréticos osmóticos (manitol, furosemida) en los pacientes cuya situación neurológica se deteriora debido al edema cerebral. o La hiperventilación puede ser útil (casos seleccionados). o Los corticosteroides no deben emplearse en el tratamiento del infarto cerebral. Hidrocefalia: Se recomienda el drenaje ventricular en los pacientes con hipertensión intracraneal debida a hidrocefalia. Ictus cerebelosos: Se recomienda la descompresión quirúrgica (craniectomía suboccipital) y evacuación de infartos cerebelosos con sufrimiento de tronco cerebral por compresión. Crisis: anticonvulsivos a los pacientes que hayan presentado crisis comiciales repetidas. Tratamiento de la fiebre y de las infecciones Profilaxis TVP/TEP Valorar Disfagia y nutrición. PATOLOGÍA CEREBROVASCULAR 17 10. ESTUDIO EN PLANTA ESTUDIO ANALÍTICO Bioquímica completa con perfil lipídico, Hb glicosilada, hormonas tiroideas, vitamina B12 y ácido fólico. Proteinograma. Hemograma y VSG. Pacientes jóvenes y casos seleccionados: o Screnning toxicológico y alcoholemia o Serología suero de sífilis, borriella, VVZ, VHB y C y VIH o Homocisteina sérica o Anticoagulante lúpico, Ac anticardiolipina, anti B2-glicoproteina o Inmunológico: ANA, Ac antiDNA, ENAs, C3, C4 y ANCA o Crioglobulinas o Estudio de trombofilia: proteina C, S y ATIII, test genéticos (Factor V Leiden, protrombina G20210A y MTHFR). Repetir a las 6-8 semanas o Estudio LCR o Electroforesis HbS (depranocitosis), Exploración OFT, biopsia meningocerebral, Actividad alfa-galactosidasa A (Enf Fabry). TC CRANEAL Ante cualquier empeoramiento clínico o de control (en el caso de tratamiento trombolítico a las 24 horas): Primeras 24 horas: o Nada o Signos precoces de infarto 24-72 horas: imágenes hipodensas en territorio infartado, con efecto masa en aumento. Perfusión de lujo (estudios con contraste). >72 horas – primera semana: hipodensidad más evidente, efecto masa variable. Infarto crónico: hipodensidad franca. Retracción estructuras próximas. RM CRANEAL - Permite ver mejor fosa posterior (ictus vertebrobasilares) e ictus lacunares. - Secuencias de perfusión/difusión: determinación aproximada del área de penumbra isquémica en el ictus agudo. - También cuando exista sospecha de trombosis de senos venosos o disección arterial (imagen en semiluna). ECO-DOPPLER TSA O DTC Se debe realizar en todos los pacientes que ingresen por ictus isquémico para despistaje de estenosis (salvo que tenga estudio angio TC o angio RM en el momento agudo). Depende mucho de la experiencia. PATOLOGÍA CEREBROVASCULAR 18 • • TSA: Clásico modo de valoración de estenosis carotídea y capacidad embolígena de la placa. DTC: Estenosis, oclusiones a nivel intracraneal. Estudio de FOP (sobre todo en pacientes jóvenes). ¿Sonotrombolisis? ANGIO TC O ANGIO RM • En pacientes dónde se confirmen estenosis vasculares en estudio Doppler se deberá ampliar estudio con estas técnicas. • El angio TC es más accesible • También permiten el estudio de vascularización intracraneal, incluyendo estudio venoso ANGIOGRAFÍA CONVENCIONAL • • • Gold standard en la valoración de cualquier patología vascular extra o intracraneal. Superior a cualquier técnica no invasiva. Problema: técnica intervencionista, riesgo bajo pero real. No siempre es la técnica diagnóstica inicial de elección ni es imprescindible para un dxo (ej: TSV, disección). ESTUDIO CARDIOLÓGICO • Ecocardiografía Transtorácica (ETT) o transesofágico (ETE): o < 45 años: siempre ETE precedida de ETT. o 45 años: ETT. Si fuera preciso (sospecha de trombosis sobre protesis, endocarditis, masas intracavitarias o FOP) se valorar ETE. • Estudio de ritmo cardiaco: o Monitorización continuar ECG en unidad de ictus o Holter 24 horas o Si alto riesgo: Holter 21 días o Reveal. PATOLOGÍA CEREBROVASCULAR 19 11. PREVENCIÓN Y PROFILAXIS El 90% de los ictus son prevenibles. PREVENCIÓN PRIMARIA Emplear tablas para valorar el riesgo vascular global: • < 10 %, bajo riesgo • 10-20 %, riesgo moderado • 20-40 %, alto riesgo • > 40 %, muy alto riesgo. En Pacientes con > 20 % riesgo, alguna clínica de enf aterosclerótica, AF de enf ateroscerótica precoz y enfermedades metabólicas con alto riesgo, hay que marcarse unos objetivos • Dieta baja en grasas, pérdida de peso, abandono tabaco/etanol y ejercicio físico regular. • HTA: el tto con ARA II, IECA, diuréticos y ACA reduce el riesgo de ictus frente al placebo (21%, 28%, 29% y 38%). Objetivo: < 140/90 mmHg (< 130/85 mmHg en diabéticos) • DLP: las estatinas reducen el riesgo de ictus en 17% frente a placebo. Objetivo: Col Total < 190 mg/dL, LDL < 130 (100 en diabéticos), HDL > 40 mg/dl, TGC < 200 mg/dl • DM: Control glucémico. Glucemias basales de 91 a 120 mg/dl. HbA1c < 7 %. • FA y otras cardiopatías embolígenas: los ACO con INR 2-3 (2.5-3.5 si prótesis mecánica) disminuyen el riesgo de ictus isquemicos frente a placebo o AA. Nuevo papel de los NACOs (Apixaban, Edoxaban, Rivaroxaban o inhibidores de FXa y Dabigatran o inhibidor de la trombina) • Tratamiento antiagregante: el AAS disminuye el riesgo de ictus, st en mujeres. PERO NO HA DEMOSTRADO BENEFICIO EN AUSENCIA DE FACTORES DE RIESGO • Estenosis asintomática de ACI: en estenosis ≥ 70% la EC reduce un 30% el riesgo de ictus a los 3 años, en centro con MM menor al 3%. Similares resultados con ASC. PATOLOGÍA CEREBROVASCULAR 20 PREVENCIÓN SECUNDARIA Los pacientes que han sufrido un evento isquémico tienen mayor riesgo de sufrir un nuevo evento vascular. Dieta baja en grasas, pérdida de peso, abandono tabaco/etanol y ejercicio físico regular. Control de otros FRV. HTA: El tto con antiHTA reduce en 24% el riesgo de nuevos ictus, en personas con HTA y en normotensos. Mismo objetivo. DLP: Estatinas a dosis altas, reducen la incidencia de ictus isquémicos. Objetivo: LDL < 100 mg/dl (incluso < 70) FA y otras cardiopatías embolígenas: los ACO (INR 2-3) disminuyen el riesgo de ictus isquemico en un 64% y 51% respecto a placebo y antiagregantes. Antiagregantes: los AA (AAS o clopidogrel) reducen un 25% el riesgo de nuevo ictus. La doble AA con ambos no ha demostrado ser superior a la monoterapia. El tto con ACO tampoco (excepto en ictus de origen cardioembólico). Estenosis sintomática de ACI: la EC o ASC disminuyen el riesgo de ictus en estenosis superiores al 50%. En las primeras 2 semanas (si es posible). PATOLOGÍA CEREBROVASCULAR 21 ICTUS HEMORRÁGICO 1. HEMORRAGIA CEREBRAL ESPONTÁNEA • Supone el 10-20 % de ictus. Mortalidad 50 % a los 30 días • Población > riesgo: raza negra e hispanos, HTA, antitrombóticos, gen ApoE (alelos e2 y 4) 1.1 CAUSAS: • HTA: Principal causa de HIC. • Malformaciones Vasculares (sobretodo MAV). • Tumores • Trastornos hemorrágicos (hemofilia, PTI, Leucemia aguda) • Anticoagulación y fibrinolíticos • Angiopatía amiloide cerebral. • Otras: Vasculitis, simpaticomiméticos, infarto hemorrágico, TCE. • Clínica: HTIC y dependiendo de la localización 1.2 TRATAMIENTO 1. Evaluación Inicial: • Soporte vital y mantenimiento vía aérea. IOT si GCS < 8. • Exploración clínica • TC cráneo urgente. Incluir angio-TC? • Ingreso en UI/UCI. • Analítica (HG, BQ y COAG) • Control glucémico y temperatura • Sueroterapia (Evitar Glucosado e hiposalino). 2. Hemostasia: • Antagonistas vit K: Vit K + Complejo protrombínico. Control INR. • NACOs: Dabigatran tiene antídoto (idarucizumab). • Heparina: Sulfato de Protamina 3. Prevenir aumento de PIC: • Control de TA: Objetivo 140 mmHg (PAS). Labetalol/Nicardipino. • Control de crisis epilépticas. No se recomienda profilaxis. • Control del dolor, agitación, fiebre y maniobras de Valsalva (tos, vómitos, esterñimiento) 4. Tratamiento PIC: • Elevar cabecero 30 º • Osmoterapia: Manitol 20%. Suero hipersalino y seguril. • NO USAR CORTICOIDES • Drenaje ventricular externo (DVE) si existe hidrocefalia. 5. Tto y prevención de complicaciones: • Screening isquemia miocárdica • Tromboprofilaxis: Compresión neumática. Iniciar Heparina a dosis bajas en pacientes en fase de resolución. • Filtro de vena cava PATOLOGÍA CEREBROVASCULAR 22 6. Tratamiento Quirúrgico? 7. Rehabilitación 8. Prevención de recurrencias: • FR de recurrencia: Lobares, edad avanzada (atribuido a mayor prevalencia de MSC y antitrombóticos), angiopatía amiloide, leucoaraiosis, microsangrados (MSC), anticoagulación, ApoE 2 y 4. • Control de la TA es la medida más efectiva (< 130/80) • Reinicio tratamiento antitrombótico 2. HEMORRAGIA SUBARACNOIDEA 2.1 EPIDEMIOLOGÍA • 5-10% de los ictus. • Más frecuente en > 50 a y en mujeres (1.2:1). • Aneurismas: Pueden ser múltiples en el 10-30 %. Factores de riesgo: Mujeres, fumadores, HTA, Hª familiar de enf cerebrovsacular. • Mortalidad: 15 % mueren antes de llegar al hospital, ¼ atendidos en urgencias mueren. De los que sobreviven un 50 % se quedan con un déficit neurológico permanente. • Enfermedades asociadas: o Enfermedades tejido conectivo (5 %): Ehler-Danlos tipo vascular o tipo IV, Neurofibromatosis tipo I, Poliquistosis renal AD. o Otros: Displasia fibromuscular, Coartación de aorta, sd. Moya-Moya, deficiencia alfa1-antitripsina, Lupus, anemia falciforme, endocarditis bacteriana e infecciones fúngicas, esclerosis tuberosa, feocromocitoma, MAV. • Factores de riesgo de HSA: o No modificables: edad, mujer, historia previa de HSA, historia familiar HSA, historia familiares primer grado diagnosticados de aneurismas. o Modificables: HTA, tabaco (aumenta además el riesgo de ruptura), alcohol, simpaticomiméticos (cocaína). o Otras: enfermedades genéticas, aneurismas de circulación anterior se rompen más frecuentemente en < 55 años, anuerismas del territorio posterior en hombres, aneurismas > 7 mm. PATOLOGÍA CEREBROVASCULAR 23 ALGORITMO DIAGNÓSTICO 2.3 TRATAMIENTO: 1. EVALUACIÓN INICIAL: Estabilizar vía aérea, respiración y circulación. 2. PREVENCIÓN Y TRATAMIENTO DEL RESANGRADO • Resangrado asocia elevada mortalidad y peor pronóstico funcional de los supervivientes. • Riesgo máximo: primeras 2-12 horas. • Factores asociados: tiempo prolongado hasta el tratamiento, peor estado neurológico al ingreso, deterioro del nivel de conciencia de inicio, cefalea centinelas previas, mayor tamaño del aneurisma, TAS > 160 mmHg • Tratamiento médico para prevenir el resangrado, previa oclusión del aneurisma: • CONTROL DE TA (< 160 mmHg). Nicardipino, Labetalol (5-20 mg) o nitroprusiato o hidralazina iv. • Tratamiento endovascular o quirúrgico: TAN PRONTO COMO SEA POSIBLE. o En aquellos pacientes donde ambas técnicas sean viables, se debe considerar el tratamiento endovascular (I,B). o Tratamiento quirúrgico: hematoma intraparenquimatoso (> 50 ml) y aneurismas de ACM. 3. MANEJO VASOESPASMO E ISQUEMIA CEREBRAL RETARDADA • 7-10 días tras la ruptura • Angiográficamente visible hasta en un 70 % (sintomático en el 30 %) • Si vasoespasmo asintomático: Monitorización en UCI y con DTC. • Tratamiento preventivo: Nimodipino y manejo hidro-electrolítico (euvolemia e hipertensión) • Tratamiento endovascular vasoespasmo sintomático: Angioplastia, inyección superselectiva de vasodilatadores. PATOLOGÍA CEREBROVASCULAR 24 4. OTRAS COMPLICACIONES NEUROLÓGICAS. • HIDROCEFALIA (20 %). El tratamiento consiste en DVE. Si cronifica: derivación de LCR permanente. • CRISIS EPILÉPTICA (20-26 %): No tratamiento profiláctico. 5. COMPLICACIONES MÉDICAS • CARDIOPULMONARES: frecuentes y con un rango de severidad variable (desde mínimos cambios ECG hasta miocardiopatía dilatada severa o síndrome de distres respiratorio agudo). Probablemente en relación con daño inducido por catecolaminas. • FIEBRE: complicación médica más común (70 %) • TROMBOEMBOLISMO: profilaxis con Heparina a las 24 horas de la oclusión del aneurisma. • ALTERACIONES GLUCOSA: La hiperglucemia se asocia a desarrollo de isquemia retardada y peor pronóstico. La hipoglucemia se asocia a peor pronóstico • HIPONATREMIA: SIADH (más frecuente en pacientes con peor situación neurológica, ruptura de aneurismas de AComA e hidrocefalia). Es un factor de mal pronóstico • ANEMIA PATOLOGÍA CEREBROVASCULAR 25