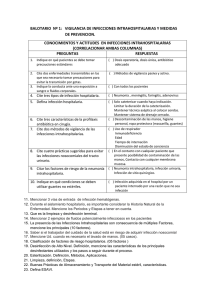
Anexo I. Sistema de vigilancia de la infección relacionada con la
Anuncio
Servicio Canario de la Salud DIRECCIÓN GENERAL PROGRAMAS ASISTENCIALES Rev 2014 ANEXO I SISTEMA DE VIGILANCIA DE LA INFECCIÓN RELACIONADA CON LA ASISTENCIA SANITARIA EN LOS HOSPITALES DE LA RED PÚBLICA DEL SISTEMA CANARIO DE LA SALUD En la elaboración de este documento han participado − Jesús Molina Cabrillana. Complejo Hospitalario Universitario Insular Materno Infantil de Las Palmas de Gran Canaria. Servicio de Medicina Preventiva. − Álvaro Torres Lana. Complejo Hospitalario Universitario Nuestra Señora de Candelaria de Tenerife. Servicio de Medicina Preventiva. − María Lecuona Fernández. Complejo Hospitalario Universitario de Canarias de Tenerife. Servicio de Microbiología y Medicina Preventiva. Unidad Funcional de Gestión de Riesgos. − Teresa Montserrat Blasco. Hospital Universitario de Gran Canaria Doctor Negrín. Servicio de Medicina Preventiva. − Pablo Jadraque Jiménez. Hospital General de La Palma. Servicio de Medicina Preventiva. − Domingo Panizo Rivas. Hospital Doctor José Molina Orosa de Lanzarote. Servicio de Medicina Preventiva. − Pino Suárez Bordón. Hospital General de Fuerteventura. Servicio de Microbiología. − Paloma García de Carlos. Servicio de Atención Especializada. Dirección General de Programas Asistenciales. Servicio Canario de la Salud − Víctor Naranjo Sintes. Servicio de Atención Especializada. Dirección General de Programas Asistenciales. Servicio Canario de la Salud. − Hilda Sánchez Janáriz. Directora General de Programas Asistenciales. Servicio Canario de la Salud. SVIRAS. Anexo I. Rev 2014. pág.2 ÍNDICE Página I. Análisis de situación………………..…………….…………………. 4 II. Objeto………………………………………………………………… 8 III. Alcance……………………………………………………………….. 8 IV. Definición…………………………………………………………….. 8 V. Objetivos………………………………………………………………. 9 VI. Implementación del sistema de vigilancia……………………………… 10 a. Aspectos Generales……………………………………………….. 10 b. Recursos…………………………………………………………… 11 c. Componentes del sistema………………………………………….. 11 d. Criterios diagnósticos………………………………………………. 12 e. Valores de referencia……………………………………………….. 12 VII. Gestión de la información………………………………………………. 13 VIII. Evaluación………………………………………………………………. 13 IX. Responsabilidades………………………………………………………… 15 X. Marco Normativo………………………………………………………… 16 XI. Bibliografía………………………………………………………………. 17 XII. Criterios del CDC para el diagnóstico de las infecciones…………… 19 SVIRAS. Anexo I. Rev 2014. pág.3 ANÁLISIS DE LA SITUACIÓN La infección relacionada con la asistencia sanitaria (IRAS) es el evento final que se produce como consecuencia de una serie de factores presentes, tanto por parte del enfermo (morbilidad asociada) como por los procesos que sobre él se realizan (instrumentaciones, higiene hospitalaria, intervenciones quirúrgicas, etc.). Por tanto para obtener una visión completa del problema es preciso monitorizar tanto el resultado (la infección), como los procesos y procedimientos asociados (lavado de manos, profilaxis quirúrgica, uso, inserción y mantenimiento de instrumentaciones, etc.) Las IRAS aumentan la morbi-mortalidad de los procesos sanitarios, aumentan la estancia hospitalaria, condicionando muchas veces ingresos de repetición y motivando mayor consumo de recursos diagnósticos y terapéuticos y producen costes personales, familiares y sociales considerables. Las IRAS tienen una etiología multifactorial y en gran medida pueden prevenirse. Su abordaje debe ser multidisciplinar, integrando la vigilancia, prevención y control basados en las mejores evidencias científicas disponibles, las estrategias de disminución de resistencia a antibióticos y la práctica adecuada de la higiene de manos. Para conocer las tasas de IRAS se pueden llevar a cabo dos tipos de abordajes metodológicos: estudios puntuales (tasas de prevalencia) y estudios a lo largo del tiempo (tasas de incidencia). Por otra parte, para evaluar procesos y procedimientos asociados se suelen calcular tasas de adherencia. Además de ello, resulta de gran importancia el uso de resultados microbiológicos como sucesos centinela. Un sistema de vigilancia de IRAS se debe basar en una mezcla de estos abordajes, de forma que se pueda llegar a conocer la endemia en un área geográfica concreta, identificar los patógenos más usuales, conocer la tendencia a lo largo del tiempo, ajustar por factores de riesgo conocidos (y por tanto comparar con otras series de similares características) y detectar oportunidades de mejora para establecer los mecanismos correctores oportunos. Para la evaluación de procesos son muy útiles los estudios de prevalencia, ya que permiten conocer la magnitud y distribución de los factores de riesgo modificables (dispositivos, profilaxis quirúrgica), así como evaluar el grado de implantación de las medidas de control y valorar su efectividad. El proyecto SENIC (Study of the Efficacy of Nosocomial Infection Control, EE.UU., 19741983) puso en evidencia que con medidas de vigilancia y control era posible reducir las infecciones nosocomiales más de un 30% y que los hospitales adheridos a programas de vigilancia presentaban unas tasas más bajas de infección hospitalaria, hecho corroborado posteriormente por otros estudios1-2. El Grupo de Estudios de Infección Hospitalaria de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica, la Sociedad Española de Medicina Preventiva, Salud Pública e Higiene y el Grupo de Trabajo de Enfermedades Infecciosas de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias presentaron conjuntamente el 1 de junio de 1999, el “Documento de consenso sobre recomendaciones y recursos necesarios para un programa de control de la infección nosocomial en los hospitales españoles”. Es este documento se hace referencia a la necesidad de que todos los hospitales cuenten con un equipo de control de la infección hospitalaria, cuya composición deberá adecuarse a las circunstancias y tamaño del centro correspondiente y que será responsable de la recogida diaria de los datos de SVIRAS. Anexo I. Rev 2014. pág.4 infección nosocomial, de la información de los resultados al personal implicado en la infección hospitalaria y de la introducción de medidas de prevención y control, incluyendo las tareas de formación continuada del personal. Un sistema de vigilancia eficaz es un elemento esencial de todo programa que pretenda reducir sus tasas. Además se considera un excelente indicador de calidad asistencial de un centro sanitario, no así las tasas de infección, ya que estas dependen de numerosas variables, entre las que destacan el riesgo de cada paciente. Por esta razón los datos de prevalencia no son útiles para comparaciones entre centros; para este propósito resulta más apropiado usar tasas ajustadas a riesgo mediante los estudios de incidencia. Tradicionalmente la prevalencia de la infección hospitalaria viene proporcionada por el estudio EPINE, el cual se realiza desde el año 1.990 en un gran número de hospitales de España. Algunos hospitales canarios vienen desarrollando sus propios estudios de prevalencia e incidencia o suelen participar en estudios multicéntricos (ENVIN-HELICS, VICONOS, etc) De manera genérica se sabe que aproximadamente 1,4 millones de personas en todo el mundo se ven afectadas a causa de una o más IRAS. En los países desarrollados entre un 5-10% de los pacientes adquieren una o más IRAS y en las Unidades de Cuidados Intensivos se ven afectados hasta un 30% de los pacientes con una mortalidad atribuible de un 44%. A nivel europeo, el Centro Europeo para la Prevención y el Control de las Enfermedades estima que alrededor de 4 millones de pacientes adquieren al menos una infección relacionada con la asistencia sanitaria al año y que de éstos unos 37.000 mueren como consecuencia de esa complicación7. El Estudio ENEAS3 obtuvo entre sus conclusiones que las infecciones relacionadas con la asistencia sanitaria representan el 25% de los efectos adversos hospitalarios y considera que al menos el 55% son evitables. El estudio EPINE4 muestra que la prevalencia de estas infecciones en nuestro país es de 7,75%, lo cual implicaría que 1 de cada 12 pacientes que ingresa en uno de nuestros centros hospitalarios adquiere una infección. En términos económicos y según la estimación de la revisión bibliográfica “Costes de la no seguridad del paciente”5, los costes derivados de las IRAS ascienden a unos 37.398 euros/por paciente infectado por SARM (Estafilococo aureus meticilina resistente), unos 24.685 euros por paciente con infección del sitio quirúrgico o 18.681 euros por paciente con neumonía de adquisición hospitalaria. En la Comunidad Autónoma de Canarias, según los datos recogidos en el Estudio EPINE, la prevalencia tanto de la infección relacionada con la asistencia sanitaria como de los pacientes con infección relacionada con la asistencia sanitaria alcanza una de las cifras más altas. Valorando la prevalencia de la IRAS según la localización se observa que las IRAS más frecuentes en nuestra comunidad son las infecciones de sitio quirúrgico (IQ), siguiendo en frecuencia las infecciones urinarias (ITU), las infecciones respiratorias (IR) y las bacteriemias. SVIRAS. Anexo I. Rev 2014. pág.5 Si bien los resultados de la estancia de prevalencia1 deben ser interpretados con cierta cautela por cuanto suponen una sobrerrepresentación de los pacientes de más estancia, suponen una información adicional en el contexto de la infección hospitalaria, por el papel que juega como factor de riesgo en la IRA una estancia prolongada. Los estudios de prevalencia permiten obtener la proporción de pacientes que presentan infección en un momento determinado. Tienen una gran utilidad sobre todo en centros hospitalarios de tamaño medio y grande permitiendo captar donde se encuentran los núcleos problemáticos. Sin embargo tienen limitaciones y sesgos derivados sobre todo del ya comentado efecto de la sobrerrepresentación de los pacientes de larga estancia. Por ello es necesario que se vean complementados con estudios de incidencia, los cuales siguen al paciente durante toda su estancia hospitalaria (o incluso un periodo post alta) y valoran las infecciones adquiridas durante la misma. La principal ventaja de los estudios de incidencia es que estiman las tasas reales de infección y la adherencia del personal al cuidado del paciente es mayor que en los estudios de prevalencia, ya que se aumentan los contactos entre el personal que realiza el estudio y los profesionales asistenciales del área de hospitalización y con ello las posibilidades de interactuar, informando de las medidas de control de la infección y del riesgo al que se ven sometidos los pacientes con los diversos procedimientos. La vigilancia epidemiológica se realiza de forma heterogénea en los hospitales canarios, basándose en diferentes circunstancias como son la experiencia previa, el modelo organizativo, el tamaño del hospital o los recursos específicos. Así, ante la diversidad de sistemas e indicadores de vigilancia epidemiológica, el patrón ascendente de la prevalencia en Canarias, la constatación de tasas elevadas de incidencias en determinados procedimientos y/o unidades hospitalarias, y la aparición frecuente de brotes producidos por microorganismos multirresistentes, se constata un escenario heterogéneo de la vigilancia y el control de las infecciones hospitalarias. Por todo lo anterior se considera necesaria la elaboración de un Plan Común de Vigilancia de la Infección Relacionada con la Asistencia Sanitaria en los centros hospitalarios del Sistema Canario de Salud, que permita la obtención de información oportuna y de calidad. Además, se considera imprescindible que todo el personal sanitario del hospital reciba de forma periódica una formación orientada a su ámbito de actividad profesional sobre la prevención de las IRAS. Los profesionales de nueva incorporación deben recibir dicha formación de forma previa o inmediatamente al inicio de sus actividades. Es necesario establecer un programa formativo del hospital en esta materia con la participación de las unidades competentes para la organización de las actividades docentes del personal, los Servicios de Medicina Preventiva y con el acuerdo de la Comisión de Infecciones. 1 La estancia de prevalencia es el número de días de hospitalización de un paciente desde el día del ingreso hasta el momento del estudio. Este concepto no es equivalente ni comparable a la estancia media o estancia de incidencia; la probabilidad de ser incluido en un estudio de prevalencia es mayor cuanto mayor sea la estancia total del enfermo. Por tanto, la estancia de prevalencia conlleva un exceso de representación de enfermos de larga estancia. SVIRAS. Anexo I. Rev 2014. pág.6 El centro sanitario debe tener diseñada una campaña continuada de formación e información sanitaria para sensibilizar a todo el personal, pacientes y visitantes, sobre el problema de las IRAS y las medidas para prevenirlas. Esto servirá para implementar las medidas de prevención y control más adecuadas para evitar las IRAS y mantener y mejorar de forma continuada la calidad técnica y la seguridad en todos los actos asistenciales. SVIRAS. Anexo I. Rev 2014. pág.7 SISTEMA DE VIGILANCIA DE LA INFECCIÓN RELACIONADA CON LA ASISTENCIA SANITARIA (SVIRAS) OBJETO Este documento pretende definir el marco del sistema de vigilancia, prevención y control de las IRAS en los centros hospitalarios de la red pública del Servicio Canario de la Salud, que haga homogéneas las actuaciones que se realizan en este área, en los centros hospitalarios de nuestra Comunidad. Promover un sistema estandarizado de vigilancia de las infecciones relacionadas con la asistencia sanitaria en los hospitales de la red pública de la Comunidad Autónoma de Canarias con el fin de contribuir a reducir las tasas de las infecciones relacionadas con la asistencia sanitaria hospitalaria, mediante la vigilancia epidemiológica activa y continuada, detectando los puntos críticos del sistema y proponiendo mecanismos para su corrección, todo ello enmarcado en la mejora de la calidad asistencial, la seguridad del paciente y la prevención y contención de la resistencia a los antimicrobianos. ALCANCE El SVIRAS deberá ser implantado en todos los hospitales de la red pública del Sistema Canario de Salud. Aquellos centros de titularidad privada que presten asistencia sanitaria en virtud de convenio o contrato de gestión de servicios a usuarios del Servicio Canario de la Salud, deberán incorporarse al Sistema de Vigilancia, adhiriéndose a la totalidad de los indicadores o a parte de ellos en función a su cartera de servicios. DEFINICIONES Se define como infección relacionada con la asistencia sanitaria (IRAS), como aquella condición, localizada o sistémica, que resulta de la reacción adversa a la presencia de agentes infecciosos o de sus toxinas y que no estaba presente, ni en fase de incubación, en el momento de admisión en el hospital. Incidencia es el número de casos nuevos de una enfermedad que aparecen en una población definida en un periodo de tiempo determinado. El numerador lo constituyen el número de casos nuevos y el denominador es la población inicial elegida o “de riesgo” para desarrollar la infección. Densidad de incidencia (DI) es una tasa instantánea que refleja la ocurrencia de enfermedad, en relación con la población libre de enfermedad. Utiliza como denominador unidades persona/tiempo o unidades de tiempo de exposición a una variable que puede ocurrir en un SVIRAS. Anexo I. Rev 2014. pág.8 periodo de tiempo para cada persona expuesta al evento de riesgo que se quiere medir (numerador). Prevalencia es el número de casos activos (existentes y nuevos) de la enfermedad en una población definida o bien durante un periodo de tiempo (prevalencia de periodo) o en un punto de tiempo especificado (punto de prevalencia). La vigilancia de la infección relacionada con la asistencia sanitaria está definida por los Centers for Disease Control (CDC) como “la recogida sistemática, el análisis e interpretación de los datos esenciales de salud para la planificación, implementación y evaluación de las prácticas de salud pública, integrado con la difusión oportuna de estos datos a todos aquellos que deban conocerlos” OBJETIVOS Objetivo General • Reducir las tasas de IRAS • Definir los criterios básicos del sistema de vigilancia, prevención y control de las IRAS en la Comunidad Autónoma de Canarias, de manera que los hospitales tengan un sistema común mínimo y lo desarrollen con criterios comunes que permitan la comparación. Objetivos Específicos • Obtener datos agregados, ajustados a riesgo de infección, que permitan la comparación entre centros y con otros sistemas de vigilancia, con tendencias temporales. • Promover la obtención y uso de la información basada en la evidencia científica para reconocer, prevenir y tratar adecuadamente las infecciones hospitalarias. • Promover estudios de investigación multicéntricos. • Promover la integración de la vigilancia de la infección relacionada con la asistencia sanitaria en los planes estratégicos de los centros sanitarios. • Contribuir a la evaluación de la calidad asistencial en cuanto los programas de vigilancia, prevención y control de las IRAS constituyen indicadores fiables de proceso y resultados. • Cumplir con los eventuales requerimientos normativos locales, nacionales o internacionales. SVIRAS. Anexo I. Rev 2014. pág.9 IMPLEMENTACIÓN DEL SISTEMA DE VIGILANCIA 1. Aspectos Generales La vigilancia, prevención y control de la infección relacionada con la asistencia sanitaria (IRAS) ha de abarcar todas las actividades del hospital. Debe tener un carácter y funcionamiento autónomo, es decir, ha de ser un dispositivo asistencial situado en un plano diferente al de la actividad clínica diaria, pues representa una evaluación continuada de la asistencia. El SVIRAS incluye los siguientes apartados: − − − Desarrollo e implantación de métodos de vigilancia activa. Equipo humano, facultativos y enfermeras, con conocimientos y experiencia en epidemiología hospitalaria dedicado a la vigilancia y control de las IRAS. Difusión periódica de la información de los datos sobre IRAS y evolución de las medidas adoptadas. Las actividades de vigilancia epidemiológica y control de las infecciones hospitalarias dependerán de los Servicios de Medicina Preventiva. En aquellos centros hospitalarios que no dispongan en su cartera de servicios de Medicina Preventiva, la Dirección Gerencia o Gerencia de Servicios Sanitarios, determinará la unidad responsable de la vigilancia, las cuales contarán con personal cualificado para el desarrollo de la misma. Puesto que cada hospital tiene objetivos concretos en función de sus características, cada uno de ellos puede añadir a sus actividades, además de los componentes propuestos en este sistema de vigilancia, aquellas otras tareas de vigilancia que considere oportunas. Para que los datos puedan ser fiables y comparables se considera necesario: − Tener en cuenta los factores que incrementan el riesgo de IRAS. Así, en aquellas infecciones en las que existen definidos índices de riesgo universalmente aceptados (infección de localización quirúrgica e índice NNIS – National Nosocomial Infections Surveillance -, área de cuidados intensivos, duración de uso de los dispositivos, etc.), las tasas deben proporcionarse de forma estratificada en función de dichos índices, mientras que en el resto de los casos deben recogerse las tasas de utilización de procedimientos de riesgo. − Conseguir la mayor homogeneidad obteniendo altos niveles de sensibilidad y especificidad en la detección de casos, mediante una metodología de detección común y el establecimiento de un sistema que controle la calidad en la recogida de la información. Las actividades derivadas de los resultados del sistema de vigilancia serán gestionadas y evaluadas por la Comisión de Infecciones (CI) del centro hospitalario. La Comisión de infección hospitalaria, profilaxis y política antibiótica se encuentra recogida en la normativa en vigor (RD 521/1987). Depende de la Comisión Central de Garantía de Calidad. En aquellos SVIRAS. Anexo I. Rev 2014. pág.10 centros en los que, por volumen de actividad y cartera de servicios no dispongan de la citada Comisión, se vincularán a aquellas con competencias en este ámbito asistencial Es indispensable la coordinación y el apoyo con los Servicios de Microbiología Clínica Hospitalarios. La identificación y caracterización del agente etiológico responsable de una infección es fundamental para la elección del tratamiento. Esta información es especialmente útil para la detección precoz de algunos brotes en los que los casos se describen mediante la identificación del patógeno responsable o por una pauta clara de resistencia a los antimicrobianos. Así mismo proporciona datos sobre la epidemiología local de las infecciones asociadas a la asistencia sanitaria. Es necesario asegurar lo siguiente: - La calidad de las técnicas del laboratorio de microbiología debe estar asegurada a fin de obtener datos válidos para las decisiones clínicas y el uso epidemiológico. - Los departamentos y servicios clínicos deben disponer de procedimientos adecuados para la recogida y el traslado de muestras al Servicio de Microbiología. - La información de los Servicio de Microbiología Clínica debe ser analizada con el fin de diferenciar las IRAS de las adquiridas en la comunidad, distinguir los casos de infección por colonización y evitar el doble recuento de los casos en los que se ha examinado más de un cultivo. La implantación del SVIRAS en los centros hospitalarios no excluye de la necesidad de cumplir los requisitos recogidos en el Sistema de Vigilancia Epidemiológica de Canarias5, entre cuyos objetivos y acciones fundamentales se encuentran la detección y análisis de los problemas de salud y las situaciones de riesgo y la difusión de la información y recomendaciones necesarias que faciliten la aplicación de medidas de control individuales y colectivas. Estos vínculos son especialmente importantes: - Durante los brotes en la comunidad que puedan afectar a los establecimientos sanitarios, porque éstos deban ocuparse de un número inesperadamente elevado de pacientes o porque puedan actuar como amplificadores de los brotes debido al mayor riesgo de infección para otros pacientes o agentes de salud. - Para la notificación de incidentes pertinentes poco habituales entre unos establecimientos y otros, como brotes o la aparición de un nuevo agente patógeno o de una importante pauta de resistencia a los microbianos. La información relativa a enfermedades de potencial interés debe ser comunicada de inmediato a las autoridades de salud pública. 2. Recursos Todos los hospitales deben disponer de un equipo humano que se ocupe de la vigilancia, prevención y control de las IRAS. La composición del mismo estará en consonancia con las SVIRAS. Anexo I. Rev 2014. pág.11 circunstancias y tamaño del hospital. Dicho equipo contará como mínimo con un personal de enfermería de control de infecciones por cada 250 camas o fracción (o si se prefiere por cada 6.000 ingresos hospitalarios) a tiempo completo y, con al menos un facultativo especialista en Medicina Preventiva o Microbiología para centros de entre 120 y 500 camas. Los centros pequeños de menos de 150 camas deberán disponer de un profesional a tiempo parcial1-10-11-13-14. El personal encargado de la recogida de los datos en todos los centros debe estar entrenado en la vigilancia y control de la IRAS y en la metodología a emplear. 3. Componentes del Sistema de vigilancia Dada la complejidad de la puesta en marcha de un sistema de vigilancia que incluya todas las infecciones relacionadas con la asistencia sanitaria, en una primera etapa se incluirán los siguientes componentes: Vigilancia de la prevalencia global de infecciones en el centro. Vigilancia de la infección de sitio quirúrgico y procesos asociados. Vigilancia de la bacteriemia asociada a cuidados sanitarios en régimen de hospitalización. Vigilancia de patógenos multirresistentes y Clostridium difficile. Estrategia de higiene de manos Cada uno de estos componentes se irá actualizando en cuanto al contenido metodológico, en base a la mayor evidencia científica disponible y con el fin de garantizar la máxima homogeneidad en la información, que permita comparaciones intercentros, especificándose los indicadores para cada componente, atendiendo a las características diferenciales de cada área de salud. Con posterioridad, en función de los resultados obtenidos y las necesidades identificadas, se ampliará la vigilancia, con especial atención a la vigilancia de la infección asociada a dispositivo en las Unidades de Medicina Intensiva, vigilancia de la infección en unidades de diálisis y la monitorización estandarizada del consumo de antibióticos. 4. Criterios diagnósticos Para el diagnóstico y clasificación de las infecciones se seguirán definiciones estandarizadas de acuerdo al conocimiento científico más reciente. En el momento de la redacción de este documento los criterios diagnósticos más comúnmente utilizados a nivel mundial son los criterios del CDC publicados en el año 2.008. Una traducción y adaptación de los mismos a nuestro medio se encuentra recogido en al final de este documento.15 5. Valores de referencia Los valores de referencia serán aquellos obtenidos con sistemas de vigilancia que utilicen metodología similar, de forma que, en función del componente, se usarán referencias específicas: SVIRAS. Anexo I. Rev 2014. pág.12 • • • • En general se usarán los estándares del National Healthcare Safety Network (NHSN) para las infecciones de diálisis y de sitio quirúrgico. En el caso de la infección del sitio quirúrgico también se tendrán en cuenta los valores de HELICSwin. Para la prevalencia se usarán los valores del EPINE. Para las infecciones de pacientes en UCI se usarán los estándares del ENVIN-HELICS Los valores de referencia pueden ir cambiando a medida que se vayan actualizando las publicaciones de las organizaciones antes mencionadas, o la publicación de nuevos estándares de otros organismos o sistemas de vigilancia que utilicen la misma metodología. GESTIÓN DE LA INFORMACIÓN La gestión de la información se realizará sólo con los datos del resumen de cada centro, los cuales serán remitidos a la Dirección General de Programas Asistenciales a la finalización del periodo de vigilancia pactado para cada componente para su evaluación. Se constituirá un Grupo Coordinador del Sistema de Vigilancia de la Infección Hospitalaria del que forman parte: − − − Jefes de Servicio de Medicina Preventiva de los hospitales participantes (o persona en quién deleguen) o facultativos con responsabilidades en el control de la infección hospitalaria en aquellos centros que no dispongan de la especialidad en su cartera de servicios. Técnicos del Servicio de Atención Especializada de la Dirección General de Programas Asistenciales. Técnicos del Servicio de Evaluación de la Calidad Asistencial y Sistemas de Información de la Dirección General de Programas Asistenciales. Entres sus funciones se encuentran: − − Determinar posibles áreas de especial interés y elaborar los protocolos generales del Sistema de Vigilancia correspondientes. Con carácter anual, se elaborará un informe con los resultados obtenidos de forma conjunta y desagregada que se remitirá a los centros participantes. Se calculará la tasa estandarizada de infección para que cada centro pueda hacer una comparación respecto al resto de centros participantes, todo ello con propósito de introducir mejoras en el caso que sea necesario. EVALUACIÓN Los Servicios de Medicina Preventiva Hospitalarios o las Unidades designadas para la vigilancia de la infección relacionada con la asistencia sanitaria, emitirán un informe anual sobre la situación de los resultados y el proceso y el impacto de las actividades implantadas. SVIRAS. Anexo I. Rev 2014. pág.13 Dicho informe será remitido por las Direcciones Gerencias Hospitalarias o Gerencias de Servicios Sanitarios a la Dirección General de Programas Asistenciales en el mes de febrero siguiente al ejercicio estudiado, haciendo referencia al cumplimiento de los objetivos y se razonarán aquellos que no se hayan podido cumplir. Se evaluarán periódicamente los siguientes indicadores: De proceso: o Existencia de un documento que defina el Sistema de Vigilancia de la Infección Relacionada con la Asistencia Sanitaria adaptado al centro y firmado por la Dirección. o Inclusión en el cuadro de mandos del hospital de indicadores de IRA. De resultado o Resultado de los indicadores definidos. o Análisis comparativo de cada indicador con el valor de referencia. o Informe anual de resultados. o Lecciones aprendidas. SVIRAS. Anexo I. Rev 2014. pág.14 RESPONSABILIDADES Director/a Gerente: es el responsable último de la implantación y gestión del sistema de vigilancia de la IN y por lo tanto de garantizar que estén disponibles los recursos humanos y materiales. Directores/as Médicos/as y de enfermería: son los responsables últimos de la organización y funcionamiento del sistema de vigilancia, incluyendo la aprobación del circuito de difusión de la información del centro. Comisión de infección hospitalaria: Conocerá e informará el sistema de vigilancia, propondrá los objetivos anuales de vigilancia, evaluará la información de la IN del centro y contribuirá a su difusión con el fin de sensibilizar al personal de su importancia y de la necesidad de colaboración en la vigilancia y el control. Jefes de Servicio/Sección/Unidad/Supervisores-as enfermería: responsables de la consecución de objetivos de su unidad y por lo tanto de que la información generada para el sistema de vigilancia sea correcta, puntual y evaluable; contribuirá a la difusión de la información sobre IRAS para sensibilizar al personal de su unidad de la importancia de la misma y de la necesidad de la colaboración de todos en su vigilancia y control. Servicio de Medicina Preventiva: es el responsable operativo del sistema de vigilancia de la IN y por lo tanto de la coordinación de la recogida de información y del análisis de datos, de la evaluación periódica de las fuentes de información y de la difusión de la misma, de acuerdo al circuito aprobado por la dirección. En aquellos centros hospitalarios que no dispongan en su cartera de servicios de Servicio de Medicina Preventiva, la Dirección designará un responsable del sistema de vigilancia. Servicio de Microbiología: es el responsable de establecer la coordinación necesaria para el funcionamiento de las alertas microbiológicas y de realizar o colaborar en la identificación de microorganismos, y especialmente en la determinación de la incidencia de bacteriemias, así como todas aquellas que le sean específicamente asignadas. SVIRAS. Anexo I. Rev 2014. pág.15 MARCO NORMATIVO 1. Ley 14/1986, de 25 de abril, General de Sanidad. 2. Real Decreto 521/1987, de 15 de abril, por el que se aprueba el Reglamento sobre estructura, organización y funcionamiento de los hospitales gestionados por el Instituto Nacional de la Salud. 3. Ley 11/1994, de 26 de julio, de Ordenación Sanitaria de Canarias. 4. Decreto 32/1995, de 24 de febrero, por el que se aprueba el Reglamento de Organización y Funcionamiento del Servicio Canario de la Salud. 5. Decreto 165/1998, de 24 de septiembre, por el que se crea la Red Canaria de Vigilancia Epidemiológica y se establecen las normas para regular su funcionamiento. 6. Orden de 15 de junio de 2000, por la que se establecen las condiciones mínimas que deben cumplir los centros hospitalarios de la Comunidad Autónoma de Canarias. 7. Programa de Gestión Convenida anual. SVIRAS. Anexo I. Rev 2014. pág.16 BIBLIOGRAFÍA 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. RW Haley, DH Culver, JW White, W Meade Morgan, TG Emori, TM Hooton. The efficacy of infection surveillance and control programs in preventing nosocomial infections in US hospitals. Am J Epidemiol 1985; 121: 182-205. R.P. Gaynes. Surveillance of nosocomial infections. In: Hospital Infections. JV Bennett, PS Brachman (ed); 1998: 65-84. Estudio Nacional de efectos adversos ligados a la hospitalización. ENEAS 2005. Madrid: Ministerio de Sanidad y Consumo 2006. Disponible en http://www.msc.es/organizacion/sns/planCalidadSNS/pdf/excelencia/opsc_sp2.pdf Grupo de trabajo EPINE (Estudio de prevalencia de las infecciones nosocomiales en España). Informe Global España 2010. Sociedad Española de Medicina Preventiva, Salud Pública e Higiene, 2010. (Accedido 18/03/2011) Disponible en: http://www.sempsph.com/sempsph/attachments/327_Informe%20EPINE-2010%20ESPAÑA.pdf Revisión bibliográfica sobre trabajos de Costes de la “No Seguridad del Paciente”. Madrid. Ministerio de Sanidad y Consumo 2008 (Accedido el 17/05/2010). http://www.msc.es/organizacion/sns/planCalidadSNS/docs/CostesNoSeguridadPacientes.pdf WHO Guidelines on Hand Hygiene in Health Care. First Global Patient Safety Challenge Clean Care is Safer Care. World Health Organization 2009. Annual Epidemiological Report on Communicable Diseases in Europe 2008. European Center for Disease Prevention and Control, 2009. Disponible en http://ecdc.europa.eu/en/publications/Publications/0812_SUR_Annual_Epidemiological_Report_200 8.pdf Sistema de Vigilancia y Control de la Infección Hospitalaria (RIHOS) en la Comunidad de Madrid. CDC. Monitoring hospital-acquired infections to promote patient safety. United States 19901999.MMWR 2000; 49: 149-153. TG Emori et al. National nosocomial infections surveillance system (NNIS): description of surveillance methods. Am J Infect Control 1991; 19: 19-35. NNIS System. Nosocomial infections rates for interhospital comparisons, limitations and possible solutions. Infect Control Hosp Epidemiol 1991; 12: 609-621. DH Culver, TC Horan, RP Gaynes, WJ Martone, WR Jarvis, TG Emori, SN Banerjee, JR Edwards, JS Tolson, TS Henderson, JM Hudges and the National Nosocomial Infections Surveillance System. Surgical wound infection rates by wound class, operative procedure and patient risk index. Am J Med 1991; 91 (suppl 3B): 152-157. N Freixas, M Sallés, L García. Cambios en el control de la infección nosocomial: nuevos retos y competencias de la enfermera de control de infección. Enferm Infecc Microbiol Clin 2009; 27 (5): 285-289. CA O’Boyle, M Jackson, SJ Henly. Staffing requeriments for infection control programs in US Elath care facilities: Delphi Project. Am J Infect Control. 2002; 30:321-333. TC Horan, M Andrus, MA Dudeck. CDC/NHSN surveillance definition of health care-associated infection and criteria for specific types of infections in the acute care setting. Am J Infect Control 2008; 36: 309-332. Componentes básicos para los programas de prevención y control de infecciones. Informe de la Segunda Reunión Oficiosa de Prevención y control de Infecciones en la Atención Sanitaria. WHO/HSE/EPR/2009.1 JE Coia, GJ Duckworth, DI Edwards, M Farrington, C Fry, H Humphreys, et al. Guidelines for the control and prevention of meticillin-resistant Staphylococcus Aureus (MRSA) in healthcare facilities. J Hosp Infection 2006; 63S: S1-S44. Erratum in: J Hosp Infect. 2006; 64: 97-8. J Rodríguez-Baño, C Bischofberger, F Álvarez-Lerma, A Asensio, T Delgado, D García-Arcal, L García-Ortega, MJ Hernández, J Molina-Cabrillana, C Pérez-Canosa, M Pujol y Grupos de Estudio de Infección Hospitalaria (GEIH), de Infección en el Paciente Crítico (GEIPC), de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) y Sociedad Española de Medicina Preventiva, Salud Pública e Higiene (SEMPSPH). Vigilancia y el control de SVIRAS. Anexo I. Rev 2014. pág.17 19. 20. 21. 22. 23. Staphylococcus aureus resistente a meticilina en hospitales españoles: documento de consenso SEIMC/SEMPSPH. Enferm Infecc Microbiol Clin. 2008 May; 26(5):285-98. TC Horan, M Andrus, MA Dudeck. CDC/NHSN surveillance definition of health care–associated infection and criteria for specific types of infections in the acute care setting. Am J Infect Control. 2008; 36:309-32. Recomendaciones del Consejo de 9 de junio de 2009 sobre la seguridad de los pacientes, en particular la prevención y lucha contra las infecciones relacionadas con la asistencia sanitaria (2009/C 151/01). Diario Oficial de la Unión Europea, 3-7-2009 J Vaqué y Grupo de trabajo EPINE de la SEMPSPH. Estudio de prevalencia de las infecciones nosocomiales en los hospitales españoles. Protocolo de trabajo. Barcelona. Marzo, 2010. MJ González Mateo. Sistema de vigilancia, prevención y control de la infección relacionada con la asistencia sanitaria en el Principado de Asturias. Dirección General de Calidad e Innovación en los Servicios Sanitarios. Consejería de Salud y Servicios Sanitarios. Principado de Asturias. Marzo 2011. JR Edwards, KD Peterson, Y Mu, S Banerjee, D Allen-Bridson, G Morrell, MA Dudeck, DA Pollock, TC Horan. National Healthcare Safety Network (NHSN) report: data summary for 2006 through 2008, issued December 2009. Am J Infect Control 2009; 37: 783-805. SVIRAS. Anexo I. Rev 2014. pág.18 CRITERIOS PARA DIAGNOSTICAR INFECCIONES NOSOCOMIALES (CDC, 2008) Fuente: Horan TC, Andrus M, Dudeck MA. CDC/NHSN surveillance definition of health care–associated infection and criteria for specific types of infections in the acute care setting. Am J Infect Control 2008; 36: 309-32. SVIRAS. Anexo I. Rev 2014. pág.19 CRITERIOS PARA EL DIAGNÓSTICO DE LAS INFECCIONES Las definiciones que se exponen a continuación son una adaptación de versión de 2008 de los criterios diagnósticos de infección nosocomial del CDC. DEFINICIONES Y CONSIDERACIONES PREVIAS Definición de infección nosocomial. El CDC define una infección nosocomial como una condición localizada o sistémica, que resulta de una reacción adversa a la presencia de un(os) agente(s) infeccioso(s) o sus toxinas. Para considerar una infección como nosocomial, no deben existir pruebas de que la infección estuviera presente o incubándose en el momento del ingreso del paciente en el centro sanitario. Las infecciones nosocomiales pueden ser producidas por agentes infecciosos procedentes de fuentes endógenas o exógenas: • Las fuentes endógenas son los lugares del cuerpo, como la piel, nariz, boca, aparato digestivo o vagina que habitualmente están colonizados por microorganismos. • Las fuentes exógenas son aquellas que son externas al paciente, tales como el personal que atiende al paciente, los visitantes, el equipamiento para atender al paciente, instrumentos médicos o el entorno sanitario. Otras consideraciones importantes a tener en cuenta son las siguientes: Información necesaria. La información usada para reconocer la presencia de una infección activa y para clasificar su localización incluye varias combinaciones de datos clínicos y los resultados analíticos y de otras exploraciones complementarias. La evidencia clínica se puede obtener a partir de la exploración directa del paciente o de la revisión de la historia clínica u otros documentos del enfermo. Diagnóstico clínico de la infección. Para ciertos tipos de infección, el diagnóstico de infección realizado por un médico a partir de una observación directa durante una intervención, una endoscopia o cualquier otra técnica diagnóstica, se considera un criterio válido de infección activa mientras no se demuestre lo contrario (por ejemplo, porque la información se anotó de forma incorrecta en la historia o el diagnóstico de sospecha no se confirmó). En ciertas localizaciones estos criterios exigirán, además, que el diagnóstico clínico de un médico se acompañe del inicio del tratamiento antibiótico adecuado. A menos que se especifique, el diagnóstico médico aislado no es un criterio aceptable para ningún tipo de infección nosocomial. Definición de infección comunitaria. Una infección se considera comunitaria si hay indicios de que el paciente la tuviera en fase clínica o de incubación en el momento del ingreso. Las siguientes normalmente no deben clasificarse como nosocomiales: 1) En Neonatología se considerarán infecciones comunitarias: SVIRAS. Anexo I. Rev 2014. pág.20 • Las que se desarrollen durante las primeras 72 horas de vida (aunque el niño hubiera estado previamente ingresado en un área de hospitalización neonatal), por un microorganismo que sea flora habitual del canal del parto (Streptococcus del grupo A, S. agalactiae, Escherichia coli, Listeria monocytogenes, Streptococcus beta hemolíticos del grupo D -enterococos o no-), y/o en los que se demuestre que están presentes en el canal genital de la madre aunque no sean flora habitual de la misma, y son el agente etiológico de la infección neonatal (Haemophilus influenzae, S. pneumoniae, etc.). • Las adquiridas por vía transplacentaria (por ejemplo, Herpes simplex, toxoplasmosis, rubeola, Citomegalovirus, y sífilis). 2) Una infección que aparece en alguna de estas circunstancias no se considera nosocomial y deberá ser catalogada como comunitaria: - La asociada a una complicación o diseminación de otra infección que ya estaba presente en el momento del ingreso, si no ha habido ningún cambio de microorganismo, ni han aparecido síntomas muy sugestivos de que el paciente ha adquirido una nueva infección. - La reactivación de una infección latente (por ejemplo, herpes zoster, herpes simplex, sífilis o tuberculosis). Las siguientes condiciones no son infecciones: • Colonización, que implica la presencia de microorganismos en la piel, en membranas mucosas, heridas abiertas, en excreciones o secreciones, pero que no causan síntomas o signos clínicos adversos. • Inflamación, como resultado de la respuesta tisular frente a traumatismo o estimulación por agentes no infecciosos, como las sustancias químicas. NOTA: Puntos discordantes entre el protocolo EPINE y los criterios de infección del CDC: • Infecciones neonatales en las primeras 72 horas de vida producidas por patógenos habituales del canal del parto: en el EPINE se consideran comunitarias, mientras que el CDC las considera nosocomiales. • Criterios para considerar como diferentes los microorganismos aislados en dos hemocultivos diferentes: los criterios empleados en el protocolo EPINE están adaptados a nuestro medio, y son más estrictos que los de los CDC. SVIRAS. Anexo I. Rev 2014. pág.21 1. CRITERIOS URINARIAS PARA DIAGNOSTICAR UNA INFECCIÓN DE LAS VÍAS Las infecciones de las vías urinarias incluyen las infecciones sintomáticas y el resto de infecciones urinarias. 1.1 Infección sintomática de las vías urinarias (código: IVU1) Una infección sintomática de las vías urinarias debe cumplir al menos 1 de los siguientes criterios: 1) El paciente tenía una sonda vesical permanente en el momento de la recogida de las muestras microbiológicas Y al menos UNO de los siguientes en ausencia de otra causa reconocible: fiebre (>38°C), hipersensibilidad suprapúbica o hipersensibilidad o dolor en el ángulo costovertebral Y el urocultivo ha sido positivo (más de 105 colonias/ml) a dos microorganismos diferentes como máximo, O BIEN, El paciente tenía sonda vesical retirada 48 horas anteriores al momento de la recogida de las muestras microbiológicas Y al menos UNO de los siguientes en ausencia de otra causa reconocible: fiebre (>38°C), hipersensibilidad suprapúbica o hipersensibilidad o dolor en el ángulo costovertebral y el urocultivo ha sido positivo (más de 105 colonias/ml) a dos microorganismos diferentes como máximo. 2) El paciente NO tenía sonda vesical en el momento de la recogida de las muestras microbiológicas NI en las 48 horas anteriores Y al menos UNO de los siguientes en ausencia de otra causa reconocible: fiebre (<38ºC) en un paciente de 65 años o menos, urgencia miccional, polaquiuria, disuria, hipersensibilidad o dolor en la región suprapúbica y el urocultivo ha sido positivo (más de 105 colonias/ml) a dos microorganismos diferentes como máximo. 3) El paciente tenía una sonda vesical permanente en el momento de la recogida de las muestras microbiológicas Y al menos UNO de los siguientes en ausencia de otra causa reconocible: fiebre (>38°C), hipersensibilidad suprapúbica o hipersensibilidad o dolor en el ángulo costovertebral, Y al menos UNO de los siguientes hallazgos: a) La tira reactiva es positiva en orina para la esterasa leucocitaria y/o nitratos. b) Piuria (>10 leucocitos por ml, o > 3 leucocitos por ml al analizar con un campo de gran aumento una muestra de orina no centrifugada). c) Visualización de microorganismos en una tinción de Gram de orina no centrifugada. . Y el urocultivo ha sido positivo (103-105 ufc/ml) a 2 microorganismos diferentes como máximo. O BIEN El paciente tenía sonda vesical retirada 48 horas anteriores al momento de la recogida de las muestras microbiológicas Y al menos UNO de los siguientes en ausencia de otra causa reconocible: SVIRAS. Anexo I. Rev 2014. pág.22 fiebre (>38ºC), urgencia miccional, polaquiuria, disuria, hipersensibilidad o dolor en la región suprapúbica o en el ángulo costovertebral y al menos uno de los siguientes hallazgos: a) La tira reactiva es positiva en orina para la esterasa leucocitaria y/o nitratos. b) Piuria (≥10 leucocitos por ml, o ≥ 3 leucocitos por ml al analizar con un campo de gran aumento una muestra de orina no centrifugada). c) Visualización de microorganismos en una tinción de Gram de orina no centrifugada. . Y el urocultivo ha sido positivo (103-105 ufc/ml) a 2 microorganismos diferentes como máximo. 4) El paciente NO tenía sonda vesical en el momento de la recogida de las muestras microbiológicas NI 48 horas anteriores Y al menos UNO de los siguientes en ausencia de otra causa reconocible: fiebre (>38ºC), urgencia miccional, polaquiuria, disuria, hipersensibilidad o dolor en la región suprapúbica o en el ángulo costovertebral y al menos uno de los siguientes hallazgos: a) b) c) La tira reactiva es positiva en orina para la esterasa leucocitaria y/o nitratos. Piuria (>10 leucocitos por ml, o > 3 leucocitos por ml al analizar con un campo de gran aumento una muestra de orina no centrifugada). Visualización de microorganismos en una tinción de Gram de orina no centrifugada. . Y el urocultivo ha sido positivo (103-105 ufc/ml) a 2 microorganismos diferentes como máximo. 5) Un paciente de 12 meses de edad o menor, con o sin sonda urinaria, que presenta cualquiera de los siguientes en ausencia de otra causa reconocible: fiebre (>38° central), hipotermia (<36° central), apnea, bradicardia, disuria, letargia o vómitos Y un urocultivo positivo (más de 105 colonias/ml) a dos microorganismos diferentes como máximo. 6) Un paciente de 12 meses de edad o menor, con al menos uno de los siguientes en ausencia de otra causa reconocible: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, disuria, letargia o vómitos y al menos uno de los siguientes: a) La tira reactiva es positiva en orina para la esterasa leucocitaria y/o nitratos. b) Piuria (> 10 leucocitos por ml o > 3 leucocitos por ml al analizar con un campo de gran aumento una muestra no centrifugada). c) Visualización de microorganismos en una tinción de Gram de orina no centrifugada. Y el urocultivo ha sido positivo (103-105 ufc/ml) a 2 microorganismos diferentes como máximo. 1.2 Infección asintomática de las vías urinarias con Bacteriemia (código IAVU) Paciente de cualquier edad, con o sin sonda urinaria, que no tiene signos o síntomas y un urocultivo positivo (más de 105 colonias /ml) a dos patógenos diferentes como máximo y un hemocultivo positivo para al menos un patógeno urinario coincidente con el del urocultivo, o por lo menos SVIRAS. Anexo I. Rev 2014. pág.23 dos hemocultivos separados en el tiempo si el microorganismo coincidente con el urocultivo es un contaminante habitual de la piel. Comentarios: La fiebre no es diagnóstica de infección urinaria en los mayores de 65 años, por lo que su presencia en este grupo de edad no les impide cumplir los criterios. Patógenos urinarios son: bacterias gram negativas (BGN),Sstaphylococcus spp, levaduras, Streptococcus spp. betahemolíticos, Enterococcus spp, G vaginales, Aerococcus urinare y Corynebacterium (ureasa positivo). 1.3 Otras infecciones de las vías urinarias (riñón, uréter, vejiga, uretra o tejidos de los espacios retroperitoneal o perinefrítico) (código: IVU2) Deben cumplir al menos uno de los siguientes criterios: 1) En el cultivo de un tejido o fluido (que no sea orina) de la zona afectada se ha aislado un microorganismo. 2) Por inspección directa, o en una intervención quirúrgica o en un estudio anatomopatológico se ha observado un signo claro de infección (ej. Absceso). 3) Dos de los siguientes en ausencia de otra causa reconocible: fiebre (>38°), dolor o tensión en la zona afectada y al menos uno de los siguientes: a) Drenaje purulento de la zona afectada. b) Aislamiento de un microorganismo en el hemocultivo que sea compatible con estas localizaciones. c) Evidencia radiológica de infección. 4) Al menos uno de los siguientes signos o síntomas en un paciente de edad menor de 12 meses en ausencia de otra causa reconocible: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, disuria, letargia o vómitos, y al menos uno de los siguientes: a) Drenaje purulento de la zona afectada. b) Aislamiento de un microorganismo en el hemocultivo que sea compatible con estas localizaciones. c) Evidencia radiológica de infección. Instrucciones: • Las infecciones que siguen a una circuncisión en neonatos deben clasificarse como CIRC (ver apartado infección de la piel y partes blandas). • Un cultivo positivo de una punta de sonda urinaria no es una prueba de laboratorio aceptable para diagnosticar una infección del tracto urinario. • Para que una muestra de orina sea valorable para el diagnóstico de una infección nosocomial, debe obtenerse de forma aséptica, utilizando una técnica adecuada (recogida limpia, cateterización de vejiga, aspiración suprapúbica). SVIRAS. Anexo I. Rev 2014. pág.24 • En lactantes, el urocultivo debería obtenerse por cateterización vesical o punción suprapúbica: un urocultivo positivo obtenido de una muestra de bolsa colectora de orina no es fiable, y debería ser confirmado por una muestra obtenida de forma aséptica por cateterización vesical o punción suprapúbica. SVIRAS. Anexo I. Rev 2014. pág.25 2 CRITERIOS PARA QUIRÚRGICO DIAGNOSTICAR UNA INFECCIÓN DEL SITIO Las infecciones de sitio quirúrgico se dividen en dos tipos: las incisionales y las de órgano o espacio. A su vez, las incisionales se subdividen en dos tipos, la superficial y la profunda. Las infecciones incisionales superficiales son aquellas que afectan sólo la piel y el tejido celular subcutáneo, mientras que las profundas afectan los tejidos blandos profundos de la incisión. La infección de órgano o espacio, abierto o manipulado durante el acto operatorio, afecta a cualquier parte de la anatomía (órgano o espacio) diferente de la incisión. 2.1 Infección superficial de la incisión Debe cumplir los siguientes criterios: Se produce durante los 30 días posteriores a la cirugía y afecta sólo piel y tejido celular subcutáneo en el lugar de la incisión y ha de hallarse presente al menos uno de los siguientes criterios: a) Exudado purulento de la incisión superficial. b) Aislamiento de un microorganismo en el cultivo de un líquido o de un tejido procedente de la incisión superficial (a partir de una muestra obtenida de forma aséptica). c) Al menos uno de los siguientes signos o síntomas de infección: dolor o hipersensibilidad al tacto o a la presión, inflamación localizada (calor, tumefacción, eritema) y la incisión superficial es abierta deliberadamente por el cirujano y existe un cultivo positivo o no se ha realizado ningún cultivo. Este criterio no se cumple si existe cultivo negativo. d) Diagnóstico médico de infección superficial de la incisión. Existen 2 tipos específicos de infección superficial de la incisión: 1) Primarias (código: ISI1). Son las infecciones superficiales producidas en la incisión primaria realizada a un paciente al que se le han realizado más de una incisión quirúrgica durante la intervención (por ejemplo, la incisión en el tórax realizada durante una intervención de by-pass coronario que emplea un injerto procedente de otra parte del cuerpo). 2) Secundarias (código: ISI2). Son las infecciones superficiales producidas en la incisión secundaria realizada a un paciente al que se le han realizado más de una incisión quirúrgica durante la intervención (por ejemplo, la incisión en la pierna realizada durante una intervención de by-pass coronario que emplea un injerto procedente de esta localización). Instrucciones: Un absceso mínimo del punto de sutura (mínima inflamación y drenaje purulento confinados a la zona de inserción del punto de sutura) no se considera infección superficial de la incisión. SVIRAS. Anexo I. Rev 2014. pág.26 • Una quemadura infectada no se considera infección superficial de la incisión (deberá catalogarse como infección de la quemadura (código: QUEM). • Si el punto por donde penetra el tubo de drenaje colocado durante una intervención quirúrgica en la piel se ha infectado, la infección no se considerará quirúrgica, sino de la piel o de los tejidos blandos, según su profundidad. • Si la infección incisional se extiende o afecta a fascias o capas musculares, deberá catalogarse como Infección profunda de la incisión - IPI. • Si una infección cumple criterios tanto de infección superficial como profunda de la incisión, deberá catalogarse como infección profunda de la incisión - IPI. • En general, en cualquier intervención quirúrgica que requiera varias incisiones en distintos sitios de una misma área corporal o espacio y que constituyan el objetivo principal de la cirugía, se considerarán todas ellas como primarias, a no ser que no se usen para el procedimiento principal (p.e: que sólo se realicen para colocar tubos de drenaje). 2.2 Infección profunda de la incisión Debe cumplir los siguientes criterios: Se produce durante los 30 días posteriores a la cirugía si no se ha colocado ningún implante2, o dentro del primer año si se había colocado alguno, y la infección está relacionada con el procedimiento quirúrgico, y la infección afecta los tejidos blandos profundos de la incisión (fascia y paredes musculares), y ha de hallarse presente al menos uno de los siguientes criterios: a) Exudado purulento de la zona profunda de la incisión pero no de los órganos o espacios. b) La incisión profunda presenta dehiscencias espontáneamente o la abre el cirujano y existe un cultivo positivo o no se ha realizado cultivo y el paciente tiene al menos uno de los siguientes signos o síntomas: fiebre (>38°), dolor localizado o hipersensibilidad al tacto o a la presión. Este criterio no se cumple si existe cultivo negativo. c) Durante una reintervención o por inspección directa o por estudio histopatológico o radiológico, se halla un absceso u otra evidencia de infección que afecta los tejidos profundos de la incisión. d) Diagnóstico médico de infección profunda de la incisión. 2 Cualquier objeto, material o tejido de origen no humano como prótesis valvular cardíaca, injerto vascular no humano, prótesis de cadera, o corazón artificial, malla de herniorrafia, que se implanta de forma permanente durante una intervención quirúrgica y no se manipula de forma rutinaria con fines diagnósticos o terapéuticos. SVIRAS. Anexo I. Rev 2014. pág.27 Existen 2 tipos específicos de infección profunda de la incisión: 1) Primarias (código: IPI1). Son las infecciones profundas producidas en la incisión primaria realizada a un paciente al que se le han realizado más de una incisión quirúrgica durante la intervención (p.e.: la incisión en el tórax realizada durante una intervención de by-pass coronario que emplea un injerto procedente de otra parte del cuerpo). 2) Secundarias (código: IPI2). Son las infecciones profundas producidas en la incisión secundaria realizada a un paciente al que se le han realizado más de una incisión quirúrgica durante la intervención (p.e.: la incisión en la pierna realizada durante una intervención de by-pass coronario que emplea un injerto procedente de esta localización). Instrucciones: Si una infección cumple criterios tanto de infección superficial como profunda de la incisión, deberá catalogarse como infección profunda de la incisión - IPI. 2.3 Infección de órgano o de espacio (código: IQOE) Una infección de órgano o de espacio afecta a cualquier parte del cuerpo distinta de la incisión (piel, músculos o fascias), abierta o manipulada durante el procedimiento operatorio. Por ejemplo, la apendicectomía con absceso subdiafragmático subsecuente sería un caso típico de infección de órgano/espacio intraabdominal. La infección de órgano o de espacio debe cumplir los siguientes criterios: Se produce en los 30 días posteriores a la intervención si no se han colocado implantes (cualquier objeto, material o tejido de origen no humano como prótesis valvular cardíaca, injerto vascular no humano, prótesis de cadera, o corazón artificial, que se implanta de forma permanente durante una intervención quirúrgica y no se manipula de forma rutinaria con fines diagnósticos o terapéuticos), o en el curso del año siguiente a la intervención si se han colocado, y la infección está relacionada con el procedimiento quirúrgico, y la infección afecta cualquier parte del cuerpo distinta de la incisión (piel, músculos o fascias), abierta o manipulada durante el procedimiento operatorio y ha de hallarse presente al menos uno de los siguientes criterios: 1) Líquido purulento recogido mediante drenaje colocado en un órgano o un espacio. 2) Aislamiento de microorganismos en muestras obtenidas de forma aséptica a partir de fluidos o tejidos procedentes de órganos o espacios. 3) Durante una reintervención, o por inspección directa, o por estudio histopatológico o radiológico, se halla un absceso u otra evidencia de infección que afecta a algún órgano o espacio. 4) Diagnóstico médico de infección quirúrgica de órgano/espacio. SVIRAS. Anexo I. Rev 2014. pág.28 Instrucciones: 1) Localizaciones específicas de la infección de órgano/espacio. • • • • • • Infección arterial o venosa Absceso mamario o mastitis Espacio discal Oído, mastoides Endometritis Ojo, excepto conjuntivitis • • • • • • • • • • • Tracto gastrointestinal Intraabdominal no especificada en otro lugar Intracraneal, absceso cerebral o de la duramadre Articular • • Mediastinitis • • • Meningitis o ventriculitis Miocarditis o pericarditis Cavidad oral (boca, lengua o encías) Osteomielits Otras infecciones del tracto urinario Otras infecciones del aparato reproductos masculino femenino Sinusitis Absceso espinal sin meningitis Tracto respiratorio superior: faringitis, laringitis, epiglotitis Infección del fondo de saco vaginal (FSAC) Endocarditis 2) Ocasionalmente, una infección de órgano/espacio drena a través de la incisión. En general estas infecciones no requieren reintervenciones y se consideran como complicaciones de la incisión, por lo que se clasificarán como infecciones incisionales profundas (IPI). SVIRAS. Anexo I. Rev 2014. pág.29 3 CRITERIOS PARA DIAGNOSTICAR UNA BACTERIEMIA 3.1 Bacteriemia confirmada por laboratorio (código: BACT) Los criterios 1 y 2 de bacteriemia confirmada por laboratorio pueden aplicarse a pacientes de cualquier edad, incluidos los <12 meses. La bacteriemia confirmada por laboratorio ha de cumplir al menos uno de los siguientes criterios: 1. En al menos un tubo de las muestras de sangre obtenidas para realizar el hemocultivo se ha aislado un microorganismo que no es un contaminante habitual de la piel3, y el microorganismo aislado en el hemocultivo no tiene relación con otro foco infeccioso. 2. Uno de los siguientes signos o síntomas: fiebre (>38°), escalofríos o hipotensión. Y en al menos dos hemocultivos que no se han practicado simultáneamente (pero con menos de 48 horas de diferencia entre sí), se ha aislado el mismo contaminante habitual de la piel3. Y los síntomas, signos o hallazgos de laboratorio no tienen relación con otro foco infeccioso. 3. Al menos uno de los siguientes síntomas o signos sin relación con otro foco infeccioso en un paciente de edad <12 meses: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, o bradicardia, y en al menos dos hemocultivos que no se han practicado simultáneamente (pero con menos de 48 horas de diferencia entre sí), se ha aislado el mismo contaminante habitual de la piel4. Comentarios: Idealmente, las muestras de sangre para hemocultivo deberían recogerse en 2-4 tubos obtenidos de distintos sitios por venopunción (p.e: venas antecubitales izquierda y derecha) y no a través de un catéter vascular. Estos tubos deberían extraerse simultáneamente o en un periodo breve de tiempo (unas pocas horas como máximo). Si las muestras no se han obtenido siguiendo esta técnica, aún es posible usar los criterios descritos arriba para catalogar las bacteriemias confirmadas por laboratorio, aunque no es la situación ideal. Aspectos a considerar al determinar si se trata del mismo microorganismo contaminante habitual de la piel el que se ha aislado en 2 hemocultivos diferentes: • Si en un hemocultivo se identifica la especie del microorganismo y en otro hemocultivo se identifica sólo el género, se asume que se trata del mismo microorganismo y se identificará a la especie como la causante de la infección (ejemplos en la Tabla 1). • Si se identifica en los dos hemocultivos la especie del patógeno contaminante pero no se realiza antibiograma o sólo se realiza en uno de los hemocultivos, se asume que se trata del mismo microorganismo. 3 P.e.: S. aureus, Enterococcus spp, E. coli, Pseudomonas spp, Klebsiella spp, Candida spp P.e.: difteroides (Corynebacterium spp), Bacillus (excepto B anthracis) spp, Propionibacterium spp, Staphylococcus coagulasa negativos (incluyendo S. epidermidis), S. viridans, Aerococcus spp, Micrococcus spp. 4 SVIRAS. Anexo I. Rev 2014. pág.30 • Si los microorganismos contaminantes habituales de la piel aislados en dos hemocultivos distintos tienen antibiogramas diferentes para uno o más antimicrobianos de las principales familias estudiadas, se asume que los microorganismos son diferentes (ejemplos en la Tabla 2). • Para los propósitos de este sistema de vigilancia, la categoría intermedia (I) del antibiograma no debe usarse para distinguir si dos microorganismos son el mismo. Tabla 1. Ejemplos para determinar la identidad de microorganismos aislados en hemocultivos diferentes Primer cultivo Segundo cultivo Catalogar como: S. epidermidis S. coagulasa-negativo S. epidermidis Bacillus spp B. cereus B. cereus S salivarius S. viridans S. salivarius Tabla 2. Ejemplos para determinar la identidad de microorganismos aislados en hemocultivos diferentes. Resultados del antibiograma (S: sensible; R: resistente) Microorganismo Antibiograma del primer cultivo Antibiograma del segundo cultivo Catalogar como: S. epidermidis Todos los antimicrobianos: S Todos los antimicrobianos: S Mismo microorganismo S. epidermidis Oxacilina: R Gentamicina: R Oxacilina: S Gentamicina: S Diferente Penicilina: R Ciprofloxacino: S Resto de antimicrobianos: S Penicilina: S Ciprofloxacino: R Resto de antimicrobianos: S Diferente Todos los antimicrobianos de las principales familias: S Todos los antimicrobianos de las principales familias: S excepto Penicilina: R Diferente Corynebacterium spp Streptococcus viridans Instrucciones: • Las flebitis purulentas confirmadas con un cultivo semicuantitativo de una punta de catéter pero en las que no se ha realizado hemocultivo o éste es negativo, deberán considerarse como flebitis o arteritis (FLEB), no como bacteriemias. • Clasificar como BACT sólo cuando se ha descartado otro foco de infección. 3.2 Sepsis clínica (código: SEPC) El diagnóstico de sepsis clínica puede usarse en neonatos y lactantes de 12 meses o menos. No puede emplearse para catalogar bacteriemias primarias en niños mayores o adultos. SVIRAS. Anexo I. Rev 2014. pág.31 Una sepsis clínica ha de cumplir el siguiente criterio: en un paciente de edad igual o inferior a 12 meses, al menos uno de los siguientes signos o síntomas si no se encuentra ninguna otra causa: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, y no se ha practicado ningún hemocultivo o no se ha aislado ningún microorganismo, y no se ha descubierto ningún otro foco infeccioso, y el médico ha prescrito el tratamiento antibiótico adecuado para una sepsis. SVIRAS. Anexo I. Rev 2014. pág.32 4 CRITERIOS PARA DIAGNOSTICAR UNA NEUMONÍA La neumonía se define independientemente del resto de infecciones de las vías respiratorias bajas. Para diagnosticarla se han incluido diversas combinaciones de signos clínicos, radiológicos y de laboratorio. Normalmente, los cultivos de las secreciones respiratorias expectoradas por el paciente no son útiles para el diagnóstico pero sí para la identificación del agente y de su perfil de resistencias. El diagnóstico efectuado a partir de una serie de radiografías es más fiable que el obtenido con una única radiografía. Existen 3 tipos específicos de neumonía: • • • Neumonía definida clínicamente (código: NEU1). Neumonía con hallazgos de laboratorio específicos (código: NEU2). Neumonía en el paciente inmunocomprometido (código: NEU3). A continuación se presentan los comentarios generales que son aplicables a todos los tipos específicos de neumonía, así como los algoritmos (Tablas 3-6, Figuras 1 y 2), e instrucciones para la declaración de los casos. Comentarios generales: 1) El diagnóstico clínico aislado de neumonía por parte de un médico no es un criterio suficiente para catalogarla como neumonía nosocomial. 2) A pesar de que se incluyen criterios específicos en el caso de los niños, los pacientes pediátricos pueden cumplir cualquier otro criterio de un tipo específico de neumonía. 3) Cuando se valore si un paciente presentó realmente una neumonía es importante distinguir entre los cambios en el estado clínico que puedan deberse a otras condiciones tales como: infarto de miocardio, embolismo pulmonar, síndrome de distrés respiratorio, atelectasias, procesos malignos, enfermedad pulmonar obstructiva crónica, enfermedad de la membrana hialina, displasia broncopulmonar, etc. Además debe prestarse atención especial cuando se evalúen pacientes intubados para distinguir entre: colonización traqueal, infecciones del tracto respiratorio superior (p.e.: traqueobronquitis) o el inicio temprano de una neumonía. Finalmente debe reconocerse que puede ser difícil determinar la neumonía nosocomial en los ancianos, niños y pacientes inmunocomprometidos porque debido a tales condiciones se pueden enmascarar los síntomas y signos habitualmente asociados a una neumonía. Se han incluido criterios específicos para estos grupos especiales incluidos en la definición de neumonía nosocomial. 4) La neumonía nosocomial puede ser caracterizada por su inicio: precoz o tardía. La precoz ocurre durante los primeros 4 días de la hospitalización y a menudo está causada por Moxarella catharralis, H influenzae y S pneumoniae. En las de inicio tardío los microorganismos habitualmente implicados son bacilos gramnegativos y S Aureus, incluyendo SAMR. Los virus (gripe A, B o VRS) pueden causar neumonía precoz o tardía mientras que los hongos, Legionella y Pnemocisitis carinii provocan neumonía tardía. SVIRAS. Anexo I. Rev 2014. pág.33 5) La neumonía debida a una aspiración (p.e: en el contexto de una intubación realizada en sala de urgencias o en sala de operaciones), es considerada como nosocomial si cumple alguno de los criterios específicos y no era una neumonía que se encontraba presente o incubándose en el momento de admisión. 6) En pacientes críticamente enfermos con estancias hospitalarias prolongadas pueden ocurrir múltiples episodios de neumonía nosocomial. A la hora de determinar si se han producido múltiples episodios de neumonía nosocomial en un único paciente, se debería buscar evidencia de la resolución de la infección inicial. La adición o cambio de patógeno por sí solo no es indicativo de un nuevo episodio de neumonía; se requiere la combinación de nuevos signos, síntomas y evidencia radiográfica u otra prueba diagnóstica adicional. 7) La positividad de la tinción de Gram (para bacterias) y la de hidróxido de potasio (KOH) (para fibras de elastina y/o hifas fúngicas) en muestras de esputo correctamente recogidas es una pieza clave para averiguar la etiología de la infección. Sin embargo las muestras de esputo se encuentran a menudo contaminadas con colonizadores de la vía aérea por lo que deben ser interpretadas con cautela. En particular, Candida se observa con frecuencia en las tinciones pero es una causa infrecuente neumonías nosocomiales. Instrucciones: 1) Hay una jerarquía de categorías específicas: Si un paciente cumple criterios para más de un tipo específico, debe declararse solamente uno: a) Si un paciente cumple criterios para NEU1 y NEU2, debe declararse como NEU2. b) Si un paciente cumple criterios para NEU2 y NEU3, debe declararse como NEU3. c) Si un paciente cumple criterios para NEU1 y NEU3, debe declararse como NEU3. 2) Se catalogarán como neumonía aquellas infecciones de tracto respiratorio inferior (p.e: absceso o empiema), concurrentes con una neumonía debida al mismo organismo. 3) El absceso pulmonar o el empiema sin neumonía se clasifican como OIRE. 4) La bronquitis, traqueítis, traqueobronquitis o bronquiolitis sin neumonía se clasificarán como IRVB. SVIRAS. Anexo I. Rev 2014. pág.34 Tabla 3. Algoritmo para la neumonía definida clínicamente (NEU1) RADIOLOGÍA 2 o más radiografías de tórax sucesivas con al menos 1 de los siguientes1,2: • Infiltrado nuevo o progresivo y persistente • Consolidación • Cavitación • Neumatoceles en <1 año. NOTA: En paciente sin enfermedad cardiaca o pulmonar subyacente (p.e.: síndrome de distrés respiratorio, displasia broncopulmonar, edema pulmonar, EPOC), es aceptable 1 radiografía de tórax definitiva. SIGNOS/SÍNTOMAS Para CUALQUIER PACIENTE, al menos 1 de los siguientes: • Fiebre (>38°) sin otra causa reconocida • Leucopenia (<4000/mm3) o leucocitosis (> 12000/mm3) Para adultos >70 años, estado mental alterado sin otra causa reconocida y al menos 2 de los siguientes: • Aparición de esputo purulento3, o cambios en las características del esputo4, o secreciones respiratorias, o requerimientos de succión • Aparición o empeoramiento de tos, disnea o taquipnea5 • Crepitantes o roncus o sibilantes • Empeoramiento del intercambio gaseoso (desaturación de O2 [p.e.: PaO2/F¡O2s240], f requerimientos de O2 o f demanda ventilatoria) CRITERIOS ALTERNATIVOS para niños <1 año: Empeoramiento del intercambio gaseoso (p.e.: desaturación O21 requerimientos de O2 o demanda ventilatoria) y al menos 3 de los siguientes: • Inestabilidad de la temperatura corporal sin otra causa reconocida. • Leucopenia (<4000/mm3) o leucocitosis (al 5000/mm3) y desviación izquierda (>10% de formas jóvenes [cayados]) • Aparición de esputo purulento, o cambios en las características del esputo, o aumento de secreciones respiratorias, o mayores requerimientos de succión • Apnea, taquipnea, aleteo nasal con retracción costal o quejido • Sibilantes, crepitantes o roncus • Tos • Bradicardia (<100 lpm) o taquicardia (>170 lpm). CRITERIOS ALTERNATIVOS para niños >1 año o <12 años, al menos 3 de los siguientes: • Fiebre (>38,4°) o hipotermia (<36,5°) sin otra causa reconocida. • Leucopenia (< 4000/mm3) o leucocitosis (£15000/ mm3) y desviación izquierda (>10% de formas jóvenes [cayados]) • Aparición de esputo purulento, o cambios en las características del esputo, o 1 secreciones respiratorias, o requerimientos de succión. • Aparición o empeoramiento de tos o disnea, apnea o taquipnea • Crepitantes o ruidos bronquiales • Empeoramiento del intercambio gaseoso (p.e.: desaturación O2 [p.e., pulsioximetría < 94%] o mayor requerim. de O2 o demanda ventilatoria). 1 2 3 4 Ocasionalmente en pacientes no ventilados, el diagnóstico de neumonía nosocomial puede ser claro basándose en síntomas, signos y una sola radiografía de tórax. Sin embargo, en pacientes con enfermedad pulmonar y cardiaca puede ser particularmente difícil. Otras condiciones no infecciosas (p.e.: edema pulmonar en una insuficiencia cardiaca congestiva) puede simular la presentación de una neumonía. Para ayudar a confirmar los casos difíciles, puede ser útil revisar radiografías el día del diagnóstico, 3 días previos al diagnóstico y en los días 2 y 7 después del diagnóstico. La neumonía puede tener una aparición y progresión rápida pero no se resuelve rápidamente; los cambios radiográficos de la neumonía se resuelven en semanas. Debido a esto, un cambio radiográfico rápido sugiere que el paciente no tiene neumonía sino otro proceso no infeccioso tal como atelectasias o insuficiencia cardiaca congestiva. Existen muchas formas de describir la apariencia radiográfica de la neumonía. Los ejemplos incluyen (pero no están limitados a): opacificación focal, áreas de condensación con incremento de densidad. A pesar de que para el radiólogo estos hallazgos no se atribuyen específicamente a la neumonía en el entorno clínico estas descripciones alternativas deberían ser consideradas seriamente como hallazgos positivos. El esputo purulento consiste en secreciones procedentes de los pulmones, bronquios o traquea que contienen > 25 neutrófilos y < 10 células epiteliales escamosas mediante examen microscópico de bajo aumento (x100). Si los informes del laboratorio locales lo informan de manera cualitativa (p.e.: "abundantes leucocitos", "pocas células escamosas") es necesario asegurarse que estas descripciones se ajustan a la definición de esputo purulento. Esta confirmación de laboratorio es requerida debido a que la descripción clínica de esputo purulento es muy variable. Una sola observación de esputo purulento o cambio en las características del esputo no es significativa, sin embargo repetidas observaciones en un periodo de 24 horas serían indicativas de aparición de un proceso infeccioso. Los cambios en las características del esputo se refieren al color, consistencia, olor y cantidad. SVIRAS. Anexo I. Rev 2014. pág.35 5 En adultos, la taquipnea es definida como > 25 respiraciones por minuto (rpm). En el caso de lactantes prematuros < 37 semanas y hasta 40 semanas de gestación se considera taquipnea >75 rpm. En lactantes <2 meses se considera > 60 rpm. Entre los 2 meses y los 12 meses, >50 rpm y en niños mayores de 1 año >30 rpm. SVIRAS. Anexo I. Rev 2014. pág.36 Tabla 4. Algoritmo para neumonías con hallazgos específicos de laboratorio (NEU2) RADIOLOGÍA 2 o más radiografías de tórax sucesivas con al menos uno de los siguientes [6,7]: • • Infiltrado nuevo o progresivo y persistente Consolidación • Cavitación • Neumatoceles en menores de 1 año NOTA: En paciente sin enfermedad cardiaca o pulmonar subyacente (p.e.: síndrome de distrés respiratorio, displasia broncopulmonar, edema pulmonar, EPOC), es aceptable 1 radiografía de tórax definitiva. 6 7 8 9 10 SIGNOS/SÍNTOMAS LABORATORIO Al menos 1 de los siguientes [11,12]: Al menos 1 de los siguientes: • • • Fiebre (> 38°) sin otra causa reconocida Leucopenia (<4000/mm3) o leucocitosis (>12000/ mm3) Para adultos > 70 años, estado mental alterado sin otra causa reconocida Y al menos 1 de los siguientes: • Aparición de esputo purulento [8], o cambios en las características del esputo [9], o incremento de secreciones respiratorias, o mayores requerimientos de succión • Aparición o empeoramiento de tos, disnea o taquipnea [10] • Crepitantes o roncus o sibilantes • Empeoramiento del intercambio gaseoso (desaturación de O2 [p.e.: PaO2/FiO2 £ 240], más requerimientos O2 o más demanda ventilatoria). • Hemocultivo (+) [13] no relacionado con otra fuente de infección • • Cultivo de líquido pleural (+) Cultivo cuantitativo (+) de muestra del tracto respiratorio inferior obtenida por lavado broncoalveolar o cepillado bronquial protegido >5% células (obtenidas por LBA) conteniendo bacterias intracelulares en el examen microscópico directo El examen histopatológico muestra al menos 1 de los siguientes: a) Formación de absceso o foco de consolidación con acumulación intensa de PMN en bronquiolos y alvéolos; b) Cultivo positivo cuantitativo [14] del parénquima pulmonar; c) Evidencia de invasión del parénquima pulmonar por hifas fungales o pseudohifas Cultivo de secreciones respiratorias (+) a virus o Chlamydia • • • • • • Detección (+) de antígenos virales o anticuerpos en secreciones respiratorias (p.e.: EIA, PCR) Cuadriplicación de los niveles de IgG en 2 muestras sucesivas para un determinado patógeno (p.e.: virus de la gripe, Chlamydia) PCR (+) para Chlamydia o Mycoplasma; Test de micro-IF (+) para Chlamydia • Cultivo o micro-IF (+) para Legionella spp. de secreciones o tejido respiratorio • • Detección de antígenos de Legionella pneumophila serogrupo 1 en orina mediante RIA o EIA Cuadriplicación del título de anticuerpos para L pneumophila > 1:128 en muestras sucesivas de suero (fase aguda y convalescenciente) mediante AIF indirectos. Ocasionalmente en pacientes no ventilados, el diagnóstico de neumonía nosocomial puede ser claro basándose en síntomas, signos y una sola radiografía de tórax. Sin embargo, en pacientes con enfermedad pulmonar y cardiaca puede ser particularmente difícil. Otras condiciones no infecciosas (p.e.: edema pulmonar en una insuficiencia cardiaca congestiva) puede simular la presentación de una neumonía. Para ayudar a confirmar los casos difíciles, puede ser útil revisar radiografías el día del diagnóstico, 3 días previos al diagnóstico y en los días 2 y 7 después del diagnóstico. La neumonía puede tener una aparición y progresión rápida pero no se resuelve rápidamente; los cambios radiográficos de la neumonía se resuelven en semanas. Debido a esto, un cambio radiográfico rápido sugiere que el paciente no tiene neumonía sino otro proceso no infeccioso tal como atelectasias o insuficiencia cardiaca congestiva. Existen muchas formas de describir la apariencia radiográfica de la neumonía. Los ejemplos incluyen (pero no están limitados a): opacificación focal, áreas de condensación con incremento de densidad. A pesar de que para el radiólogo estos hallazgos no se atribuyen específicamente a la neumonía en el entorno clínico estas descripciones alternativas deberían ser consideradas seriamente como hallazgos positivos. El esputo purulento consiste en secreciones procedentes de los pulmones, bronquios o traquea que contienen >25 neutrófilos y <10 células epiteliales escamosas mediante examen microscópico de bajo aumento (x100). Si los informes del laboratorio locales lo informan de manera cualitativa (p.e.: "abundantes leucocitos", "pocas células escamosas”) es necesario asegurarse que estas descripciones se ajustan a la definición de esputo purulento. Esta confirmación de laboratorio es requerida debido a que la descripción clínica de esputo purulento es muy variable. Una sola observación de esputo purulento o cambio en las características del esputo no es significativa, sin embargo repetidas observaciones en un periodo de 24 horas serían indicativas de aparición de un proceso infeccioso. Los cambios en las características del esputo se refieren al color, consistencia, olor y cantidad. En adultos, la taquipnea es definida como >25 respiraciones por minuto (rpm). En el caso de lactantes prematuros <37 semanas y hasta 40 semanas de gestación se considera taquipnea >75 rpm. En lactantes <2 meses se considera >60 rpm. Entre los 2 meses y los 12 meses, >50 rpm y en niños mayores de 1 año >30 rpm. SVIRAS. Anexo I. Rev 2014. pág.37 11 12 13 14 Tras la aparición de un caso confirmado por laboratorio de neumonía debida al virus respiratorio sincitial (VRS), adenovirus o virus de la gripe en el entorno hospitalario, el diagnóstico presuntivo por parte del médico en casos consecutivos con signos y síntomas similares se acepta como criterio válido para neumonía nosocomial debida a estos patógenos. En la tinción de Gram de secreciones respiratorias de pacientes con neumonía debida a Legionella spp, Mycoplasma o virus, pueden verse pocos microorganismos. Se debe prestar especial atención a la etiología de la neumonía en un paciente con hemocultivo positivo y evidencia radiográfica de neumonía, especialmente si el paciente presenta catéteres intravasculares o urinarios. En general, en un paciente inmunocompetente, los hemocultivos positivos a Staphilococcus plasmocoagulasa negativo, contaminantes comunes de la piel y las levaduras no constituirían el agente etiológico de la neumonía. Utilizar como referencia los valores que aparecen en la Tabla 11. Un aspirado endotraqueal no es una muestra mínimamente contaminada, por lo tanto no cumpliría con los criterios de laboratorio de la tabla de referencia n° 11. SVIRAS. Anexo I. Rev 2014. pág.38 Tabla 5. Algoritmos para neumonía en pacientes inmunocomprometidos (NEU3) RADIOLOGÍA SIGNOS/SÍNTOMAS LABORATORIO 2 o más radiografías de tórax Pacientes inmunocomprometidos 17 Al menos 1 de los siguientes: sucesivas con al menos 1 de los que tengan al menos 1 de los • Hemocultivo (+) y cultivo de siguientes1516: siguientes: esputo (+) a Candida, 22 • • Infiltrado nuevo o • Fiebre (> 38°) sin otra causa Evidencia de hongos o progresivo y reconocida Pneumocytis jiroveci persistente. • Para adultos >70 años, estado (examen microscópico • Consolidación mental alterado sin otra causa directo o cultivo positivo) reconocida • Cavitación en una muestra del tracto 18 • Neumatoceles en <1 • Aparición de esputo purulento , respiratorio inferior o cambios en las características del obtenida por lavado año esputo19, o secreciones bronocoalveolar o respiratorias, o requerimientos cepillado broquial NOTA: En paciente sin de succión enfermedad cardiaca o pulmonar protegido subyacente (p.e.: síndrome de • Aparición o empeoramiento de Cualquiera de los criterios tos, o disnea o taquipnea distrés respiratorio, displasia de laboratorio definidos broncopulmonar, edema • Crepitantes o roncus o para NEU2. pulmonar, EPOC), es aceptable sibilantes 1 radiografía de tórax definitiva. • Empeoramiento del intercambio gaseoso (desaturación de O2 [p.e.PaO2/FiO2 <240], requerimientos O2 o demanda ventilatoria) • Hemoptisis • Dolor pleurítico. 15 Ocasionalmente en pacientes no ventilados, el diagnóstico de neumonía nosocomial puede ser claro basándose en síntomas, signos y una sola radiografía de tórax. Sin embargo, en pacientes con enfermedad pulmonar y cardiaca puede ser particularmente difícil. Otras condiciones no infecciosas (p.e.: edema pulmonar en una insuficiencia cardiaca congestiva) puede simular la presentación de una neumonía. Para ayudar a confirmar los casos difíciles, puede ser útil revisar radiografías el día del diagnóstico, 3 días previos al diagnóstico y en los días 2 y 7 después del diagnóstico. La neumonía puede tener una aparición y progresión rápida pero no se resuelve rápidamente; los cambios radiográficos de la neumonía se resuelven en semanas. Debido a esto, un cambio radiográfico rápido sugiere que el paciente no tiene neumonía sino otro proceso no infeccioso tal como atelectasias o insuficiencia cardiaca congestiva. 16 Existen muchas formas de describir la apariencia radiográfica de la neumonía. Los ejemplos incluyen (pero no están limitados a): opacificación focal, áreas de condensación con incremento de densidad. A pesar de que para el radiólogo estos hallazgos no se atribuyen específicamente a la neumonía en el entorno clínico estas descripciones alternativas deberían ser consideradas seriamente como hallazgos positivos. 17 Pacientes inmunocomprometidos son aquellos con neutropenia (recuento absoluto de neutrófilos <500/mm3), leucemia, linfoma, VIH con recuento de CD4 <200, o esplenectomizados; quienes han sido trasplantados recientemente, están en terapia citotóxica o reciben corticoides a dosis altas (p.e.: >40 mg de prednisona en adultos o dosis equivalentes) diariamente durante al menos 2 semanas. 18 El esputo purulento consiste en secreciones procedentes de los pulmones, bronquios o traquea que contienen >25 neutrófilos y <10 células epiteliales escamosas mediante examen microscópico de bajo aumento (x100). Si los informes del laboratorio locales lo informan de manera cualitativa (p.e.: "abundantes leucocitos", "pocas células escamosas") es necesario asegurarse que estas descripciones se ajustan a la definición de esputo purulento. Esta confirmación de laboratorio es requerida debido a que la descripción clínica de esputo purulento es muy variable. 19 Una sola observación de esputo purulento o cambio en las características del esputo no es significativa, sin embargo repetidas observaciones en un periodo de 24 horas serían indicativas de aparición de un proceso infeccioso. Los cambios en las características del esputo se refieren al color, consistencia, olor y cantidad. 20 En adultos, la taquipnea es definida como >25 respiraciones por minuto (rpm). En el caso de lactantes prematuros < 37 semanas y hasta 40 semanas de gestación se considera taquipnea >75 rpm. En lactantes <2 meses se considera >60 rpm. Entre los 2 meses y los 12 meses, > 50 rpm y en niños mayores de 1 año >30 rpm. 21 Las muestras de esputo y para hemocultivo deben ser recogidas con un intervalo máximo de 48 horas entre ambas. SVIRAS. Anexo I. Rev 2014. pág.39 22 Los cultivos semicuantitativos o no cuantitativos de esputo obtenidos mediante tos intensa, inducción o aspiración o lavado son aceptables. Si los resultados de cultivos cuantitativos están disponibles, consultar los algoritmos para neumonías que incluyan hallazgos específicos de laboratorio. SVIRAS. Anexo I. Rev 2014. pág.40 Tabla 6. Valores de referencia para cultivos utilizados en el diagnóstico de neumonía Muestra recogida / Técnica Parénquima pulmonar * Muestras obtenidas por broncoscopia Lavado broncoalveolar Lavado broncoalveolar protegido Cepillado bronquial protegido ________ Valores > 10 ufc/g de tejido >104 ufc/ml >103 ufc/ml >103 ufc/ml Muestras no obtenidas por broncoscopia (a ciegas) Lavado broncoalveolar > 104 ufc/ml Lavado broncoalveolar protegido ____________________________> 103 ufc/ml ____ ufc: unidades formadoras de colonias. * Muestras obtenidas mediante biopsia a cielo abierto y muestras obtenidas en el postmortem inmediato mediante biopsia transtorácica o transbronquial. SVIRAS. Anexo I. Rev 2014. pág.41 SVIRAS. Anexo I. Rev 2014. pág.42 SVIRAS. Anexo I. Rev 2014. pág.43 5 CRITERIOS PARA DIAGNOSTICAR RESPIRATORIAS BAJAS UNA INFECCIÓN DE LAS VÍAS 5.1 Bronquitis, traqueobronquitis, bronquiolitis o traqueítis, sin neumonía (IRVB) Las infecciones traqueobronquiales deben cumplir al menos uno de los siguientes criterios: 1) No hay evidencias clínicas o radiológicas de neumonía, y al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), tos, aparición o aumento de la producción de esputo, roncus, sibilantes, y al menos uno de los siguientes: a) En el cultivo de una muestra de esputo obtenida por aspiración traqueal o broncoscopia se ha aislado un microorganismo. b) Resultado positivo de una prueba para la detección de antígenos en las secreciones respiratorias. 2) En un paciente <12 meses sin evidencias clínicas o radiológicas de neumonía, al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38° rectal), tos, aparición o aumento de la producción de secreciones respiratorias, roncus, sibilantes, distrés respiratorio, apnea o bradicardia y al menos uno de los siguientes: a) En el cultivo de una muestra de esputo obtenida por aspiración traqueal o broncoscopia se ha aislado un microorganismo. b) Resultado positivo de una prueba para la detección de antígenos en las secreciones respiratorias. c) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. Instrucciones: • Una bronquitis crónica en un paciente con enfermedad pulmonar crónica no se catalogará como IRVB a menos que existan pruebas (p.e.: cambio en el microorganismo aislado) de una infección aguda secundaria. 5.2 Otras infecciones del aparato respiratorio (código: OIAR) Las otras infecciones del aparato respiratorio deben cumplir al menos uno de los siguientes criterios: 1) En el frotis de una muestra de tejidos o líquidos pulmonares, incluyendo líquido pleural, se ha observado un microorganismo o se ha aislado al hacer el cultivo. 2) En una intervención quirúrgica o en un estudio anatomopatológico se ha observado un absceso pulmonar o un empiema. 3) En la exploración radiológica del tórax se ha observado un signo de absceso. SVIRAS. Anexo I. Rev 2014. pág.44 Instrucciones: • Si existe una infección concurrente del tracto respiratorio inferior y una neumonía causadas por el mismo organismo, se catalogará como neumonía. • Los abscesos pulmonares o empiemas sin neumonía se catalogarán como OIAR. SVIRAS. Anexo I. Rev 2014. pág.45 6 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN DEL APARATO DIGESTIVO Las infecciones del aparato digestivo incluyen las gastroenteritis, las hepatitis agudas y crónicas, las enterocolitis necrotizantes, las infecciones del tracto gastrointestinal y aquellas infecciones intraabdominales que no se han definido en ningún otro apartado. 6.1 Gastroenteritis (código: GAST) Una gastroenteritis debe cumplir al menos uno de los siguientes criterios: 1) Diarrea de aparición aguda (heces líquidas durante más de 12 horas), con o sin vómitos o fiebre (>38°), si tras el diagnóstico diferencial con una etiología no infecciosa (exploración complementaria, un tratamiento, agudización de un trastorno crónico o estrés psicológico, p.e.) ésta última es poco probable. 2) Al menos dos de los siguientes signos o síntomas en ausencia de otra causa que los explique: náuseas, vómitos, dolor abdominal o cefalea, y al menos uno de los siguientes: a) En un cultivo de heces o en un frotis rectal se ha aislado un microorganismo enteropatógeno. b) En un estudio al microscopio óptico o electrónico se ha observado un microorganismo enteropatógeno. c) Resultado positivo de una prueba para la detección de antígenos o anticuerpos en sangre o en heces. d) En un cultivo celular se han observado cambios citopáticos que permiten diagnosticar la presencia de un enteropatógeno. e) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. 6.2 Hepatitis aguda (código: HEAG) Una hepatitis aguda debe cumplir el siguiente criterio: Al menos dos de los siguientes signos o síntomas en ausencia de otra causa que los explique: fiebre (>38°), anorexia, náuseas, vómitos, dolor abdominal, ictericia o antecedentes de transfusión durante los 3 meses previos, y al menos uno de los siguientes: a) Resultado positivo de los marcadores de infección aguda por el virus de la hepatitis A, hepatitis B, hepatitis C o delta. b) Pruebas de función hepática alteradas (elevación de las transaminasas (ALT/AST) y de la bilirrubina, p.e.). c) En orina o en secreciones orofaríngeas se ha detectado Cytomegalovirus. SVIRAS. Anexo I. Rev 2014. pág.46 6.3 Enterocolitis necrotizante del lactante (código: ENTL) La enterocolitis necrotizante del lactante ha de cumplir el siguiente criterio: Al menos dos de los siguientes signos o síntomas sin otra causa que los explique: vómitos, distensión abdominal o residuos alimentarios en heces, y presencia de sangre en heces (oculta o no) de forma persistente, y al menos uno de los siguientes criterios radiológicos: a) Neumoperitoneo b) Neumatosis intestinal c) Asas intestinales rígidas de forma persistente. 6.4 Infección del tracto gastrointestinal (esófago, estómago, intestino delgado, intestino grueso y recto) excluyendo gastroenteritis y apendicitis (código: ITGI) Una infección del tracto gastrointestinal (excluyendo gastroenteritis y apendicitis) debe cumplir al menos uno de los siguientes criterios: 1) En una intervención quirúrgica, o en un estudio anatomopatológico se ha observado un absceso u otro signo evidente de infección. 2) Al menos dos de los siguientes sin otra causa que los explique y son compatibles con estas localizaciones: fiebre (>38°), náuseas, vómitos, dolor o tensión abdominal, y al menos uno de los siguientes: a) En el cultivo de un drenaje o de una muestra de tejido obtenida en una intervención quirúrgica, una endoscopia o de un tubo de drenaje colocado en una intervención se ha aislado un microorganismo. b) En el estudio de un drenaje o de una muestra de tejido obtenida en una intervención quirúrgica, una endoscopia o de un tubo de drenaje insertado durante una intervención se han observado microorganismos en las tinciones de Gram o con KOH o células gigantes multinucleadas en el estudio microscópico. c) En un hemocultivo se ha aislado un microorganismo. d) Evidencia radiológica de infección. e) Hallazgos patológicos en la endoscopia (esofagitis o proctitis por Candida, p.e.). 6.5 Infección intraabdominal (vesícula biliar, vías biliares, hígado -a excepción de las hepatitis-, bazo, páncreas, peritoneo, espacio subfrénico o subdiafragmático, y tejidos o zonas intraabdominales que no se han definido en ningún otro apartado; incluye apendicitis) (código: IABD) Una infección intrabdominal debe cumplir al menos uno de los siguientes criterios: SVIRAS. Anexo I. Rev 2014. pág.47 1) En el cultivo de un producto patológico purulento obtenido en una intervención quirúrgica o por aspiración con aguja se ha aislado un microorganismo. 2) En una intervención quirúrgica, o en un estudio anatomopatológico se ha observado un absceso u otro signo evidente de infección. 3) Al menos dos de los siguientes sin otra causa que los explique: fiebre (>38°), náuseas, vómitos, dolor o tensión abdominal, y al menos uno de los siguientes: a) En el cultivo del drenaje de un tubo colocado durante una intervención (por ejemplo, sistema cerrado, tubo abierto o en T) se ha aislado un microorganismo. b) En la tinción de Gram de un drenaje o de una muestra de tejido obtenida en una intervención quirúrgica por aspiración con aguja se han observado microorganismos. c) En un hemocultivo se ha aislado un microorganismo y hay evidencia radiológica de infección. SVIRAS. Anexo I. Rev 2014. pág.48 7 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN DEL APARATO GENITAL Se consideran infecciones del aparato genital la endometritis, las infecciones de la episiotomía o del fondo de saco vaginal, y el resto de infecciones del aparato genital masculino y femenino. 7.1 Endometritis (código: ENDM) Una endometritis debe satisfacer al menos uno de los siguientes criterios: 1) En el cultivo del fluido de una muestra de tejido obtenida durante una intervención quirúrgica, aspiración con aguja o raspado, se ha aislado un microorganismo. 2) Al menos dos de los siguientes sin otra causa que los explique: drenaje purulento del útero, fiebre (>38°), dolor abdominal o tensión uterina. Instrucciones: • Una endometritis postparto se considerará como infección nosocomial a menos que el líquido amniótico estuviera infectado en el momento del ingreso o que la paciente fuera ingresada 48 horas después de la rotura de membranas. 7.2 Infección de la episiotomía (código: EPIS) Una infección de la episiotomía debe cumplir al menos uno de los siguientes criterios: 1) Drenaje purulento de la episiotomía. 2) Absceso en la episiotomía. 7.3 Infección del fondo de saco vaginal (código: FSAC) Una infección del fondo de saco vaginal debe cumplir al menos uno de los siguientes criterios: 1) Drenaje purulento del fondo de saco vaginal. 2) Absceso en el fondo de saco vaginal. 3) En el cultivo del fluido o de una biopsia del fondo de saco vaginal se ha aislado un patógeno. SVIRAS. Anexo I. Rev 2014. pág.49 7.4 Otras infecciones del aparato genital (epidídimo, testículos, próstata, vagina, ovarios, útero o cualquier otro tejido profundo de la pelvis, a excepción de la endometritis o de la infección del fondo de saco vaginal) (código: OIAG) Las otras infecciones del aparato genital masculino o femenino deben cumplir al menos uno de los siguientes criterios: 1) En el cultivo del fluido o de una muestra del órgano afectado se ha aislado un microorganismo. 2) En una intervención quirúrgica o en un estudio anatomopatológico se ha observado un absceso u otro signo claro de infección. 3) Al menos dos de los siguientes en ausencia de otra causa que los explique: fiebre (>38°), náuseas, vómitos, dolor, tensión o disuria, y al menos uno de los siguientes: a) En el hemocultivos se ha aislado un microorganismo. b) Existe un diagnóstico médico. SVIRAS. Anexo I. Rev 2014. pág.50 8 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN DE LA PIEL O DE PARTES BLANDAS Las infecciones de la piel o de partes blandas incluyen las infecciones de piel (exceptuando la infección superficial de la herida quirúrgica), de partes blandas, de una úlcera de decúbito o quemadura, los abscesos mamarios, las mastitis, las onfalitis, las pustulosis del lactante y las infecciones de la herida de la circuncisión. 8.1 Infección de la piel (código: PIEL) Una infección de la piel debe satisfacer al menos uno de los siguientes criterios: 1) Supuración, pústulas, vesículas o forúnculos. 2) Al menos dos de los siguientes en la zona afectada, sin otra causa que los explique: dolor espontáneo o a la palpación, tumefacción, eritema o calor, y al menos uno de los siguientes: a) En el cultivo de un aspirado o de un drenaje de la zona afectada se ha aislado un microorganismo (si forma parte de la flora normal de la piel5, el cultivo debe ser puro y de un único microorganismo). b) En un hemocultivo se ha aislado un microorganismo. c) Resultado positivo de una prueba para la detección de antígenos en el tejido afectado o en sangre6. d) En el estudio microscópico del tejido afectado se han observado células gigantes multinucleadas. e) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. 8.2 Infección de partes blandas (fascitis necrotizante, gangrena infecciosa, celulitis necrotizante, miositis infecciosa, linfadenitis o linfangitis) (código: BLAN) Una infección de partes blandas debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de un tejido o drenaje de la zona afectada se ha aislado un microorganismo. 2) Supuración de la zona afectada. 3) En una intervención quirúrgica o estudio anatomopatológico se ha observado un absceso u otro signo claro de infección. 4) Al menos dos de los siguientes en la zona afectada, sin otra causa que los explique: dolor localizado o tensión, tumefacción o eritema o calor, y al menos uno de los siguientes: 5 P.e.: difteroides (Corynebacterium spp), Bacillus (excepto B anthracis) spp, Propionibacterium spp, Staphylococcus coagulasa negativos (incluyendo S. epidermidis), S. viridans, Aerococcus spp, Micrococcus spp 6 P.e.: Herpes simplex, Varicela zoster, H. influenzae, N. meningitidis, S. pneumoniae, Streptococcus grupo B, Candida spp SVIRAS. Anexo I. Rev 2014. pág.51 a) En un hemocultivo se ha aislado un microorganismo. b) Resultado positivo de la prueba para la detección de antígenos en sangre u orina7. c) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. 8.3 Infección de una úlcera de decúbito o por presión (código: ULCE) La infección de una úlcera de decúbito o por presión debe cumplir el siguiente criterio: Al menos dos de los siguientes sin otra causa que los explique: eritema, tensión o tumefacción de los bordes de la herida, y al menos uno de los siguientes: a) En el cultivo de un aspirado o de una biopsia de los bordes de la úlcera se ha aislado un microorganismo. b) En un hemocultivo se ha aislado un microorganismo. Comentarios: • Ni la presencia en la úlcera de drenaje purulento ni los cultivos positivos obtenidos de la superficie de la úlcera son pruebas suficientes de infección. • La forma correcta de obtener muestras de la úlcera para cultivar implica el aspirado de fluido mediante aguja o la biopsia de los márgenes de la úlcera. 8.4 Infección de una quemadura (código: QUEM) Una infección de una quemadura debe cumplir al menos uno de los siguientes criterios: 1) Cambio del aspecto de la quemadura (la escara se desprende precozmente, o se vuelve de color marrón oscuro, negro o violáceo, o aparece un edema alrededor de la herida, p.e.) y en el examen histológico de la biopsia de la quemadura se ha observado que los microorganismos invaden el tejido viable que la limita. 2) Cambio del aspecto de la quemadura (la escara se desprende demasiado pronto, o se vuelve de color marrón oscuro, negro o violáceo, o aparece un edema alrededor de la herida, p.e.), y al menos uno de los siguientes: a) En un hemocultivo se ha aislado un microorganismo y no se ha encontrado ningún otro foco infeccioso. b) En una biopsia o en un raspado de la lesión se ha aislado el virus Herpes simplex, se han identificado inclusiones diagnósticas en el estudio histológico con microscopio óptico o electrónico, o se han visualizado partículas víricas con 7 P.e.: Herpes simplex, Varicela zoster, H. influenzae, N. meningitidis, S. pneumoniae, Streptococcus grupo B, Candida spp. SVIRAS. Anexo I. Rev 2014. pág.52 el microscopio electrónico. 3) Al menos dos de los siguientes en un paciente con quemaduras: fiebre (>38°) o hipotermia (<36°), hipotensión (presión sistólica < 90 mmHg), oliguria (< 20 ml/hr), hiperglucemia (teniendo en cuenta la tolerancia a los carbohidratos que hasta entonces había tenido el paciente) o confusión mental, y al menos uno de los siguientes: a) En el examen histológico de una biopsia de la quemadura se observan microorganismos que han invadido el tejido viable que la limita. b) En un hemocultivo se ha aislado un microorganismo y no se ha encontrado ningún otro foco infeccioso. c) En una biopsia o en un raspado de la lesión se ha aislado el virus Herpes simplex, se han identificado inclusiones diagnósticas en el estudio histológico con microscopio óptico o electrónico, o se han visualizado partículas víricas con el microscopio electrónico. Instrucciones: • El drenaje purulento en la quemadura no es adecuado para el diagnóstico de infección, ya que puede indicar un cuidado incompleto de la quemadura. • La presencia de fiebre aislada en un paciente quemado no es adecuada para el diagnóstico de infección, la fiebre puede ser el resultado del trauma tisular o de presencia de infección en otra localización. 8.5 Absceso mamario o mastitis (código: MAMA) Un absceso mamario o mastitis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de una biopsia del tejido afectado o de líquido obtenido mediante incisión y drenaje o aspiración con aguja se ha aislado un microorganismo. 2) En una intervención quirúrgica o en un estudio anatomopatológico se ha observado un absceso u otro signo claro de infección. 3) Fiebre, inflamación local de la mama y existencia de un diagnóstico médico de absceso mamario o mastitis. Instrucciones: Los abscesos mamarios aparecen con más frecuencia después del parto. Aquellos que aparezcan en los 7 días siguientes al parto deben considerarse infecciones nosocomiales aunque la mujer ya no esté ingresada. SVIRAS. Anexo I. Rev 2014. pág.53 8.6 Onfalitis neonatal (código: ONFA) Una onfalitis neonatal (< 30 días de vida) y debe cumplir al menos uno de los siguientes criterios: 1) Eritema y supuración purulenta en el ombligo. 2) Eritema y/o drenaje seroso por el ombligo, y al menos uno de los siguientes: a) En el cultivo del drenaje o del líquido aspirado con aguja se ha aislado un microorganismo. b) En un hemocultivo se ha aislado un microorganismo. Instrucciones: La onfalitis neonatal se considerará infección nosocomial si aparece en un recién nacido durante el ingreso o en la semana siguiente al alta hospitalaria. 8.7 Pustulosis del lactante (código: PUST) Una pustulosis del lactante (niños < 12 meses de edad) debe cumplir al menos uno de los siguientes criterios: 1) El lactante tiene una o más pústulas y existe un diagnóstico médico de infección cutánea. 2) El lactante tiene una o más pústulas y el médico ha prescrito el tratamiento antibiótico adecuado. Instrucciones: La pustulosis del lactante se considerará infección nosocomial si aparece en un lactante durante el ingreso o en la semana siguiente al alta hospitalaria. 8.8 Infección de la herida de la circuncisión en un recién nacido (código: CIRC) Una infección de la herida de la circuncisión en un recién nacido (< 30 días de vida) debe cumplir al menos uno de los siguientes criterios: 1) En un recién nacido la herida de la circuncisión supura. 2) Al menos uno de los siguientes signos o síntomas en un recién nacido sin otra causa que los explique: eritema, inflamación, o dolor al palpar la herida de la circuncisión, y en el cultivo de la herida se ha aislado un patógeno. SVIRAS. Anexo I. Rev 2014. pág.54 3) Al menos uno de los siguientes signos o síntomas en un recién nacido sin otra causa que los explique: eritema, inflamación o tensión de la herida de la circuncisión, y en un cultivo de la herida se ha aislado un patógeno contaminante de la piel8, y el médico ha prescrito el tratamiento antibiótico adecuado o ha realizado el diagnóstico de infección. 8 P.e.: difteroides (Corynebacterium spp), Bacillus (excepto B anthracis) spp, Propionibacterium spp, Staphylococcus coagulasa negativos (incluyendo S. epidermidis), S. viridans, Aerococcus spp, Micrococcus spp SVIRAS. Anexo I. Rev 2014. pág.55 9 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN OSTEO-ARTICULAR Las infecciones osteoarticulares incluyen las osteomielitis, las infecciones articulares o de la cápsula y las infecciones del disco intervertebral. 9.1 Osteomielitis (código: OSTE) Una osteomielitis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de una biopsia ósea se ha aislado un microorganismo. 2) En una intervención o estudio anatomopatológico se han observado signos claros de osteomielitis. 3) Al menos dos de los siguientes sin otra causa que los explique: fiebre (>38°), tumefacción, tensión, aumento de la temperatura o drenaje de la zona sospechosa de infección, y al menos uno de los siguientes: a) En un hemocultivo se ha aislado un microorganismo. b) Resultado positivo de una prueba para la detección de antígenos en la sangre (p.e.: H influenzae, S. pneumoniae). c) Evidencia radiológica o gammagráfica de infección. 9.2 Infección articular o de la cápsula (código: ARTI) Una infección articular o de la cápsula debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo de líquido articular o de una biopsia de la cápsula sinovial se ha aislado un microorganismo. 2) En una intervención o estudio anatomopatológico se han observado signos evidentes de infección de la articulación o de la cápsula. 3) Al menos dos de los siguientes si no hay ninguna otra causa que los explique: dolor articular, tensión, tumefacción, calor, signos de derrame o limitación de la movilidad, y al menos uno de los siguientes: a) En un frotis del líquido articular se observan microorganismos y leucocitos. b) Resultado positivo de una prueba para la detección de antígenos en sangre, orina o fluido articular. c) Las características bioquímicas y el recuento leucocitario del líquido articular son compatibles con una artritis infecciosa y no se explican por un enfermedad reumática. SVIRAS. Anexo I. Rev 2014. pág.56 d) Evidencia radiológica o gammagráfica de infección. 9.3 Infección del disco intervertebral (código: DISC) Una infección del disco intervertebral debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de una muestra de tejido del disco interverterbral obtenida durante una intervención quirúrgica o por aspiración con aguja se ha aislado un microorganismo. 2) En una intervención o estudio anatomopatológico se han observado signos claros de infección. 3) Fiebre (>38°) sin ninguna otra causa que lo explique o dolor en la zona afectada, y evidencia radiológica o gammagráfica de infección. 4) Fiebre (>38°) sin ninguna otra causa que lo explique y dolor en la zona afectada, y resultado positivo de una prueba para la detección de antígenos en sangre u orina (p.e.: H. influenzae, S. pneumoniae, N. meningitidis, Streptococcus grupo B). SVIRAS. Anexo I. Rev 2014. pág.57 10 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN OCULAR, DEL OÍDO, NARIZ, FARINGE O BOCA Las infecciones oculares incluyen las conjuntivitis y el resto de infecciones oculares. Las infecciones del oído incluyen las otitis externas, medias e internas y las mastoiditis. Las infecciones nasales, faríngeas y bucales incluyen la sinusitis, las infecciones de vías respiratorias altas y las de cavidad oral. 10.1 Conjuntivitis (código: CONJ) Una conjuntivitis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de un exudado purulento obtenido de la conjuntiva o de órganos accesorios como el párpado, la córnea, las glándulas de Meibomio o los lacrimales, se ha aislado un microorganismo. 2) Dolor o enrojecimiento conjuntival o periocular, y al menos uno de los siguientes: a) En la tinción de Gram del exudado se han observado leucocitos y microorganismos. b) Exudado purulento. c) Resultado positivo de una prueba para la detección de antígenos en un exudado o frotis conjuntival. d) En la observación microscópica de un exudado o frotis conjuntival se han observado células multinucleadas. e) Resultado positivo de un cultivo para virus del exudado conjuntival. f) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. Instrucciones: No se catalogará como conjuntivitis una infección conjuntival que suceda en el contexto de una enfermedad viral diseminada (por ejemplo: sarampión, varicela, o infecciones de las vías respiratorias altas). 10.2 Infecciones oculares no conjuntivales (código: OJOS) Una infección ocular no conjuntival debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de cámara anterior o posterior o de humor vítreo se ha aislado un microorganismo. 2) Al menos dos de los siguientes si no hay ninguna otra causa que los explique: dolor ocular, anomalías de la visión o hipopion, y al menos uno de los siguientes: a) Existe un diagnóstico médico. b) Resultado positivo de una prueba para detección de antígenos en sangre (p.e.: H. influenzae, S. pneumoniae). SVIRAS. Anexo I. Rev 2014. pág.58 c) En un hemocultivo se ha aislado un microorganismo. 10.3 Otitis externa (código: OTEX) Una otitis externa debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo del drenaje purulento del conducto auditivo externo se ha aislado un patógeno. 2) Al menos uno de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), dolor, eritema o supuración del conducto auditivo externo, y en la tinción de Gram del drenaje purulento se han observado microorganismos. 10.4 Otitis media (código: OTME) Una otitis media debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo de contenido del oído medio obtenido por timpanocentesis o cirugía se ha aislado un patógeno. 2) Al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), dolor a nivel del tímpano, inflamación, retracción o disminución de la movilidad de la membrana timpánica o presencia de líquido detrás de esta membrana. 10.5 Otitis interna (código: OTIN) Una otitis interna debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo de contenido del oído interno obtenido en una intervención quirúrgica se ha aislado un patógeno. 2) Existe un diagnóstico médico. 10.6 Mastoiditis (código: MTDS) Una mastoiditis debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo del drenaje purulento de la mastoides se ha aislado un patógeno. 2) Al menos dos de los siguientes sin otra causa que los explique: fiebre (>38°), dolor espontáneo o a la palpación, eritema, cefalea o parálisis facial, y al menos uno de los siguientes: a) En la tinción de Gram de material purulento procedente de la mastoides se SVIRAS. Anexo I. Rev 2014. pág.59 han observado patógenos. b) Resultado positivo de una prueba para la detección de antígenos en sangre. 10.7 Infección de cavidad oral (boca, lengua o encías) (código: BOCA) Una infección de cavidad oral debe cumplir al menos uno de los siguientes criterios: 1) En un cultivo de material purulento procedente de tejidos bucales se ha aislado un microorganismo. 2) En la exploración clínica, una intervención quirúrgica, o un estudio anatomopatológico se ha observado un absceso u otro signo claro de infección de la cavidad oral. 3) Uno de los siguientes sin otra causa que los explique: absceso, úlcera, placas o lesiones de color blanco en la mucosa oral, y al menos uno de los siguientes: a) En la tinción de Gram se han observado microorganismos. b) Resultado positivo de la tinción con hidróxido de potasio (KOH). c) En examen microscópico del frotis bucal se han observado células gigantes multinucleadas. d) Resultado positivo de una prueba para la detección de antígenos en las secreciones bucales. e) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. f) Diagnóstico médico y tratamiento antifúngico oral o tópico. Instrucciones: Las infecciones herpéticas recurrentes no se catalogarán como infecciones nosocomiales. 10.8 Sinusitis (código: SINU) Una sinusitis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo del producto patológico purulento de un seno se ha aislado un microorganismo. 2) Uno de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), dolor espontáneo o a la palpación del seno afectado, cefalea, exudado purulento u obstrucción nasal, y al menos uno de los siguientes: a) Prueba de la transiluminación positiva. b) Evidencia radiológica de infección. SVIRAS. Anexo I. Rev 2014. pág.60 10.9 Infección de las vías respiratorias altas (código: IRVA) Una infección de las vías respiratorias altas debe cumplir al menos uno de los siguientes criterios: 1) Durante la exploración clínica, una intervención quirúrgica, o en un estudio anatomopatológico se ha observado un absceso. 2) Al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), eritema de la faringe, faringitis ulcerosa, tos, voz ronca o exudado purulento en la garganta, y al menos uno de los siguientes: a) En un cultivo de la zona afectada se ha aislado un microorganismo. b) En un hemocultivo se ha aislado un microorganismo. c) Resultado positivo de una prueba para la detección de antígenos en sangre o secreciones respiratorias. d) El título de anticuerpos específicos IgM es diagnóstico o el título de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. e) Existe un diagnóstico médico. 3) Uno de los siguientes en un paciente de edad igual o inferior a 12 meses sin otra causa que los explique: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, rinorrea o exudado purulento en la garganta, y al menos uno de los siguientes: a) En un cultivo de la zona afectada se ha aislado un microorganismo. b) En un hemocultivo se ha aislado un microorganismo. c) Resultado positivo de una prueba para la detección de antígenos en sangre o en las secreciones respiratorias. d) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. e) Existe un diagnóstico médico. SVIRAS. Anexo I. Rev 2014. pág.61 11 CRITERIOS PARA DIAGNOSTICAR CARDIOVASCULAR UNA INFECCIÓN DEL SISTEMA Las infecciones del sistema cardiovascular incluyen las arteritis, las flebitis, las endocarditis, las miocarditis o pericarditis y las mediastinitis. Las mediastinitis se incluyen en este grupo porque es más frecuente observarlas después de una intervención cardíaca. 11.1 Flebitis o arteritis (código: FLEB) Una flebitis o arteritis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de una biopsia arterial o venosa obtenida por disección quirúrgica se ha aislado un microorganismo y los hemocultivos han sido negativos o no se han practicado. 2) Durante una intervención o en el estudio anatomopatológico se han observado signos de infección de la zona vascular correspondiente. 3) Al menos uno de los siguientes signos o síntomas sin otra causa que lo explique: fiebre (>38°), dolor, eritema o calor en la zona vascular afectada, y en el cultivo semicuantitativo del extremo intravascular de la cánula se han aislado > 15 ufc, y los hemocultivos han sido negativos o no se han practicado. 4) Drenaje purulento de la zona vascular afectada y los hemocultivos han sido negativos o no se han practicado. 5) Al menos uno de los siguientes signos o síntomas en un paciente <12 meses de edad: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, letargia, dolor, eritema o calor en la zona vascular afectada, y en el cultivo semicuantitativo del extremo intravascular de la cánula se han aislado más de 15 ufc, y los hemocultivos han sido negativos o no se han practicado. 11.2 Endocarditis (código: ECAR) Una endocarditis de una válvula natural o protésica debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de la válvula o de la vegetación se ha aislado un microorganismo. 2) Al menos dos de de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), aparición de un soplo o cambio del que ya existía, fenómenos embólicos, manifestaciones cutáneas (petequias, hemorragias en astilla, nódulos subcutáneos dolorosos), insuficiencia cardíaca congestiva o anomalías de la conducción cardíaca, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) Se ha aislado el mismo microorganismo en dos hemocultivos. b) Si los cultivos de la válvula han sido negativos o no se han practicado, la observación de SVIRAS. Anexo I. Rev 2014. pág.62 microorganismos en la tinción Gram de la válvula. c) En una intervención quirúrgica o en la autopsia se ha observado una vegetación valvular. d) Resultado positivo de una prueba para la detección de antígenos en sangre u orina (p.e.: H. influenzae, S. pneumoniae, N. meningitidis, Streptococcus grupo B). e) Evidencia de una nueva vegetación en el ecocardiograma. 3) Al menos dos o más de los siguientes signos o síntomas en un paciente <12 meses de edad: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, aparición de un soplo o cambio de las características del que ya existía, fenómenos embólicos, manifestaciones cutáneas, insuficiencia cardíaca congestiva o anomalías de la conducción cardíaca, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) Se ha aislado el mismo microorganismo en dos hemocultivos. b) Si los cultivos de la válvula han sido negativos o no se han practicado, la observación de microorganismos en la tinción Gram de la válvula. c) En una intervención quirúrgica o en la autopsia se ha observado una vegetación valvular. d) Resultado positivo de una prueba para la detección de antígenos en sangre u orina (p.e.: H. influenzae, S. pneumoniae, N meningitidis, Streptococcus grupo B). e) Evidencia de una nueva vegetación en el ecocardiograma. 11.3 Miocarditis o pericarditis (código: MCAR) Una miocarditis o pericarditis debe cumplir alguno de los siguientes criterios: 1) En el cultivo de una muestra de tejido pericárdico obtenida en una intervención quirúrgica o por aspiración con aguja se ha aislado un microorganismo. 2) Al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), dolor torácico, pulso paradójico o dilatación cardíaca, y al menos uno de los siguientes: a) Anomalías en el electrocardiograma compatibles con una miocarditis o pericarditis. b) Resultado positivo de una prueba para la detección de antígenos en sangre (p.e.: H. influenzae, S. pneumoniae). a) En un estudio histológico se han observado signos de miocarditis o de pericarditis. b) Cuadruplicación del título de anticuerpos específicos de tipo con o sin aislamiento de un virus en faringe o heces. c) Signos de derrame pericárdico en un ecocardiograma, resonancia magnética nuclear, angiografía u otra evidencia radiológica de infección. 3) Al menos dos de los siguientes signos o síntomas en un paciente <12 meses de edad: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, pulso paradójico o dilatación cardíaca, y al menos uno de los siguientes: a) Anomalías en el electrocardiograma compatibles con una miocarditis o pericarditis. SVIRAS. Anexo I. Rev 2014. pág.63 b) Resultado positivo de una prueba para la detección de antígenos en sangre (p.e.: H. influenzae, S. pneumoniae). c) En un estudio histológico del tejido cardíaco se han observado signos de miocarditis o de pericarditis. d) Cuadruplicación del título de anticuerpos específicos de tipo con o sin aislamiento de un virus en faringe o heces. e) Signos de derrame pericárdico en un ecocardiograma, resonancia magnética nuclear, angiografía u otra evidencia radiológica de infección. 11.4 Mediastinitis (código: MEDI) Una mediastinitis debe cumplir al menos uno de los siguientes criterios: 1) En el cultivo de una muestra de tejido mediastínico obtenida en una intervención quirúrgica o por aspiración con aguja fina se ha aislado un microorganismo. 2) Evidencia de mediastinitis en una intervención quirúrgica o en el estudio anatomopatológico. 3) Al menos uno de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38°), dolor torácico o inestabilidad esternal, y al menos uno de los siguientes: a) Drenaje purulento de la zona mediastínica. b) En un hemocultivo o en un cultivo de un drenaje del área mediastínica se ha aislado un microorganismo. c) Ensanchamiento del mediastino en la exploración radiológica. 4) Al menos uno de los siguientes signos o síntomas en un paciente <12 meses de edad: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, o inestabilidad esternal, y al menos uno de los siguientes: a) Drenaje purulento de la zona mediastínica. b) En un hemocultivo o en un cultivo de un drenaje del área mediastínica se ha aislado un microorganismo. c) Ensanchamiento del mediastino en la exploración radiológica. SVIRAS. Anexo I. Rev 2014. pág.64 12 CRITERIOS PARA DIAGNOSTICAR UNA NERVIOSO CENTRAL INFECCIÓN DEL SISTEMA Las infecciones del sistema nervioso central incluyen las infecciones intracraneales, las meningitis o ventriculitis y los abscesos espinales sin meningitis. 12.1 Infección intracraneal (absceso cerebral, subdural o epidural y la encefalitis) (código: CRAN) Una infección intracraneal debe cumplir al menos uno de los siguientes criterios: 1. En el cultivo de una muestra de tejido cerebral o de duramadre se ha aislado un microorganismo. 2. En una intervención o estudio anatomopatológico se ha observado un absceso o signos evidentes de infección intracraneal. 3. Al menos dos de los siguientes signos o síntomas sin otra causa que los explique: cefalea, vértigos, fiebre (>38°), signos de localización neurológica, disminución del nivel de conciencia, síndrome confusional, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) En el examen microscópico de una muestra de tejido cerebral o de un absceso cerebral obtenido por aspiración con aguja o de una biopsia practicada en una intervención quirúrgica o en la autopsia se ha observado un microorganismo. b) Resultado positivo de una prueba para la detección de antígenos en sangre u orina. c) Evidencia radiológica de infección. d) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. 4. En un paciente de edad < 12 meses, al menos dos de los siguientes signos o síntomas sin otra causa que los explique: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, signos de localización neurológica, disminución del nivel de conciencia, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) En el examen microscópico de una muestra de tejido cerebral o de un absceso cerebral obtenido por aspiración con aguja o de una biopsia practicada en una intervención quirúrgica o en la autopsia se ha observado un microorganismo. b) Resultado positivo de una prueba para la detección de antígenos en sangre u orina. c) Evidencia radiológica de infección. d) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. Instrucciones: Si coexisten un absceso cerebral y meningitis, la infección se catalogará como infección intracraneal (CRAN). SVIRAS. Anexo I. Rev 2014. pág.65 12.2 Meningitis o ventriculitis (código: MENI) Una meningitis o ventriculitis debe cumplir al menos uno de los siguientes criterios: 1. En el cultivo del líquido cefalorraquídeo (LCR) se ha aislado un microorganismo. 2. Cualquiera de los siguientes si no hay ninguna otra causa que los explique: fiebre (>38°), cefalea, rigidez de nuca, signos meníngeos, signos de irritación o déficit de un nervio craneal o irritabilidad, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) Aumento del número de células en el LCR, de la proteinorraquia y/o descenso de la glucorraquia. b) En la tinción de Gram del LCR se han observado microorganismos. c) En un hemocultivo se ha aislado un microorganismo. d) Resultado positivo de una prueba para la detección de antígenos en sangre, orina o LCR. e) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. 3. Al menos uno de los siguientes signos o síntomas en un paciente de edad <12 meses sin otra causa que los explique: fiebre (>38° rectal), hipotermia (<37° rectal), apnea, bradicardia, rigidez de nuca, signos meníngeos, signos de irritación o déficit de un nervio craneal o irritabilidad, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) Aumento del número de células en el LCR, de la proteinorraquia y/o descenso de la glucorraquia. b) En la tinción de Gram del LCR se han observado microorganismos. c) En un hemocultivo se ha aislado un microorganismo. d) Resultado positivo de una prueba para la detección de antígenos en sangre, orina o LCR. e) El título de anticuerpos específicos IgM es diagnóstico o el de anticuerpos IgG se ha cuadruplicado en dos muestras sucesivas. Instrucciones: • Una infección de la derivación del líquido cefalorraquídeo se considerará como infección del lugar de la intervención quirúrgica si se produce <1 año desde su inserción; si se produce más tarde o después de la manipulación de la derivación, se catalogará como meningitis o ventriculitis (MENI). • Si coexisten un absceso cerebral y meningitis, la infección se catalogará como infección intracraneal (CRAN). SVIRAS. Anexo I. Rev 2014. pág.66 12.3 Absceso espinal sin meningitis (código: AESP) Un absceso espinal sin meningitis (es decir, un absceso epidural o subdural medular que no afecte al líquido cefalorraquídeo ni a las estructuras óseas de alrededor) debe cumplir alguno de los siguientes criterios: 1) En el cultivo de un absceso localizado en el espacio subdural o epidural se ha aislado un microorganismo. 2) En una intervención quirúrgica, una autopsia o en un estudio anatomopatológico se ha observado un absceso epidural o subdural intrarraquídeo. 3) Cualquiera de los siguientes si no hay ninguna otra causa que los explique: fiebre (> 38°), dorsalgias, tensión localizada, radiculitis, paraparesia o paraplejia, y el médico ha prescrito el tratamiento antibiótico adecuado (si se había diagnosticado antes de la muerte), y al menos uno de los siguientes: a) En un hemocultivo se ha aislado un microorganismo. b) Evidencia radiológica de un absceso espinal. 13 CRITERIOS PARA DIAGNOSTICAR UNA INFECCIÓN SISTÉMICA (código: SIST) Una infección sistémica es aquella que afecta a múltiples órganos o sistemas, sin un foco de infección claro. Estas infecciones suelen ser de origen vírico (p.e: sarampión, parotiditis, rubeola, varicela, eritema infeccioso), con signos y síntomas no explicables por otra causa y compatibles con la infección de múltiples órganos o sistemas. Instrucciones: - - Use este código para las infecciones virales que involucran múltiples órganos (p.e: sarampión, parotiditis, rubeola, varicela, eritema infeccioso). Estas infecciones a menudo se diagnostican sólo por criterios clínicos. No usar este código para las infecciones con múltiples sitios metastáticos, tales como endocarditis bacteriana; solo se debe informa del foco primario de estas infecciones. No clasificar la fiebre de origen desconocido (FOD) como SIST. Las sepsis neonatales se clasifican como SEPC SVIRAS. Anexo I. Rev 2014. pág.67 Tabla 7. Localización de las infecciones Código Localización Infecciones de las vías urinarias Infección sintomática de las vías urinarias IVU1 Otras infecciones de las vías urinarias(riñónm uréter, vejiga, uretra o tejidos de los espacios IVU2 retroperitoneal o perinefrítico) Pág 22 Código Localización Infecciones osteoarticulares Osteomielitis OSTE 24 ARTI ISI2 IPI1 26 26 CONJ Infección profunda de la incisión (primaria) 27 OJOS 27 28 OTEX OTME OTIN MTDS BOCA SINU Neumonía definida clínicamente Neumonía definida por hallazgos de laboratorio Neumonía en pacientes NEU3 inmunocomprometidos Infecciones de vías respiratorias bajas Bronquitis, traqueobronquitis, bronquiolitis o IRVB traqueítis, sin neumonía Otras infecciones del aparato respiratorio OIAR Infecciones del aparato digestivo Gastroenteritis GAST Hepatitis aguda HEAG Enterocolitis necrotizante del lactante ENTL Infección del tracto gastrointestinal ITGI Infección intraabdominal IABD Infecciones del aparato genital Endometritis ENDM Infección de la episiotomía EPIS Infección del fondo de saco vaginal FSAC Otras infecciones del aparato genital OIAG Infecciones de la piel y partes blandas Infección de la piel PIEL Infección de partes blandas BLAN Infección de una úlcera de decúbito o por ULCE presión QUEM Infección de una quemadura MAMA Absceso mamario o mastitis Onfalitis neonatal ONFA Pustulosis del lactante PUST Infección de la herida de la circuncisión en un CIRC recién nacido NEU2 55 Infección superficial de la incisión (primaria) Infección superficial de la incisión (secundaria) Infección profunda de la incisión (secundaria) IPI2 Infección de órgano o de espacio IQOE Bacteriemia Bacteriemia confirmada por laboratorio BACT Sepsis clínica SEPC Neumonía NEU1 55 Infección del disco 56 intervertebral Infecciones oculares, de oído, nariz, faringe, boca Infecciones sitio quirúrgico ISI1 Infección articular o de la cápsula Pág DISC 30 31 Conjuntivitis 57 Infecciones oculares no conjuntivales Otitis externa Otitis media Otitis interna Mastoiditis Infección de cavidad oral Sinusitis Infección de vías respiratorias altas 58 58 58 58 59 59 57 33 IRVA 37 Infecciones del sistema cardiovascular 39 FLEB Flebitis o arteritis 61 ECAR Endocarditis 61 44 MCAR Miocarditis o pericarditis 62 44 Mediastinitis MEDI Infecciones del Sistema Nervioso Central Infección intracraneal CRAN Meningitis o ventriculitis MENI Absceso espinal sin meningitis AESP Infección sistémica Infección sistémica SIST 46 46 47 47 47 49 49 49 49 51 51 66 66 53 53 54 54 SVIRAS. Anexo I. Rev 2014. pág.68 60 63 64 65 66 66
 0
0
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados