descargar artículo - Revista de Patología Respiratoria
Anuncio

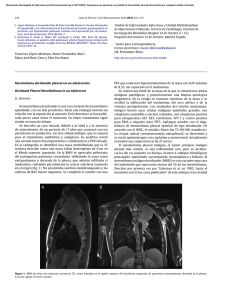
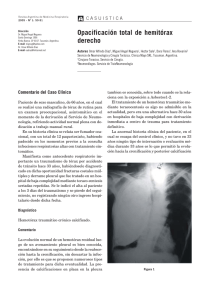
Pemetrexed como tratamiento de mesotelioma pleural R. Moreno Zabaleta, V. Villena Garrido, L. Comeche Casanova, R. García García, F. González Torralba Servicio de Neumología. Hospital 12 de Octubre. Madrid Se describe el caso de un varón de 63 años de edad sin antecedentes previos de interés, salvo contacto con asbesto que presenta un mesotelioma pleural maligno. En la ecografía torácica y la tomografía computarizada torácica se observa una gran masa pleural unida al diafragma además del derrame pleural en hemitórax derecho. El enfermó inició tratamiento quimioterápico con pemetrexed y cisplatino, observándose en la tomografía computarizada una clara disminución del tamaño de la masa pleural a los seis meses de iniciar este tratamiento. Este artículo describe la posible utilización de pemetrexed en pauta combinada con carboplatino como tratamiento quimioterápico válido de un mesotelioma pleural maligno que presenta masas pleurales al diagnóstico. Palabras clave: Mesotelioma pleural maligno; Pemetrexed; Carboplatino; Ecografía torácica; Tomografía computerizada. A case of a 63-year-old male with no previous background of interest, except contact with asbestos who had a malignant pleural mesothelioma is described. The chest ultrasonography and chest computed tomography showed a large pleural mass joined to the diaphragm in addition to pleural effusion in the right hemothorax. The patient initiated chemotherapy with pemetrexed and cisplatin, a clear decrease in the size of the pleural mass being observed in the computed tomography at six months of initiating this treatment. This article describes the possible use of pemetrexed in regimes combined with carboplatin as valid chemotherapy treatment of a malignant pleural mesothelioma that has pleural masses on diagnosis. Key words: Malignant pleural mesothelioma; Pemetrexed; Carboplatin; Thoracic ultrasonography; Computed tomography. INTRODUCCIÓN El mesotelioma pleural maligno es un tumor proveniente de las células serosas de la pleura, de rápida invasión local y con un mal pronóstico a corto plazo. Está fundamentalmente asociado a la exposición al asbesto, estando aumentado el riesgo de padecerlo con la exposición durante largos periodos de tiempo. Su aparición suele ocurrir entre veinte y cincuenta años tras la primera exposición al asbesto, por lo que suele afectar a personas de entre cincuenta y setenta años. El pronóstico del mesotelioma pleural es desfavorable, con una mediana de supervivencia de entre nueve y trece meses desde el diagnóstico1. Recientemente se han obtenido mejores resultados con el uso de un nuevo agente antifolato, el pemetrexed, bien sea en pautas de monoterapia o combinado con otros agentes quimioterápicos. Presentamos a un varón de 63 años con mesotelioma pleural maligno que presentó disminución de las masas pleurales tras seis ciclos de quimioterapia con pemetrexed asociado a carboplatino. Correspondencia: Raúl Moreno Zabaleta. Servicio de Neumología. Hospital 12 de Octubre. Avenida de Córdoba s/n. 28041 Madrid e-mail: [email protected] REV PATOL RESPIR 2006; 9(4): 191-193 CASO CLÍNICO Varón de 63 años con contacto con asbesto de forma indirecta ocasional. Ex-fumador, con un índice acumulado de 70 paquetes/año. Diagnosticado de enfermedad pulmonar obstructiva crónica moderada. Acudió a la consulta de Neumología presentando clínica de 3-4 semanas de evolución de incremento de su disnea basal, junto con dolor ocasional en la zona costal derecha superior y pérdida de peso no bien cuantificada. No presentaba otros síntomas en el interrogatorio por órganos y aparatos. En la exploración física presentaba buen estado general, y estaba febril y normotenso. Sin adenopatías en ningún terreno accesible a la palpación, con una auscultación cardiaca normal y una auscultación pulmonar con disminución del murmullo vesicular en la base del hemitórax derecho. El hemograma presentaba 12.900 leucocitos/mm3, con fórmula normal, una hemoglobina de 14,7 g/dl, un hematócrito de 45,1% y unas plaquetas de 406.000/ul. La bioquímica sérica era completamente normal. La coagulación también estaba dentro de los límites de la normalidad. La espirometría mostraba un patrón mixto de predominio obstructivo: FVC 2.520 ml (65%), FEV1 1.450 ml (48%), FEV1/FVC 58% (73%). En la radiografía de tórax se objetivaba derrame pleural derecho, con posibles imágenes nodulares en hemitórax derecho en las zonas en las que no se apreciaba derrame. En la ecografía to191 secundario del tratamiento fue una trombopenia que nunca fue inferior de 80.000 plaquetas. Junto a los quimioterápicos se le administró antes de iniciar el tratamiento ácido fólico, durante todo el tratamiento un complejo polivitamínico y cianocobalamina, y tras el tercer ciclo, darbepoetina. Tras los seis ciclos de quimioterapia las masas pleurales habían disminuido significativamente (Fig. 2B). Figura 1. Masa pleural supradiafragmática vista en ecografía torácica. rácica se observaba, además del derrame pleural, una lesión de carácter sólido unida al diafragma (Fig. 1). En la tomografía axial computarizada (TC) torácica se observaron imágenes de implantes pleurales de diferente tamaño a diversos niveles en hemitórax derecho (Fig. 2A), en zona anterior de hemitórax izquierdo y derrame pleural derecho. Mediante toracocentesis se obtuvo un líquido seroso que cumplía los criterios de exudado, con unas proteínas totales de 5,32 g/dl, una LDH de 208 UI/l, una glucosa de 99 g/dl, una amilasa de 77 UI/l, un colesterol de 83 mg/dl, unos triglicéridos de 28 mg/dl, un hematócrito de 1,3%, un pH de 7.48, leucocitos 1.100/m3 con un 85% de mononucleares y una albúmina de 2,49. Los marcadores tumorales en líquido pleural fueron de CA 15.3: 9,7 UI/ml.; CA 549: 4,7 UI/ml.; CA724; 2,8 UI/ml.; CEA 8,46 UI/ml. Con una biopsia pleural cerrada se obtuvo el diagnóstico de mesotelioma pleural de características sarcomatoides y con este diagnóstico se envió al paciente al servicio de Oncología Médica para valoración e iniciación de tratamiento. El tratamiento quimioterápico administrado consistió en seis ciclos de 850 mg de pemetrexed (Alimta) y 470 mg de carboplatino, con excelente tolerancia clínica. El periodo entre la administración de cada ciclo fue de veinte días. El principal efecto A DISCUSIÓN El pemetrexed (Alimta) es un nuevo agente quimioterápico antifolato que se ha comenzado a utilizar como fármaco de primera línea en distintos cánceres2. Este fármaco entra en la célula a través del transportador de los folatos reducidos de forma similar al ácido fólico, y una vez dentro, es poliglutamado por la folilpoliglutamato sintetasa, por lo que la forma pentaglutamada es la forma activa del fármaco. El pemetrexed inhibe múltiples enzimas de la síntesis de purinas y pirimidinas, fundamentalmente la timidilato sintetasa, aunque también, en menor medida, la dihidrofolato reductasa y la aminoácido carboxidorribonucleótido formal transferasa. Esta capacidad de actuar sobre distintas enzimas lo diferencia del resto de los antifolatos. Además, presenta una alta capacidad de permanecer en la célula, lo que permite una administración en dosis de cada 21 días. El fármaco se elimina en un 80% por la orina3. Los efectos secundarios se deben fundamentalmente al déficit de folatos que provoca, pudiendo aparecer neutropenia, trombopenia, rash, estomatitis, y diarrea o vómito3. La toxicidad se puede monitorizar con la elevación de la homocisteína en plasma3, y disminuye con la administración de ácido fólico los días antes de comenzar el tratamiento, y de vitamina B12 durante el tratamiento3,4. El pemetrexed ha demostrado actividad contra mesotelioma pleural en estudios en fase II administrado en monoterapia, con grados de respuesta en torno al 16%5. Un estudio multicéntrico en fase III compuesto por 448 pacientes con mesotelioma pleural, ha demostrado mejoría en la supervivencia de los pacientes tratados con pemetrexed más cisplatino con respecto a los tratados con cisplatino sólo. La mediana de supervivencia del grupo tratado con pemetrexed y cisplatino fue de 13,3 meses frente a los 10,0 meses del grupo control. En este mismo estu- B Figura 2. Tomografía computarizada de alta resolución de tórax: evolución de la masa pleural antes y después del tratamiento con pemetrexed. 192 REVISTA DE PATOLOGÍA RESPIRATORIA VOL. 9 Nº 4 - OCTUBRE-DICIEMBRE 2006 dio, el tiempo medio de progresión de la enfermedad fue de 5,7 meses en el grupo tratado con pemetrexed y cisplatino, mientras que en el grupo tratado sólo con cisplatino fue de 3,9 meses. Además, el grupo tratado con pemetrexed y cisplatino tuvo una respuesta al tratamiento del 41,3% frente al 16,7 del grupo control. La pauta de administración en este estudio fue de 500 mg/m2 de pemetrexed en infusión intravenosa durante 10 minutos y 75 mg/m2 de cisplatino a las dos horas, en ciclos cada 21 días, entre cuatro y seis ciclos6,7. El carboplatino interacciona con el DNA formando uniones intracadena e intercadena, cuyos índices de respuesta en monoterapia en el mesotelioma pleural varían entre el 5 y el 16%. Al ser más fácil de manejar y con menos efectos secundarios, es un fármaco muy utilizado en tratamientos combinados. La principal toxicidad del carboplatino, que limita su dosis, es la mielosupresión, fundamentalmente la trombopenia. Un estudio en fase I evaluó la acción del pemetrexed en combinación con carboplatino en el tratamiento de 27 enfermos con mesotelioma pleural, la mayoría de ellos de estirpe epitelial (59%). La respuesta al tratamiento en este estudio es de 32%, con una mediana de supervivencia de 13,5 meses8. Recientemente, también se han encontrado en un estudio en fase II similares índices de respuesta al tratamiento y supervivencia con la combinación de pemetrexed y carboplatino que con la combinación de pemetrexed con cisplatino, pero con una mejor tolerancia al tratamiento9. El paciente que presentamos presentaba una imagen de gran masa pleural que se observaba claramente en la ecografía torácica al diagnóstico y en el TC torácico. Tras seis ciclos de tratamiento con pemetrexed más carboplatino además de la buena evo- lución clínica se objetivó una clara disminución del tamaño de la masa tumoral en el TC de control. BIBLIOGRAFÍA 1. Peto J, Decarli A, La Vecchia C, Levi F, Negri E. The European mesothelioma epidemia. Br J Cancer 1999; 79: 666-72. 2. Solomon B, Bunn PA Jr. Clinical activity of pemetrexed: a multitargeted antifolate anticancer agent. Future Oncol 2005; 1: 733-46. 3. Thodtmann R, Depenbrock H, Dumez H, Blatter J, Johnson RD, van Oosterom A, et al. Clinical and pharmacokinetic phase I study of multitargeted a tifolate (LY231514) in combination with cisplatin. J Clin Oncol 1999; 17: 3009-16. 4. Villela LR, Stanford BL, Shah SR. Pemetrexed, a novel antifolato therapeutic alternative for cancer chemotherapy. Pharmacotherapy 2006; 26: 641-54. 5. Shin DM, Scagliotti G, Kindler H. Phase II study of ALIMTA (pemetrexed disodium) single agent in patients with malignant pleural mesothelioma. Eur J Cancer 2001; 27 (suppl 6): 21. 6. Vogelzang NJ, Rusthoven JJ, Symanowski J, Denham C, Kaukel E, Ruffie P, et al. Phase III study of pemetrexed in conbination with cisplatin versus cisplatin alone in patients with malignant pleural mesothelioma. J Clin Oncol 2003; 21: 2636-44. 7. Hazarika M, White RM, Brian Booth P, Wang YC, Lee Ham DY, Liang CY, et al. Pemetrexed in malignant pleural mesothelioma. Clin Cancer Res 2005; 11: 982-92. 8. Hughes A, Calvert P, Azzabi A, Plummer R, Johnson R, Rusthoven J, et al. Phase I clinical and pharmacokinetics study of pemetrexed and carboplatin in patients with malignant pleural mesothelioma. J Clin Oncol 2003; 20: 3533-44. 9. Ceresoli G, Zucali P, Favaretto G, Grossa F, Bidoli P, Del Conte G, Ceribelli A, et al. Phase II study of pemetrexed plus carboplatino in malignant pleural mesotelioma. J Clin Oncol 2006; 24: 1443-8. R. Moreno Zabaleta et al. Pemetrexed como tratamiento de mesotelioma pleural 193