FARMACOLOGIA
Anuncio
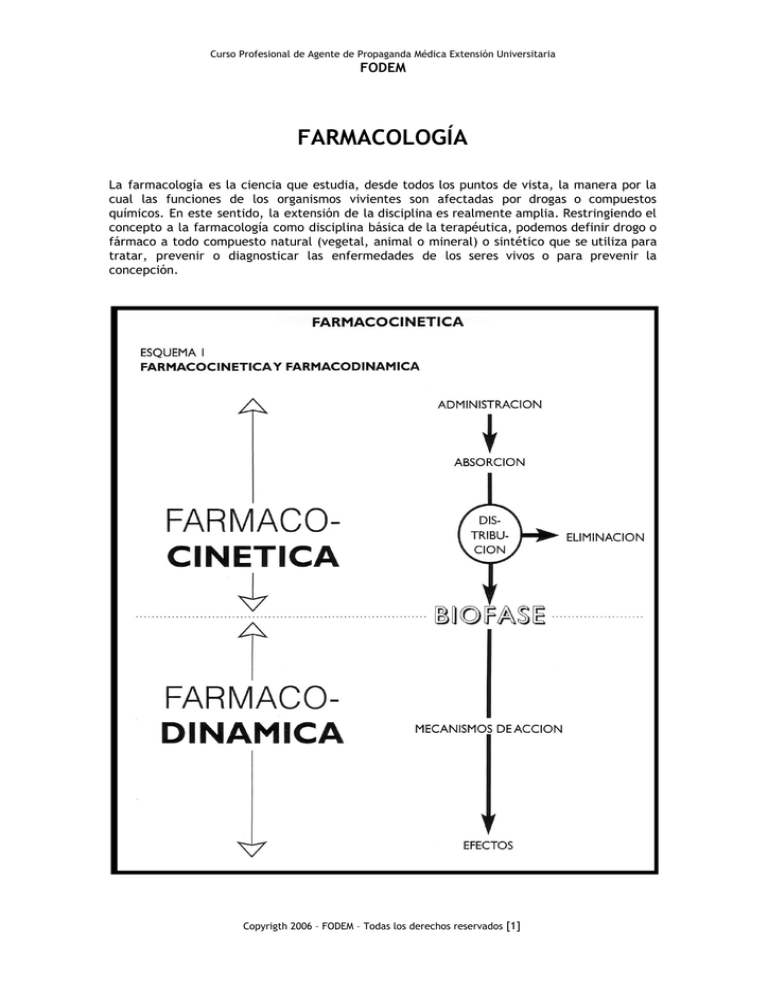
Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM FARMACOLOGÍA La farmacología es la ciencia que estudia, desde todos los puntos de vista, la manera por la cual las funciones de los organismos vivientes son afectadas por drogas o compuestos químicos. En este sentido, la extensión de la disciplina es realmente amplia. Restringiendo el concepto a la farmacología como disciplina básica de la terapéutica, podemos definir drogo o fármaco a todo compuesto natural (vegetal, animal o mineral) o sintético que se utiliza para tratar, prevenir o diagnosticar las enfermedades de los seres vivos o para prevenir la concepción. Copyrigth 2006 – FODEM – Todas los derechos reservados [1] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Siguiendo el criterio de un Comité de Expertos en Farmacología Clínica de la Organización Mundial de la Salud (1970), la farmacocinética es tanto el conjunto de procesos que determina la concentración de droga en la biofase, como el estudio de los mismos. Copyrigth 2006 – FODEM – Todas los derechos reservados [2] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM La farmacocinética debe interpretarse como un proceso dinámico, donde todos los procesos ocurren simultáneamente. El esquema 2 señala as diversas vías que puede seguir una molécula activa de una droga. Puede determinarse que una fracción del fármaco administrado sigue un cierto proceso farmacocinético, mientras otra fracción sigue otro, pero no podemos nunca prever si una molécula aislada seguirá un proceso u otro. Es decir, podemos predecir estadísticamente el destino del conjunto de las moléculas administradas, pero el destino de una molécula individual es aleatorio y no predecible con certeza. Comenzaremos estudiando los mecanismos de pasaje de barreras biológicas y la distribución de drogas, pues están en el centro de los procesos de farmacocinética y su comprensión es esencia para una adecuada interpretación de los demás Luego nos referiremos a la biotransformación, seguida por el papel farmacocinético del aparato digestivo, del riñón y de otros órganos, que en general se conocen como de absorción o excreción, pero que no cumplen exclusivamente ese papel. PASAJE ATRAVES DE MEMBRANAS BIOLOGICAS El pasaje (o transferencia) de los fármacos a través de membranas biológicas puede efectuarse por diferentes mecanismos, siendo los más relevantes los siguientes (esquema 3): - Difusión simple. - Difusión facilitada. -Transporte de pares iónicos. - Filtración. -Transporte sodio dependiente. -Transporte activo. - Pinocitosis. Copyrigth 2006 – FODEM – Todas los derechos reservados [3] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Copyrigth 2006 – FODEM – Todas los derechos reservados [4] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 3. Pasaje a través de membranas biológicas Tanto los procesos llamados activos como los pasivos, utilizan energía, pues no existe ningún fenómeno en el universo que no lo requiera. Los procesos activos utilizan la almacenada en uniones fosfato de alta energía, liberada por hidrólisis del ATP Copyrigth 2006 – FODEM – Todas los derechos reservados [5] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Los procesos pasivos utilizan energía proveniente de gradientes electroquímicos o de presión hidrostática. DIFUSION SIMPLE (Esquema 4) Es la movilización, sin consumo de ATP ni utilización de mecanismos de transporte, de las moléculas de un fármaco desde el sitio de mayor al de menor concentración, a través de los lípidos de la membrana. Es el mecanismo por el cual la inmensa mayoría de las drogas atraviesan las membranas celulares. Esquema 4. Difusión Simple Copyrigth 2006 – FODEM – Todas los derechos reservados [6] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Los principales factores que determinan la velocidad de la difusión simple son: la liposoubilidad, el tamaño y la ionización moleculares. Liposolubilidad Manteniendo constantes las otras variables, la velocidad de difusión simple es directamente proporcional a la liposolubilidad de la droga. Tamaño molecular Manteniendo constantes las otras variables, la velocidad de difusión es inversamente proporcional al tamaño molecular: las moléculas de bajo peso molecular (moléculas pequeñas) difunden más rápidamente. Ionización molecular La mayoría de los fármacos son ácidos o bases débiles, pudiendo presentarse en los medios líquidos (como son los orgánicos) en parte ionizadas y en parte no. Las moléculas ionizadas (polares) se caracterizan por ser más hidrosolubles, mientras que las no ionizadas son más liposolubles:la permeabilidad a las moléculas no ionizadas es 108 veces mayor que para las ionizadas de la misma droga. Por lo tanto, tiene suma importancia la fracción no ionizada para determinar la velocidad de pasaje de un fármaco a través de las membranas: manteniendo constantes las otras variables, cuanto mayor es la fracción no ionizada, tanto mayor es la velocidad de pasaje de un fármaco. Para poder calcular la fracción no ionizada de una droga en cualquier medio del organismo, es necesario conocer: - Si la droga es un ácido o una base. El pKa de la droga. El pH del medio orgánico. Atrapamiento iónico. Naturaleza ácida o básica del fármaco Es una propiedad intrínseca de cada droga y depende de su capacidad de ceder (ácido) o de aceptar (base) protones. La mayor o menor cesión o aceptación de protones es dependiente del pH del medio. pKa de la droga Se denomina pKa al pH en el cual la droga se encuentra con el 50% de sus moléculas en estado de ionización y la otra mitad en estado de no ionización. Tanto los ácidos como las bases pueden tener un pKa superior o inferior a 7, por lo que el pKa no define la naturaleza ácida o básica de una sustancia. Hay drogas que poseen más de un grupo ionizable. El pKa para cada grupo es distinto. Basta que se ionice uno de los grupos en una molécula, para que la misma no pueda atravesar fácilmente la membrana, y por esto sólo nos interesa el pKa más bajo (para un ácido) o el más alto (para una base). El pH del medio orgánico El pH del medio determina la fracción no ionizada de los ácidos y bases, (pH = log1 ) (H+) Toda vez que el pH del medio es inferior al pKa de la droga, predomina la fracción no ionizada de los ácidos y la ionizada de las bases. Lo contrario sucede cuando el pH es superior al pKa. El pH del medio interno oscila dentro de un rango estrecho (7,39 - 7,43) debido a la presencia de los sistemas amortiguadores (buffers). A nivel de las secreciones mucosas se pueden observar pH muy diferentes (p. ej., en el estómago el pH es inferior a 3 y en yeyuno es superior a 6). El pH del citosol, en la mayoría de las células, es aproximadamente 7; pero en ciertos compartimientos, el pH puede ser muy diferente (p. ej.: 5 en los lisosomas). Atrapamiento iónico (Esquema 5) Copyrigth 2006 – FODEM – Todas los derechos reservados [7] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Cuando existe una diferencia de pH entre uno y otro lado de una membrana plasmática, cualquier sustancia ácida o básica, cuyas moléculas no ionizadas difundan a través de la misma, alcanzará estados estacionarios con distinta concentración en cada compartimiento líquido. Como en estado estacionario las concentraciones de la droga no ionizada son iguales a ambos lados de la membrana, la droga alcanzará mayor concentración total en el compartimiento en el que haya mayor fracción ionizada. A esto se lo denomina atrapamiento iónico (ver ejemplo en la tabla 1). OTROS MECANISMOS DE PASAJE DE MEMBRANA Copyrigth 2006 – FODEM – Todas los derechos reservados [8] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Difusión facilitada Sustancias prácticamente insolubles en lípidos (p. ej., glucosa) pueden unirse a una estructura de la membrana denominada portador o carrier; el complejo droga-portador difunde de acuerdo a las leyes de la difusión simple. A este mecanismo se lo denomina difusión facilitada. Sus características más importantes son: - Saturabilidad - Selectividad - Competición - Reversibilidad - Bidireccionalidad Ultra filtración Algunas barreras epiteliales como el glomérulo renal y los capilares tisulares (con excepción del SNC), tienen poros a través de los cuales pueden pasar casi todas las drogas, excepto las macromoléculas. Cuando hay un gradiente de presión hidrostática entre ambos lados de la membrana, el agua se desplaza a favor de ese gradiente y con el agua pasan todos los solutos cuyo tamaño sea inferior al de los poros, manteniendo constante su concentración en el agua que los arrastra. A este proceso se lo llama ultrafiltración. Transporte sodio dependiente Es un transporte contra gradiente de una droga, que utiliza un portador y su fuente de energía es el gradiente de sodio entre ambos lados de la membrana. Transporte activo Es un mecanismo poco frecuente para los fármacos. Los ejemplos más importantes se refieren a endocitosis. DISTRIBUCION DE LOS FARMACOS (Esquema b) La distribución está en el centro de todos los procesos farmacacinéticos. El agua del plasma es el vehículo que comunica los diversos compartimientos anatómicos entre sí. A la droga disuelta en el agua del plasma se la denomina droga libre (por oposicion a la unida a proteínas o células sanguíneas). La droga libre en plasma pasa al líquido intersticial, y luego pasa o no a las células, pudiendo acumularse en algunas de ellas. El pasaje al líquido intersticial se efectúa, en general, a través de poros, pero en algunos tejidos existen barreras de características especiales (p.ej. sistema nervioso central, placenta, testículo). Copyrigth 2006 – FODEM – Todas los derechos reservados [9] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 6. Distribución de Drogas UNION DE DROGAS A PROTEINAS PLASMATICAS Cuando una droga entra al compartimiento plasmático, interacciona con las proteínas plasmáticas. La unión droga-proteínas puede ser reversible (la mayor parte de las drogas) o irreversible (p. ej. agentes alquilantes). Pueden existir fenómenos de competición entre 2 drogas que se unen a la misma proteína. La fracción de droga unida a proteína es muy variable, pudiendo ser desde casi nula hasta prácticamente el 100% según la droga y su concentración; generalmente, tiene importancia clínica cuando es mayor del 80%, aunque en algunos casos particulares, una unión menor también puede ser importante. Copyrigth 2006 – FODEM – Todas los derechos reservados [10] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 7 Unión de drogas a proteínas plasmáticas Para algunas drogas que son sustancias propias del organismo, existen proteínas específicas. Las drogas ácidas y neutras se unen fundamentalmente a la albúmina. En cambio, las básicas lo hacen a la albúmina α 1 glicoproteinas ácidas. Una mayor fracción de droga unida a proteínas plasmáticas puede estar asociada a una mayor o menor vida media o no tener ninguna relación con ella. Lo mismo sucede con la duración de los efectos. La relación entre fracción unida a proteínas, vida media y duración del efecto depende de múltiples variables, entre las cuales la unión a proteínas es sólo una de ellas, y no sirve par si sola para predecir sus consecuencias. La mayor o menor fracción unida a proteínas, no implica de por sí ninguna ventaja ni desventaja particular respecto a la efectividad terapéutica, dado que aún cuando la droga ligada a proteínas sea inactiva, la dosis usual de las drogas es tal que la fracción libre tiene concentración suficiente como para ser efectiva. Copyrigth 2006 – FODEM – Todas los derechos reservados [11] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Al disminuir la fracción de droga unida, aumenta la fracción de droga libre. En cambia, la concentración de droga libre puede aumentar o no. La concentración de droga libre no aumenta si la misma se redistribuye o elimina rápidamente. Variables que modifican la fracción de droga unida a proteínas plasmáticas La fracción de droga unida a proteínas es aproximadamente constante mientras la concentración de droga libre esté por debajo del nivel de saturación. La concentración de las proteínas influye directamente en la fracción unida. El pH y la composición electrolítica del medio, así como la presencia de competidores a la alteración de la molécula protéica, puede afectar a las drogas y/o a las proteínas modificando la afinidad, y por lo tanto pueden modificarse las fracciones de droga libre. Redistribución Una droga por vía intravenosa en primer lugar se diluirá en la sangre e irá distribuyéndose, pero no llega rápidamente a un estado estacionario, pues inicialmente alcanza mayores niveles en los órganos con mayor flujo sanguíneo absoluto (por ej. cerebro, riñón, pulmón) que en los de menor flujo (por ej. celular subcutáneo). A medida que pasa el tiempo, tenderá a aproximarse a un estado estacionario, en un período de tiempo variable según la droga, pasando desde los tejidos mencionados al plasma y de aquí a otros tejidos. A este proceso lo llamamos redistribución. BIOTRANSFORMACION DE DROGAS Denominamos biotransformación o metabolismo a la modificación de una molécula por medio de una reacción química catalizada por enzimas. CINETICA ENZIMATICA La velocidad de reacción enzimática es modificada por la temperatura, el pH, la fuerza iónica y composición electrolítica del medio, factores estos que pueden variar- por causas fisiológicas patológicas. Pera las dos variables más importantes in viva son las concentraciones de enzima y de sustrato. PRINCIPALES REACCIONES DE BIOTRANSFORMACION DE DROGAS Oxidorreducciones (Esquema 8) Esta reacción consiste en la transferencia de electrones desde un dador a un aceptor: La pérdida del electrón constituye una oxidación, la incorporación del mismo constituye una reducción. Hidrólisis En la hidrólisis una droga reacciona con agua, dando origen a dos moléculas de menor peso molecular. Las enzimas que las catalizan se denominan hidrolasas. Las drogas más frecuentemente hidrolizadas son ésteres y amidas. Reacciones sintéticas Se denominan reacciones sintéticas o de fase II a aquellas que agregan un radical químico a una droga. Por contraste, se denominan reacciones no sintéticas o de fase 1 a las oxidorreducciones e hidrólisis. Lo referido a fase I y II, se basa en que muchas drogas sufren una oxidorreducción antes de la reacción sintética, pero ello no es constante. Conjugación con ácido glucurónico Es el proceso sintético más frecuente en el adulto. Acetilaciones Son reacciones de gran importancia farmacogenética. METABOLISMO MICROSOMAL Copyrigth 2006 – FODEM – Todas los derechos reservados [12] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Utilizaremos esta denominación abreviada para referirnos a las oxidasas de función mixta y a la UDP-glucuroniltransferasa localizadas en el retículo endoplásmico liso (que forma parte de los microsomas en el ultracentrifugado). Inductores e inhibidores Los sustratos de este sistema enzimático son inductores del mismo pero no todos son igualmente importantes. Los inductores más importantes en clínica son el fenobarbital, la fenitoína, la rifampicina, el etanol, sustancias del humo del tabaco, etc. Entre los inhibidores de importancia clínica, citaremos a la cimetidina, a los bloqueantes de los canales del calcio y al cetoconazol. Esquema 8 Reacciones metabólicas microsomales y no microsomales. METABOLISMO NO MICROSOMAL Entre las enzimas metabolizadoras de drogas localizadas en las mitocrondrias son importantes las monoaminooxidasas A y B (MAO A y B). En el citosol existen enzimas metabolizadoras de drogas, tales como la NAD*: alcohol deshidrogenasa y la catecol-O-metiltransferasa. (* NAD: NicotinAdeninDinucleotido) Copyrigth 2006 – FODEM – Todas los derechos reservados [13] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM En la membrana celular existen enzimas, especialmente las relacionadas con la terminación del efecto de algunos neurotransmisores. Merece citarse la acetilcolinesterasa. Bacterias patógenas para el hombre pueden metabolizar drogas. Esto adquiere importancia porque constituye un mecanismo de resistencia por parte de las bacterias (por ej., para aminoglucósidos, penicilinas). CONSECUENCIAS DEL METABOLISMO DE DROGAS (Esquema 9) Como regla general, los metabolitos son más polares, más hidrosolubles y menos liposolubles que la droga original. Frecuentemente, los metabolitos son inactivos o mucho menos activos que la droga original, pero esto no siempre es así y no debe tomarse como regla. Esquema 9 Consecuencias de la biotransformación Si la droga administrada es activa, un metabolito también puede serlo (p ej., digitoxina -->digoxina). Copyrigth 2006 – FODEM – Todas los derechos reservados [14] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Una droga inactiva puede activarse y ser sus metabolitos los que actúan. Estas sustancias (prodrogas) se caracterizan por ser inactivas si se aplican localmente o in vitro si no está presente el sistema enzimático activador (por ej., ciclofosfamida, paratión). Hablamos de activación metabólica o bioactivación. El hígado, la mucosa intestinal y el plasma son sitios importantes de activación de prodrogas. Si el metabolito de una droga es menos efectivo pero más tóxico que la droga madre, la inducción enzimática puede resultar en un aumento de la toxicidad de la droga. El metabolismo de drogas puede modificar el metabolismo celular. Durante el metabolismo de algunas drogas, se forman metabolitos intermedios altamente reactivos, que muchas veces tienen existencia efímera, pero que poseen una elevada toxicidad. Estos metabolitos pueden ser radicales libres o compuestos electrofílicos. A veces, la toxicidad del metabolito intermedio se produce a distancia, pero generalmente afecta a la célula metabolizadora. CINETICA DE ELIMINACION En los modelos farmacocinéticos, se considera eliminación a la disminución de los niveles de droga en cualquier compartimiento, sin importar el proceso involucrado. Si, por ejemplo, se estudia la cinética de absorción de una droga, lo que se hace es analizar la eliminación de la droga desde el sitio de absorción hacia el compartimiento central. CINETICA DE ORDEN 0 Y DE ORDEN I (Esquema 10) Cuando la velocidad de eliminación es proporcional a la concentración de la droga, se dice que la cinética de eliminación es de orden 1. Cuando la velocidad de eliminación es constante para cualquier concentración de la droga, se dice que la cinética de eliminación es de orden D. Si se grafican estos datos utilizando escala aritmética en ambas coordenadas, se obtiene una línea recta en el caso de la cinética de orden 0, y una curva si la cinética es de orden 1. Esto es lógico si se toma en cuenta que para obtener una recta, para iguales intervalos de tiempo debe haber iguales descensos de concentración, hecho que ocurre solamente en la cinética de orden 0. Si se emplea un gráfico semilogarítmico se obtiene una recta en el caso de la cinética de orden 1, pero no con la cinética de orden 0. ¿Cuándo se observa una u otra cinética? Si el mecanismo por el cual se elimina una droga está saturado, la velocidad de eliminación será constante (orden 0), pues al estar saturado ese mecanismo no puede acelerarse al aumentar la concentración del fármaco. En cambio, si el mecanismo es no saturable o las concentraciones de droga son muy inferiores al nivel de saturación, al aumentar la concentración de la droga se incrementará proporcionalmente la velocidad de eliminación (orden 1). Copyrigth 2006 – FODEM – Todas los derechos reservados [15] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 10 Tipos de cinética de eliminación Copyrigth 2006 – FODEM – Todas los derechos reservados [16] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM RELACION ENTRE DOSISYVELOCIDAD DE ELIMINACION La filtración glomerular es el único mecanismo de eliminación que en la práctica puede considerarse no saturable. Si graficamos velocidades de eliminación en función de la concentración de droga, se obtiene una línea recta (figura XI), arriba), por lo que se dice que esta droga tiene cinética lineal. Como se mantiene la línea recta cualquiera sea la dosis que uno administre, también se la llama cinética dosis independiente. Copyrigth 2006 – FODEM – Todas los derechos reservados [17] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 11 Tipos de cinética de eliminación En el caso de droga que se elimina por un mecanismo saturable, con dosis bajas (que originan concentraciones bajas) la cinética es prácticamente de orden 1, mientras que con dosis muy altas (que dan origen a concentraciones muy altas) la cinética es prácticamente de orden 0, quedando una zona intermedia. Como el trazado no es una recta, se habla de cinética no lineal. Como el tipo de cinética (orden 1 u orden 0) depende de la dosis, se la denomina también cinética dosis dependiente. En la misma figura 11 puede observarse que, para una misma droga, la velocidad de eliminación es mayor cuando se alcanza la cinética de orden 0, que cuando se observa la de orden 1. En resumen, si bien la eliminación de drogas por mecanismos saturables es más frecuente que la eliminación casi exclusiva por filtración glomerular, la mayor parte de las drogas tienen eliminación prácticamente dosis independiente dentro del rango terapéutico. PARAMETROS FARMACOCINETICOS Vida media y constante de velocidad de eliminación de orden 1 (Esquema 12) Vida media es el tiempo en el cual la concentración de la droga en un compartimiento sE reduce a la mitad. Este tiempo es una constante en la cinética de orden 1, pero no en la de orden 0. La vida media permite estandarizar la cinética de orden 1 y formular conceptos generales sobre la misma. Si las concentraciones de droga se expresan como porcentaje de la concentración máxima y el tiempo se expresa en número de vidas medias, todas las drogas con cinética de orden I dan gráficos idénticos. Si se observa una curva logarítmica de concentración-tiempo correspondiente a cinética de orden 1 (fig. 10 abajo, derecha), se comprueba que es una recta con pendiente negativa. Puede observarse en la figura 11 que la pendiente disminuye a medida que la cinética se acerca al orden 0, es decir, la vida media va aumentando. Esto es lo que se observa generalmente con las drogas de cinética dosis dependiente: la vida media se prolonga al aumentar la dosis. Por ejemplo, si se administran 325 mg de aspirina, la vida media del ácido salicílico es de aproximadamente 2 h, si se administra 1g de aspirina, la vida media se acerca a las 4 h y en las intoxicaciones se han determinado vidas medias cercanas a las 20 h. La mayor parte de las drogas tienen más de un mecanismo de eliminación, y no todos se saturan con igual concentración de droga. Ello implica que cuando un mecanismo de eliminación se ha saturado, los otros siguen eliminando la droga con cinética de orden 1. Por este motivo, es excepcional observar cinética de orden 0 en farmacología o en toxicología in vivo. La aspirina es un buen ejemplo de este fenómeno. Copyrigth 2006 – FODEM – Todas los derechos reservados [18] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 12 Copyrigth 2006 – FODEM – Todas los derechos reservados [19] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Clearance Vida media de eliminación Clearance en castellano significa depuración. Aquí mantendremos el término inglés, que es el habitualmente usado. Clearance es el volumen de plasma que es completamente depurado de droga en una unidad de tiempo. Como las drogas pueden eliminarse por riñón, hígado u otros órganos, debe distinguirse el clearance total (CIT), de los clearance correspondientes a cada órgano. Volumen aparente de distribución En un modelo unicompartimental, es el volumen que ocuparía la droga si en todo el organismo tuviera igual concentración que en el plasma. Es decir, suponemos que la concentración en el plasma es la misma que la que tiene la droga en todo el organismo. Esquema 13 Excreción renal de drogas Copyrigth 2006 – FODEM – Todas los derechos reservados [20] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Biodisponibilidad (Esquema 14) ¿Qué sucede si se administra un medicamento por vía bucal? (Esquema 15). Antes de absorberse, la droga debe liberarse desde el preparado farmacéutico. Una vez liberada, la droga puede ser degradada por el ácido clorhídrico (p. ej. penicilina G) o por bacterias intestinales (p. ej. digoxina). La mucosa intestinal también tiene capacidad de metabolizar drogas. Además, la absorción de la droga puede ser incompleta (p. ej. ampicilina). Una vez absorbida, la droga llega por la vena porta al hígado, donde puede ser extraída (efecto de primer paso hepático). Recién al llegar al ventrículo derecho la droga se encuentra en la misma situación que si se hubiera administrado por vía intravenosa. Se supone, entonces, que toda la droga que llega al ventrículo derecho llega a la circulación sistémica y que se podrá medir su concentración tomando una muestra de una vena periférica. A esta droga que llega a la circulación sistémica se la denomina droga biodisponible. Esquema 14 Excreción renal de drogas Copyrigth 2006 – FODEM – Todas los derechos reservados [21] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Vida media de absorción Es la única medida directa de velocidad de absorción. Cuanto más rápida la absorción, menor es la vida media de absorción. Latencia (o retardo) de absorción (lag time) Es el tiempo transcurrido entre la administración de la droga y la detección de la droga en plasma. Este tiempo es influenciado por diversos factores: -Velocidad de disolución de la droga. -Velocidad de vaciado gástrico. - Eliminación presistémica. Pico plasmático El pico se refiere a la máxima concentración plasmática. Se mide tanto el valor del pico como el momento en que el mismo se produce. Un pico más alto y más precoz indica mayor velocidad de absorción, mientras que uno más alto pero más tardío, menor velocidad de eliminación. Extensión del concepto de relación entre dosis y cinética de eliminación. Como ya se dijo, al estudiar la absorción de un medicamento, estudiamos en realidad cómo se elimina desde el intestino hacia el plasma. Por lo tanto, se aplican a la absorción de las drogas los mismos conceptos que se discutieron para la eliminación: hay drogas con mecanismos saturables de absorción, cuya biodisponibilidad disminuye al aumentar la dosis (p. ej. metotrexato). Entonces, la eliminación, la absorción, la unión a proteínas (ver ejemplo del salicilato), la distribución, etc., pueden ser cada una dosis dependiente o dosis independientes. Copyrigth 2006 – FODEM – Todas los derechos reservados [22] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 15 Administración por vía bucal Bioequivalencia Dos preparados Son bioequivalentes si tienen la misma biodisponibilidad. Las diferencias de biodisponibilidad de diversos medicamentos can el mismo fármaco (suponiendo que ambos tienen igual cantidad de draga) son debidas a diferencias de velocidad de disolución, las que pueden deberse ya sea a diferencias de técnica farmacéutica o a diferencias de calidad de la droga empleada. PRINCIPIOS GENERALES DE DOSIFICAClON Cuando se debe decidir la dosificación de una draga, debe tomarse en cuenta su cinética de acumulación, sus propiedades farmacodinámicas, su toxicidad y las necesidades terapéuticas. En genera, cuanto menos dosis diarias se administren, tanto más cómoda para el paciente. En primer lugar, es necesario establecer si se requieren o no niveles terapéuticos permanentes. Si se necesitan niveles terapéuticos permanentes, es necesario tomar en cuenta la relación entre los niveles tóxicos y los terapéuticos. La cantidad de droga constante y que se administra a intervalos regulares se denomina dosis de mantenimiento. Si se requiere una dosificación acumulativa, la dosis de mantenimiento se calcula en forma tal que la cantidad de droga biodisponible sea igual a la eliminación en un intervalo entre dosis una vez alcanzada la meseta. Copyrigth 2006 – FODEM – Todas los derechos reservados [23] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 16 Influencia de las velocidades de absorción y eliminación sobre el pico plasmático FARMACODINAMIA (Esquema 1) Resulta evidente que para comprender la esencia de cómo la introducción de una sustancia particular afecta el funcionamiento de una célula dada o de un órgano o sistema, es fundamental el conocimiento preciso de la maquinaria bioquímica y fisiológica que resulta modificada por la acción del fármaco. En ese sentido es fundamental hacer notar que las drogas no crean funciones nuevas: simplemente aumentan o disminuyen (estimulan o inhiben) las funciones propias de una célula, tejido u organismo (según sea el nivel de acción que se evalúe). Si se considera que las ciencias básicas en las que se sustenta el conocimiento científico de la farmacología no tienen más de 100 años de desarrollo intensivo, se comprende que la farmacología con bases científicas es una disciplina realmente joven. De los datos experimentales y clínicos de los últimos 50 años referidos a la acción de los fármacos surgen interpretaciones racionales de los mecanismos por los cuales los fármacos actúan y que conforman las bases conceptuales de la farmacodinamia, dentro de la farmacología general. ACCIONY EFECTO FARMACOLOGICO La acción de una droga es la modificación de las funciones propias de una célula en el sentido de su aumento o disminución. Los fármacos no crean nuevas funciones. Ejemplo: la acción simpaticomimética de la noradrenalina por estimulación de sus receptores específicos ubicados en distintos órganos efectores. En este caso se trata de un fármaco con acción farmacológica propia. Pero también cuando se evalúa la acción, o efecto de un fármaco a nivel orgarnísmico (organismo entero), éste puede actuar por mecanismos psicológicos (sugestión) lo que es propio de los placebos. Al componente psicológico de la acción o efecto de un fármaco activo o no se lo llama -en general- efecto placebo. El efecto o respuesta de un fármaco es la apreciación o evaluación de la acción del mismo empleando procedimientos técnicos simples o complejos. En el caso (ejemplo) de la noradrenalina, el efecto hipertensor (consecuencia de su acción simpaticomimética), se Copyrigth 2006 – FODEM – Todas los derechos reservados [24] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM evalúa con un manómetro como aumento de la presión arterial. El órgano en el que se produce la acción cuyo efecto se mide se designa órgano efector o efector. El proceso por el cual se ejerce la acción farmacológica que se evalúa en el órgano efector, se designa mecanismo de acción; en este caso, la estimulación de los receptores α-adrenérgicos del músculo liso vascular que al producir una vasoconstricción generalizada (nivel funcional o modo de acción) desencadena el efecto hipertensor. NIVELES DE ACCION DE FARMACOS De los conceptos anteriormente desarrollados surgen los niveles de acción de los fármacos que se describen a continuación. Nivel molecular Comprende el estudio de las interacciones entre las moléculas de las drogas y moléculas identificables de sistemas biológicos: receptores, enzimas, mecanismos de transporte y componentes moleculares del aparato genético, todas ellas interacciones específicas. El sitio en que se verifica la interacción, esto es, el sitio de la acción molecular de un fármaco, se designa biofase. También en la biofase se ejercen las acciones de las drogas inespecíficas que actúan en altos valores de saturación relativa, induciendo alteraciones en las propiedades fisicoquímicas de las células o tejidos blanco (target, en inglés). Nivel subcelular Corresponde a las acciones evaluadas en organoides o componentes subcelulares en los que se ubican los receptores involucrados en el nivel molecular: membrana celular, citosol, mitocondrias, microtúbulos, vesículas sinápticas, etc. Nivel celular Comprende el estudio de la acción del fármaco sobre las células que resultan afectadas por el mismo. Nivel tisular Involucra las acciones de las drogas sobre los órganos o tejidos en los que se ejerce la acción del fármaco. Nivel organísmico Implica el análisis de las acciones en el organismo entero e importa no sólo por su propia relevancia, sino también porque mecanismos homeostáticos, sólo apreciables a este nivel, pueden generar efectos secundarios tanto o más importantes que los primarios. MECANISMO DE ACCION DE LAS DROGAS Cualquiera sea el efecto que una droga produzca sobre el organismo, el mismo resulta siempre de su interacción con ciertos componentes o constituyentes de las células. O, en otras palabras, las moléculas del fármaco deberán ejercer alguna influencia química sobre uno o más de los constituyentescelulares, para producir la respuesta farmacológica. Por lo cual, las moléculas del fármaco deberán aproximarse a las moléculas que constituyen las células, lo suficiente como para alterar el funcionamiento de las mismas. Ese sitio al cual deben ineludiblemente acceder los fármacos para inducir la respuesta farmacológica, se designa biofose, esto es, la fase en la que se ejerce la acción farmacológica o biológica de la droga. La acción farmacológica es la consecuencia de la combinación o interacción inicial fármaco-célula. Esta, a su vez, desencadenará una serie de eventos o modificaciones físicas, químicas o fisiológicas conocidas como efecto 0 efectos farmacológicos. DROGAS DE ACCION ESPECÍFICA E INESPECIFICA Copyrigth 2006 – FODEM – Todas los derechos reservados [25] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM En este sentido, las posibilidades de combinación de las moléculas de fármacos a los tejidos pueden ser considerablemente diferentes y dos grandes grupos o polos de fármacos pueden definirse: por una parte, las drogas con acción específica y, por la otra, las que actúan primariamente induciendo cambios en las propiedades físicoquímicas de las células y que se definen como drogas de acción inespecífca. Drogas de acción inespecífica Drogas estructuralmente no específicas son aquéllas en las cuales la actividad farmacológica no está directamente subordinada a la estructura química, actúan en altos niveles de saturación relativa. Drogas de acción específica En este caso, el mecanismo de la acción farmacológica es medido a través de una interacción con elementos celulares específicos, denominados receptores. En un sentido general, los receptores son elementos macromoleculares con los cuales interactúan las drogas para producir sus efectos biológicos característicos. Una vez que las drogas alcanzan, a través de procesos farmacocinéticos el sitio de acción o biofase se unen específicamente a los receptores celulares de reconocimiento, propiedad que es patrimonio de su afinidad y a partir de su ligadura, promueven una serie de modificaciones encadenadas, que representan un quantum de activación celular, dependiente de su eficacia o actividad intrínseca. La activación de los receptores y de los elementos celulares con los que se vinculan, generan efectos celulares muy disímiles que son propios de las funciones de cada elemento celular: los fármacos no crean nuevas funciones, simplemente activan o inhiben las funciones propias de las células y, en consecuencia, de las estructuras celulares organizadas (tejidos, órganos, sistemas). CURVAS DOSIS-RESPUESTA El efecto farmacológico o respuesta biológica consecutiva a la interacción droga-receptor es susceptible de medición o cuantificación. Las respuestas son por lo general graduales, esto es, existe una relación sistemática y continua entre la dosis aplicada y la magnitud o intensidad del efecto que dicha dosis produce. La representación gráfica de la intensidad del efecto en función de la concentración o dosis aplicada, se designa curva dosis-respuesta o curva concentración-efecto (CDR) y adopta una forma sigmoidea cuando en la abscisa se representan los logaritmos de las dosis (Esquema 17). Copyrigth 2006 – FODEM – Todas los derechos reservados [26] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 17 Graficación del efecto de una droga Copyrigth 2006 – FODEM – Todas los derechos reservados [27] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM INTERACCION DE DROGAS A NIVEL DEL RECEPTOR Dos (o más) drogas pueden interactuar simultáneamente a diversos niveles: - en la fase farmacéutica o exposición a la droga, responsable de la concentración de la misma en el sitio de absorción. - en la fase farmacocinética, que cubre los procesos de absorción, transporte y distribución, conversión metabólica, excreción, etc., que determina la concentración del agente activo en el sitio de acción o biofase. - en la fase farmacodinámica que corresponde a la interacción entre el agente activo y sus sitios moleculares de acción hasta alcanzar el efecto final. INTERACCIONES FARMACODINAMICAS Explicamos anteriormente que dos parámetros diferentes definen la actividad de una droga: su afinidad (con la que está relacionada la potencia) y su eficacia o actividad intrínsecas en relación directa con la actividad de la misma MECANISMOS DE TRANSDUCCION Luego de la interacción de un agonista con el receptor correspondiente se produce una serie de eventos moleculares que terminan en la modificación del estado funcional de la célula efectora, es decir, en la producción de una definida acción farmacológica. Desde un punto de vista general, los diferentes tipos de receptores involucrados en los mecanismos de transducción hasta hoy conocidos pueden clasificarse en: - Receptores de membrana conformando canales iónicos. - Receptores de membrana asociados a proteinas ligadoras de nucleótidos de guanina. - Receptores de membrana con actividad tirosina quinasa. - Receptores intracelulares. RECEPTORES DE MEMBRANA CONFORMANDO CANALES IONICOS Los principales receptores de membrana que, a su vez, contienen intrínsicamente un canal iónico están representados por: - Receptores colinérgicos nicotinicos. - Receptores para aminoácidos excitatorios (glutamato y aspartato). - Receptores para aminoácidos inhibidores (glicina y GABA). Receptores colinérgicos nicotínicos (Esquemas 18 y 19) El receptor colinérgico nicotínico mejor caracterizado en su estructura molecular es el que se encuentra a nivel del músculo esquelético. Receptores a aminoácidos excitatorios Los neurotransmisores aminoácidos excitatorios del sistema nervioso central están representados por el glutamato y e) aspartato. Receptores a aminoácidos inhibitorios Los principales neurotransmisores aminoacídicos inhibitorios son la glicina y el ácido gamma-aminobutírico (GABA), los cuales se caracterizan por actuar sobre receptores específicos que contienen intrínsecamente un canal aniónico. La glicina es el neurotransmisor inhibitorio de mayor relevancia a nivel del tronco cerebral y médula espinal. El GABA es un neurotransmisor inhibitorio de gran relevancia en distintas funciones del SNC y que actúa a través de la activación de 2 subtipos de receptores. Receptores de membrana unidos a proteínas ligadoras de nucleótidos de guanina Copyrigth 2006 – FODEM – Todas los derechos reservados [28] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Los receptores de membrana que, cuando son activados por un agonista, transducen los efectos por intermedio de proteínas reguladas por nudeótidos de guanina (denominadas proteínas G) pueden diferenciarse en tres grupos principales: - Receptores acoplados a adenililciclasa. - Receptores acoplados a hidrólisis de fosfoinosítidos. - Receptores acoplados a canales iónicos. Esquema 18 Estructura del receptor nicotínico de músculo esqueletico Copyrigth 2006 – FODEM – Todas los derechos reservados [29] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 19 Ubicación de los receptores Esquema 20 Adenalilciclasa y fosfolipasa C Copyrigth 2006 – FODEM – Todas los derechos reservados [30] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM - Receptores acoplados a adenililciclasa. - Receptores acoplados a hidrólisis de fosfoinosítidos. - Receptores acoplados a canales iónicos. Receptores acoplados a adenililciclasa, (Esquema 20) La adenililciclasa es una enzima que se ubica en las membranas plasmáticas de las células de prácticamente todos los tejidos. Su actividad está modulada principalmente por dos sistemas: uno estimulante y otro inhibitorio que se activan a través de agonistas de diferentes receptores. Receptores asociados a la hidrólisis de fosfoinosítidos Un número relevante de diferentes tipos de receptores, que se activan por múltiples drogas y hormonas, se caracterizan por tener como mecanismo de transducción la hidrólisis de una clase de fosfolípidos de membrana denominados fosfoinosítidos. TABLA II EJEMPLOS DE RECEPTORES ACOPLADOS A LA HIDROLISIS DE FOSFOINOSITIDO α1- adrenérgico M I - y M3- colinérgicos (muscarínicos) H 1 - histaminérgico B 2para bradiquinina 5-HT - seratonérgico 2 Receptores acoplados a canales iónicos Existen evidencias indicativas que luego de la activación de ciertos receptores se produce la apertura de determinados canales iónicos (que no forman parte del receptor activado) por intermediación de proteínas G. Receptores de membrana con actividad tirosina quinasa Este mecanismo de acción ha sido demostrado para diferentes agonistas a través de la estimulación de sus receptores específicos. Receptores intracelulares Los receptores de localización intracelular más relevantes están representados por: - Receptores para esteroides (glucocorticoides, mineralocorticoides, esteroides sexuales, vitaminas). - Receptores para hormona tiroidea. - Receptores para inductores del metabolismo de drogas (barbitúricos, hidrocarburos policíclicos, etc). VARIACIONES DE LAS RESPUESTAS A LOS FARMACOS Supersensibilidad Es el proceso por el cual se potencia la acción de un fármaco ante situaciones especiales del individuo. En el caso de la interacción de fármacos se restringe el concepto al caso en el que una droga inactiva por sí misma, es capaz de potenciar la acción de una droga activa. Supersensibilidad farmacocinética Se desarrolla antes de la interacción de la droga con el receptor, por aumento de la concentración de la misma en la biofase. Puede desarrollarse en cualquiera de los pasos farmacocinéticos: absorción, distribución, metabolismo y excreción. Copyrigth 2006 – FODEM – Todas los derechos reservados [31] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Supersensibilidad farmacodinámica Se desarrolla a nivel de los mecanismos celulares responsables de la respuesta biológica o efecto, ya sea a nivel de receptor o a nivel de los mecanismos efectores. TAQUIFILAXIAYTOLERANCIA Es relativamente común que el efecto de un fármaco disminuya cuando se lo administra de manera continuada o repetida. Una amplia gama de factores aparecen involucrados en este fenómeno de variación de la sensibilidad al fármaco. Se distinguen dos procesos diferentes: la taquifilaxia y la tolerancia, que analizaremos por separado. Taquifilaxia Taquiflaxia es la rápida disminución de la sensibilidad a una droga por la exposición a dosis sucesivas separadas por intervalos cortos. Tolerancia El término tolerancia se aplica para el caso de una disminución gradual de la respuesta o efectividad de la droga cuando se la administra repetidamente en períodos prolongados de tiempo. El término resistencia se utiliza comúnmente para describir la falta de efectividad de las drogas antimicrobianas (quimioterápicos). En clínica, la tolerancia se manifiesta como la necesidad de aumentar la dosis para producir el efecto deseado, en un proceso de curso temporal lento. FARMACOLOGIA CLINICA En su sentido más amplio, la farmacología clínica es la parte de la farmacología que utiliza como sujeto experimental al ser humano. Dentro del amplio campo que ella abarca, nos limita remos al desarrollo de nuevos medicamentos, a la farmacovigilancia, a las reacciones adversas de los medicamentos, a sus interacciones y a la evaluación riesgos/beneficios (Esquema 21). DESARROLLO DE NUEVOS MEDICAMENTOS La investigación y desarrollo de un nuevo medicamento es un proceso largo y complejo que no se agota con la aprobación del mismo para su comercialización por las autoridades sanitarias pertinentes, sino que continúa durante todo el tiempo en que ese medicamento sigue en uso terapéutico. Este proceso sigue una secuencia lógica de procedimientos experimentales y clínicos interrelacionados entre sí. Etapas del desarrollo de una nueva droga: Copyrigth 2006 – FODEM – Todas los derechos reservados [32] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Cada etapa requiere de una planificación minuciosa y de la participación de un gran grupo multidisciplinario de personas, además de los recursos económicos necesarios. Descubrimiento y Síntesis Actualmente, la síntesis química es la forma habitual de obtención de drogas, si bien es cierto que perduran otras formas de obtención (fermentación para la producción de antibióticos, extracción de alcaloides, etc.) y que se está utilizando cada vez más la ingeniería genética. Mediante el diseño de drogas asistido por computadora, se puede obtener una molécula (cabeza de serie) con un perfil farmacológico específico cercano al que se intenta reproducir en la realidad. A partir de ella se sintetiza un grupo de análogos, con el que se efectúan las pruebas biológicas para seleccionar entre ellos al fármaco que se utilizará para el nuevo medicamento. Una vez seleccionada la molécula, se determinan sus propiedades físico-químicas y se inician los desarrollos farmacéutico y farmacológico; éste se divide en 2 partes: farmacología preclínica y farmacología clínica. Copyrigth 2006 – FODEM – Todas los derechos reservados [33] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 21 Farmacología clínica: Ubicación dentro de la farmacología. Copyrigth 2006 – FODEM – Todas los derechos reservados [34] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 22 Fases de la farmacología clínica FARMACOLOGIA PRECLINICA (Esquema 23) Copyrigth 2006 – FODEM – Todas los derechos reservados [35] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Antes de ensayar cualquier medicamento en el hombre debe existir un adecuado y amplio estudio farmacológico en animales de experimentación, que brinde la información farmacodinámica, farmacocinética y toxicológica necesaria y suficiente para decidir el paso a la etapa clínica con un relativo margen de seguridad. Esta primera etapa en el desarrollo de un nuevo medicamento se conoce como farmacología preclínica o fase 0 de la farmacología clínica. Esquema 23 Farmacología precilinica INDICES TERAPEUTICOS Y DE SEGURIDAD Copyrigth 2006 – FODEM – Todas los derechos reservados [36] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM (Esquema 24) Ambos índices establecen una relación entre la toxicidad de la droga en estudio y su eficacia. Esquema 24 Farmacología precilinica Copyrigth 2006 – FODEM – Todas los derechos reservados [37] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM EVALUACION CLINICA DE EFICACIAY SEGURIDAD DE LOS MEDICAMENTOS Dentro del plan de evaluación de un nuevo medicamento, la etapa que sigue a la farmacología preclínica se denomina farmacología clínica. Su objeto de estudio no se limita a las nuevas moléculas, sino que incluye nuevas formas farmacéuticas, nuevas vías de administración o nuevas indicaciones. En estos últimos 3 casos no siempre se requiere una fase preclínica previa. La administración de un nuevo medicamento en el hombre se hace según una secuencia lógica de etapas llamadas fases de la farmacología clínica y la herramienta que se utiliza en cada una de ellas para cumplir con sus objetivos (evaluar eficacia y seguridad) es el ensayo clínico. Ensayo clínico (Esquema 25) Un ensayo clínico es un experimento éticamente justificado y correctamente diseñado, cuyo objetivo es responder a un problema planteado con precisión. Esta definición hace énfasis en 3 aspectos fundamentales: los recaudos éticos, la necesidad de responder a un problema concreto v la necesidad de un diseño experimental científicamente correcto. Esquema 25 Investigación Clìnica Copyrigth 2006 – FODEM – Todas los derechos reservados [38] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM FASES DE LA FARMACOLOGIA CLINICA (Esquemas 26 - 27 - 28 - 29 - 30) Se distinguen 4 fases, identificadas con números romanos. Para las fases I, II y III, se requiere la aprobación para ensayo clínico por parte de las autoridades sanitarias; para la fase IV, la aprobación para la comercialización del producto. Esquema 26 Copyrigth 2006 – FODEM – Todas los derechos reservados [39] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 27 Copyrigth 2006 – FODEM – Todas los derechos reservados [40] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 28 Esquema 29 Copyrigth 2006 – FODEM – Todas los derechos reservados [41] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM REACCIONES ADVERSAS (Esquema 31) Esquema 30 Para referirse a las consecuencias indeseables de la administración de un medicamento, se utilizan los términos efectos adversos y reacciones adversas, que emplearemos indistintamente. El primero hace énfasis en los efectos de la droga; el segundo, en la respuesta del paciente. No existe ningún término que implique ambos hechos a la vez, pero ambos aspectos son igualmente importantes. Para analizar las reacciones adversas, es necesario tomar en cuenta su frecuencia, su severidad, su relación causal con el medicamento y los mecanismos involucrados. Copyrigth 2006 – FODEM – Todas los derechos reservados [42] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 31 Reacciones Adversas TIPOS DE REACCIONES ADVERSAS (Esquema 32) Por su mecanismo, pueden distinguirse varios tipos de reacciones adversas: efecto nocebo, reacciones adversas claramente dosis-dependientes (efectos colaterales, efectos secundarios, intoxicaciones), reacciones adversas aparentemente dosis-independientes (idiosincracia, hipersensibilidad), síndromes por supresión y farmacodependencia. Copyrigth 2006 – FODEM – Todas los derechos reservados [43] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM Esquema 32 Tipos de reacciones adversas ACCION FARMACOLOGICA: Es la consecuencia de la combinación o interacción inicial fármaco -célula. ANTAGONISMO: Es la disminución farmacológica de una droga por acción de otra. - AGONISTA: Es la sustancia química que activa receptores y producen una respuesta. - AGONISTA PARCIAL: No es capaz de producir el máximo de respuesta. - AGONIST A COMPETITIVO: Disminuye la respuesta por evitar la concentración en el receptor. A los parciales y competitivos se los conoce también como ANTAGONISTAS. Copyrigth 2006 – FODEM – Todas los derechos reservados [44] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM BIODISPONIBILIDAD: Es la llegada de la droga a la circulación sistemática. Es el porcentaje o cantidad relativa de la dosis administrada que alcanza el plasma en función del tiempo. Se refiere a la droga madre o a la droga intacta. BIOFASE: Es el medio y/o lugar en que una droga está a disposición de actuar con los receptores. BIOTRANSFORMACION O METABOLISMO: Es la modificación de una molécula por medio de una reacción química catalizada por enzimas. BIOEQUIVALENCIA: Que tienen la misma biodisporilibilidad. CINETICA DE ELIMINACION: De orden 0: Cuando la velocidad de eliminación es constante para cualquier concentración de droga. De orden 1: Cuando esta velocidad de eliminación es proporcional a ala concentración de 1a droga. CLEARENCE O DEPURACION: Es el volumen de plasma que es completamente depurado de droga en una unida de tiempo. DOSIS: Es la cantidad de droga que debe administrarse a un ser vivo para producir un efecto determinado. DOSIFICACION: Es la estimación de la dosis para un fin determinado. DOSIS TERAPEITTICA O EFECTIVA MINIMA: Es la mínima dosis que produce el efecto deseado o esperado. DOSIS EFECTIVA 50 O DOSIS MEDIA: Es la que produce el efecto estudiado en el 50 % de la población reaccionante. DOSIS LETAL 50: Es la que produce la muerte en e1 50% de la población estudiada; sirve como índice de toxicidad de una droga. DOSIS USUAL: (no debe confundirse con dosis inedia). Es con la cual se espera obtener el efecto terapéutico. DROGA: Es todo compuesto natural, semisintético o sintético que se utiliza para tratar, prevenir o diagnosticar enfermedades en los seres vivos. DROGA DE ACCION ESPECIFICA: El mecanismo de acción es medido a través de una interacción con los receptores. DROGA DE ACCION INESFECIFICA: Es aquella en la cual la actividad farmacológica no está directamente subordinada a la estructura química, sino al alto nivel de saturación relativa. DROGA INACTIVA: Es aquella que actúa a través de sus metabolitos y para ello debe transformarse en activa por activación enzilnática o biactivación. A la droga inactiva se la denomina PRODROGA. EFECTO FARMACOLOGICO: Es la apreciación o evaluación de la acción de un fármaco empleando procedimientos técnicos; esta acción se evalúa en e1 órgano efector y este proceso se denomina mecanismo de acción. ELIMINACIÓN: Disminución de los niveles de la droga en cualquier compartimiento, sin importar el proceso involucrado; es decir, desaparece de la droga de la Biofase, y esta eliminación puede ocurrir por biotransformación o por excreción. EFICACIA: Es la ocupación de los receptores específicos. No se debe confundir con POTENCIA, ya que no son sinónimos, pues no se hallan necesariamente relacionados. A medida que aumenta la droga (dosis) ocupa más receptores, hasta que se ocupan de todos los específicos disponibles, y por más que se aumente la dosis, el efecto no aumentará. FARMACOLOGIA: Ciencia que estudia la manera por la cual las funciones de los organismos vivientes son afectadas por drogas o compuestos químicos. FARMACOCINETICA: Es tanto el estudio del conjunto de procesos que determinan la concentración de la droga en la 13iofiáse, como el estudia de los mismos. FARMACODINAMIA: Es el estudio de la acción de las drogas sobre los seres vivos. Debemos aclarar que las drogas no crean funciones nuevas, simplemente aumentan o disminuyen las funciones propias de la célula, tejido u organismo. IDIOSINCRACIA: Es una respuesta anormal, cualitativamente diferente de los efectos farmacológicos característicos de la droga, independientemente de la dosis, de bajo índice de porcentaje y debido a características propias de cada individuo. Copyrigth 2006 – FODEM – Todas los derechos reservados [45] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM INTOLERANCIA: Es una respuesta muy exagerada a las dosis usuales de un medicamento; es una desviación cuantitativa de una respuesta normal, cuya calidad no cambia. LATENCIA O RETARDO DE ABSORCIÓN: Es el tiempo transcurrido entre la administración de la droga y la detección de la misma en el plasma. LIGADURA PROTEICA: Los fármacos poseen ligadura proteica reversible tanto a nivel plasmático como tisular. La fracción de droga libre es la que nos interesa para la acción farmacológica. La unión es fácilmente reversible. Sólo parte del fármaco se une a proteínas. Ph: El Ph del medio orgánico determina la fracción no ionizada de los ácidos y bases. Ph= log 1 H+ El Ph del medio interno oscila dentro de un rango estrecho (7.39 y 7.43) debido a la presencia de sistemas amortiguadores. pKa de la droga: Es el Ph en el cual la droga se encuentra con el 50% de sus moléculas en estado de ionización y la otra mitad en estado de no ionización. El valor del pKa puede ser superior o inferior a 7, tanto sea en ácidos como en bases, por lo que el pKa no define la naturaleza ácida o básica de una sustancia. PICO PLASMATICO: Se refiere a la máxima concentración plasmática. Se mide tanto el valor del pico como el momento en que se produce. Es decir indica velocidad de absorción y/o menor velocidad de eliminación. POTENCIA: Es la inversa de la dosis. Droga más potente no significa que sea clínicamente superior, por eso no es tan importante la dosis como eficacia. PLACEBO: Sustancia sin acción o actividad específica.,- producen efectos psicológicos, especialmente sugestivos, lo que debe tenerse en cuenta cada vez que se administre cualquier droga, ya que la sugestión es capaz de producir curación por sí sola, especialmente en enfermedades sin base patológica. Se utilizan en estudios "doble ciego", en donde ni el médico ni el paciente saben si se suministra droga activa o placebo. RECEPTOR: Son estructuras moleculares situadas en la biofase de la célula efectora. Desde el punto de vista farmacológico, definimos a los receptores como a las estructuras localizadas en la membrana plasmática con las que interacciona una droga, y es a través de esta interacción específica conocida como interacción droga - receptor donde y corno se mide el mecanismo específico de acción. RANGO TERAPEUTICO: El objetivo terapéutico consiste en mantener niveles estables y constantes de droga en el plasma y luego mantenerlo dentro de un rango. Este rango está farmacológicamente ubicado en un espacio cuyo techo superior está marcado por lo que se llama concentración tóxima mínima y el piso inferior por lo que llamamos concentración terapéutica mínima. SINERGISMO: Es el aumento de la acción farmacológica de una droga por el empleo de otra, de acción farmacológicamente similar. Las ventajas que se obtienen es evitar o disminuir los efectos adversos o colaterales; lograr rapidez y duración de los efectos terapéuticos. Puede tratarse de un sinergismo de suma o aditivo, cuando las drogas se unen a los mismos receptores; puede tratarse de un sinergismo de potenciación, cuando las drogas que se administran simultáneamente reaccionan con distintos receptores para producir el mismo efecto. SUPERSENSIBILIDAD: Es el proceso por e1 cual se potencia la acción de un fármaco ante situaciones especiales del individuo. Puede ser farmacocinétiramente por aumento de la concentración de la droga en la biofase; o farmacológicamente cuando se desarrolla a nivel de los mecanismos celulares responsables de la respuesta biológica, ya sea a nivel de receptor o a nivel de los mecanismos efectores. SUSTANCIA POLAR: Es toda aquella sustancia que forma puentes de H' con H2o (se rodea de molécula de agua). Sustancia muy bidrofílica, Cuando una droga es muy polar y posee una gran superficie (alto peso molecular), el agregada de agua a su alrededor 1a polarizará aún más. Por lo tanto va a disminuir su pasaje a través de las membranas. Las moléculas polares se absorben con gran dificultad en el tracto digestivo; no atraviesan la barrera hemato-encefáclica y son difícilmente metabolizadas. (Ej: aminoglucósidos). Copyrigth 2006 – FODEM – Todas los derechos reservados [46] Curso Profesional de Agente de Propaganda Médica Extensión Universitaria FODEM TAQUIFILAXIA: Representa la anulación o por lo menos la disminución de la respuesta a ala droga, tras su repetida administración a cortos intervalos de tiempo. Se desarrolla rápidamente y es reversible. TOLERANCIA: Es la respuesta de muy baja intensidad ante la administración de la dosis usual de un determinado fármaco. Es una resistencia exagerada del individuo, inusitada, de carácter duradero, a responder a la dosis ordinaria de una droga. Puede extenderse a otras químicamente relacionadas, y esto se llama tolerancia cruzada. En clínica, la tolerancia se manifiesta como la necesidad de aumentar la dosis para producir el efecto deseado; es un proceso de curso temporal lento. (Es habitual en los drogadictos). TIPOS DE RECEPTORES: Existen distintos tipos de receptores. A) Receptores de membrana plasmática: 1) Asociados o acoplados a las proteínas G. 2) Acoplados a canales iónicos. 3) Asociados a una actividad fosfolipasa específica para: fosfo inositol difosfato; inositol trifosfato; di-acetil glicerol. B) Receptores intracelulares: 1) Nucleares. 2) Mitocondriales. 3) Citoplasmáticos. VIDA MEDIA: Es el tiempo en el cual una droga disminuye su concentración plasmática a la mitad. Constituye uno de los parámetros más importantes de la farmacocinética, pues permite idear un esquema de dosificación. La droga libre es siempre la droga activa. Copyrigth 2006 – FODEM – Todas los derechos reservados [47]








