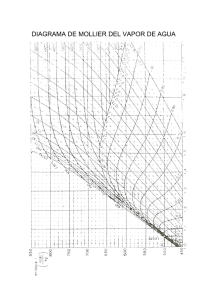
750 y su constante de formación es K Cu(NH ) [Cu ][NH ] = = × [ ] . 5
Anuncio
![750 y su constante de formación es K Cu(NH ) [Cu ][NH ] = = × [ ] . 5](http://s2.studylib.es/store/data/008468339_1-7cb62f1a9924a5c19532c033585fed72-768x994.png)
750 CAPÍTULO 16 Equilibrios ácido-base y equilibrios de solubilidad 'JHVSB Izquierda: Disolución acuosa de sulfato de cobre(II). Centro: Después de la adición de unas pocas gotas de una disolución acuosa concentrada de amoniaco, se forma un precipitado color azul pálido de Cu(OH)2. Derecha: Cuando se agrega más disolución acuosa concentrada de amoniaco, el precipitado de Cu(OH)2 se disuelve para formar un ion complejo Cu(NH3)42+ de color azul intenso. y su constante de formación es Kf = [Cu(NH3 )24+ ] [Cu2+ ][NH3 ]4 = 5.0 × 1013 El valor tan grande de Kf indica que el ion complejo es muy estable en disolución y explica que haya una concentración muy baja de iones cobre(II) en el equilibrio. EJEMPLO 16.15 Se agregan 0.20 moles de CuSO4 a un litro de disolución de NH3 1.20 M. ¿Cuál es la concentración de iones Cu2+ en el equilibrio? &TUSBUFHJB La adición de CuSO4 a la disolución de NH3 da como resultado la formación del ion complejo Cu2+(ac) + 4NH3(ac) Cu(NH3)42+(ac) (continúa) TABLA 16.4 Ion complejo Ag(NH3)2+ Ag(CN)2– Cu(CN)42– Cu(NH3)42+ Cd(CN)42– Cdl42– HgCl42– HgI42– Hg(CN)42– Co(NH3)63+ Zn(NH3)42+ Constantes de formación de iones complejos seleccionados en agua a 25°C Expresión de equilibrio Ag+ Ag+ Cu2+ Cu2+ Cd2+ Cd2+ Hg2+ Hg2+ Hg2+ Co3+ Zn2+ + + + + + + + + + + + 2NH3 2CN– 4CN– 4NH3 4CN– 4I– 4Cl– 4I– 4CN– 6NH3 4NH3 Ag(NH3)2+ Ag(CN)2– Cu(CN)42– Cu(NH3)42– Cd(CN)42– CdI42– HgCl42– HgI42– Hg(CN)42– Co(NH3)63+ Zn(NH3)42+ Constante de formación (Kf ) 1.5 1.0 1.0 5.0 7.1 2.0 1.7 2.0 2.5 5.0 2.9 × × × × × × × × × × × 107 1021 1025 1013 1016 106 1016 1030 1041 1031 109