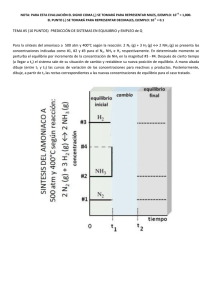
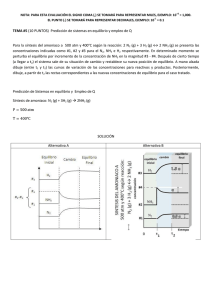
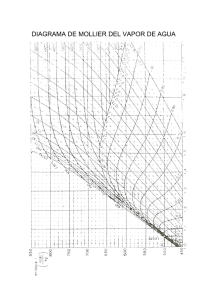
19
COMPLEJOS.
Un ion c o m p l e j o s e c o m p o n e de un á t o m o c e n t r a l que a c t ú a c o m o r e c e p t o r d e
p a r e s e l e c t r ó n i c o s y d e g r u p o s l l g a n d o s que a c t ú a n c o m o d a d o r e s de p a r e s e l e c t r ó n i c o s f o r m a n d o e n l a c e s c o o r d i n a d o s o d a t i v o s . L o s complejos s e f o r m a n e s p e c i a l m e n t e c o n l o s e l e m e n t o s de t r a n s i c i ó n , l o s c u a l e s en su n o t a c i ó n e s p e c t r a l
q u e d a n c o n v a r i o s o r b i t a l e s s e m i l l e n o s . (o'^>-i'*'cs "^ )
E x p e r inne n tal m e nte .«e o b s e r v a l o s d i f e r e n t e s c a m b i o s de c o l o r que t o m a n l o s
c o m p l e j o s d e b i d o al o r d e n de l a f u e r z a c r e a d a p o r l o s l l g a n d o s , un o e d e n que s e
e s p e r a r í a p o r l o s e f e c t o s e l e c t r o s t á t i c o s y t e n i e n d o en c u e n t a el d e s p l a z a m i e n t o s
de i o n e s s e f o r m a l a s e r l e e s p e c t r o q u í m l c a d e b i d o a l a s d i f e r e n t e s c o l o r a c i o n e s
observadas
CN
>
plrldina
> C2O.
'>H20>F~>RC0
> ( 5 H >C1
y B ^ ^ l '
L o s c o m p l e j o s son de b a s t a n t e u s o en q u í m i c a a n a l í t i c a p a r a l a p e p a r a d ó n e Ident i f i c a c i ó n de I o n e s m e t á l i c o s ^ p o r e j e m p l o l a p l a t a se s e p a r a d e l Hg^ CI2 y d e l
P b CI2 d i s o l v i e n d o con H i d r ó x i d o de a m o n i o c o n e l fin de o b t e n e r un c o m p l e j o de
p l a t a (Ag (NH3 )-) , o t r o s c a s o s s e r í a n l a C l o r o f i l a c o m p l e j o de m a g n e s i o y
p o r f l r l n a s u s t i t u i d a , l a h e m o g l o b i n a e s t á c o n f o r m a d a p o r h i e r r o y una p o r f i r i n a
s u s t i t u i d a (la p o r f l r l n a e s p a r t e de l a e s t r u c t u r a b á s i c a de u n a p r o t e í n a ) .
REGLAS PARA FORMAR
COMPLEJOS
1.
S í m b o l o d e l á t o m o c e n t r a l s e c o l o c a de p r i m e r o s e g u i d o p o r l o s U p a n d o a n l ó nlcos (-), catlónicos ( + ).
2,
L a f ó r m u l a d e l lón o m o l é c u l a c o m p l e j a d e b e e n c e r r a r s e en p a r é n t e s i s c u a drados.
NOMENCLATURA
1,
L o s l l g a n d o s n e u t r o s y c a t i o n e s s e n o m b r a n en o r d e n a l f a b é t i c o y s i s e r e p i ten u t i l i c e l o s p r e f i j o s d i , t r i , t e t r a , p e n t a , h e x a .
Llgandos neutros
H O
A quo
NH'3
Amonla
CO
Carbonll
NO
Nltrosll
AlH,
Tetrahldroalumlnato
4
L i g a n d o a n i ó n i c o s l l e v a n la t e r m i n a c i ó n " O "
OH
S2-
Hldroxo
Tío
T—*•
CN
CI-
2
ÑO,"
co^"^-
Sulfato
soy
2.
Ciano
Nitro
Cloro
Nitrato
Carbonato
Noml:)re del m e t a l i n d i c a n d o s u n ú m e r o de o x i d a c i ó n con n ú m e r o s
romanos
""•ÍQTA: Si e l c o m p l e j o e s un a n i ó n e l m e t a l l l e v a la t e r m i n a c i ó n " A t o "
Ejemplo: Cuprato, ferrato, platínalo, estáñalo, aurato , cinato, (Z^),
cobaltato .
E j e m p l o de a n i o n e s c o m p l e j o s
(el m e t a l t e r m i n a en Ato)
4H e x a c i a n o f e r r a t o (II)
fp, CL J ^/.
Au fCN)
¿ Zn (OH)
H e x a c i a n o f e r r a t o (III)
r
D í c i a n o A u r a t o (I)
4j
T e t r a H l d r o x o C i n a t o (II)
Tetracloro
platlnato
(II)
Complejos catión icos
ÍÁg (NH3)2]"^
D i a m o n l a p l a t a (I)
/Co (NH3). C O , 1 +
C a r b o n a t o t e t r a A m o n l a C o b a l t o (III)
fCo ( N H , ) ^ CL"] +
D i c l o r o t e t r a A m o n i o C o b a l t o (III)
Neutros
Ll ¿ A l H . I
T e t r a H l d r o A l u m í n a l o de L i t i o
Ni (CO)^
T e t r a c a r b o n l l N í q u e l (0)
PREGUNTAS Y PROBLEMAS
1.
Investiga la d i f e r e n c i a fundamental e n t r o los s i g u i e n t e s t é r m i n o s :
E l e c t r o v a l e n c i a , c o v a l e n c i a , c o v a l e n c i a n o r m a l , c a r g a f o r m a l , n ú m e r o s de
 0
0