PRACTICA-REACCION DE CANNIZZARO - q
Anuncio
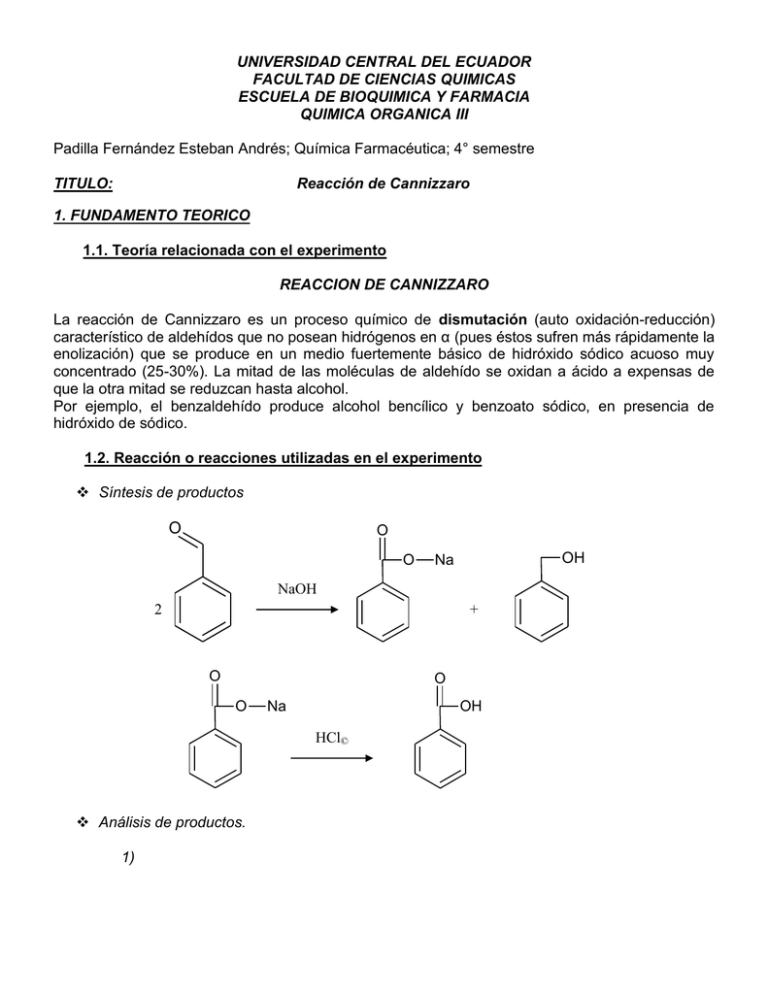
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUIMICA Y FARMACIA QUIMICA ORGANICA III Padilla Fernández Esteban Andrés; Química Farmacéutica; 4° semestre TITULO: Reacción de Cannizzaro 1. FUNDAMENTO TEORICO 1.1. Teoría relacionada con el experimento REACCION DE CANNIZZARO La reacción de Cannizzaro es un proceso químico de dismutación (auto oxidación-reducción) característico de aldehídos que no posean hidrógenos en α (pues éstos sufren más rápidamente la enolización) que se produce en un medio fuertemente básico de hidróxido sódico acuoso muy concentrado (25-30%). La mitad de las moléculas de aldehído se oxidan a ácido a expensas de que la otra mitad se reduzcan hasta alcohol. Por ejemplo, el benzaldehído produce alcohol bencílico y benzoato sódico, en presencia de hidróxido de sódico. 1.2. Reacción o reacciones utilizadas en el experimento Síntesis de productos O O O OH Na NaOH 2 + O O O Na OH HCl© Análisis de productos. 1) O O O OH Na NaOH 0,1 N 2) O O O OH NaIO3 10% NaI 10% I2 (ac) + H2O + O O Na 3) OH Cl ZnCl2 + H2O HCl© 1.3. Mecanismos de reacción Síntesis de productos: Na Análisis de productos 2. METODOLOGIA EXPERIMENTAL 2.1. Materiales y equipos Materiales y Equipos 1 Frasco de tapa hermética 1 Embudo de separación 2 Vaso de precipitación de 250 ml 1 Embudo de Büchner 1 Embudo de vidrio 1 Equipo de destilación simple 2 Erlenmeyer de 250 ml y 125 ml 1 Equipo de reflujo de 250 ml 10 Tubos de ensayo Varillas de agitación Pipetas graduadas Papel filtro Papel indicador Balanza analítica Potenciómetro 2.2. Reactivos y sustancias Acido clorhídrico concentrado Agua destilada Benzaldehído Éter dietílico Hidróxido de sodio Hielo Sulfato de sodio anhidro Bicarbonato de sodio Yodato de potasio 10% Yoduro de potasio 10% Indicador de almidón Hidróxido de sodio 0,1N valorado Acido clorhídrico 0,1N valorado Rojo congo 0,1% Rojo de metilo 0,1% 2.3. Procedimiento REACCION DE BISMUTACION DE CANNIZZARO: Síntesis de acido benzoico y alcohol bencílico En un frasco con tapa hermética colocar 5 ml de benzaldehído y 4,5 g de NaOH disueltos en 5 ml de agua, se tapa firmemente y se agita vigorosamente hasta que aparezca un producto sólido y un líquido incoloro. La agitación se continua por 45 minutos constantemente y luego por 20 minutos mas con agitación periódica. Concluido este tiempo, se añade agua hasta lograr la solubilización de todo el benzoato de sodio formado, evitando el exceso de agua. La solución se traslada a un embudo de separación y se añaden 20 ml de cloroformo o éter dietílico, para extraer el alcohol bencílico formado, se repite la extracción por una ocasión mas. Las fases orgánicas se juntan y se guardan en un frasco con tapa de rosca en refrigeración. La fase acuosa se traslada a un vaso y se precipita por adición de HCl©, el acido benzoico obtenido. Se enfría la mezcla y se filtra por succión. Se purifica por recristalización en agua. El sólido se seca y se pesa para el calculo del rendimiento. La fase orgánica, se destila en baño de agua para recuperar todo el solvente y el residuo, que corresponde al alcohol bencílico se mide para calcular el rendimiento. Análisis de productos Ácido benzoico 1. Reacción con bicarbonato de sodio. Muestras líquidas: a 3 ml de muestra, añadir unos miligramos de bicarbonato de sodio. Observar si existe desprendimiento de CO2, debido al desplazamiento del ácido carbónico Muestras sólidas: disolver 0,5 g de muestra en 5 ml de agua destilada (pH=7), y agregar en la solución unos mg de bicarbonato de sodio sólido. Si la muestra no es soluble en frío, calentar hasta disolución y realizar la prueba. 2. Reacción al papel tornasol. Muestras líquidas: en 3 ml de muestra, acercar un papel tornasol, observar si existe reacción ácida. Muestras sólidas: disolver 0,5 g de muestra en 5 ml de agua destilada (pH=7), y acercar un papel tornasol. Si la muestra no es soluble en frío, calentar hasta disolución y realizar la prueba. 3. Reacción yodato-yoduro. En un tubo de ensayos mezclar 1 ml de solución de yodato de potasio 10% con 1 ml de solución de yoduro de potasio 10%. En un segundo tubo de ensayos disolver 10 mg de ácido benzoico (o salicílico) en 1 ml de agua, calentar si es necesario. Sobre este tubo añadir la mezcla yodato yoduro. Observar la inmediata liberación de yodo (marrón) en la reacción. Si no se observa, añadir gotas de indicador de almidón, observar el color azul del complejo formado. 4. Determinación del equivalente de neutralización mediante titulación potenciometrica. Muestras insolubles en agua. Pesar en balanza analítica 0,2 gramos de muestra y disolver en 10 ml de hidróxido de sodio 0,1N medido cuantitativamente, reflujar por 30 minutos, enfriar. Titular el exceso de hidróxido con ácido clorhídrico 0,1N; utilizando un pH metro para verificar los cambios de pH. Blanco. Reflujar por 30 minutos 10 ml de hidróxido de sodio 0,1N medido cuantitativamente, enfriar. Titular el hidróxido con ácido clorhídrico 0,1N; utilizando un pH metro para verificar los cambios de pH. Determinar gráficamente el punto de equivalencia, con cualquiera de los gráficos siguientes. En el eje de las ordenadas anote los valores de pH y en el de las abscisas los volúmenes de solución valorada agregada. En el eje de las ordenadas el cociente de los valores de diferencias de pH y los valores de las diferencias de volumen agregado y en las abscisas los volúmenes de solución valorada agregada. Calcular el equivalente de neutralización del ácido. Alcohol bencílico En un erlenmeyer de 500 ml ponga 4 g de cloruro de cinc, 40 ml de alcohol bencílico, 21 ml de ácido clorhídrico concentrado. Tomar el tiempo de reacción. Agite la mezcla durante 15 a 20 minutos. Pase a un embudo de separación y deje reposar la mezcla hasta que las capas se separen completamente. Elimine con cuidado la capa ácida y lave la capa orgánica con tres porciones de agua y al final con 50 ml de solución de bicarbonato de sodio al 5%, por dos ocasiones, deseche la fase acuosa. Seque la fase orgánica con sulfato de sodio anhidro. Filtre el líquido en un balón de destilación seco y destile. Recoja la fracción que destila entre 50-51 °C. 2.4. Diagrama de flujo REACCION DE CANNIZZARO (Síntesis de acido benzoico y alcohol bencílico) En frasco con tapa hermética agragar 5 ml benzaldehído y 4,5 g de NaOH dicueltos de 5 ml de agua. Agitar fuertemente durante 1 hora, pasado este tiempo añadir agua hasta solubilizar C6H5COONa formado Fase orgánica destilar en baño de agua recuperando solvente y el residuo, es el alcohol bencílico Fase acuosa trasladar a un vaso y agregar HCl(C) precipitando el C6H5COOH obtenido y filtrar por succion. Trasladar a a embudo de separación y extraer con 20 ml de éter dietílico, dos veces. 2.5. Ficha de seguridad y constantes físicas de reactivos y productos FICHA DE SEGURIDAD DEL BENZALDEHIDO FICHA DE SEGURIDAD DEL ACIDO BENZOICO ACIDO BENZOICO Acido bencenocarboxílico Acido fenilcarboxílico C7H6O2/C6 H5COOH Masa molecular: 122.1 TIPOS DE PELIGRO/ EXPOSICION PELIGROS/SINTOMAS AGUDOS Combustible. PREVENCION Evitar las llamas. Polvo, agua pulverizada, espuma, dióxido de carbono. INCENDIO EXPLOSION LUCHA CONTRA INCENDIOS/ PRIMEROS AUXILIOS Las partículas finamente Evitar el depósito del dispersas forman mezclas polvo; sistema cerrado, explosivas en el aire. equipo eléctrico y de alumbrado a prueba de explosión del polvo. En caso de incendio: mantener fríos los bidones y demás instalaciones rociando con agua. EXPOSICION Inhalación Tos. Piel Extracción localizada o protección respiratoria. Aire limpio, reposo. Enrojecimiento. Guantes protectores. Quitar las ropas contaminadas, aclarar y lavar la piel con agua y jabón. Enrojecimiento, dolor. Gafas ajustadas de seguridad. Enjuagar con agua abundante durante varios minutos (quitar las lentes de contacto, si puede hacerse con facilidad) y proporcionar asistencia médica. Ojos Ingestión Dolor abdominal, náuseas, No comer, ni beber, ni vómitos. fumar durante el trabajo. Lavarse las manos antes de comer. DERRAMES Y FUGAS ALMACENAMIENTO Barrer la sustancia derramada Ventilación a ras del suelo. e introducirla en un recipiente de plástico y eliminar el residuo con agua abundante. Enjuagar la boca, provocar el vómito (¡UNICAMENTE EN PERSONAS CONSCIENTES!) y proporcionar asistencia médica. ENVASADO Y ETIQUETADO D A T O S I M P 0 R T A N T E ESTADO FISICO; ASPECTO Polvo o cristales blancos. RIESGO DE INHALACION No puede indicarse la velocidad a la que se alcanza una concentración nociva en el aire por evaporación de PELIGROS FISICOS Es posible la explosión del polvo si se esta sustancia a 20°C. encuentra mezclado con el aire en forma pulverulenta o granular. EFECTOS DE EXPOSICION DE CORTA DURACION La sustancia irrita los ojos, la piel y el PELIGROS QUIMICOS tracto respiratorio. La disolución en agua es un ácido débil. Reacciona con oxidantes. EFECTOS DE EXPOSICION PROLONGADA O REPETIDA El contacto prolongado o repetido LIMITES DE EXPOSICION puede producir sensibilización de la TLV no establecido. piel. VIAS DE EXPOSICION La sustancia se puede absorber por inhalación y por ingestión. Punto de ebullición: 249°C Punto de fusión: 122°C (véanse Notas) Densidad relativa (agua = 1): 1.3 PROPIEDADES Solubilidad en agua, g/100 ml a FISICAS 20°C: 0.29 Presión de vapor, Pa a 96°C: 133 Densidad relativa de vapor (aire = 1): 4.2 Densidad relativa de la mezcla vapor/aire a 20°C (aire = 1): 1 Punto de inflamación: 121°C (c.c.) Temperatura de autoignición: 570°C Coeficiente de reparto octanol/agua: 1.87 FICHA DE SEGURIDAD DEL ALCOHOL BENCILICO FICHA DE SEGURIDAD DEL HIDROXIDO DE SODIO 3. REGISTRO DE DATOS EXPERIMENTALES Producto: síntesis y análisis acido benzoico Peso (g) papel filtro Peso (g) papel filtro mas acido benzoico Peso (g) acido benzoico Equivalente de neutralización Peso (g) acido benzoico N NaOH valorado N HCl valorado Reacciones de identificación Determinación del carácter ácido Reacción con bicarbonato de sodio Reacción al papel tornasol Reacción de yodato-yoduro Producto: síntesis y análisis alcohol bencílico Volumen (ml) alcohol bencílico obtenido Tiempo (seg o min) de reacción de Lucas 4. CALCULOS Cálculo del rendimiento: % 𝑅𝑒𝑛𝑑𝑖𝑚𝑖𝑒𝑛𝑡𝑜 = 𝑚 𝑔 𝑟𝑒𝑎𝑙 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑥 100 𝑚 𝑔 𝑡𝑒𝑜𝑟𝑖𝑐𝑎 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 % 𝑅𝑒𝑛𝑑𝑖𝑚𝑖𝑒𝑛𝑡𝑜 = 𝑉 𝑚𝑙 𝑟𝑒𝑎𝑙 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑥 100 𝑉 𝑚𝑙 𝑡𝑒𝑜𝑟𝑖𝑐𝑎 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 Cálculo del equivalente de neutralización: 𝑁𝑎𝑂𝐻 + 𝐻𝐶𝑙 ↔ 𝑁𝑎𝐶𝑙 + 𝐻2 𝑂 # 𝐸𝑞𝑁𝑎𝑂𝐻 = #𝐸𝑞𝐻𝐶𝑙 𝑁𝑁𝑎𝑂𝐻 . 𝑉𝑁𝑎𝑂𝐻 = 𝑁𝐻𝐶𝑙 . 𝑉𝐻𝐶𝑙 𝑉𝑁𝑎𝑂𝐻 (𝑒𝑥𝑐 ) = 𝑁𝐻𝐶𝑙 . 𝑉𝐻𝐶𝑙 𝑁𝑁𝑎𝑂𝐻 𝑉𝑁𝑎𝑂𝐻 (𝑟𝑒𝑎𝑐𝑐𝑖𝑜𝑛𝑎 ) = 𝑉𝑁𝑎𝑂𝐻 (𝑡𝑜𝑡𝑎𝑙 ) − 𝑉𝑁𝑎𝑂𝐻 (𝑛𝑜 𝑟𝑒𝑎𝑐𝑐𝑖𝑜𝑛𝑎 𝐶6 𝐻5 𝐶𝑂𝑂𝐻 + 𝑁𝑎𝑂𝐻 ↔ 𝐶6 𝐻5 𝐶𝑂𝑂𝑁𝑎 + 𝐻2 𝑂 #𝐸𝑞𝐶6 𝐻5 𝐶𝑂𝑂𝐻 = #𝐸𝑞𝑁𝑎𝑂𝐻 𝑟𝑒𝑎𝑐𝑐𝑖𝑜𝑛𝑎 ) 𝑚 𝑔 𝐶6 𝐻5 𝐶𝑂𝑂𝐻 = 𝑁𝑁𝑎𝑂𝐻 . 𝑉𝑁𝑎𝑂𝐻 𝑃𝑒𝑞𝐶6 𝐻5 𝐶𝑂𝑂𝐻 𝑃𝑒𝑞𝐶6 𝐻5 𝐶𝑂𝑂𝐻 = 𝑚 𝑔 𝐶6 𝐻5 𝐶𝑂𝑂𝐻 𝑁𝑁𝑎𝑂𝐻 . 𝑉𝑁𝑎𝑂𝐻 5. APLICACIÓN DE LOS PRODUCTOS APLICACIONES DEL ACIDO BENZOICO El ácido benzoico, los benzoatos y los ésteres del ácido benzoico son compuestos comúnmente encontrados en la mayoría de las frutas, especialmente en las bayas; siendo los arándanos una fuente rica del mismo. Adicionalmente, los benzoatos se encuentran de manera natural en las setas o champiñones, la canela, el clavo de olor y en algunos productos lácteos (debido a la fermentación bacteriana). Con fines comerciales, estos compuestos son preparados químicamente a partir del tolueno. Son usados como conservantes en los productos ácidos, ya que actúan en contra de las levaduras y las bacterias, siendo poco efectivos en contra de los hongos. Así mismo, son ineficaces en productos cuyo pH tiene un valor superior a 5 (ligeramente ácido o neutro). Las altas concentraciones resultan en un sabor agrio, lo cual limita su aplicación. Entre el grupo de los diversos compuestos, los benzoatos son normalmente preferidos debido a su mejor solubilidad. El ácido benzoico y los benzoatos son ampliamente utilizados en los productos ácidos o los ligeramente ácidos. No tiene efectos colaterales en las concentraciones utilizadas. En algunas personas, el ácido benzoico y los benzoatos pueden liberar histamina, la cual ocasiona reacciones pseudoalérgicas. La ingesta máxima diaria es de 5 mg/kg de peso corporal. APLICACIONES DEL ALCOHOL BENCILICO El alcohol bencílico es un buen medio punto de ebullición disolvente. Las principales aplicaciones: disolvente de pintura, tinta solvente, disolvente de plexiglás, el agente de revelado fotográfico, estabilizador de PVC, medicina, disolvente de resina sintética, ungüento o medicina líquida, solvente para productos cárnicos sello de tinta-pad y el aceite de bolígrafo, desengrasante de alfombra; cráter de limpieza, estabilizador de disolvente de silicona; éster bencílico o éter intermedio. El alcohol bencílico es una especie de fijador del perfume muy útil. Es un condimento indispensable cuando jazmín, nardo o ylang es mixta, y utilizados para componer el jabón y cosméticos a diario. 6. REFERENCIAS BIBLIOGRAFICAS Buscador: Google, http://docencia.izt.uam.mx/cuhp/QuimOrgIII/PracLabQO3.pdf. Lunes, 30 de mayo de 2011, 16:32 Buscador: Google, http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/Ficheros/10 1a200/nspn0102.pdf. Lunes, 30 de mayo de 2011, 18:45 Buscador: Google, http://www.aditivosalimentarios.com/index.php/codigo/210/Acidobenzoico. Martes, 31 de mayo de 2011, 16:15 Buscador: Google, http://www.cisproquim.org.co/HOJAS_SEGURIDAD/Hidroxido_de_Sodio.pdf. Martes, 31 de mayo de 2011, 21:32 L.G. WADE, JR.; “Química Orgánica”, quinta edición, PEARSON EDUCACIÓN, S.A., Madrid, 2004. Pág. 459,460 VOGEL Arthur, Textbook of Practical Organic Chemistry, 3th Edition, Great Britain, 1959, Ed. Longman, pág. 706, 711, 712.