Gestante a término con trombosis de la vena cava inferior
Anuncio

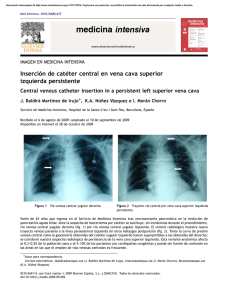
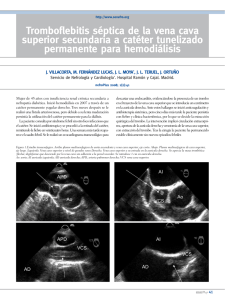
Documento descargado de http://www.elsevier.es el 30/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. (Rev. Esp. Anestesiol. Reanim. 2010; 57: 307-310) CASO CLÍNICO Gestante a término con trombosis de la vena cava inferior: tratamiento anestésico en el parto E. Fernández1,a, N. Dueñas1,a, A. Villafranca1,a, M. Perea2,a, B. Amorós2,b, L. Bermejo2,a, Departamento de Anestesiología. Hospital General Universitario Gregorio Marañón. Madrid. bDepartamento de Anestesiología. Hospital Universitario de Guadalajara. a Resumen Parturient at full term with inferior vena cava thrombosis: anesthesia during surgical delivery Una cesárea de emergencia es una situación de riesgo debido a las complicaciones potenciales que puede sufrir el binomio materno-fetal. En el caso que presentamos, este riesgo se incrementó por la presencia de un trombo masivo en la vena femoral común izquierda de la madre que se extendía hacia la vena cava. Se trataba de una mujer de 31 años, sin antecedentes de interés y en la 41ª semana de gestación, que estaba programada para inducción del parto por gestación prolongada. Ingresó en el servicio de urgencias dos días antes de la fecha prevista para la inducción, donde fue diagnosticada de trombosis venosa profunda en el miembro inferior izquierdo. Fue trasladada a la unidad de recuperación post-anestésica, donde los diferentes servicios implicados (Ginecología, Hematología, Radiología Intervencionista y Anestesiología) debatieron las varias opciones terapéuticas, trombectomía, filtro de vena cava, o el tratamiento anticoagulante con heparina no fraccionada intravenosa. Dado que la trombosis venosa profunda coincidía con el parto, el tratamiento anestésico y la elección del tratamiento eran trascendentes, para garantizar la máxima seguridad a la madre y al feto y y prevenir la aparición de complicaciones como un tromboembolismo pulmonar masivo. Emergency cesarean section is a high-risk situation because of potential maternal-fetal complications. We report a case in which risk increased due to a massive thrombus in the mother’s left common femoral vein extending to the vena cava. A 31-year-old woman with no relevant medical history in the 41st week of pregnancy was scheduled for induction. Two days before the planned induction she was admitted to the emergency department, where she was diagnosed with deep vein thrombosis in the left lower limb. She was transferred to the postanesthetic recovery unit, where a multidisciplinary team (from gynecology, hematology, interventional radiology, and anesthesiology) discussed various therapeutic options (thrombectomy, vena cava filter, or anticoagulation by intravenous infusion of unfractionated heparin). Given that deep vein thrombosis coincided with obstetric delivery, it was crucial to decide on anesthetic and therapeutic approaches that would assure maternal and fetal safety and prevent such complications as massive pulmonary thromboembolism. Palabras clave: Embarazo. Cesárea. Trombosis venosa profunda. Filtro de vena cava inferior. Tratamiento anticoagulante. Key words: Pregnancy. Cesarean section. Deep vein thrombosis. Inferior vena cava filter. Anticoagulant therapy. Introducción mínima o producir edema y pérdida del endotelio vascular. Los factores subyacentes de la trombosis venosa profunda (TVP) son hipercoagulabilidad, éstasis venoso, y el daño vascular (tríada de Virchow). La TVP es más grave que la superficial, sobre todo debido a las posibles complicaciones que se pueden derivar de la misma como embolismo pulmonar, o el síndrome post-trombótico. La incidencia de TVP en el embarazo es 5 veces mayor que en mujeres no embarazadas, es decir es de aproximadamente 3,24 casos/1.000 mujeres/año. El mayor riesgo se observa durante las primeras 6 semanas del periodo postparto, seguido por el tercer trimestre de gestación. Se estima que alrededor del 84% de La presencia de un trombo y la respuesta inflamatoria que la acompaña es conocida como trombosis venosa y tromboflebitis. Esta respuesta puede ser Médico Residente. 2Médico Adjunto. 1 Correspondencia: Dr. Eugenio Fernández Medina. C/ Sierra de Atapuerca, 21, Portal B, 6º C 28050 Madrid E-mail: [email protected] Aceptado para su publicación en abril de 2010. 49 Summary 307 Documento descargado de http://www.elsevier.es el 30/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 5, 2010 los episodios de TVP se producen en el miembro inferior izquierdo1-3. Durante el embarazo normal, se ha descrito un aumento en los niveles de factores de coagulación. En el 40% de las mujeres embarazadas se observa la resistencia adquirida a los anticoagulantes endógenos (proteínas C y S). La fibrinolisis está fisiológicamente alterada en el embarazo por un aumento en las concentraciones de los inhibidores del activador del plasminógeno (PAI-1 y PAI-2, esta última producida por la placenta)1-3. Existe también una reducción del 50-60% en el flujo venoso, sobre todo a partir de la semana 25ª de gestación hasta 6 semanas después del parto. De otro lado, los vasos pélvicos pueden sufrir daños durante el parto. Entre los factores de riesgo para la TVP durante el embarazo se incluyen trastornos de la coagulación (factor V de Leiden, 20.210 mutación del gen de la protrombina, anticuerpos antifosfolípido, o la deficiencia de proteínas C y S), hemorragia preparto, parto por cesárea, el tabaquismo, el consumo previo de anticonceptivos orales, obesidad, edad mayor de 35 años, la inmovilidad, la preeclampsia, una TVP anterior, la insuficiencia venosa crónica, la hiperemesis gravídica, la raza negra, la diabetes, o las infecciones durante el periodo postparto1-3. Fig. 1. Aumento de tamaño pierna izquierda en TVP. Caso clínico Se trata de una mujer de 31 años de edad, 65 kg de peso y 168 cm de talla, sin antecedentes patológicos de interés en la 41 semana de su primera gestación. No presenta ninguno de los factores de riesgo de TVP. El embarazo era controlado y sin complicaciones significativas (durante la gestación). Se había programadao para la inducción del parto por gestación prolongada. Dos días antes de la inducción, acudió al servicio de urgencias con un dolor repentino en la extremidad inferior izquierda (10/10 en la escala visual analgésica), acompañado de hinchazón, aumento del tamaño y temperatura de la pierna izquierda (Fig. 1), con pulsos periféricos conservados e impotencia funcional. Se realizó un eco-Doppler, con diagnóstico de trombo iliofemoral de gran tamaño (Fig. 2). Se administraron 60 mg de enoxaparina sódica subcutánea, 1 g de paracetamol IV, y al no ceder el dolor 25 mg de meperidina IV. Se trasladó a la Unidad de Recuperación Postanestésica, donde se monitorizó la presión arterial no invasiva, electrocardiograma (ECG), las contracciones uterinas, y la saturación arterial de oxígeno (SaO2), así como la frecuencia cardíaca fetal con un cardiotocógrafo externo. No hubo signos de sufrimiento fetal ni de inestabilidad materna. El dolor remitió con una bomba de morfina controlada por la paciente. Se decidió iniciar tratamiento anticoagulante con heparina no fraccionada intravenosa (25.000 UI en 250 mL de solución salina normal a 12 ml/h) buscando un 308 Fig. 2. Ecografía de miembros inferiores que muestra dentro del círculo punteado una trombosis iliofemoral. tiempo de tromboplastina parcial activado (TTPA) en torno a 50-60 segundos. La paciente no presentó dificultad respiratoria, dolor torácico, mareos o síncope. Después de consultar con los Servicios de Ginecología, Hematología, Radiología Intervencionista y Cirugía Vascular, se decidió continuar el tratamiento conservador durante las siguientes 48 horas para tratar de estabilizar el trombo y reducir el riesgo de una embolia pulmonar y se programó el parto por cesárea. Otras opciones más invasivas, tales como un filtro en la vena cava inferior o trombectomía profilácticos fueron des50 Documento descargado de http://www.elsevier.es el 30/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. E. FERNÁNDEZ ET AL– Gestante a término con trombosis de la vena cava inferior: tratamiento anestésico en el parto cartados por los riesgos que implican y por la situación clínica estable. Veinticuatro horas después de su ingreso comenzó con trabajo de parto espontáneo, que progresó rápidamente a pesar de tratamiento con un antagonista competitivo de los receptores de oxitocina humana (atosiban). Se decidió suspender la bomba de heparina. Las pruebas de coagulación reflejaban en ese momento un TTPA de 69,8 s (rango de referencia, 25-39 s). No se revirtió con sulfato de protamina antes de la cirugía, y se asumió el riesgo de sangrado frente al embolismo pulmonar. Dos horas después, tras monitorizar los siguientes parámetros: SaO2, ECG, presión arterial invasiva (cánula en la arteria radial derecha después de la prueba de Allen), el gasto cardiaco (Vigileo Flotrac. Edwards Lifesciences Co.), diuresis horaria y EtCO2, se procedió a cesárea a través de histerotomía segmentaria transversal con anestesia general. Ésta consistió en inducción de secuencia rápida (remifentanilo 1 µg/kg, propofol 2 mg/kg, succinilcolina 1,5 mg/kg) y mantenimiento con fentanilo 3 µg/kg/h y Fi sevoflurano 2%. Las pérdidas hemáticas fueron leves y la paciente permaneció hemodinámicamente estable, con un gasto cardiaco entre 3,8 y 6 l/min. Una vez extubada sin incidencias se traslada a la unidad de reanimación para control postoperatorio. La heparina no fraccionada se reinició 2 horas más tarde, y el análisis de ingreso mostraba un TTPA de 29,1 segundos. El postoperatorio inmediato transcurrió sin complicaciones. Fue dada de alta de la unidad 4 días después del parto. Se introdujo acenocumarol VO el séptimo día después de la cirugía para obtener un INR de 3 aproximadamente. La heparina no fraccionada iv se suspendió el día 10º. Doce días después de la cirugía la paciente experimentó un episodio de dolor e hinchazón de la extremidad. Se aplicó una media de compresión y enoxaparina sc 60 mg. Una nueva ecografía-Doppler de emergencia no reveló ningún nuevo coágulo en el sitio del trombo inicial y sí la dilatación de la vena iliofemoral o síndrome postrombótico. El hemograma, pruebas de coagulación, bioquímica y los resultados de ECG fueron normales, sin clínica de embolia pulmonar. La paciente mejoró progresivamente y fue dada de alta a su domicilio a los 19 días, con acenocumarol 4 mg (según el control INR) y HBPM por vía subcutánea 40 mg/24 horas, medidas posturales y medias de compresión. Se realizó estudio por el servicio de hematología con el fin de descartar trombofilias, sobre todo de cara a futuras gestaciones. El futuro fue negtivo. Los anticoagulantes orales se suspendieron seis meses después del parto. Discusión Existen tres opciones terapéuticas para las TVP durante el embarazo, la administración de anticoagulantes, la inserción de un filtro en la vena cava inferior, y la cirugía (trombectomía y ligadura de la vena cava). Aunque el tratamiento de elección en caso de tromboembolismo durante el embarazo sigue siendo el tra51 tamiento anticoagulante3,4, el resto de opciones terapéuticas deben considerarse a título individual, al igual que los riesgos y beneficios de las acciones más invasivas. En este caso consideramos como factores más importantes en esta situación la historia clínica, la estabilidad hemodinámica, la experiencia del personal, y la consulta de la literatura científica. El método más utilizado es la terapia anticoagulante. La heparina no atraviesa la placenta y, por tanto, no afecta al feto. La HBPM tiene varias ventajas sobre la heparina no fraccionada, su mayor vida media, la posibilidad de administrar dosis diarias, y un menor riesgo de trombocitopenia inducida por heparina, hemorragia y osteoporosis materna. La heparina no fraccionada o heparina sódica se suele elegir en situaciones en las que los procedimientos (quirúrgicos o no) son inminentes, como en nuestro caso, debido a su vida media corta y reversibilidad con sulfato de protamina. El efecto debe ser medido por el TTPA. Cuando nuestra paciente empezó a tener contracciones de forma espontánea, se combinaron los anticoagulantes y atosiban, a fin de ganar tiempo para estabilizar el trombo y su adhesión a la pared, y reducir así la posibilidad de desprendimiento del trombo cuando la presión natural, ejercida por el útero grávido sobre la cava desapareciera tras el parto. La mayoría de autores recomiendan la suspensión de la heparina no fraccionada intravenosa de 4-6 horas antes de la hora prevista para la cirugía y control del TTPA antes de la incisión3. Si comienza a sangrar espontáneamente, o se evidencia aumento de hemorragia en el comienzo de la cesárea, el sulfato de protamina debe administrarse para reducir el riesgo de hemorragia. Es importante volver a introducir la terapia anticoagulante durante el puerperio inmediato, para reducir al mínimo el tiempo que el paciente esté sin anticoagulación. La paciente debe deambular tan pronto como sea posible a fin de favorecer el retorno venoso y reducir el síndrome post-trombótico de insuficiencia venosa que se produce hasta en el 60% de los casos2. Si bien los anticoagulantes pueden prevenir el crecimiento y liberación de un trombo, y disminuir el riesgo de embolismo pulmonar y trombosis venosa profunda, no disuelven el trombo que causa la oclusión, ni reducen la obstrucción del flujo venoso. El filtro de vena cava inferior, de inserción percutánea, es una alternativa a los anticoagulantes cuando fallan o están contraindicados2. Hemos encontrado una serie de casos en los que este enfoque complementa el tratamiento anticoagulante para reducir el riesgo de embolismo pulmonar5. Es una práctica más común que la ligadura venosa y trombectomía en la actualidad debido a sus bajas tasas de morbilidad. Además, los 309 Documento descargado de http://www.elsevier.es el 30/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 5, 2010 filtros transitorios parecen más adecuados en una paciente joven en el que se retirará el dispositivo en unos 15 días. Es importante tener en cuenta que no está exento de complicaciones como la rotura venosa y la rotura o la migración del filtro (más común en mujeres embarazadas debido a la compresión de la vena cava inferior por cambios en la anatomía). También se encontró que la recomendación para la inserción en el caso de la TVP masiva dentro de las 2 semanas antes del parto no tenía un nivel de evidencia científica6. Según Köcher et al4, algunos autores están a favor de este enfoque7,8, mientras que otros están en contra9. La colocación de un filtro en la vena cava inferior es considerada pues, como la segunda opción en los pacientes que sufren una TVP masiva. La trombectomía y ligadura de la vena cava inferior se reservan para pacientes con contraindicaciones para el tratamiento anticoagulante o cuyo tratamiento anticoagulante ha fracasado, y para los casos de embolia pulmonar o inestabilidad hemodinámica1,2. El enfoque conservador que adoptamos fue guiado por la experiencia previa en nuestro departamento de maternidad en pacientes con TVP masiva que recibieron heparina. Sin embargo, éste fue nuestro primer caso en que la TVP coincidía con el parto. Pareció lo más razonable descartar la cirugía y la colocación de un filtro en la vena cava inferior, mientras la paciente estaba estable y tras una evaluación completa de la situación clínica, así como de las posibles complicaciones de madre y feto. Se han encontrado casos similares en la literatura10,11, aunque no en el embarazo. En cuanto al tratamiento anestésico, las dos opciones disponibles son la anestesia general o una anestesia neuroaxial (epidural o subaracnoidea). Dada la situación clínica estable de nuestra paciente en un primer momento, se decidió el tratamiento con heparina no fraccionada intravenosa y programar un parto por cesárea para 48 horas después, por lo que la anestesia neuroaxial (subaracnoidea) podría ser una opción, dejando un margen adecuado tras suspender la infusión de heparina no fraccionada y proceder con la inyección intradural. La inyección epidural se descartó debido al alto riesgo de hematoma y la compresión medular como consecuencia de la terapia anticoagulante3. El inicio de trabajo espontáneo de parto a las 24 horas nos obligó a modificar nuestro planteamiento inicial y realizar un parto por cesárea con anestesia general. Fue planificado cuidadosamente con los departamentos de obstetricia y hematología. El depar- 310 tamento de obstetricia consideró que la cesárea era un enfoque más adecuado en este caso, a pesar del aumento del riesgo de hemorragia. Así pues podemos concluir que el enfoque terapéutico debe basarse en una adecuada coordinación entre los diferentes servicios implicados, el uso conservador de los anticoagulantes, y el control de su acción con el TTPA, para estabilizar el trombo cuando no hay signos de embolia pulmonar y el paciente se encuentra hemodinámicamente estable. Si esta opción no es posible, entonces la colocación de un filtro en la vena cava inferior, trombectomía, o incluso la ligadura venosa podrían desempeñar un papel. La terapia anticoagulante debe ser reiniciada de nuevo lo más pronto posible después de la cirugía. Agradecimientos Nuestro agradecimiento al Dr. Luis Olmedilla por sus correcciones y asesoramiento. Agradecemos a los servicios en nuestro hospital de hematología, ginecología, y radiología por su ayuda para escribir este artículo y por su cooperación. BIBLIOGRAFÍA 1. Pomp ER, Lenselink AM. Pregnancy, the postpartum period and prothrombotic defects: risk of venous thrombosis in the MEGA study. J Thromb Haemost. 2008;6(4):632-7. 2. Marik PE, Plante LA. Venous thromboembolic disease and pregnancy. N Engl J Med. 2008;359(19):2025-33. 3. Ginsberg JS, Bates SM. Management of venous thromboembolism during pregnancy. J Thromb Haemost. 2003;1(7):1435-42. 4. Köcher M. Krcova V, Cerna M, Prochazka M. Retrievable Günther Tulip Vena Cava Filter in the prevention of pulmonary embolism in patients with acute deep venous thrombosis in perinatal period. Eur J Radiol. 2009;70(1):165-9. 5. Cheung MC, Asch MR. Temporary inferior vena cava filter use in pregnancy. J Thromb Haemost. 2005;3(5):1096-7. 6. Baglin TP, Brush J, Streiff M. Guidelines on use of vena cava filters. Br J Haematol. 2006;134(6):590-5. 7. AbuRahma AF, Boland JP. Management of deep vein thrombosis of the lower extremity in pregnancy: a challenging dilemma. Am Surg. 1999;65(2):164-5. 8. AbuRahma AF, Mullins DA. Endovascular caval interruption in pregnant patients with deep vein thrombosis of the lower extremity. J Vasc Surg. 2001;33(2):375-8. 9. Decousus HD, Leizorovicz A, Parent F, Page Y, et al. A clinical trial of vena cava filter in the prevention of pulmonary embolism in patients with proximal deep-vein thrombosis. N Eng J Med. 1998;338(7):40915. 10. Martínez D, Villalva V. Trombosis venosa profunda como manifestación clínica inicial de un aneurisma de la arteria femoral común. Angiología. 2006;58(4):331-4. 11. De Vicente JC, Pérez A, García MI, Gredilla E, Reinoso F. Trombosis en vena cava inferior tras cirugía correctora de atresia tricuspídea (Técnica de Fontan) en paciente pediátrico. Rev. Esp. Anestesiol. Reanim. 2003;50(8):472-6. 52